验证是药厂实施GMP的主要环节
作者:陈灼湖 吉慧文
单位:
陈灼湖 福州福兴医药有限公司;吉慧文 福州世纪星制药有限公司
关键词:
海峡药学9903100 我国自1988年颁布第一个《药品生产质量管理规范》(GMP)指导药品生产以来,极大地推动了药品生产企业的质量管理活动,对提高药品质量,保证人民用药安全起着重要的作用。随着改革开放的不断深入,我国医药工业又有了飞跃的发展,医药工业管理的科学水平得以不断的提高,为适应这种飞速发展的需要,积极参与国际医药市场竞争,我国于1992年对GMP进行了第一次修订,使条文更加完善,管理更为法制化、规范化、科学化。一批制药企业(车间)相继通过药品GMP达标和认证。经过几年的实践与总结,我国于1998年又重新修订了GMP,并于1999年8月1日正式实施。
, http://www.100md.com
《药品生产质量管理规范》(1998年修订)是在总结了前两版《规范》实践经验的基础上,紧密结合我国国情而修订的。《规范》(1998年修订)条理更为清晰,标准更为明确,便于实施过程中的具体操作,又注重与国际标准接轨,利于与其它国家交流GMP工作。现就我们的学习谈一点肤浅的认识。
1 突出管理,强调验证 纵观我国颁布的各版GMP的章节与条文,不难看出,各版本一次比一次更趋于完善,更趋于可操作性,更切合我国国情,更有利于与国际标准接轨。对比如下:
表1 我国GMP各版本章节、条文对比*
GMP
1988年
GMP
1992年修订
, 百拇医药
GMP
1998年修订
第一章
总则
总则
总则
第二章
人员
人员
机构与人员
第三章
厂房
厂房
, http://www.100md.com
厂房与设施
第四章
设备
设备
设备
第五章
卫生
卫生
物料
第六章
原料
原料、辅料
及包装材料
, 百拇医药
卫生
第七章
生产操作
生产管理
验证
第八章
包装与贴签
包装与贴签
文件
第九章
生产管理与
质量管理文件
生产管理与
, 百拇医药
质量管理文件
生产管理
第十章
质量管理部门
质量管理部门
质量管理
第十一章
自检
自检
产品销售与收回
第十二章
销售记录
销售记录
, http://www.100md.com
投诉与不良反应报告
第十三章
用户意见与
不良反应报告
用户意见与
不良反应报告
自检
第十四章
附则
附则
附则
条文
共49条
, http://www.100md.com
共78条
共88条
*未包括GMP(1998年修订)附录部份章节
从表一可以看出:① 条文从49条增至78条再增至88条,逐版增多。内容不断充实;② 章节不变,皆为14章。1998年修订本与1992年修订本相比较,1998年修订本章节内容不仅包括了1992年修订本的各章节内容(其中包装与贴签并入生产管理章中),且内容更趋完善及可操作性。不仅强调了人员与厂房的重要性,而且突出了与之相对应的机构与设施的重要性;不仅强调了物料的定点供给,并且明确规定了“药品生产企业应建立药品退货和收回的书面程序,并有记录”,从而实现了从物料采购到厂家设施、人员机构、生产设备、生产工艺及产品售后质量跟踪全过程的质量监控管理。尤其重要的是GMP(1998年修订)将验证突出成章,达到预防为主,变管结果为管因素,依靠科学管理的理论、程序和方法,使药品生产的全过程始终处于受控状态,从而确认生产质量管理系统有关要求的合理性,达到产品质量连续、稳定的均一性,使药品生产企业做到质量优良、生产有序最低消耗,最佳服务。
, http://www.100md.com
2 验证是GMP的重要组成部份 众所周知,质量是企业的生命,从GMP的角度来理解质量,则质量是一个综合的反映系统“即经过设计并形成文件的,已经实施和经过检定的,并通过人员、设备和其它原料提供保证,使产品(质量)具有适宜于使用目的的连续一致性”。GMP(1998年修订本)之所以强调验证,就是依据质量这一内涵与国际上采用的先进的药品质量管理手段相接轨,将质量概念从单纯符合标准的狭义质量,发展为贯穿于产品开发、设计、工艺流程、采购、仓贮,检验、销售、售后服务和生产管理等各个环节在内的广义质量。
药品最重要的属性就是质量。药品质量是按照GMP设计和生产出来的,而不仅仅是按药品的标准检验出来的。GMP(1998年修订本)强调验证正是“用以证明在药品生产和检验中所用的厂房设施及设备,原辅材料、生产工艺、质量控制方法等是否确实达到预期目的的一系列活动。”这一系列活动从质量控制入手,把实际结果与设计、计划或标准相对照,不断地采取措施,使实施结果符合我们预先设计、计划或标准的结果,从而实现质量的保证。在药品生产过程中,从人员职责,各岗位有与之相适应的专业技术人员,并经岗位技能培训,持证上岗入手,到生产设备与生产能力相适应及规范的操作、清洁SOP;原辅材料、包装材料、成品、半成品、中间体有严格的质控措施、质量标准及检验方案;厂房设施能确保适应生产所需的洁净要求及温、湿度、照明度要求,并有良好的仓贮条件;生产过程能严格按生产工艺规程及SOP进行规范操作的全过程的可控性,从而实现强化药品生产企业的质量意识,降低生产事故机率,降低事故处理费用,减少不符合质量标准的批次,降低不合格品费用,以保证药品的有效性,安全性,均一性,稳定性。同时保证企业的经济效益。
, http://www.100md.com
综上所述,验证实际上就是药品生产企业将GMP的原则条文切实具体地运用到生产管理全过程的重要科学手段,是药品生产企业实施GMP的重要环节。如果药品生产企业在实施GMP过程中,不经验证,则其实施必带有盲目性,缺乏依据,生产出来的药品质量也是不可靠的。试想如果制药企业对空气净化系统不进行验证,就无法知道洁净室的空气洁净度是否满足所生产的剂型的需要,又如何保证该药品质量的安全、稳定均一呢?如果工艺用水系统不进行验证,是否符合工艺用水要求都不知道,又如何保证产品的质量呢?不经验证,就无法提供必要的验证文件,又如何证明生产企业是按GMP进行全过程的监控管理,又如何与国际标准接轨,参与国际市场竞争呢?因此,验证是药品生产企业质量保证的重要组成部份;是向用户及第三方提供信任,使他们相信产品能满足内在质量要求,表明提供的都是符合规定要求的产品的最直接的证明和活动。
3 验证的实施与内容 GMP(1998年修订)指出:“药品生产验证应包括厂房、设施及设备安装确认,运行确认,性能确认和产品验证。产品的生产工艺及关键设施,设备应按验证方案进行验证。当影响产品质量的主要因素,如工艺、质量控制方法,主要原辅料、主要生产设备等发生改变时,以及生产一定周期后,应进行再验证。”所以要使生产的药品符合设计的质量,就必须对药品生产的全过程进行验证。对生产过程进行适应性、稳定性、安全性、可行性、整体性等方面的验证。具体讲,验证内容包括了:生产人员、生产设备及检验仪器、生产用原辅材料及包装材料、生产制造工艺及检验方法、厂房设施及环境卫生等内容。而对这些具体内容又该如何进行验证?GMP(1998年修订)明确指出:“应根据验证对象提出验证项目,制定验证方案并组织实施。验证工作完成后,应写出验证报告,由验证工作负责人审核,批准。验证过程中的数据和分析内容应以文件形式归档保存。验证文件应包括验证方案、验证报告、评价和建议,批准人等。”具体程序及内容如下。
, http://www.100md.com
3.1 验证工作基本程序: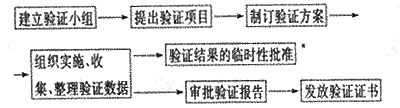
由于验证的书面总结和审批需要较长的时间,因此,在验证实验完成后,只要结果正常,验证总负责人可以临时批准已验证的生产过程及产品投入生产。因验证需要而处于待验的产品,也可按验证结果决定是否出厂。
3.2 验证工作基本内容 3.2.1 厂房、设备及设施验证:对厂房工程的竣工验收及对设备选型、性能特点和安装效果等评价; 3.2.2 质控部门及计量部门的验证:必须在其他验证开始之前首先完成。计量部门的验证按国家计量部门法规进行; 3.2.3 生产过程的验证:在完成3.2.1、3.2.2之后进行。其中工艺条件要考虑实际生产中可能遇到的条件,包括最差情况的条件,并要保证结果的重现性; 3.2.4 产品验证:在3.2.3验证合格的基础上进行全过程的验证,以证明产品符合预定的质量标准。
, 百拇医药
3.3 验证过程中数据和分析内容均应以文件形式保存,文件应包括以下内容: 验证项目与周期; 验证目的、验证方案及批准人; 厂房及设备设施的安装验证报告; 生产过程验证报告:该工序的验证目的;生产方法和操作规程。质量标准、取样办法和检验操作规程;验证报告,包括所用试验仪器校正记录,试验原始数据及整理、验证小结; 产品验证报告,验证批的试验数据; 评价和建议,包括再验证的时间,建议; 验证证书。
随着改革开放的深入,“入关”的临近,我国医药行业将面临越来越严峻的挑战。实施GMP管理,强化全过程的验证,使药品生产的全过程处于受控状态,始终如一地连续生产出令人信赖的产品,将是各药品生产企业实现无缺陷管理,迎接挑战,与国际标准接轨,竞争于国际医药市场的必由之路。
参考文献
1.苏怀德:国家医药管理局教材办公室,1995;5
2.缪德骅等:药品生产管理规范(GMP)实施指南1992,企业管理出版社,1993;5
3.李钧:药品生产质量管理规范读本,中国医药科技出版社,北京,1997;10
4.药品生产质量管理规范:1988年,1992年修订本,1998年修订本(国家药品监督管理局), 百拇医药
单位:
陈灼湖 福州福兴医药有限公司;吉慧文 福州世纪星制药有限公司
关键词:
海峡药学9903100 我国自1988年颁布第一个《药品生产质量管理规范》(GMP)指导药品生产以来,极大地推动了药品生产企业的质量管理活动,对提高药品质量,保证人民用药安全起着重要的作用。随着改革开放的不断深入,我国医药工业又有了飞跃的发展,医药工业管理的科学水平得以不断的提高,为适应这种飞速发展的需要,积极参与国际医药市场竞争,我国于1992年对GMP进行了第一次修订,使条文更加完善,管理更为法制化、规范化、科学化。一批制药企业(车间)相继通过药品GMP达标和认证。经过几年的实践与总结,我国于1998年又重新修订了GMP,并于1999年8月1日正式实施。
, http://www.100md.com
《药品生产质量管理规范》(1998年修订)是在总结了前两版《规范》实践经验的基础上,紧密结合我国国情而修订的。《规范》(1998年修订)条理更为清晰,标准更为明确,便于实施过程中的具体操作,又注重与国际标准接轨,利于与其它国家交流GMP工作。现就我们的学习谈一点肤浅的认识。
1 突出管理,强调验证 纵观我国颁布的各版GMP的章节与条文,不难看出,各版本一次比一次更趋于完善,更趋于可操作性,更切合我国国情,更有利于与国际标准接轨。对比如下:
表1 我国GMP各版本章节、条文对比*
GMP
1988年
GMP
1992年修订
, 百拇医药
GMP
1998年修订
第一章
总则
总则
总则
第二章
人员
人员
机构与人员
第三章
厂房
厂房
, http://www.100md.com
厂房与设施
第四章
设备
设备
设备
第五章
卫生
卫生
物料
第六章
原料
原料、辅料
及包装材料
, 百拇医药
卫生
第七章
生产操作
生产管理
验证
第八章
包装与贴签
包装与贴签
文件
第九章
生产管理与
质量管理文件
生产管理与
, 百拇医药
质量管理文件
生产管理
第十章
质量管理部门
质量管理部门
质量管理
第十一章
自检
自检
产品销售与收回
第十二章
销售记录
销售记录
, http://www.100md.com
投诉与不良反应报告
第十三章
用户意见与
不良反应报告
用户意见与
不良反应报告
自检
第十四章
附则
附则
附则
条文
共49条
, http://www.100md.com
共78条
共88条
*未包括GMP(1998年修订)附录部份章节
从表一可以看出:① 条文从49条增至78条再增至88条,逐版增多。内容不断充实;② 章节不变,皆为14章。1998年修订本与1992年修订本相比较,1998年修订本章节内容不仅包括了1992年修订本的各章节内容(其中包装与贴签并入生产管理章中),且内容更趋完善及可操作性。不仅强调了人员与厂房的重要性,而且突出了与之相对应的机构与设施的重要性;不仅强调了物料的定点供给,并且明确规定了“药品生产企业应建立药品退货和收回的书面程序,并有记录”,从而实现了从物料采购到厂家设施、人员机构、生产设备、生产工艺及产品售后质量跟踪全过程的质量监控管理。尤其重要的是GMP(1998年修订)将验证突出成章,达到预防为主,变管结果为管因素,依靠科学管理的理论、程序和方法,使药品生产的全过程始终处于受控状态,从而确认生产质量管理系统有关要求的合理性,达到产品质量连续、稳定的均一性,使药品生产企业做到质量优良、生产有序最低消耗,最佳服务。
, http://www.100md.com
2 验证是GMP的重要组成部份 众所周知,质量是企业的生命,从GMP的角度来理解质量,则质量是一个综合的反映系统“即经过设计并形成文件的,已经实施和经过检定的,并通过人员、设备和其它原料提供保证,使产品(质量)具有适宜于使用目的的连续一致性”。GMP(1998年修订本)之所以强调验证,就是依据质量这一内涵与国际上采用的先进的药品质量管理手段相接轨,将质量概念从单纯符合标准的狭义质量,发展为贯穿于产品开发、设计、工艺流程、采购、仓贮,检验、销售、售后服务和生产管理等各个环节在内的广义质量。
药品最重要的属性就是质量。药品质量是按照GMP设计和生产出来的,而不仅仅是按药品的标准检验出来的。GMP(1998年修订本)强调验证正是“用以证明在药品生产和检验中所用的厂房设施及设备,原辅材料、生产工艺、质量控制方法等是否确实达到预期目的的一系列活动。”这一系列活动从质量控制入手,把实际结果与设计、计划或标准相对照,不断地采取措施,使实施结果符合我们预先设计、计划或标准的结果,从而实现质量的保证。在药品生产过程中,从人员职责,各岗位有与之相适应的专业技术人员,并经岗位技能培训,持证上岗入手,到生产设备与生产能力相适应及规范的操作、清洁SOP;原辅材料、包装材料、成品、半成品、中间体有严格的质控措施、质量标准及检验方案;厂房设施能确保适应生产所需的洁净要求及温、湿度、照明度要求,并有良好的仓贮条件;生产过程能严格按生产工艺规程及SOP进行规范操作的全过程的可控性,从而实现强化药品生产企业的质量意识,降低生产事故机率,降低事故处理费用,减少不符合质量标准的批次,降低不合格品费用,以保证药品的有效性,安全性,均一性,稳定性。同时保证企业的经济效益。
, http://www.100md.com
综上所述,验证实际上就是药品生产企业将GMP的原则条文切实具体地运用到生产管理全过程的重要科学手段,是药品生产企业实施GMP的重要环节。如果药品生产企业在实施GMP过程中,不经验证,则其实施必带有盲目性,缺乏依据,生产出来的药品质量也是不可靠的。试想如果制药企业对空气净化系统不进行验证,就无法知道洁净室的空气洁净度是否满足所生产的剂型的需要,又如何保证该药品质量的安全、稳定均一呢?如果工艺用水系统不进行验证,是否符合工艺用水要求都不知道,又如何保证产品的质量呢?不经验证,就无法提供必要的验证文件,又如何证明生产企业是按GMP进行全过程的监控管理,又如何与国际标准接轨,参与国际市场竞争呢?因此,验证是药品生产企业质量保证的重要组成部份;是向用户及第三方提供信任,使他们相信产品能满足内在质量要求,表明提供的都是符合规定要求的产品的最直接的证明和活动。
3 验证的实施与内容 GMP(1998年修订)指出:“药品生产验证应包括厂房、设施及设备安装确认,运行确认,性能确认和产品验证。产品的生产工艺及关键设施,设备应按验证方案进行验证。当影响产品质量的主要因素,如工艺、质量控制方法,主要原辅料、主要生产设备等发生改变时,以及生产一定周期后,应进行再验证。”所以要使生产的药品符合设计的质量,就必须对药品生产的全过程进行验证。对生产过程进行适应性、稳定性、安全性、可行性、整体性等方面的验证。具体讲,验证内容包括了:生产人员、生产设备及检验仪器、生产用原辅材料及包装材料、生产制造工艺及检验方法、厂房设施及环境卫生等内容。而对这些具体内容又该如何进行验证?GMP(1998年修订)明确指出:“应根据验证对象提出验证项目,制定验证方案并组织实施。验证工作完成后,应写出验证报告,由验证工作负责人审核,批准。验证过程中的数据和分析内容应以文件形式归档保存。验证文件应包括验证方案、验证报告、评价和建议,批准人等。”具体程序及内容如下。
, http://www.100md.com
3.1 验证工作基本程序:

由于验证的书面总结和审批需要较长的时间,因此,在验证实验完成后,只要结果正常,验证总负责人可以临时批准已验证的生产过程及产品投入生产。因验证需要而处于待验的产品,也可按验证结果决定是否出厂。
3.2 验证工作基本内容 3.2.1 厂房、设备及设施验证:对厂房工程的竣工验收及对设备选型、性能特点和安装效果等评价; 3.2.2 质控部门及计量部门的验证:必须在其他验证开始之前首先完成。计量部门的验证按国家计量部门法规进行; 3.2.3 生产过程的验证:在完成3.2.1、3.2.2之后进行。其中工艺条件要考虑实际生产中可能遇到的条件,包括最差情况的条件,并要保证结果的重现性; 3.2.4 产品验证:在3.2.3验证合格的基础上进行全过程的验证,以证明产品符合预定的质量标准。
, 百拇医药
3.3 验证过程中数据和分析内容均应以文件形式保存,文件应包括以下内容: 验证项目与周期; 验证目的、验证方案及批准人; 厂房及设备设施的安装验证报告; 生产过程验证报告:该工序的验证目的;生产方法和操作规程。质量标准、取样办法和检验操作规程;验证报告,包括所用试验仪器校正记录,试验原始数据及整理、验证小结; 产品验证报告,验证批的试验数据; 评价和建议,包括再验证的时间,建议; 验证证书。
随着改革开放的深入,“入关”的临近,我国医药行业将面临越来越严峻的挑战。实施GMP管理,强化全过程的验证,使药品生产的全过程处于受控状态,始终如一地连续生产出令人信赖的产品,将是各药品生产企业实现无缺陷管理,迎接挑战,与国际标准接轨,竞争于国际医药市场的必由之路。
参考文献
1.苏怀德:国家医药管理局教材办公室,1995;5
2.缪德骅等:药品生产管理规范(GMP)实施指南1992,企业管理出版社,1993;5
3.李钧:药品生产质量管理规范读本,中国医药科技出版社,北京,1997;10
4.药品生产质量管理规范:1988年,1992年修订本,1998年修订本(国家药品监督管理局), 百拇医药