新型降钙素的基因合成与克隆表达
作者:张玉彬 吴 滔 王旻 吴梧桐 郑 珩 张兆林 刘晓军
单位:中国药科大学生物制药学院,南京210009
关键词:降钙素;新型降钙素;基因工程;融合表达
药物生物技术990301
摘 要 借助计算机辅助设计了一种新的人降钙素类似物(新型降钙素)。根据密码子偏爱性原理及基因工程操作原则设计了它的基因,运用化学法和酶法相结合的技术合成了该基因,并克隆到质粒pUC19中,DNA测序验证正确。该基因被克隆到融合型表达载体pGEX-2T中,重组融合型表达载体nCT/pGEX-2T转化E.coliBL21,培养表达,SDS-PAGE分析可见Mr约31000的融合蛋白带,融合蛋白占细胞内总蛋白的34%。Western Blotting分析证明该新型降钙素获得表达。
, 百拇医药
Chemical Synthesis,Cloning and Expression of
the Gene for Novel Human Calcitonin Analogue
Zhang Yubin,Wu Tao, Wang Min,Wu Wutong,Zheng Heng,Zhang Zhaolin,Liu Xiaojun
(College of Biopharmaceutics,China Pharmaceutical University,Nanjing 210009)
Abstract The novel hCT analogue was designed by Computer Aid D esign Technology (CAD). The novel calcitonin gene(126bp)was synthesized by the combination of c hemical synthesis and Klenow polymerase extension. The synthetic gene was ins er ted into fusion expression vector pGEX-2T with BamHⅠ/EcoRⅠ sites. This plas mid w as transformed into E.coli BL21 strain. The major band of about 31000 fusion prot ein could be detected by SDS-PAGE analysis and the fusion protein is more than 34% of total cellular protein.The novel hCT analogue was confirmed by Western B lotting analysis.
, 百拇医药
Key Words Calcitonin ,Human calcitonin analogue,Genetic enginee rring,Fusion expression
降钙素是由32个氨基酸残基组成的多肽类激素,它在体内起着钙-磷代谢调节的功能,已被用于治疗骨质疏松症、高血钙症及Paget′s症等[1]。临床主要使用的是鲑鱼降钙素,长期使用约有40%~70%的患者出现抗体相关的耐受性,限制了它的长期使用[2]。而人的降钙素活性又很低,仅为鲑鱼的2%~5%,其半衰期也较短[3]。因此,很有必要研究开发一种活性高、半衰期长、抗原性低的人降钙素类似物。
我们对各种来源的降钙素进行分析比较,结合最新研究成果,提出了增加降钙素C-末端的亲水性可提高降钙素与其受体亲和力及提高人降钙素的等电点将有助于延长降钙素半衰期的设想。据此,我们借助计算机辅助设计了一种新的人降钙素类似物(简称新型降钙素,novelhumancalcitoninanalogue,nCT)。计算机分析表明它的C-末端亲水性增加,等电点提高(pI8.7),抗原性图谱与人的降钙素相同,满足了设计要求。运用基因工程技术中融合蛋白表达法制备了该新型降钙素,大鼠体内降血钙试验表明它具有显著的降血钙作用。
, 百拇医药
1 材 料
1.1 质粒及菌株
pUC19,pGEX-2T,E.coliJM105,E.coliBL21均为瑞典Pharmacia公司产品,1.2 酶及化学试剂
BamHⅠ,EcoRⅠ,T4-DNA连接酶,Klenow酶,X-gal,IPTG均为美国Promega公司产品。兔抗人降钙素抗体和ABC免疫组化检测试剂盒购自华美生物工程公司.其余常用试剂均为进口或国产分析纯。
1.3 仪器
DNA合成仪Oligo1000型 美国Beckman公司。373A型DNA测序仪 美国ABI公司。CS-930型薄层扫描仪 日本岛津公司。NovaBlot电转移仪 瑞典Pharmacia公司。
, http://www.100md.com 2 方 法
2.1 新型降钙素的分子设计
以人和鲑鱼的降钙素为先导化合物,设计了大量人降钙素的类似物。借助于计算机辅助设计技术,将设计的各种人降钙素类似物用蛋白质分析软件分析预测其新分子的C-末端亲水性,等电点(pI)和抗原性等参数,选择符合设计要求的类似物作为新型降钙素。
2.2 新型降钙素的基因设计与合成
根据设计的新型降钙素的氨基酸序列和基因工程操作原理,选用大肠杆菌偏爱的密码子设计出它的基因DNA序列,委托中科院北微所基因合成中心应用BeckmanOligo1000DNA合成仪合成该基因的两条部分单链A72和B72。取上述人工合成并纯化的单链DNA片段A72和B72各80pmol,在终体积80μl的退火缓冲液中混匀,置90℃水浴5min后,缓慢冷却至室温,加入5mol/LNaCl至终浓度为300mmol/L和3倍体积乙醇,-20℃放置过夜,离心去上清,抽干除净残留乙醇。沉淀的DNA溶解于Klenow酶反应的1×缓冲液中,内含有dNTPs(终浓度各0.5mmol/L)和5U的Klenow酶,终体积25μl,37℃反应1h,乙醇沉淀后获得双链DNA片段(126bp)[4]。
, 百拇医药
2.3 融合表达载体的构建
合成的双链DNA用EcoRⅠ和BamHⅠ双酶切后,克隆到pUC19/EcoRⅠ、BamHⅠ载体中,其操作按分子克隆手册中的实验方法稍加修改进行[5]。阳性重组质粒经质粒大小比较、酶切鉴定和DNA测序验证,其中DNA测序委托中科院上海植生所采用ABI373A型DNA测序仪测定。经测序验证正确的质粒按分子克隆方法经酶切、PAGE电泳后“压碎浸泡”法回收新型降钙素基因,并克隆到融合表达载体pGEX-2T/EcoRⅠ、BamHⅠ中[6,7],转化E.coliBL21,挑选阳性重组质粒,并进行质粒大小比较和酶切鉴定。
2.4 融合蛋白的表达与鉴定
重组菌在2×YT培养基中37℃恒温振荡培养至A600nm=0.6,加入IPTG至终浓度0.1mmol/L,继续培养4h。离心收集菌体,进行15%SDS-PAGE分析,拍照记录和双波长扫描分析。
, http://www.100md.com
2.5 Western-blotting分析
将电泳后的SDS-PAGE胶与硝酸纤维素膜分别在电转移液中浸泡5min,安装好电转移装置,于0.8mA/cm2电转移1h。将膜取下,经封闭、洗涤后,加入兔抗hCT的抗体,4℃放置过夜。洗涤后加入生物素化二抗(羊抗兔IgG),37℃保温30min,洗涤后加入ABC工作液(Avidin-Biotin-PeroxidaseComplex),37℃保温30min,洗涤后,加新鲜配制的底物溶液(4-氯-1-萘酚),显色完成后,洗涤,拍照记录。
3 结 果
3.1 新型降钙素的结构和基因设计
借助计算机辅助设计,通过大量的分析计算发现了一种新的人降钙素类似物符合设计要求,其分子结构如图1所示。它的C-末端亲水性增加,等电点提高(pI8.7),抗原性图谱与人的降钙素相同。根据密码子偏爱性原理及基因工程操作原则,设计了该新型降钙素基因(见图1)。N-端添加Met密码ATG是为了用溴化氰将新型降钙素前体从融合蛋白中释放出来而设计的。C-末端Pro后添加Arg密码子CGT是为了新型降钙素的C-末端酰胺化而设计的。5′和3′-端BamHⅠ和EcoRⅠ酶切位点是为了将基因克隆到载体中而添加的,另外还增添了保护碱基。
, http://www.100md.com
Fig 1 Sequence of nCT gene and its encoding amino acids
3.2 基因的合成与克隆
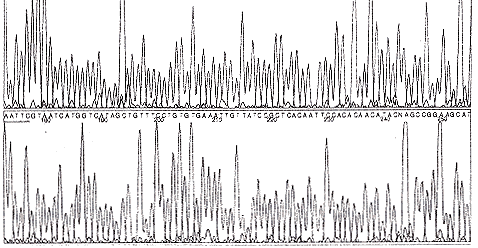
根据基因结构人工合成两条72碱基的DNA单链(A72和B72),其寡核苷酸序列为A72:5′-CGC GGA TCC ATG TGC GGT AAC CTG TCT ACC TGC GTT CTG GGT ACC TAC ACC CAG G A C TTC AAC AAA TTC CAC-3′ B72:5′-CCG GAA TTC TCA TTA ACG CGG AGC ACC AAC A CC GAT AGC GGT GCG CGG GAA GGT GTG GAA TTT GTT GAA GTC-3′通过两条链中间18个互补碱基的配对,使两条链退火,再利用Klenow酶补平,获得双链DNA,并经EcoRⅠ和BamHⅠ双酶切后插入到pUC19中,于含有X-gal的LB平板上挑选阳性转化菌落,经酶切鉴定及DNA测序验证得到含正确基因的重组质粒,并命名为nCT/pUC19。重组质粒中外源基因DNA测序结果正确(见图2)。
, http://www.100md.com
Fig 2 DNA Sequence of the recombinant plasmid nCT/pUC19
3.3 融合表达载体的构建
将nCT/pUC19质粒中的nCT基因用EcoRⅠ、BamHⅠ酶切后,克隆到pGEX-2T/EcoRⅠ、BamHⅠ载体中,阳性重组质粒经电泳大小比较及酶切鉴定证明新型降钙素基因插入到融合型表达载体中(见图3)。该重组载体命名为nCT/pGEX-2T。将重组融合表达载体转化E.coliBL21,其工程菌命名为nCT/pGEX-2T/BL21.

(a) Agarose electrophoresis of plasmids
, 百拇医药
1,6.λDNA/HindⅢ 2.nCT/pUC19
3.pUC19 4.nCT/pGEX-2T 5.pGEX -2T

(b) Restriction endonuclease analysis of recombinant plasmids by PAGE
1.DNA Marker pGEM-3Zf(+)/HaeⅢ 2.Synthetic nCT dsDNA
3.nCT/pUC19 with BamHⅠ and EcoRⅠ digestion
4.nCT/pGEX-2T with BamHⅠ and EcoRⅠ digestion
, http://www.100md.com
Fig 3 Analysis of recombinant plasmids
3.4 新型降钙素的表达与鉴定
基因工程菌nCT/pGEX-2T/BL21经IPTG诱导表达后,用SDS-PAGE电泳分析可见Mr约31000加深条带。它比pGEX-2T/BL21的表达产物主带Mr28000大约3000,表明GST(谷胱甘肽转移酶)后融合了新型降钙素(见图4)。凝胶扫描显示表达产物占细胞内总蛋白的34%。表达的融合蛋白经Western-Blotting分析证明融合蛋白中含有新型降钙素(见图5)。
1.Standard protein marker
2.pGEX-2T/BL21 (GST)
, http://www.100md.com
3.nCT/pGEX-2T/BL21 (GST+nCT)
4.Host strain BL21
Fig 4 SDS-PAGE result of expression proteins

1.Standard Protein Marker
2.GST-nCT expressed in nCT/pGEX-2T/BL21
3.GST expressed in pGEX-2T/BL21
Fig 5 Western-bloting of fusion protein containing nCT.
, 百拇医药
4 讨 论
用基因工程法制备新型降钙素,在基因设计时选用大肠杆菌偏爱的密码子,这将有助于真核基因在大肠杆菌中的高效表达。另外,根据密码子简并性,在结构基因的中部有意设计了一个限制性酶切位点(KpnⅠ),这将为后续的基因操作带来方便。在基因合成中采用了化学和酶法相结合的技术可以节省基因化学合成的成本[8],我们合成了两条72碱基的长寡核苷酸链,以制备dsDNA.但从实验结果看,所合成的寡核苷酸链不宜太长,长链的合成将容易产生缺失碱基的现象。在所测序的十几个重组质粒中,无论是手工测序或自动测序均未发现完全正确的基因序列。由于在基因中设计了KpnⅠ酶切位点,所以采用剪切和拼接法获得完全正确的基因。这比利用点突点或其它方法修正基因更为方便。
本研究中Western-blotting分析时,采用了兔抗人降钙素的抗体检测融合蛋白中的新型降钙素。检测的显色反应非常灵敏,表明新型降钙素分子与人的降钙素分子的抗原性很相似。这是由于新型降钙素分子中绝大数肽段与人降钙素的相同,符合多克隆抗体与抗原的三大类型反应:抗体与部分变性蛋白或完整蛋白某一部分肽段的反应;抗体与抗原的天然特异性表位起反应;抗体与变性蛋白起反应。有关新型降钙素的分离纯化及活性测定将另文发表。
, 百拇医药
国家科技部生命科学技术中心博士基金资助项目(95-B-11)
参考文献
1 Wolfe HJ. Calcitonin:Perspectives in current concepts. J Endo In v,1982,5(3)∶423
2 刘忠厚.骨质疏松症.北京:化学工业出版社,1992.113
3 龚岳亭.生物活性肽.上海:上海科技出版社,1985.252
4 李伯良,胡明,杨新颖.人胰岛素生长因子Ⅰ基因的人工合成、克隆及其表达.生物化学与生物物理学报,1994,26(2)∶153
5 萨姆布鲁克J,弗里奇E F,曼尼阿蒂斯T著.分子克隆实验指南.金冬雁,黎孟枫译.第2版.北京:科学出版社,1993. 19
, http://www.100md.com
6 Smith D B ,Johnson K S. Single step purification of polypeptides expressed in Escherichia coli as fusions with glutathione S-transferase.Gene,1988,67(1)∶31
7 Ray M V L, Duyne P V, Bertelsen A H, et al. Production of Recombinant Salmon C alatonin by In vitro Amidation of an Escherichia coli produced precursor peptide.Bio/Technology, 1993,11(1)∶64
8 Ivanov I,Tam J, Wishart P. Chemical synthesis and expression of the human calcitonin gene. Gene, 1987,59(2)∶223
收稿日期:1998-11-26, http://www.100md.com
单位:中国药科大学生物制药学院,南京210009
关键词:降钙素;新型降钙素;基因工程;融合表达
药物生物技术990301
摘 要 借助计算机辅助设计了一种新的人降钙素类似物(新型降钙素)。根据密码子偏爱性原理及基因工程操作原则设计了它的基因,运用化学法和酶法相结合的技术合成了该基因,并克隆到质粒pUC19中,DNA测序验证正确。该基因被克隆到融合型表达载体pGEX-2T中,重组融合型表达载体nCT/pGEX-2T转化E.coliBL21,培养表达,SDS-PAGE分析可见Mr约31000的融合蛋白带,融合蛋白占细胞内总蛋白的34%。Western Blotting分析证明该新型降钙素获得表达。
, 百拇医药
Chemical Synthesis,Cloning and Expression of
the Gene for Novel Human Calcitonin Analogue
Zhang Yubin,Wu Tao, Wang Min,Wu Wutong,Zheng Heng,Zhang Zhaolin,Liu Xiaojun
(College of Biopharmaceutics,China Pharmaceutical University,Nanjing 210009)
Abstract The novel hCT analogue was designed by Computer Aid D esign Technology (CAD). The novel calcitonin gene(126bp)was synthesized by the combination of c hemical synthesis and Klenow polymerase extension. The synthetic gene was ins er ted into fusion expression vector pGEX-2T with BamHⅠ/EcoRⅠ sites. This plas mid w as transformed into E.coli BL21 strain. The major band of about 31000 fusion prot ein could be detected by SDS-PAGE analysis and the fusion protein is more than 34% of total cellular protein.The novel hCT analogue was confirmed by Western B lotting analysis.
, 百拇医药
Key Words Calcitonin ,Human calcitonin analogue,Genetic enginee rring,Fusion expression
降钙素是由32个氨基酸残基组成的多肽类激素,它在体内起着钙-磷代谢调节的功能,已被用于治疗骨质疏松症、高血钙症及Paget′s症等[1]。临床主要使用的是鲑鱼降钙素,长期使用约有40%~70%的患者出现抗体相关的耐受性,限制了它的长期使用[2]。而人的降钙素活性又很低,仅为鲑鱼的2%~5%,其半衰期也较短[3]。因此,很有必要研究开发一种活性高、半衰期长、抗原性低的人降钙素类似物。
我们对各种来源的降钙素进行分析比较,结合最新研究成果,提出了增加降钙素C-末端的亲水性可提高降钙素与其受体亲和力及提高人降钙素的等电点将有助于延长降钙素半衰期的设想。据此,我们借助计算机辅助设计了一种新的人降钙素类似物(简称新型降钙素,novelhumancalcitoninanalogue,nCT)。计算机分析表明它的C-末端亲水性增加,等电点提高(pI8.7),抗原性图谱与人的降钙素相同,满足了设计要求。运用基因工程技术中融合蛋白表达法制备了该新型降钙素,大鼠体内降血钙试验表明它具有显著的降血钙作用。
, 百拇医药
1 材 料
1.1 质粒及菌株
pUC19,pGEX-2T,E.coliJM105,E.coliBL21均为瑞典Pharmacia公司产品,1.2 酶及化学试剂
BamHⅠ,EcoRⅠ,T4-DNA连接酶,Klenow酶,X-gal,IPTG均为美国Promega公司产品。兔抗人降钙素抗体和ABC免疫组化检测试剂盒购自华美生物工程公司.其余常用试剂均为进口或国产分析纯。
1.3 仪器
DNA合成仪Oligo1000型 美国Beckman公司。373A型DNA测序仪 美国ABI公司。CS-930型薄层扫描仪 日本岛津公司。NovaBlot电转移仪 瑞典Pharmacia公司。
, http://www.100md.com 2 方 法
2.1 新型降钙素的分子设计
以人和鲑鱼的降钙素为先导化合物,设计了大量人降钙素的类似物。借助于计算机辅助设计技术,将设计的各种人降钙素类似物用蛋白质分析软件分析预测其新分子的C-末端亲水性,等电点(pI)和抗原性等参数,选择符合设计要求的类似物作为新型降钙素。
2.2 新型降钙素的基因设计与合成
根据设计的新型降钙素的氨基酸序列和基因工程操作原理,选用大肠杆菌偏爱的密码子设计出它的基因DNA序列,委托中科院北微所基因合成中心应用BeckmanOligo1000DNA合成仪合成该基因的两条部分单链A72和B72。取上述人工合成并纯化的单链DNA片段A72和B72各80pmol,在终体积80μl的退火缓冲液中混匀,置90℃水浴5min后,缓慢冷却至室温,加入5mol/LNaCl至终浓度为300mmol/L和3倍体积乙醇,-20℃放置过夜,离心去上清,抽干除净残留乙醇。沉淀的DNA溶解于Klenow酶反应的1×缓冲液中,内含有dNTPs(终浓度各0.5mmol/L)和5U的Klenow酶,终体积25μl,37℃反应1h,乙醇沉淀后获得双链DNA片段(126bp)[4]。
, 百拇医药
2.3 融合表达载体的构建
合成的双链DNA用EcoRⅠ和BamHⅠ双酶切后,克隆到pUC19/EcoRⅠ、BamHⅠ载体中,其操作按分子克隆手册中的实验方法稍加修改进行[5]。阳性重组质粒经质粒大小比较、酶切鉴定和DNA测序验证,其中DNA测序委托中科院上海植生所采用ABI373A型DNA测序仪测定。经测序验证正确的质粒按分子克隆方法经酶切、PAGE电泳后“压碎浸泡”法回收新型降钙素基因,并克隆到融合表达载体pGEX-2T/EcoRⅠ、BamHⅠ中[6,7],转化E.coliBL21,挑选阳性重组质粒,并进行质粒大小比较和酶切鉴定。
2.4 融合蛋白的表达与鉴定
重组菌在2×YT培养基中37℃恒温振荡培养至A600nm=0.6,加入IPTG至终浓度0.1mmol/L,继续培养4h。离心收集菌体,进行15%SDS-PAGE分析,拍照记录和双波长扫描分析。
, http://www.100md.com
2.5 Western-blotting分析
将电泳后的SDS-PAGE胶与硝酸纤维素膜分别在电转移液中浸泡5min,安装好电转移装置,于0.8mA/cm2电转移1h。将膜取下,经封闭、洗涤后,加入兔抗hCT的抗体,4℃放置过夜。洗涤后加入生物素化二抗(羊抗兔IgG),37℃保温30min,洗涤后加入ABC工作液(Avidin-Biotin-PeroxidaseComplex),37℃保温30min,洗涤后,加新鲜配制的底物溶液(4-氯-1-萘酚),显色完成后,洗涤,拍照记录。
3 结 果
3.1 新型降钙素的结构和基因设计
借助计算机辅助设计,通过大量的分析计算发现了一种新的人降钙素类似物符合设计要求,其分子结构如图1所示。它的C-末端亲水性增加,等电点提高(pI8.7),抗原性图谱与人的降钙素相同。根据密码子偏爱性原理及基因工程操作原则,设计了该新型降钙素基因(见图1)。N-端添加Met密码ATG是为了用溴化氰将新型降钙素前体从融合蛋白中释放出来而设计的。C-末端Pro后添加Arg密码子CGT是为了新型降钙素的C-末端酰胺化而设计的。5′和3′-端BamHⅠ和EcoRⅠ酶切位点是为了将基因克隆到载体中而添加的,另外还增添了保护碱基。

, http://www.100md.com
Fig 1 Sequence of nCT gene and its encoding amino acids
3.2 基因的合成与克隆
根据基因结构人工合成两条72碱基的DNA单链(A72和B72),其寡核苷酸序列为A72:5′-CGC GGA TCC ATG TGC GGT AAC CTG TCT ACC TGC GTT CTG GGT ACC TAC ACC CAG G A C TTC AAC AAA TTC CAC-3′ B72:5′-CCG GAA TTC TCA TTA ACG CGG AGC ACC AAC A CC GAT AGC GGT GCG CGG GAA GGT GTG GAA TTT GTT GAA GTC-3′通过两条链中间18个互补碱基的配对,使两条链退火,再利用Klenow酶补平,获得双链DNA,并经EcoRⅠ和BamHⅠ双酶切后插入到pUC19中,于含有X-gal的LB平板上挑选阳性转化菌落,经酶切鉴定及DNA测序验证得到含正确基因的重组质粒,并命名为nCT/pUC19。重组质粒中外源基因DNA测序结果正确(见图2)。


, http://www.100md.com
Fig 2 DNA Sequence of the recombinant plasmid nCT/pUC19
3.3 融合表达载体的构建
将nCT/pUC19质粒中的nCT基因用EcoRⅠ、BamHⅠ酶切后,克隆到pGEX-2T/EcoRⅠ、BamHⅠ载体中,阳性重组质粒经电泳大小比较及酶切鉴定证明新型降钙素基因插入到融合型表达载体中(见图3)。该重组载体命名为nCT/pGEX-2T。将重组融合表达载体转化E.coliBL21,其工程菌命名为nCT/pGEX-2T/BL21.


(a) Agarose electrophoresis of plasmids
, 百拇医药
1,6.λDNA/HindⅢ 2.nCT/pUC19
3.pUC19 4.nCT/pGEX-2T 5.pGEX -2T


(b) Restriction endonuclease analysis of recombinant plasmids by PAGE
1.DNA Marker pGEM-3Zf(+)/HaeⅢ 2.Synthetic nCT dsDNA
3.nCT/pUC19 with BamHⅠ and EcoRⅠ digestion
4.nCT/pGEX-2T with BamHⅠ and EcoRⅠ digestion
, http://www.100md.com
Fig 3 Analysis of recombinant plasmids
3.4 新型降钙素的表达与鉴定
基因工程菌nCT/pGEX-2T/BL21经IPTG诱导表达后,用SDS-PAGE电泳分析可见Mr约31000加深条带。它比pGEX-2T/BL21的表达产物主带Mr28000大约3000,表明GST(谷胱甘肽转移酶)后融合了新型降钙素(见图4)。凝胶扫描显示表达产物占细胞内总蛋白的34%。表达的融合蛋白经Western-Blotting分析证明融合蛋白中含有新型降钙素(见图5)。

1.Standard protein marker
2.pGEX-2T/BL21 (GST)
, http://www.100md.com
3.nCT/pGEX-2T/BL21 (GST+nCT)
4.Host strain BL21
Fig 4 SDS-PAGE result of expression proteins


1.Standard Protein Marker
2.GST-nCT expressed in nCT/pGEX-2T/BL21
3.GST expressed in pGEX-2T/BL21
Fig 5 Western-bloting of fusion protein containing nCT.
, 百拇医药
4 讨 论
用基因工程法制备新型降钙素,在基因设计时选用大肠杆菌偏爱的密码子,这将有助于真核基因在大肠杆菌中的高效表达。另外,根据密码子简并性,在结构基因的中部有意设计了一个限制性酶切位点(KpnⅠ),这将为后续的基因操作带来方便。在基因合成中采用了化学和酶法相结合的技术可以节省基因化学合成的成本[8],我们合成了两条72碱基的长寡核苷酸链,以制备dsDNA.但从实验结果看,所合成的寡核苷酸链不宜太长,长链的合成将容易产生缺失碱基的现象。在所测序的十几个重组质粒中,无论是手工测序或自动测序均未发现完全正确的基因序列。由于在基因中设计了KpnⅠ酶切位点,所以采用剪切和拼接法获得完全正确的基因。这比利用点突点或其它方法修正基因更为方便。
本研究中Western-blotting分析时,采用了兔抗人降钙素的抗体检测融合蛋白中的新型降钙素。检测的显色反应非常灵敏,表明新型降钙素分子与人的降钙素分子的抗原性很相似。这是由于新型降钙素分子中绝大数肽段与人降钙素的相同,符合多克隆抗体与抗原的三大类型反应:抗体与部分变性蛋白或完整蛋白某一部分肽段的反应;抗体与抗原的天然特异性表位起反应;抗体与变性蛋白起反应。有关新型降钙素的分离纯化及活性测定将另文发表。
, 百拇医药
国家科技部生命科学技术中心博士基金资助项目(95-B-11)
参考文献
1 Wolfe HJ. Calcitonin:Perspectives in current concepts. J Endo In v,1982,5(3)∶423
2 刘忠厚.骨质疏松症.北京:化学工业出版社,1992.113
3 龚岳亭.生物活性肽.上海:上海科技出版社,1985.252
4 李伯良,胡明,杨新颖.人胰岛素生长因子Ⅰ基因的人工合成、克隆及其表达.生物化学与生物物理学报,1994,26(2)∶153
5 萨姆布鲁克J,弗里奇E F,曼尼阿蒂斯T著.分子克隆实验指南.金冬雁,黎孟枫译.第2版.北京:科学出版社,1993. 19
, http://www.100md.com
6 Smith D B ,Johnson K S. Single step purification of polypeptides expressed in Escherichia coli as fusions with glutathione S-transferase.Gene,1988,67(1)∶31
7 Ray M V L, Duyne P V, Bertelsen A H, et al. Production of Recombinant Salmon C alatonin by In vitro Amidation of an Escherichia coli produced precursor peptide.Bio/Technology, 1993,11(1)∶64
8 Ivanov I,Tam J, Wishart P. Chemical synthesis and expression of the human calcitonin gene. Gene, 1987,59(2)∶223
收稿日期:1998-11-26, http://www.100md.com