�������ɶ�HUVEC����ճ�����ӵ�Ӱ��*
���ߣ�������1 ��ά��1 ���2 �� ΰ1p|@r&, ��Ĵҽҩ
��λ�������� ��ά�� �� ΰ ɽ��ҽ�ƴ�ѧ����ҽԺ����� ���� 240012�� ��� ɽ��ҽ�ƴ�ѧ����ҽѧԺ��ҽѧ������p|@r&, ��Ĵҽҩ
�ؼ��ʣ��������� ���꾲����Ƥϸ��(HUVEC) ϸ������ ճ������p|@r&, ��Ĵҽҩ
����ѧ��־990111 ժ Ҫ �о��������ɡ�rIL-1ra����Ƥϸ������ճ�����ӵ�Ӱ�죬Ϊ��֢��Ӧ�IJ��������ṩ������������rTNF����rIL-1��LPS�յ����������꾲����Ƥϸ��(HUVEC)���Ե������ɻ�rIL-1ra����LPS��rIL-1�յ���HUVEC������Cell-ELISA�����ճ������ICMA-1��ELAM-1�ı�������rTNF����rIL-1��LPS���HUVEC����ICAM-1��ELAM-1���������ɡ�rIL-1ra����rIL-1�յ���ճ�����ӱ�������������ɡ�rIL-1ra�Բ�ͬ��������HUVEC����ICAM-1��ELAM-1��p|@r&, ��Ĵҽҩ
��ͼ�� R392.11p|@r&, ��Ĵҽҩ
EFFECTS OF DEXAMETHASONE ON EXPRESSION OF ADHESION MOLECULES BY ACTIVATED HUVECp|@r&, ��Ĵҽҩ
Zhang Qingyin��He Weijing��Hou Guihua��Liweip|@r&, ��Ĵҽҩ
(Affiliated Hospital of Shandong Medical University��Jinan 250012)p|@r&, ��Ĵҽҩ
Abstract In order to study the effects of Dexamethasone and rIL-1ra on the expression of adhesion molecules by activated endothelial cells��and to provide evidence for pathologic course of inflammatory reaction.Cell-ELISA method was used to detect ICAM-1 and ELAM-1 expression on human umbilical vein cells(HUVEC) stimulated with rTNF����IL-1 and LPS.The results showed rTNF����rIL-1 and LPS could induce the expression of ICAM-1 and ELAM-1 on HUVEC��whereas dexamethasone and rIL-1ra inhibited HUVEC to express ICAM-1 and ELAM-1 on HUVEC induced with rIL-1.The findings indicate that Dexamethasone and rIL-1ra might inhibit the expression of adhesion molecule ICAM-1 and ELAM-1 by different mechanism respectively
Key words Dexamethasone��Human umbilical vein endothelial cells(HUVEC)��Cytokine��Adhesion molecules3+j, ��Ĵҽҩ
��֢��Ӧ�����У���Ƥϸ���ȿ�����Ϊϸ�����ӡ������������õİ�ϸ�����ֿɷ���ϸ�����ӡ��鵼ϸ��ճ����������ϸ�����ܰ�ϸ����Խ��Ƥ������֢��λɱ��������Ƥϸ������ճ�������й�[1]��ϸ����ճ������-1(Intercellular adhesion molecule-1��ICAM-1)����Ƥϸ����ϸ��ճ������(Endothelial leukocyte adhesion molecule-1��ELAM-1)�����ڻ��Ѫ����Ƥϸ��Ĥ�ϱ��ijЩ�о������������ϸ����ͨ��������������ICAM-1��VCAM-1����ã�ճ����Ѫ����Ƥϸ���ı���[2]�����о�����Cell-ELISA�������ճ�����ӵı��̽����Ƥϸ��ճ�����ӵı����Ӱ�����ء�3+j, ��Ĵҽҩ
1 ���Ϻͷ���3+j, ��Ĵҽҩ
1.1 ����3+j, ��Ĵҽҩ
1.1.1 ����걾��������������������ȡ������������걾ȡ��ɽ��ҽ�ƴ�ѧ����ҽԺ��������3+j, ��Ĵҽҩ
1.1.2 �Լ���������RPMI1640����Һ��GIBCO��˾��Ʒ���ں���ù��100 U/ml����ù��100��g/ml��ʹ��ʱ����20%����ţѪ�塣�ȵ���ø��Sigma��˾��Ʒ����RPMI1640����Һ���0.25%Ũ�ȣ�rIL-1��10��U/ml��rTNF �� 5��U/ml�����ڱ��������ҽѧ��˾��Anti-ICAM-1��1.2mg/ml��Anti-ELAM-1��1.8mg/ml��British Biotechnology(Oxford UK)��Ʒ����ΪС��IgG1��rIL-1ra 650 ��g/ml������ҽ�ƴ�ѧ����ѧ���������������ڻ�������������5mg/ml������������ҩ��˾��LPS��5mg/ml��ΪSigma��˾��Ʒ��3+j, ��Ĵҽҩ
1.2 ����3+j, ��Ĵҽҩ
1.2.1 HUVECԭ������������������12h�ڵ��������pH7.2��PBS��ϴ�侲����������ɫΪֹ��Ȼ��ע��0.25%�ȵ���ø����37��Cˮԡ15��18min���ռ��꾲��������Һ������20%FCS��RPMI 1640����Һ��ϴ�����ĺ������壬��20%FCS��RPMI1640�Ƴ�ϸ����Һ������ϸ���ܶȷ�����1%����Ԥ������96�װ��ϣ���37��C 5%CO2���������������γ����ܵ����ȥ���������壬��ϴ���HUVEC��������ICAM-1��ELAM-1�������顣
1.2.2 ճ������ICAM-���ELAM-1������յ����ں���HUVEC�����96�װ��ڣ��ֱ����rTNF�� 500U/ml��rIL-1 100 U/ml��LPS 1 ��g/ml�յ�6h����ICAM-1��ELAM-1�ı������rTNF�� 500U/ml��rIL-1 100U/ml��LPS 1��g/ml�ֱ�͵�������100 nMͬʱ����HUVEC 6h���Ӳ�ͬŨ�ȵĵ���������1 ��g/ml LPS�յ�HUVEC 6h��rIL-1(1��g/ml)��rIL-1(1 ��g/ml)+��������(10nM)�յ�HUVEC 6h����ICAM-1��ELAM-1���rIL-1ra�������HUVEC��Ȼ����rIL-1�յ���.f, ��Ĵҽҩ
1.2.3 ICAM-1��ELAM-1��ԭ�ļ��[3]��ϸ���������ú��HUVEC���㣬��pH7.2��PBS��ϴ���飬��1%���ȩ4��C�̶�30min���ú�0.05% Tween 20��PBSϴ��3�Σ���3%BSA���40min��200 ��l/�ף�ϴ����������ICAM-1(0.4��g/ml)��ELAM-1(0.6��g/ml)������50��l/�ף�37��C��1h��ϴ��3�κ��HRP��ǵ�����IgG 100 ��l/�ף�37��C 1h��Ԥ�½�����TBM-H2O2 100 ��l��37��C��ɫ15min����2N H2SO4��ֹ��Ӧ��450nm����ȡ���ܶ�ֵ��ʵ��ⶨOD450���̼���OD450-������OD450��ICAM-1��ELAM-1���������й�ʽ���㣺 .f, ��Ĵҽҩ
.f, ��Ĵҽҩ
1.2.4 ͳ��ѧ����������t����.f, ��Ĵҽҩ
2 ���.f, ��Ĵҽҩ
2.1 rTNF ����rIL-1��LPS��HUVE����ICAM-1��ELAM-1��Ӱ�� ѡ��rTNF �� 500U/ml��rIL-1 100U/ml��LPS 1 ��g/ml�յ�HUVEC����6h����ICAM-1��ELAM-1�ı�������ʾ��3���յ����Ӿ��������յ�2��ճ�����ӵı�����Ը���δ�̼���HUVEC(P<0.05)������ճ�����ӵı���֮��δ�����Բ���(P>0.05)����ͼ1��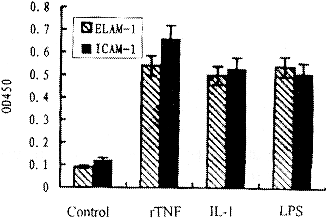 .f, ��Ĵҽҩ
.f, ��Ĵҽҩ
ͼ1 rTNF����rIL-1��LPS��HUVEC����ICAM-1��ELAM-1��Ӱ��(n��8)
Fig 1 Effects of rTNF����rIL-1 and LPS on expression of ICAM-1 and ELAM-1 by HUVEC(n��8)jh9u, ��Ĵҽҩ
2.2 �������ɶ�rTNF����rIL-1��LPS�յ���HVUEC����ELAM-1��Ӱ�� ����rTNF�� 500U/ml��rIL-1 100U/ml��LPS1��g/ml���ֱ�͵�������100 nMͬʱ����HUVEC6h���̼������յ���ELAM-1�����ٷֶ��ձ���İٷ��ʱ�ʾ����ͼ2�������ʾ������������������rIL-1��LPS�յ���ELAM-1���100 nM�ĵ������ɿ�ʹrIL-1�յ���ELAM-1�����½�60%��ʹLPS�յ���ELAM-1���オ69%������rTNF���յ���ELAM-1������Ӱ�졣 jh9u, ��Ĵҽҩ
jh9u, ��Ĵҽҩ
ͼ2 �������ɶ�rTNF����rIL-1��LPS�յ�ELAM-1�����Ӱ��(n��8)jh9u, ��Ĵҽҩ
Fig 2 Effects of Dexamethasone on ELAM-1 expression induced by rTNF����rIL-1 and LPS(n��8)jh9u, ��Ĵҽҩ
2.3 ������������ICAM-1��ELAM-1����ļ�������ЧӦ ��ͬ�����ĵ������ɣ���1��g/ml LPS�յ���HUVEC����ICAM-1��ELAM-1���ӣ����ֲ�ͬ���������ã�0.1nM�ĵ������ɼ��ɱ������Ե��������ã���Ũ��������10 nMʱ������ЧӦ�����ֵ����ͼ3��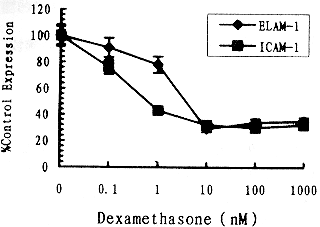 jh9u, ��Ĵҽҩ
jh9u, ��Ĵҽҩ
ͼ3 �������ɶ�LPS�յ���ICAM-1��ELAM-1����ļ�����������ЧӦ(n��5)jh9u, ��Ĵҽҩ
Fig 3 Dose-dependent inhibitory effects of Dexamethasone on expression of ICAM-1 and ELAM-1 induced by LPS(n��5)jh9u, ��Ĵҽҩ
2.4 �������ɶ�rIL-1�յ���ICAM-1��ELAM-1������������� rIL-1(1��g/ml)��rIL-1(1��g/ml)+��������(10 nM)�յ�HUVEC����ICAM-1��ELAM-1��������ʾ��rIL-1��rIL-1+�������ɴ������ICAM-1��ELAM-1�������Ը��ڵ��õ������ɺ�δ�յ���(P<0.05)��rIL-1��rIL-1+�������ɴ������ICAM-1��ELAM-1����������Բ���(P<0.05)����ͼ4��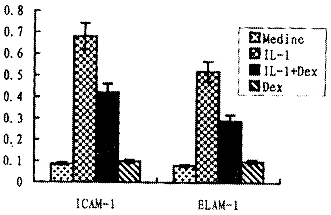
ͼ4 �������ɶ�rIL-1�յ�ICAM-1��ELAM-1�������������(n��8)+?/, http://www.100md.com
Fig 4 Inhibitory effects of Dexamethasone on the expression of ICAM-1 and ELAM-1(n��8)+?/, http://www.100md.com
2.5 rIL-1 ra��rIL-1�յ���HUVEC����ELAM-1���������� ��ͬŨ�ȵ�rIL-1ra����HUVECԤ����10min��Ȼ���ټ�rIL-1 100U/ml��6h���ELAM-1�ı��ʵ�����10ng/ml��100ng/ml��rIL-1ra��������ELAM-1�ı��1 000ng/mlʱ��������Ե�����ЧӦ����rIL-1raŨ������10 000ng/mlʱ��ELAM-1�ı��オ��56%��LPS�յ���ELAM-1�ı������ܱ�rIL-1ra����,����1��+?/, http://www.100md.com
��1 rIL-1ra��rIL-1�յ�HUVEC����ELAM-1����������+?/, http://www.100md.com
Tab 1 Inhibitory effect of rIL-1ra on ELAM-1 expression by HUVEC induced with rIL-1 rIL-1ra concentration+?/, http://www.100md.com
(��103 ng/ml)+?/, http://www.100md.com
% control expression��s+?/, http://www.100md.com
rIL-1(100U/ml)+?/, http://www.100md.com
LPS(1��g/ml)+?/, http://www.100md.com
0.01+?/, http://www.100md.com
102��2.8*+?/, http://www.100md.com
96��5.6+?/, http://www.100md.com
0.1+?/, http://www.100md.com
105��7.1*+?/, http://www.100md.com
106��3.9+?/, http://www.100md.com
1.0
85��5.5**|/0, http://www.100md.com
102��8.1|/0, http://www.100md.com
10.0|/0, http://www.100md.com
56��8.1**|/0, http://www.100md.com
98��11.7|/0, http://www.100md.com
100.0|/0, http://www.100md.com
54��3.4**|/0, http://www.100md.com
102��6.4|/0, http://www.100md.com
*P>0.05�� ����**P<0.01 compared with LPS|/0, http://www.100md.com
3 ����|/0, http://www.100md.com
����֢��֯�У���ϸ����Ѫ����Ƥϸ������ճ���ǰ�ϸ����Ѫ���ڿ��ߺ�������Ѫ�ܱ����ǰ�ᣬҲ��������ϸ������Ѫ����Ƥ�Ļ���������֢�����а�ϸ��ճ����Խ��Ƥ������ճ�����ӵı����йأ��ڼ�����֢��Ӧ�����ڣ���Ƥϸ������ELAM-1���ӣ����Ժ�������ϸ�����ܰ�ϸ���Լ�����ϸ������������������ϣ�����Ƥϸ��ICAM-1�����������Ҫ�鵼������ϸ��������ϸ����ճ��[1]��|/0, http://www.100md.com
��Ƥϸ��ճ�������ڰ�ϸ��Ǩ�ƹ����е�����Ҳ�в��죬ELAM-1�ڰ�ϸ����Ѫ����Ƥ��ճ��ʱ����Ҫ���ã�ICAM-1���ϸ�������CD11/CD18�����ϱ�����ʼ���λ�㡣����ϸ����������ϸ�������P-selectin��ELAM-1��ϣ���Ҫ�鵼��Щϸ������Ƥϸ�����������Ȼ���ϸ�����������ӵļ�����ICAM-1����ǿճ������һ���ٽ���ϸ����Խ��Ƥ[2]��|/0, http://www.100md.com
��Ƥ����̴���һ��Ӧ�ù㷺����Ч�Ŀ���ҩ��俹������δ��ȫ���ˡ����б����������ɿɼ���ǰ��֢ϸ�����ӵĺϳ�[5]�����Ƽ��Ժ�������֢��Ӧ�а�ϸ������Ƥϸ����ճ��[6]��������ϸ�����Ӽ����ճ������mRNA����ת¼[7]�����ǶԵ������ɵ���HUVECճ������ICAM-1��ELAM-1���������о�����������������ɿ���������rIL-1��LPS�յ���ICAM-1��ELAM-1�ı����ˣ������������ư�ϸ��������֢��λ������ͨ��������Ƥϸ��ճ�����ӵı�������á�
IL-1ra���ھ����Խ��HUVEC�����IL-1���壬�����IL-1������ѧЧӦ��������IL-1raԤ����HUVEC��rIL-1�յ���ELAM-1����ɱ����ơ�����ʵ��֤��IL-1ra���п���ЧӦ[8]��[k*5[, ��Ĵҽҩ
*ɽ��ʡ��Ȼ��ѧ����������ѧ����������Ŀ(��Ŀ�ţ�Q94C0717)[k*5[, ��Ĵҽҩ
��һ���ߣ��У�33�꣬˶ʿ������ҽʦ[k*5[, ��Ĵҽҩ
�ο�����[k*5[, ��Ĵҽҩ
[1] Pober TS�� Cotran R.Cytokine and endothelial cell Biology.Physiol Review��1990��70��427[k*5[, ��Ĵҽҩ
[2] Oppenheimer-marks N��Davis LS��Bogue DT��et al.Differential utilization of ICAM-1 and VCAM-1 during the adhesion and transendothelial migration of human T lymphocytes��1991��147��2913[k*5[, ��Ĵҽҩ
[3] Vanhee D��Delneste Y��Lassalle P��et al.Madulation of endothelial cell adhesion molecule expression in a situation of chronic inflammatory stimulation.Cell Immunol��1994��155��446[k*5[, ��Ĵҽҩ
[4] Frank Bennett C��Condon TP��Grimm S��et al.Inhibition of endothelial cell adhesion molecule expression with antisense oligonucleotides.J Immunol��1994��152��3530[k*5[, ��Ĵҽҩ
[5] Kern JA��Lamb RJ��Reed JC��et al.Dexamethasone inhibition of interleukin-1(production by human monocyte postranscriptional mechanisms.J Clin Invest��1988��81��237[k*5[, ��Ĵҽҩ
[6] Bevilacqua MP.Endothelial-leukocyte adhesion mole-cules.Annu Rev Immunol��1993��11��767[k*5[, ��Ĵҽҩ
[7] Cronstein BN��Kimmel SC��levin RI��et al��A mechanism for the antiinflammatory effectory of corticosteroids��The glucocorticoid receptor regulates leukocyte adhesion to endothelial cells and expression of endothelial-leukocyte adhesion molecule-1 and intercellular adhesion molecule 1.Proc Natl Acad Sci USA��1992��89��9991[k*5[, ��Ĵҽҩ
[8] Conti P��Panara MR��Fridas S��et al.Inhibition of granuloma formation induced by potassium permanganate in the mouse by a specific human recombinant receptor antagonist for interleukin-1(hrIL-1ra).Cell Immunol��1993��147��446[k*5[, ��Ĵҽҩ
(1998-02-16�ո壻1998-07-13��)(������1 ��ά��1 ���2 �� ΰ1)
��λ�������� ��ά�� �� ΰ ɽ��ҽ�ƴ�ѧ����ҽԺ����� ���� 240012�� ��� ɽ��ҽ�ƴ�ѧ����ҽѧԺ��ҽѧ������p|@r&, ��Ĵҽҩ
�ؼ��ʣ��������� ���꾲����Ƥϸ��(HUVEC) ϸ������ ճ������p|@r&, ��Ĵҽҩ
����ѧ��־990111 ժ Ҫ �о��������ɡ�rIL-1ra����Ƥϸ������ճ�����ӵ�Ӱ�죬Ϊ��֢��Ӧ�IJ��������ṩ������������rTNF����rIL-1��LPS�յ����������꾲����Ƥϸ��(HUVEC)���Ե������ɻ�rIL-1ra����LPS��rIL-1�յ���HUVEC������Cell-ELISA�����ճ������ICMA-1��ELAM-1�ı�������rTNF����rIL-1��LPS���HUVEC����ICAM-1��ELAM-1���������ɡ�rIL-1ra����rIL-1�յ���ճ�����ӱ�������������ɡ�rIL-1ra�Բ�ͬ��������HUVEC����ICAM-1��ELAM-1��p|@r&, ��Ĵҽҩ
��ͼ�� R392.11p|@r&, ��Ĵҽҩ
EFFECTS OF DEXAMETHASONE ON EXPRESSION OF ADHESION MOLECULES BY ACTIVATED HUVECp|@r&, ��Ĵҽҩ
Zhang Qingyin��He Weijing��Hou Guihua��Liweip|@r&, ��Ĵҽҩ
(Affiliated Hospital of Shandong Medical University��Jinan 250012)p|@r&, ��Ĵҽҩ
Abstract In order to study the effects of Dexamethasone and rIL-1ra on the expression of adhesion molecules by activated endothelial cells��and to provide evidence for pathologic course of inflammatory reaction.Cell-ELISA method was used to detect ICAM-1 and ELAM-1 expression on human umbilical vein cells(HUVEC) stimulated with rTNF����IL-1 and LPS.The results showed rTNF����rIL-1 and LPS could induce the expression of ICAM-1 and ELAM-1 on HUVEC��whereas dexamethasone and rIL-1ra inhibited HUVEC to express ICAM-1 and ELAM-1 on HUVEC induced with rIL-1.The findings indicate that Dexamethasone and rIL-1ra might inhibit the expression of adhesion molecule ICAM-1 and ELAM-1 by different mechanism respectively
Key words Dexamethasone��Human umbilical vein endothelial cells(HUVEC)��Cytokine��Adhesion molecules3+j, ��Ĵҽҩ
��֢��Ӧ�����У���Ƥϸ���ȿ�����Ϊϸ�����ӡ������������õİ�ϸ�����ֿɷ���ϸ�����ӡ��鵼ϸ��ճ����������ϸ�����ܰ�ϸ����Խ��Ƥ������֢��λɱ��������Ƥϸ������ճ�������й�[1]��ϸ����ճ������-1(Intercellular adhesion molecule-1��ICAM-1)����Ƥϸ����ϸ��ճ������(Endothelial leukocyte adhesion molecule-1��ELAM-1)�����ڻ��Ѫ����Ƥϸ��Ĥ�ϱ��ijЩ�о������������ϸ����ͨ��������������ICAM-1��VCAM-1����ã�ճ����Ѫ����Ƥϸ���ı���[2]�����о�����Cell-ELISA�������ճ�����ӵı��̽����Ƥϸ��ճ�����ӵı����Ӱ�����ء�3+j, ��Ĵҽҩ
1 ���Ϻͷ���3+j, ��Ĵҽҩ
1.1 ����3+j, ��Ĵҽҩ
1.1.1 ����걾��������������������ȡ������������걾ȡ��ɽ��ҽ�ƴ�ѧ����ҽԺ��������3+j, ��Ĵҽҩ
1.1.2 �Լ���������RPMI1640����Һ��GIBCO��˾��Ʒ���ں���ù��100 U/ml����ù��100��g/ml��ʹ��ʱ����20%����ţѪ�塣�ȵ���ø��Sigma��˾��Ʒ����RPMI1640����Һ���0.25%Ũ�ȣ�rIL-1��10��U/ml��rTNF �� 5��U/ml�����ڱ��������ҽѧ��˾��Anti-ICAM-1��1.2mg/ml��Anti-ELAM-1��1.8mg/ml��British Biotechnology(Oxford UK)��Ʒ����ΪС��IgG1��rIL-1ra 650 ��g/ml������ҽ�ƴ�ѧ����ѧ���������������ڻ�������������5mg/ml������������ҩ��˾��LPS��5mg/ml��ΪSigma��˾��Ʒ��3+j, ��Ĵҽҩ
1.2 ����3+j, ��Ĵҽҩ
1.2.1 HUVECԭ������������������12h�ڵ��������pH7.2��PBS��ϴ�侲����������ɫΪֹ��Ȼ��ע��0.25%�ȵ���ø����37��Cˮԡ15��18min���ռ��꾲��������Һ������20%FCS��RPMI 1640����Һ��ϴ�����ĺ������壬��20%FCS��RPMI1640�Ƴ�ϸ����Һ������ϸ���ܶȷ�����1%����Ԥ������96�װ��ϣ���37��C 5%CO2���������������γ����ܵ����ȥ���������壬��ϴ���HUVEC��������ICAM-1��ELAM-1�������顣
1.2.2 ճ������ICAM-���ELAM-1������յ����ں���HUVEC�����96�װ��ڣ��ֱ����rTNF�� 500U/ml��rIL-1 100 U/ml��LPS 1 ��g/ml�յ�6h����ICAM-1��ELAM-1�ı������rTNF�� 500U/ml��rIL-1 100U/ml��LPS 1��g/ml�ֱ�͵�������100 nMͬʱ����HUVEC 6h���Ӳ�ͬŨ�ȵĵ���������1 ��g/ml LPS�յ�HUVEC 6h��rIL-1(1��g/ml)��rIL-1(1 ��g/ml)+��������(10nM)�յ�HUVEC 6h����ICAM-1��ELAM-1���rIL-1ra�������HUVEC��Ȼ����rIL-1�յ���.f, ��Ĵҽҩ
1.2.3 ICAM-1��ELAM-1��ԭ�ļ��[3]��ϸ���������ú��HUVEC���㣬��pH7.2��PBS��ϴ���飬��1%���ȩ4��C�̶�30min���ú�0.05% Tween 20��PBSϴ��3�Σ���3%BSA���40min��200 ��l/�ף�ϴ����������ICAM-1(0.4��g/ml)��ELAM-1(0.6��g/ml)������50��l/�ף�37��C��1h��ϴ��3�κ��HRP��ǵ�����IgG 100 ��l/�ף�37��C 1h��Ԥ�½�����TBM-H2O2 100 ��l��37��C��ɫ15min����2N H2SO4��ֹ��Ӧ��450nm����ȡ���ܶ�ֵ��ʵ��ⶨOD450���̼���OD450-������OD450��ICAM-1��ELAM-1���������й�ʽ���㣺
 .f, ��Ĵҽҩ
.f, ��Ĵҽҩ1.2.4 ͳ��ѧ����������t����.f, ��Ĵҽҩ
2 ���.f, ��Ĵҽҩ
2.1 rTNF ����rIL-1��LPS��HUVE����ICAM-1��ELAM-1��Ӱ�� ѡ��rTNF �� 500U/ml��rIL-1 100U/ml��LPS 1 ��g/ml�յ�HUVEC����6h����ICAM-1��ELAM-1�ı�������ʾ��3���յ����Ӿ��������յ�2��ճ�����ӵı�����Ը���δ�̼���HUVEC(P<0.05)������ճ�����ӵı���֮��δ�����Բ���(P>0.05)����ͼ1��
 .f, ��Ĵҽҩ
.f, ��Ĵҽҩͼ1 rTNF����rIL-1��LPS��HUVEC����ICAM-1��ELAM-1��Ӱ��(n��8)
Fig 1 Effects of rTNF����rIL-1 and LPS on expression of ICAM-1 and ELAM-1 by HUVEC(n��8)jh9u, ��Ĵҽҩ
2.2 �������ɶ�rTNF����rIL-1��LPS�յ���HVUEC����ELAM-1��Ӱ�� ����rTNF�� 500U/ml��rIL-1 100U/ml��LPS1��g/ml���ֱ�͵�������100 nMͬʱ����HUVEC6h���̼������յ���ELAM-1�����ٷֶ��ձ���İٷ��ʱ�ʾ����ͼ2�������ʾ������������������rIL-1��LPS�յ���ELAM-1���100 nM�ĵ������ɿ�ʹrIL-1�յ���ELAM-1�����½�60%��ʹLPS�յ���ELAM-1���オ69%������rTNF���յ���ELAM-1������Ӱ�졣
 jh9u, ��Ĵҽҩ
jh9u, ��Ĵҽҩͼ2 �������ɶ�rTNF����rIL-1��LPS�յ�ELAM-1�����Ӱ��(n��8)jh9u, ��Ĵҽҩ
Fig 2 Effects of Dexamethasone on ELAM-1 expression induced by rTNF����rIL-1 and LPS(n��8)jh9u, ��Ĵҽҩ
2.3 ������������ICAM-1��ELAM-1����ļ�������ЧӦ ��ͬ�����ĵ������ɣ���1��g/ml LPS�յ���HUVEC����ICAM-1��ELAM-1���ӣ����ֲ�ͬ���������ã�0.1nM�ĵ������ɼ��ɱ������Ե��������ã���Ũ��������10 nMʱ������ЧӦ�����ֵ����ͼ3��
 jh9u, ��Ĵҽҩ
jh9u, ��Ĵҽҩͼ3 �������ɶ�LPS�յ���ICAM-1��ELAM-1����ļ�����������ЧӦ(n��5)jh9u, ��Ĵҽҩ
Fig 3 Dose-dependent inhibitory effects of Dexamethasone on expression of ICAM-1 and ELAM-1 induced by LPS(n��5)jh9u, ��Ĵҽҩ
2.4 �������ɶ�rIL-1�յ���ICAM-1��ELAM-1������������� rIL-1(1��g/ml)��rIL-1(1��g/ml)+��������(10 nM)�յ�HUVEC����ICAM-1��ELAM-1��������ʾ��rIL-1��rIL-1+�������ɴ������ICAM-1��ELAM-1�������Ը��ڵ��õ������ɺ�δ�յ���(P<0.05)��rIL-1��rIL-1+�������ɴ������ICAM-1��ELAM-1����������Բ���(P<0.05)����ͼ4��

ͼ4 �������ɶ�rIL-1�յ�ICAM-1��ELAM-1�������������(n��8)+?/, http://www.100md.com
Fig 4 Inhibitory effects of Dexamethasone on the expression of ICAM-1 and ELAM-1(n��8)+?/, http://www.100md.com
2.5 rIL-1 ra��rIL-1�յ���HUVEC����ELAM-1���������� ��ͬŨ�ȵ�rIL-1ra����HUVECԤ����10min��Ȼ���ټ�rIL-1 100U/ml��6h���ELAM-1�ı��ʵ�����10ng/ml��100ng/ml��rIL-1ra��������ELAM-1�ı��1 000ng/mlʱ��������Ե�����ЧӦ����rIL-1raŨ������10 000ng/mlʱ��ELAM-1�ı��オ��56%��LPS�յ���ELAM-1�ı������ܱ�rIL-1ra����,����1��+?/, http://www.100md.com
��1 rIL-1ra��rIL-1�յ�HUVEC����ELAM-1����������+?/, http://www.100md.com
Tab 1 Inhibitory effect of rIL-1ra on ELAM-1 expression by HUVEC induced with rIL-1 rIL-1ra concentration+?/, http://www.100md.com
(��103 ng/ml)+?/, http://www.100md.com
% control expression��s+?/, http://www.100md.com
rIL-1(100U/ml)+?/, http://www.100md.com
LPS(1��g/ml)+?/, http://www.100md.com
0.01+?/, http://www.100md.com
102��2.8*+?/, http://www.100md.com
96��5.6+?/, http://www.100md.com
0.1+?/, http://www.100md.com
105��7.1*+?/, http://www.100md.com
106��3.9+?/, http://www.100md.com
1.0
85��5.5**|/0, http://www.100md.com
102��8.1|/0, http://www.100md.com
10.0|/0, http://www.100md.com
56��8.1**|/0, http://www.100md.com
98��11.7|/0, http://www.100md.com
100.0|/0, http://www.100md.com
54��3.4**|/0, http://www.100md.com
102��6.4|/0, http://www.100md.com
*P>0.05�� ����**P<0.01 compared with LPS|/0, http://www.100md.com
3 ����|/0, http://www.100md.com
����֢��֯�У���ϸ����Ѫ����Ƥϸ������ճ���ǰ�ϸ����Ѫ���ڿ��ߺ�������Ѫ�ܱ����ǰ�ᣬҲ��������ϸ������Ѫ����Ƥ�Ļ���������֢�����а�ϸ��ճ����Խ��Ƥ������ճ�����ӵı����йأ��ڼ�����֢��Ӧ�����ڣ���Ƥϸ������ELAM-1���ӣ����Ժ�������ϸ�����ܰ�ϸ���Լ�����ϸ������������������ϣ�����Ƥϸ��ICAM-1�����������Ҫ�鵼������ϸ��������ϸ����ճ��[1]��|/0, http://www.100md.com
��Ƥϸ��ճ�������ڰ�ϸ��Ǩ�ƹ����е�����Ҳ�в��죬ELAM-1�ڰ�ϸ����Ѫ����Ƥ��ճ��ʱ����Ҫ���ã�ICAM-1���ϸ�������CD11/CD18�����ϱ�����ʼ���λ�㡣����ϸ����������ϸ�������P-selectin��ELAM-1��ϣ���Ҫ�鵼��Щϸ������Ƥϸ�����������Ȼ���ϸ�����������ӵļ�����ICAM-1����ǿճ������һ���ٽ���ϸ����Խ��Ƥ[2]��|/0, http://www.100md.com
��Ƥ����̴���һ��Ӧ�ù㷺����Ч�Ŀ���ҩ��俹������δ��ȫ���ˡ����б����������ɿɼ���ǰ��֢ϸ�����ӵĺϳ�[5]�����Ƽ��Ժ�������֢��Ӧ�а�ϸ������Ƥϸ����ճ��[6]��������ϸ�����Ӽ����ճ������mRNA����ת¼[7]�����ǶԵ������ɵ���HUVECճ������ICAM-1��ELAM-1���������о�����������������ɿ���������rIL-1��LPS�յ���ICAM-1��ELAM-1�ı����ˣ������������ư�ϸ��������֢��λ������ͨ��������Ƥϸ��ճ�����ӵı�������á�
IL-1ra���ھ����Խ��HUVEC�����IL-1���壬�����IL-1������ѧЧӦ��������IL-1raԤ����HUVEC��rIL-1�յ���ELAM-1����ɱ����ơ�����ʵ��֤��IL-1ra���п���ЧӦ[8]��[k*5[, ��Ĵҽҩ
*ɽ��ʡ��Ȼ��ѧ����������ѧ����������Ŀ(��Ŀ�ţ�Q94C0717)[k*5[, ��Ĵҽҩ
��һ���ߣ��У�33�꣬˶ʿ������ҽʦ[k*5[, ��Ĵҽҩ
�ο�����[k*5[, ��Ĵҽҩ
[1] Pober TS�� Cotran R.Cytokine and endothelial cell Biology.Physiol Review��1990��70��427[k*5[, ��Ĵҽҩ
[2] Oppenheimer-marks N��Davis LS��Bogue DT��et al.Differential utilization of ICAM-1 and VCAM-1 during the adhesion and transendothelial migration of human T lymphocytes��1991��147��2913[k*5[, ��Ĵҽҩ
[3] Vanhee D��Delneste Y��Lassalle P��et al.Madulation of endothelial cell adhesion molecule expression in a situation of chronic inflammatory stimulation.Cell Immunol��1994��155��446[k*5[, ��Ĵҽҩ
[4] Frank Bennett C��Condon TP��Grimm S��et al.Inhibition of endothelial cell adhesion molecule expression with antisense oligonucleotides.J Immunol��1994��152��3530[k*5[, ��Ĵҽҩ
[5] Kern JA��Lamb RJ��Reed JC��et al.Dexamethasone inhibition of interleukin-1(production by human monocyte postranscriptional mechanisms.J Clin Invest��1988��81��237[k*5[, ��Ĵҽҩ
[6] Bevilacqua MP.Endothelial-leukocyte adhesion mole-cules.Annu Rev Immunol��1993��11��767[k*5[, ��Ĵҽҩ
[7] Cronstein BN��Kimmel SC��levin RI��et al��A mechanism for the antiinflammatory effectory of corticosteroids��The glucocorticoid receptor regulates leukocyte adhesion to endothelial cells and expression of endothelial-leukocyte adhesion molecule-1 and intercellular adhesion molecule 1.Proc Natl Acad Sci USA��1992��89��9991[k*5[, ��Ĵҽҩ
[8] Conti P��Panara MR��Fridas S��et al.Inhibition of granuloma formation induced by potassium permanganate in the mouse by a specific human recombinant receptor antagonist for interleukin-1(hrIL-1ra).Cell Immunol��1993��147��446[k*5[, ��Ĵҽҩ
(1998-02-16�ո壻1998-07-13��)(������1 ��ά��1 ���2 �� ΰ1)