脑腔隙性梗塞
作者:罗 毅*
单位:1 中国人民解放军总医院, 邮政编码 北京100853
关键词:
微循环学杂志990117
编者按: 脑梗塞与脑腔隙性梗塞是近年脑血管病研究领域较为热门的研究课题。 本期讲座我们约请著名病理学专家就脑腔隙性梗塞的病理学、 病理生理学以及诊断学的研究历史与现状进行较为系统和全面的概述, 以期为广大从事与之相关研究的读者开阔思路提供参考。
脑腔隙性梗塞是常见的脑血管疾病之一。 过去由于很多脑腔隙性梗塞病人没有表现出局灶体征, 甚至完全没有症状, 临床上很难做出脑腔隙性梗塞的诊断, 只有在病理检查时, 才能明确脑腔隙性梗塞的病变。 在CT、 核磁共振出现后, 在很多没有体征的患者中, 明确显示出脑腔隙性梗塞病灶的改变, 脑腔隙性梗塞才引起人们的重视, 对它的研究逐渐增多。 但目前认识尚不一致, 一些问题有待研究。
, 百拇医药
1 何谓脑腔隙性梗塞
迄今为止, 人们对“脑腔隙性梗塞”的认识还不一致, 其内涵和外延都没有合理的界定。 笼统地说, 脑腔隙性梗塞是目前观察到的病变范围最小、 部位不一、 症状不定的一组脑小血管梗塞(或出血)。 “腔隙”一词, 源于法语“充满液体的小腔洞”[1]。 最早, Marie(1901)根据50例病理解剖观察, 描述腔隙是“组织崩溃的腔隙病灶”, “腔隙病灶的组织象是扯裂、 破坏”。 腔隙是由脑深穿动脉的动脉硬化性变化, 发生闭塞或出血而形成[2]。 其后, 脑腔隙性梗塞一词主要用于病理描述。 现在, 由于CT、 MRI的应用, 临床上已认识到, 脑腔隙性梗塞并不是少见的, 也不是只限于老年人的脑血管病变。 脑腔隙性梗塞现已用于临床诊断, 而且近年来国内外对脑腔隙性梗塞的研究论文有明显增多(表1)。
表 1 近十三年脑腔隙性梗塞文献数(篇) 文种
, 百拇医药
年 份 (19~)
86
87
88
89
90
91
92
93
94
95
96
97
, 百拇医药 98
中文1)
1
2
0
0
3
0
0
0
12
13
21
10
, 百拇医药
3
西文2)
5
3
1
6
6
11
9
7
11
38
10
7
, http://www.100md.com
10
注: 1) 中文文献根据CBMDISC及CMCC数据库; 2) 西文文献根据MEDLIN数据库
2 脑腔隙性梗塞的病理改变
2.1 基本病理改变
2.1.1 小血管壁的改变: 豆纹动脉、 视丘深穿支、 或基底动脉的旁正中支等脑的穿通动脉(小动脉或细动脉)发生管壁增厚、 纤维蛋白样坏死, 脂质玻璃样变, 微血管瘤等病理改变。
2.1.2 微栓子形成: 来自心脏、 近心端大血管的微栓子, 使小血管闭塞或破裂出血, 引发该领域内小的梗塞灶或出血灶。
2.1.3 脑实质改变: 肉眼观察脑切面上有灰白色、 腔洞样小软化灶, 多为空腔, 形成“腔隙”, 偶见其内有少许纤维样物。 腔隙的数目不定, 可只有一个、 数个或十数个[2]。 镜下见小的腔隙梗塞灶, 内有格子细胞(图1), 含铁血黄素的吞噬细胞, 血管及结缔组织增生(图2), 腔壁胶原纤维及胶质纤维增生、 可见肥胖星形细胞(图3)。 脑实质内小动脉管壁HE染色呈均匀一致的嗜酸性。 可见微血管粥样瘤。 除腔隙改变之外, 可有软脑膜增厚、 不透明, 脑、 基底节萎缩, 胼胝体变薄, 脑室扩大等病理改变。
, http://www.100md.com
图1 腔隙梗塞灶内的格子细胞 HE染色 ×400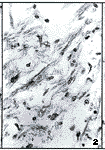
图2 腔隙梗塞灶内毛细血管及结缔组织增生 HE染色 ×400
图3 腔壁外周的肥胖星形细胞 HE染色 ×400
2.2 腔隙的发生部位
脑腔隙性梗塞的发生部位相当广泛, 主要出现在基底节区、 放射冠、 丘脑、 脑叶、 脑干, 在小脑甚至胼胝体都可出现。 根据Fisher等的病理、 CT、 MRI的检查报道[3~5], 腔隙性梗塞发生在基底节区占46.8%~67.7%, 是最多见的部位, 其次为内囊、 放射冠、 脑室周围和桥脑(表2)。
, 百拇医药
表 2 文献记载腔隙梗塞部位的分布 部 位
Ferrand1)
n=88
Fisher1)
n=114
沈言修2)
n=124
侯玉华3)
n=157
腔梗数
%
, 百拇医药
腔梗数
%
腔梗数
%
腔梗数
%
基底节区
135
67.7
176
46.8
125
52.5
, http://www.100md.com
97
61.8
放射冠
46
12.2
57
23.9
18
11.5
丘 脑
41
19.1
52
, http://www.100md.com
13.8
20
8.4
8
5.1
脑 叶
12
5.6
30
8.0
31
13.0
25
, http://www.100md.com 15.9
脑 干
24
11.2
59
15.7
5
2.1
4
2.5
小 脑
6
1.6
5
, 百拇医药
3.2
胼胝体
3
1.4
7
1.9
总 计
215
100
376
100
238
100
, 百拇医药 157
100
注: 1) 尸检资料; 2) CT扫描资料; 3) MRI资料
2.3 腔隙的大小
根据病理和MRI检查, 腔隙性梗塞的病变面积大小不一, 小者, 其直径为0.5 mm, 大者, 其直径可达20 mm。 Fisher(1965)曾将腔隙灶的直径在10 mm以上的腔隙, 称为巨腔隙, 1982年他把腔隙灶直径的上限定为20 mm[6]。现在多数人认为腔隙灶直径应在≤15 mm范围。 有报道认为梗塞血管的直径可以在40~50 μm左右, 所形成的腔隙灶直径可以小到0.5 mm。
对于直径小于0.5 mm的病灶应与Durand-Fardel提出的“筛孔”区别。 “筛孔是在大脑切面上可见髓质内有些孔洞, 每个孔洞中都有一支血管”[7]。 Marie进一步说明:“很明显, 这些孔洞是血管周围间隙的扩大, 因为孔洞都很小, 脑实质无明显破坏, 而是脑实质的退缩”所致。 在影像学特别是MRI检查时, 应与腔隙性梗塞区别。
, 百拇医药
3 脑腔隙梗塞的病理生理基础
脑腔隙性梗塞是一类脑血管病, 病变的血管区段是小动脉、 细动脉, 发病机制是管壁、 管内(血液)、 管周异常, 形成脑局部梗塞或出血。 因此脑腔隙梗塞的病理生理基础是脑循环特别是脑微循环障碍。
3.1 正常脑血流和氧耗
脑的总血流量平均为840~1 000 ml/min, 或相当于心输出量的15%。 灰质为快速血流(70~80 ml.min-1/100 g); 白质为慢速血流(20~30 ml.min-1/100 g)。 白质的血流量是灰质的1/3~1/4。 脑血流量与灌注压和血管抵抗有关。 粗略地说, 脑血流量=脑灌注压/脑血管抵抗。 脑灌注压相当于平均动脉压与颈内静脉压之差, 正常情况下颈内静脉压不明显, 因此平均动脉压可视为有效的灌注压。 脑血管抵抗因子包括血管的大小和血液粘度。
, 百拇医药
正常情况下, 大脑耗氧率为3.55 ml*min-1/100 g, 消耗葡萄糖为6.8 mg*min-1/100 g。 脑血流、 代谢、 功能三者是紧密耦联的, 即脑功能活跃的区域(时间), 如代谢增高, 脑血流量也增加, 脑代谢降低时脑血流量也减少。 Fax等用PET(正电子断层扫描)详细检查脑不同部位的改变, 发现视觉刺激后枕叶血流增加50%, 耗氧量增加5%, 糖代谢增加51%, 总能量增加约10%。
3.2 脑局部缺血时脑微循环的改变
由于脑具有较完善的压流自动调节机制, 血压在8~24 kPa波动时, 能有效地维持较恒定的脑血流量。 当灌注压下降到自家调节的低限(8 kPa)以下时, 脑血流量减少, 出现脑缺血。 在脑的细动脉、 细静脉之间, 小动脉、 小静脉之间, 存在短路枝[8]。 灰质及白质深层可见细动脉和细静脉间有短路枝, 调节脑局部血流状态。 由于全身性或脑局部性病变, 血液不流经毛细血管而主要通过短路枝循环, 则发生脑局部缺氧。 在灰质可出现神经细胞的灶性坏死或假分层坏死、 小出血灶, 在白质则出现小脱髓灶、 小梗塞灶、 小出血灶。 这可能是发生脑腔隙性梗塞的病理生理基础之一。 不可逆性缺血灶的近心端, 发生过度灌注综合症。 远心端发生缺血性半暗区, 半暗区周围为灌注不足区, 常呈现脑水肿。 缺血灶血管自家调节机能丧失、 血管麻痹, 此时如给血管扩张剂, 只能扩张病灶周边的正常血管, 使病灶血流更加减少(称为盗血综合征)。 在较大的梗塞灶上述现象更明显。
, http://www.100md.com
3.3 脑缺血时神经细胞的坏死
当脑血流降至15~20 ml.min-1/100 g(或灰质CBF降到正常的40%、 白质CBF降到正常的35%)时, 神经细胞的动作电位和诱发电位便消失; 若降至5~6 ml*min-1/100 g以下时, ATP耗尽、 细胞膜衰竭[9]。 脑缺血会引起细胞分子变化, 包括细胞的信号(神经递质、 神经调节器)、 信号传导(受体、 离子通道、 第二信使、 磷酸化反应)、 代谢(碳水化合物、 蛋白、 脂肪酸、 自由基)以及基因调节和表达等功能障碍。 轻度缺血仅使易损伤的细胞死亡(如海马CA1和CA4的锥体细胞), 当缺血时间>1 h时, 便从脑血流最低区向周围扩展, 发生不同大小的梗塞、 软化、 坏死。
3.4 腔隙梗塞的危险因子影响
脑腔隙性梗塞的发生机理十分复杂, 尚有不少问题需要研究。 在了解脑腔隙性梗塞病理生理的基础之上, 需要明确腔隙性梗塞的危险因子。 动脉硬化、 高血压、 糖尿病、 高血脂、 吸烟、 冠心病等都是脑腔隙性梗塞的重要危险因子, 其中高血压与腔隙梗塞的并发率最高[10](表3)。 高血压动脉硬化时, 基底动脉延长、 曲屈, 使深穿动脉受拉移位、 扭曲变形, 易受损害。 基底节的灌注压高、 CBF/CBV比率高于皮质, 提示易引起深穿动脉的血管坏死, 特别是高血压病人[11]。 脑小动脉的管壁结构薄弱, 长期高血压作用使管壁发生脂质透明变性、 纤维蛋白坏死、 微动脉粥样瘤等, 若梗塞则形成软化灶, 破裂则为小出血灶。
, http://www.100md.com
表 3 167例脑腔隙梗塞的危险因子尸检资料 危 险 因 子
%
高血压、 吸烟、 糖尿病
82
高血压
64
冠状动脉病
47
吸烟
46
家族性心肌梗塞史
35
, 百拇医药 糖尿病
34
家族性卒中史
17
未发现危险因子
18
因此, 认识腔隙梗塞的病理生理基础、 明确发病的危险因子, 是早期而有效地制定脑腔隙性梗塞的防治原则和选择措施的前提。
4 脑腔隙性梗塞的临床
4.1 腔隙性梗塞的发现率
利用病理、 CT、 MRI检查, 现在在脑梗塞中腔隙性梗塞的发现率为10%~27.8%。 Chamorro(1991)在1 273例脑梗塞中发现腔隙性梗塞337例, 占26%[12], Fisher(1992)报道腔隙性梗塞占所有脑卒中的10%~25%[1], Rothrock(1993)发现腔隙性梗塞在500例脑梗塞中占27%[13], Nadian(1993)的212例中, 腔隙性梗塞59例, 占27.8%[14]。 应当指出, 病理、 CT、 MRI平扫所观察到的是已出现病变的形态结构改变, 这些手段不能或很难反映早期脑局部组织的功能、 代谢变化。 而PET检查却能较早地发现局部脑组织处于脑的功能、 代谢改变状态时的变化。 当PET应用于脑检查时, 腔隙性梗塞的发现率可能会更高。
, 百拇医药
4.2 腔隙性梗塞的临床征象
由于腔隙性梗塞的基本病变发生在小的、 众多的深穿支动脉, 因部位不同、 血管区段不一、 受损的数量不等以及病变发展阶段的差别, 病人的临床表现比较混杂, 尚不能给出统一、 明确、 具体、 特异的临床征象。
4.2.1 沈氏等的腔隙性梗塞(腔隙性卒中)综合征的临床征象型[4,5,12](表4)
表 4 文献记载腔隙性卒中综合征临床分型 症状、 体征
Chamorro
沈言修
侯玉华
例数
, 百拇医药 %
例数
%
例数
%
纯运动性卒中
181
57.0
40
32.3
68
43.3
感觉运动性卒中
, http://www.100md.com 63
20.0
35
28.2
6
3.8
纯感觉性卒中
21
7.0
1
0.8
17
10.8
, http://www.100md.com 共济失调性偏瘫
33
10.0
2
1.6
4
3.0
构音障碍、 笨拙手
18
6.0
3
1.9
偏侧舞蹈投掷
, 百拇医药
1
0.8
脑血管性痴呆
8
6.5
2
1.3
帕金森综合征
3
2.4
2
1.3
不能分型
, 百拇医药 7
5.6
17
10.9
无症状
24
19.4
21
13.4
总 计
316
100
124
, 百拇医药 100
157
100
(1) 纯运动性卒中(偏瘫): 出现率为32.3%~57.0%, 最为多见。 表现一侧面及上、 下肢的轻瘫, 程度相等。 其病理基础主要是内囊, 其次为桥脑血管梗塞。
(2) 感觉、 运动性卒中(偏瘫): 出现率仅次于前者, 除侯玉华报道为3.8%外, 其出现率多为20.0%~28.2%。 表现为偏侧肢体无力和深、 浅感觉丧失。 多数病例为脉络膜前动脉领域的血管梗塞。
(3) 共济失调偏瘫和构音障碍综合征: 共济失调偏瘫和构音障碍综合征是二个密切相关的腔隙性卒中综合征, 前者是一侧肢体力弱伴共济失调, 后者说话不清、 面肌无力、 轻度肢体力弱。 二者通常被认为是桥脑的血管梗塞。
, 百拇医药
(4) 纯感觉卒中: 一侧肢体有感觉障碍, 是视丘腹后核血管梗塞。
(5) 半身舞蹈—半身投掷综合征: 是视丘底核的血管梗塞。
(6) 血管性痴呆或帕金森综合征: 是广泛的、 多灶性皮质下白质或底节的血管梗塞。
4.2.2 上述10种分型可以概括成三类: (1) 局灶体征明确类, 如1、 2、 3、 4、 5项, 其出现率约为75%左右; (2) 有神经系统的症状、 但无局灶体征, 不能分型类, 约占9%; (3) 无症状, 约占据16%左右。
4.2.3 脑腔隙性梗塞的诊断和治疗: 脑腔隙性梗塞的诊断是比较复杂的问题, 单独根据临床症状和体征很难做出确切的诊断。 过去, 脑腔隙性梗塞的诊断主要依靠病理检查; 现在, 临床上则主要根据MRI(图4、 5)和CT(图6); 钆增强核磁共振对脑腔隙梗塞的诊断比MRI平扫更敏感, 直径<15 mm的病灶, 67.3%的病人的病变影像得到增强。 直径>15 mm的病灶能100%的显示。 功能性MRI检查, 如弥散加权MRI能于缺血的早期发现病变。 利用15O2.H2O进行PET检查, 发病2~6 h出现脑氧代谢明显降低, 脑氧代谢率<1.5 ml即出现坏死。 单光子断层扫描(SPECT)可取得近似PET的结果。 这些检查方法在临床应用时, 脑腔隙性梗塞的诊断将会更早、 更确实, 有利于早期发现、 早期防治。 由于梗死病灶的半暗区仍有生存的可能, 故此在治疗上要努力促进半暗区病变的好转。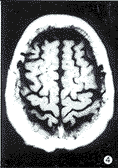
, http://www.100md.com
图4 MRI T1加权像。多发性腔隙梗塞灶为长T1信号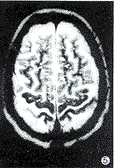
图5 MRI T2加权像。多发性腔隙梗塞灶为长T2信号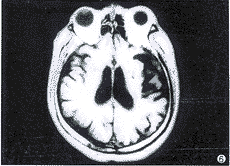
图6 CT断层扫描。单发的腔隙梗塞灶
参考文献
[1] Fisher CM, Minematsu K. Lacunar stroke: Diagnosis, evaluation, and management. Heart Disease and Stroke, 1992, 1:353~356.
, http://www.100md.com
[2] Marie P. Des foyers lacunaires de desintegration. Autres differents etats cavtaires du cerveau. Revue de Medecine, 1901, T21:281.
[3] Fisher CM. Lacunes: Small, deep infarcts. Neurology, 1965, 15:74~784.
[4] 沈言修, 张文记, 王占立. 腔隙梗塞—CT与临床关系. 中华神经精神科杂志, 1987, (2):105~108.
[5] 侯玉华, 薛燕礼, 潘奇芳. 腔隙性脑梗塞的MRI与临床. 中风与神经疾病杂志, 1995, 12(3):172~173.
[6] Fisher CM. Lacunar stroke and infarcts: A review. Neurology, 1982, 32:871~876.
, 百拇医药
[7] 刘贻德. 腔隙、 腔隙性梗塞与腔隙状态. 临床神经病学杂志, 1994, 7(1):5~7.
[8] 田牛. 微循环. 北京: 科学出版社, 1980. 126.
[9] 侯熙德. 缺血性脑梗塞的病理生理. 国外医学脑血管分册, 1994, 2(增刊):增10~增15.
[10] Tuszynski MH, Petito CK, Levy DE. Risk factors and clinical manifestations of pathologically verified lacunar infarctions. Stroke 1989, 20(8):990~999.
[11] Yamaguchi S. Hemodynamics in the cerebral cortex and besal ganglia, observation on normal volunteers and patients with lacunes using PET. Rinsho Shinkeigaku, 1991, 31(10):1 070~1 076.
, 百拇医药
[12] Chamorro A. Clinical computed tomographic correlations of lacunar infarction in the stroke Data Bank. Stroke, 1991, 22(2):175~181.
[13] Rothrock JF. An analysis of ischemic stroke in an urbon Southern California population. The University of California, San Diago, Stroke Data Bank. Arch Intern Med, 1993, 153(5):629~624.
[14] Nadean SE. Factors associated with occurrence of large vessel and lacunar cerebral infarctions. J Neurol Sci, 1993, 114(2):156~159.
本文1998-11-01收到, 1999-01-29接受, 百拇医药(罗 毅*)
单位:1 中国人民解放军总医院, 邮政编码 北京100853
关键词:
微循环学杂志990117
编者按: 脑梗塞与脑腔隙性梗塞是近年脑血管病研究领域较为热门的研究课题。 本期讲座我们约请著名病理学专家就脑腔隙性梗塞的病理学、 病理生理学以及诊断学的研究历史与现状进行较为系统和全面的概述, 以期为广大从事与之相关研究的读者开阔思路提供参考。
脑腔隙性梗塞是常见的脑血管疾病之一。 过去由于很多脑腔隙性梗塞病人没有表现出局灶体征, 甚至完全没有症状, 临床上很难做出脑腔隙性梗塞的诊断, 只有在病理检查时, 才能明确脑腔隙性梗塞的病变。 在CT、 核磁共振出现后, 在很多没有体征的患者中, 明确显示出脑腔隙性梗塞病灶的改变, 脑腔隙性梗塞才引起人们的重视, 对它的研究逐渐增多。 但目前认识尚不一致, 一些问题有待研究。
, 百拇医药
1 何谓脑腔隙性梗塞
迄今为止, 人们对“脑腔隙性梗塞”的认识还不一致, 其内涵和外延都没有合理的界定。 笼统地说, 脑腔隙性梗塞是目前观察到的病变范围最小、 部位不一、 症状不定的一组脑小血管梗塞(或出血)。 “腔隙”一词, 源于法语“充满液体的小腔洞”[1]。 最早, Marie(1901)根据50例病理解剖观察, 描述腔隙是“组织崩溃的腔隙病灶”, “腔隙病灶的组织象是扯裂、 破坏”。 腔隙是由脑深穿动脉的动脉硬化性变化, 发生闭塞或出血而形成[2]。 其后, 脑腔隙性梗塞一词主要用于病理描述。 现在, 由于CT、 MRI的应用, 临床上已认识到, 脑腔隙性梗塞并不是少见的, 也不是只限于老年人的脑血管病变。 脑腔隙性梗塞现已用于临床诊断, 而且近年来国内外对脑腔隙性梗塞的研究论文有明显增多(表1)。
表 1 近十三年脑腔隙性梗塞文献数(篇) 文种
, 百拇医药
年 份 (19~)
86
87
88
89
90
91
92
93
94
95
96
97
, 百拇医药 98
中文1)
1
2
0
0
3
0
0
0
12
13
21
10
, 百拇医药
3
西文2)
5
3
1
6
6
11
9
7
11
38
10
7
, http://www.100md.com
10
注: 1) 中文文献根据CBMDISC及CMCC数据库; 2) 西文文献根据MEDLIN数据库
2 脑腔隙性梗塞的病理改变
2.1 基本病理改变
2.1.1 小血管壁的改变: 豆纹动脉、 视丘深穿支、 或基底动脉的旁正中支等脑的穿通动脉(小动脉或细动脉)发生管壁增厚、 纤维蛋白样坏死, 脂质玻璃样变, 微血管瘤等病理改变。
2.1.2 微栓子形成: 来自心脏、 近心端大血管的微栓子, 使小血管闭塞或破裂出血, 引发该领域内小的梗塞灶或出血灶。
2.1.3 脑实质改变: 肉眼观察脑切面上有灰白色、 腔洞样小软化灶, 多为空腔, 形成“腔隙”, 偶见其内有少许纤维样物。 腔隙的数目不定, 可只有一个、 数个或十数个[2]。 镜下见小的腔隙梗塞灶, 内有格子细胞(图1), 含铁血黄素的吞噬细胞, 血管及结缔组织增生(图2), 腔壁胶原纤维及胶质纤维增生、 可见肥胖星形细胞(图3)。 脑实质内小动脉管壁HE染色呈均匀一致的嗜酸性。 可见微血管粥样瘤。 除腔隙改变之外, 可有软脑膜增厚、 不透明, 脑、 基底节萎缩, 胼胝体变薄, 脑室扩大等病理改变。

, http://www.100md.com
图1 腔隙梗塞灶内的格子细胞 HE染色 ×400

图2 腔隙梗塞灶内毛细血管及结缔组织增生 HE染色 ×400

图3 腔壁外周的肥胖星形细胞 HE染色 ×400
2.2 腔隙的发生部位
脑腔隙性梗塞的发生部位相当广泛, 主要出现在基底节区、 放射冠、 丘脑、 脑叶、 脑干, 在小脑甚至胼胝体都可出现。 根据Fisher等的病理、 CT、 MRI的检查报道[3~5], 腔隙性梗塞发生在基底节区占46.8%~67.7%, 是最多见的部位, 其次为内囊、 放射冠、 脑室周围和桥脑(表2)。
, 百拇医药
表 2 文献记载腔隙梗塞部位的分布 部 位
Ferrand1)
n=88
Fisher1)
n=114
沈言修2)
n=124
侯玉华3)
n=157
腔梗数
%
, 百拇医药
腔梗数
%
腔梗数
%
腔梗数
%
基底节区
135
67.7
176
46.8
125
52.5
, http://www.100md.com
97
61.8
放射冠
46
12.2
57
23.9
18
11.5
丘 脑
41
19.1
52
, http://www.100md.com
13.8
20
8.4
8
5.1
脑 叶
12
5.6
30
8.0
31
13.0
25
, http://www.100md.com 15.9
脑 干
24
11.2
59
15.7
5
2.1
4
2.5
小 脑
6
1.6
5
, 百拇医药
3.2
胼胝体
3
1.4
7
1.9
总 计
215
100
376
100
238
100
, 百拇医药 157
100
注: 1) 尸检资料; 2) CT扫描资料; 3) MRI资料
2.3 腔隙的大小
根据病理和MRI检查, 腔隙性梗塞的病变面积大小不一, 小者, 其直径为0.5 mm, 大者, 其直径可达20 mm。 Fisher(1965)曾将腔隙灶的直径在10 mm以上的腔隙, 称为巨腔隙, 1982年他把腔隙灶直径的上限定为20 mm[6]。现在多数人认为腔隙灶直径应在≤15 mm范围。 有报道认为梗塞血管的直径可以在40~50 μm左右, 所形成的腔隙灶直径可以小到0.5 mm。
对于直径小于0.5 mm的病灶应与Durand-Fardel提出的“筛孔”区别。 “筛孔是在大脑切面上可见髓质内有些孔洞, 每个孔洞中都有一支血管”[7]。 Marie进一步说明:“很明显, 这些孔洞是血管周围间隙的扩大, 因为孔洞都很小, 脑实质无明显破坏, 而是脑实质的退缩”所致。 在影像学特别是MRI检查时, 应与腔隙性梗塞区别。
, 百拇医药
3 脑腔隙梗塞的病理生理基础
脑腔隙性梗塞是一类脑血管病, 病变的血管区段是小动脉、 细动脉, 发病机制是管壁、 管内(血液)、 管周异常, 形成脑局部梗塞或出血。 因此脑腔隙梗塞的病理生理基础是脑循环特别是脑微循环障碍。
3.1 正常脑血流和氧耗
脑的总血流量平均为840~1 000 ml/min, 或相当于心输出量的15%。 灰质为快速血流(70~80 ml.min-1/100 g); 白质为慢速血流(20~30 ml.min-1/100 g)。 白质的血流量是灰质的1/3~1/4。 脑血流量与灌注压和血管抵抗有关。 粗略地说, 脑血流量=脑灌注压/脑血管抵抗。 脑灌注压相当于平均动脉压与颈内静脉压之差, 正常情况下颈内静脉压不明显, 因此平均动脉压可视为有效的灌注压。 脑血管抵抗因子包括血管的大小和血液粘度。
, 百拇医药
正常情况下, 大脑耗氧率为3.55 ml*min-1/100 g, 消耗葡萄糖为6.8 mg*min-1/100 g。 脑血流、 代谢、 功能三者是紧密耦联的, 即脑功能活跃的区域(时间), 如代谢增高, 脑血流量也增加, 脑代谢降低时脑血流量也减少。 Fax等用PET(正电子断层扫描)详细检查脑不同部位的改变, 发现视觉刺激后枕叶血流增加50%, 耗氧量增加5%, 糖代谢增加51%, 总能量增加约10%。
3.2 脑局部缺血时脑微循环的改变
由于脑具有较完善的压流自动调节机制, 血压在8~24 kPa波动时, 能有效地维持较恒定的脑血流量。 当灌注压下降到自家调节的低限(8 kPa)以下时, 脑血流量减少, 出现脑缺血。 在脑的细动脉、 细静脉之间, 小动脉、 小静脉之间, 存在短路枝[8]。 灰质及白质深层可见细动脉和细静脉间有短路枝, 调节脑局部血流状态。 由于全身性或脑局部性病变, 血液不流经毛细血管而主要通过短路枝循环, 则发生脑局部缺氧。 在灰质可出现神经细胞的灶性坏死或假分层坏死、 小出血灶, 在白质则出现小脱髓灶、 小梗塞灶、 小出血灶。 这可能是发生脑腔隙性梗塞的病理生理基础之一。 不可逆性缺血灶的近心端, 发生过度灌注综合症。 远心端发生缺血性半暗区, 半暗区周围为灌注不足区, 常呈现脑水肿。 缺血灶血管自家调节机能丧失、 血管麻痹, 此时如给血管扩张剂, 只能扩张病灶周边的正常血管, 使病灶血流更加减少(称为盗血综合征)。 在较大的梗塞灶上述现象更明显。
, http://www.100md.com
3.3 脑缺血时神经细胞的坏死
当脑血流降至15~20 ml.min-1/100 g(或灰质CBF降到正常的40%、 白质CBF降到正常的35%)时, 神经细胞的动作电位和诱发电位便消失; 若降至5~6 ml*min-1/100 g以下时, ATP耗尽、 细胞膜衰竭[9]。 脑缺血会引起细胞分子变化, 包括细胞的信号(神经递质、 神经调节器)、 信号传导(受体、 离子通道、 第二信使、 磷酸化反应)、 代谢(碳水化合物、 蛋白、 脂肪酸、 自由基)以及基因调节和表达等功能障碍。 轻度缺血仅使易损伤的细胞死亡(如海马CA1和CA4的锥体细胞), 当缺血时间>1 h时, 便从脑血流最低区向周围扩展, 发生不同大小的梗塞、 软化、 坏死。
3.4 腔隙梗塞的危险因子影响
脑腔隙性梗塞的发生机理十分复杂, 尚有不少问题需要研究。 在了解脑腔隙性梗塞病理生理的基础之上, 需要明确腔隙性梗塞的危险因子。 动脉硬化、 高血压、 糖尿病、 高血脂、 吸烟、 冠心病等都是脑腔隙性梗塞的重要危险因子, 其中高血压与腔隙梗塞的并发率最高[10](表3)。 高血压动脉硬化时, 基底动脉延长、 曲屈, 使深穿动脉受拉移位、 扭曲变形, 易受损害。 基底节的灌注压高、 CBF/CBV比率高于皮质, 提示易引起深穿动脉的血管坏死, 特别是高血压病人[11]。 脑小动脉的管壁结构薄弱, 长期高血压作用使管壁发生脂质透明变性、 纤维蛋白坏死、 微动脉粥样瘤等, 若梗塞则形成软化灶, 破裂则为小出血灶。
, http://www.100md.com
表 3 167例脑腔隙梗塞的危险因子尸检资料 危 险 因 子
%
高血压、 吸烟、 糖尿病
82
高血压
64
冠状动脉病
47
吸烟
46
家族性心肌梗塞史
35
, 百拇医药 糖尿病
34
家族性卒中史
17
未发现危险因子
18
因此, 认识腔隙梗塞的病理生理基础、 明确发病的危险因子, 是早期而有效地制定脑腔隙性梗塞的防治原则和选择措施的前提。
4 脑腔隙性梗塞的临床
4.1 腔隙性梗塞的发现率
利用病理、 CT、 MRI检查, 现在在脑梗塞中腔隙性梗塞的发现率为10%~27.8%。 Chamorro(1991)在1 273例脑梗塞中发现腔隙性梗塞337例, 占26%[12], Fisher(1992)报道腔隙性梗塞占所有脑卒中的10%~25%[1], Rothrock(1993)发现腔隙性梗塞在500例脑梗塞中占27%[13], Nadian(1993)的212例中, 腔隙性梗塞59例, 占27.8%[14]。 应当指出, 病理、 CT、 MRI平扫所观察到的是已出现病变的形态结构改变, 这些手段不能或很难反映早期脑局部组织的功能、 代谢变化。 而PET检查却能较早地发现局部脑组织处于脑的功能、 代谢改变状态时的变化。 当PET应用于脑检查时, 腔隙性梗塞的发现率可能会更高。
, 百拇医药
4.2 腔隙性梗塞的临床征象
由于腔隙性梗塞的基本病变发生在小的、 众多的深穿支动脉, 因部位不同、 血管区段不一、 受损的数量不等以及病变发展阶段的差别, 病人的临床表现比较混杂, 尚不能给出统一、 明确、 具体、 特异的临床征象。
4.2.1 沈氏等的腔隙性梗塞(腔隙性卒中)综合征的临床征象型[4,5,12](表4)
表 4 文献记载腔隙性卒中综合征临床分型 症状、 体征
Chamorro
沈言修
侯玉华
例数
, 百拇医药 %
例数
%
例数
%
纯运动性卒中
181
57.0
40
32.3
68
43.3
感觉运动性卒中
, http://www.100md.com 63
20.0
35
28.2
6
3.8
纯感觉性卒中
21
7.0
1
0.8
17
10.8
, http://www.100md.com 共济失调性偏瘫
33
10.0
2
1.6
4
3.0
构音障碍、 笨拙手
18
6.0
3
1.9
偏侧舞蹈投掷
, 百拇医药
1
0.8
脑血管性痴呆
8
6.5
2
1.3
帕金森综合征
3
2.4
2
1.3
不能分型
, 百拇医药 7
5.6
17
10.9
无症状
24
19.4
21
13.4
总 计
316
100
124
, 百拇医药 100
157
100
(1) 纯运动性卒中(偏瘫): 出现率为32.3%~57.0%, 最为多见。 表现一侧面及上、 下肢的轻瘫, 程度相等。 其病理基础主要是内囊, 其次为桥脑血管梗塞。
(2) 感觉、 运动性卒中(偏瘫): 出现率仅次于前者, 除侯玉华报道为3.8%外, 其出现率多为20.0%~28.2%。 表现为偏侧肢体无力和深、 浅感觉丧失。 多数病例为脉络膜前动脉领域的血管梗塞。
(3) 共济失调偏瘫和构音障碍综合征: 共济失调偏瘫和构音障碍综合征是二个密切相关的腔隙性卒中综合征, 前者是一侧肢体力弱伴共济失调, 后者说话不清、 面肌无力、 轻度肢体力弱。 二者通常被认为是桥脑的血管梗塞。
, 百拇医药
(4) 纯感觉卒中: 一侧肢体有感觉障碍, 是视丘腹后核血管梗塞。
(5) 半身舞蹈—半身投掷综合征: 是视丘底核的血管梗塞。
(6) 血管性痴呆或帕金森综合征: 是广泛的、 多灶性皮质下白质或底节的血管梗塞。
4.2.2 上述10种分型可以概括成三类: (1) 局灶体征明确类, 如1、 2、 3、 4、 5项, 其出现率约为75%左右; (2) 有神经系统的症状、 但无局灶体征, 不能分型类, 约占9%; (3) 无症状, 约占据16%左右。
4.2.3 脑腔隙性梗塞的诊断和治疗: 脑腔隙性梗塞的诊断是比较复杂的问题, 单独根据临床症状和体征很难做出确切的诊断。 过去, 脑腔隙性梗塞的诊断主要依靠病理检查; 现在, 临床上则主要根据MRI(图4、 5)和CT(图6); 钆增强核磁共振对脑腔隙梗塞的诊断比MRI平扫更敏感, 直径<15 mm的病灶, 67.3%的病人的病变影像得到增强。 直径>15 mm的病灶能100%的显示。 功能性MRI检查, 如弥散加权MRI能于缺血的早期发现病变。 利用15O2.H2O进行PET检查, 发病2~6 h出现脑氧代谢明显降低, 脑氧代谢率<1.5 ml即出现坏死。 单光子断层扫描(SPECT)可取得近似PET的结果。 这些检查方法在临床应用时, 脑腔隙性梗塞的诊断将会更早、 更确实, 有利于早期发现、 早期防治。 由于梗死病灶的半暗区仍有生存的可能, 故此在治疗上要努力促进半暗区病变的好转。

, http://www.100md.com
图4 MRI T1加权像。多发性腔隙梗塞灶为长T1信号

图5 MRI T2加权像。多发性腔隙梗塞灶为长T2信号

图6 CT断层扫描。单发的腔隙梗塞灶
参考文献
[1] Fisher CM, Minematsu K. Lacunar stroke: Diagnosis, evaluation, and management. Heart Disease and Stroke, 1992, 1:353~356.
, http://www.100md.com
[2] Marie P. Des foyers lacunaires de desintegration. Autres differents etats cavtaires du cerveau. Revue de Medecine, 1901, T21:281.
[3] Fisher CM. Lacunes: Small, deep infarcts. Neurology, 1965, 15:74~784.
[4] 沈言修, 张文记, 王占立. 腔隙梗塞—CT与临床关系. 中华神经精神科杂志, 1987, (2):105~108.
[5] 侯玉华, 薛燕礼, 潘奇芳. 腔隙性脑梗塞的MRI与临床. 中风与神经疾病杂志, 1995, 12(3):172~173.
[6] Fisher CM. Lacunar stroke and infarcts: A review. Neurology, 1982, 32:871~876.
, 百拇医药
[7] 刘贻德. 腔隙、 腔隙性梗塞与腔隙状态. 临床神经病学杂志, 1994, 7(1):5~7.
[8] 田牛. 微循环. 北京: 科学出版社, 1980. 126.
[9] 侯熙德. 缺血性脑梗塞的病理生理. 国外医学脑血管分册, 1994, 2(增刊):增10~增15.
[10] Tuszynski MH, Petito CK, Levy DE. Risk factors and clinical manifestations of pathologically verified lacunar infarctions. Stroke 1989, 20(8):990~999.
[11] Yamaguchi S. Hemodynamics in the cerebral cortex and besal ganglia, observation on normal volunteers and patients with lacunes using PET. Rinsho Shinkeigaku, 1991, 31(10):1 070~1 076.
, 百拇医药
[12] Chamorro A. Clinical computed tomographic correlations of lacunar infarction in the stroke Data Bank. Stroke, 1991, 22(2):175~181.
[13] Rothrock JF. An analysis of ischemic stroke in an urbon Southern California population. The University of California, San Diago, Stroke Data Bank. Arch Intern Med, 1993, 153(5):629~624.
[14] Nadean SE. Factors associated with occurrence of large vessel and lacunar cerebral infarctions. J Neurol Sci, 1993, 114(2):156~159.
本文1998-11-01收到, 1999-01-29接受, 百拇医药(罗 毅*)