血源性乙型肝炎疫苗接种后11年效果及免疫记忆
作者:徐慧文 庄贵华 王学良 陈全景 陈志军
单位:710061 西安医科大学流行病学教研室
关键词:肝炎疫苗,乙型;接种;免疫记忆
中华预防医学杂志000217 摘 要:目的 观察乙型肝炎疫苗接种10年后远期效果,为确定复种时间提供依据。方法 按随机、双盲、安慰剂对照严格设计,对乙型肝炎疫苗接种11年后效果及免疫记忆进行观察。结果 11年疫苗免疫原性和保护率仍好,对HBV感染保护率73.5%,但9~11年观察时段HBV感染率疫苗组和安慰剂组差异已无显著性(7.89%与13.25%);11年有免疫记忆存在,但较10年内明显减弱。结论 接种后11年疫苗效果已开始下降,应继续追踪观察,以期得出确切结论。
Efficacy and immune memory of plasma-derived hepatitis B vaccine 11 years after primary immunization
, 百拇医药
XU Huiwen, ZHUANG Guihua, WANG Xueliang, et al.
Department of Epidemiology, Xi′an Medical University, Xi′an 710061,China
Abstract:Objective To evaluate the long-term efficacy of hepatitis B vaccine 10 years after primary immunization to provide scientific basis for the time of revaccination. Methods The study was strictly designed with randomization, double-blinding, and placebo-controlled method to observe the efficacy and immune memory 11 years following hepatitis B vaccination. Results Immunogenicity and protective rate of vaccine were still kept well 11 years after immunization with a protective rate against HBV infection of 73.5%. But, there was no significant difference in HBV infection rates between vaccine group and placebo-controlled group (7.89% vs. 13.25%, P>0.1) nine to 11 years following immunization. There still existed immune memeory 11 years after immunization, but it was significantly weaker than that within the first 10 years after immunization. Conclusion The efficacy of the vaccine had begun to drop 11years after immunization, which should be followed up further to reach a clear conclusion.
, 百拇医药
Key words:Hepatitis B vaccines;Vaccination;Immunologic memory
1986年,采用随机、双盲、安慰剂对照方法进行了乙型肝炎(乙肝)疫苗现场实验研究,9年结果显示疫苗效果良好[1]。在此基础上,1997年4月继续对疫苗接种11年效果进行了观察;同年9月,同时观察初种后11年免疫记忆情况。试图对乙肝疫苗接种10年后的远期效果作深入、全面地评价。
对象与方法
1.1997年4月,对原疫苗组126人、安慰剂组135人进行初种后第11年(T132)随访采血,方法参见文献[1]。同年9月,对疫苗组T132时抗-HBs S/N值降至10以下、且HBsAg阴性者36人注射一针5 μg重组乙肝疫苗(北京生物制品研究所,批号97054)。分别于注射后第1、4周采血检测HBV 3项指标。
, http://www.100md.com
2.血清检测按密码双盲原则进行[1]。HBsAg S/N值在2.1~10者重测1次,仍≥2.1者判为阳性。HBsAg阳性者6个月后再采血检测1次,判断HBsAg慢性携带。用ELISA法检测抗-HBc,先用上海科华试剂,再用北京四环试剂复测,两次同为阳性者判为阳性。
3.回忆应答的判断:于接种后第1、4周2次采血检测抗-HBs,S/N值4倍增长,且≥10者为有应答。其他指标的定义参见文献[1]。
结果
1.资料完整性:应查261人,实查184人,失访率29.5%。疫苗组、安慰剂组失访率分别为33.3%(42/126)和25.9%(35/135),差异无显著性(P>0.1)。无因病失访者,失访原因两组差异无显著性。
2.疫苗免疫原性:T132时疫苗组抗-HBs S/N≥2.1、≥10的阳性率和GMT仍显著高于安慰剂组,分别为72.7%、52.3%、9.7和26.0%、15.0%、1.2(P<0.01);与第9年(T108)比较差异无显著性(P>0.05);较第6年(T72)各项指标均明显下降(P<0.05,图1)。 图1 疫苗组与安慰剂组各期抗-HBs阳性率和GMT
图1 疫苗组与安慰剂组各期抗-HBs阳性率和GMT
, 百拇医药
3.疫苗长期保护效果:疫苗组、安慰剂组各期人年HBV感染率如图2所示,均显示安慰剂组显著高于疫苗组。11年来,疫苗组共发生28例HBV感染,安慰剂组发生84例,相应人年HBV感染率为2.58%(28/1 083.7)和9.75%(84/861.5),保护率为73.5%。与第9年81.6%相比,略有下降。若仅以HBsAg阳转作为评价指标,疫苗组发生1例,安慰剂组发生10例,均为一过性阳转,无慢性携带,人年感染率分别为0.09%(1/1 169.2)和0.81%(10/1 231.0),保护率为88.9%。与第9年87.0%相比,保持一致。疫苗组未见显性乙肝病例,安慰剂组于T108时发生1例。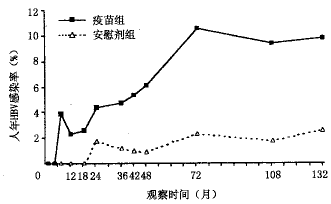 图2 疫苗组与安慰剂组各期人年HBV感染率
图2 疫苗组与安慰剂组各期人年HBV感染率
11年来共进行了12次随访采血。比较不同观察时段两组人年HBV感染率(图3)。在T108以前,除T18~T24外各时段安慰剂组显著高于疫苗组,T108~T132时段两组差异不显著,疫苗组为7.89%(12/152.0),安慰剂组13.25%(11/83.0,P>0.1)。此时段疫苗组发生的12例单项抗-HBc阳转者中,原应答良好者10人,无弱应答者2人,经分析均与T108和T12抗体水平低下有关。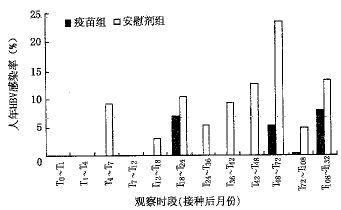 图3 疫苗组与安慰剂组各观察时段人年HBV感染率
图3 疫苗组与安慰剂组各观察时段人年HBV感染率
, 百拇医药
11年中,无弱应答11人中6例HBV感染,应答良好115人中发生22例,两组人年HBV感染率分别为8.75%(6/68.6)和2.17%(22/1 015.3),P<0.05。
4.初种11年后的免疫记忆: 第1周时随访到31人,6人出现回忆应答,发生率为19.4%。未出现回忆应答的25人中,第4周随访到21人,15人出现回忆应答,发生率为71.4%。抗体GMT注射前为2.1,注射后1周为8.9,注射后4周为26.0,分别增加4.2和12.4倍。
讨论
11年来,为使失访率降到最低限度,并能获得可靠的第一手资料,科研人员多次追访每例研究对象。11年随访率为70%,两组失访率和失访原因无明显差异。国外9~10年观察的随访率40%~60%[2,3]。
11年保护率虽为73.5%,但T108~T132时段两组HBV感染率差异却无显著性。国外10年内的研究多认为[3,4],疫苗组HBV感染者多为初种时无、弱应答者。本研究的12例HBV感染者中,10例为原应答良好者,说明应答良好者抗体下降到保护水平以下时,虽有自然加强在调整抗体水平,但亦难以避免受感染。
, http://www.100md.com
本研究所见的HBV感染者,多数为单项抗-HBc 阳转。本研究11年观察结果说明[5,6],单项抗-HBc阳性者多数与HBV感染有关。本研究是在有严格安慰剂对照下进行的,因假阳性而产生的偏倚在对比观察中已得到控制。
11年的免疫记忆与国外报道5~7年抗体上升26~147倍[7]、国内7年抗体上升57倍相比[8],有明显减弱。
本研究提示,接种后11年乙肝疫苗预防效果已开始下降,复种问题是否应提到议事日程?应作进一步追踪观察。
参考文献
[1]徐慧文, 左弘, 庄贵华, 等. 国产血源性乙型肝炎疫苗接种后九年效果评价. 中华预防医学杂志, 1998, 32:205-207.
[2]Chen HL, Chang MH, Ni YH, et al. Seroepidemiology of hepatitis B virus infection in children: ten years of mass vaccination in Taiwan. JAMA, 1996, 276:906-908.
, http://www.100md.com
[3]Wainwright RB, Bulkow LR, Parkinson AJ, et al. Protection provided by hepatitis B vaccine in a Yupik Eskimo population- results of a 10-year study. J Infect Dis, 1997, 175:674-677.
[4]Hadler SC, Judson FN, O′Malley PM, et al. Studies of hepatitis B vaccine in homosexual men. Vol 194. London:John Libbey Eurotext Ltd,1990. 165-175.
[5]徐慧文, 王学良, 庄贵华, 等. 乙肝疫苗接种无弱应答与遗传关系的研究. 解放军预防医学杂志, 1998, 16:104-108.
, http://www.100md.com
[6]Jilg W, Sieger E, Zachoval R, et al. Individuals with antibodies hepatitis B core antigen as the only serological marker for hepatitis B infection: high percentage of carriers of hepatitis B and C virus. J Hepatol, 1995, 23:14-20.
[7]West DJ, Calandra GB. Vaccine induced immunologic memory for hepatitis B surface antigen: implications for policy on booster vaccination. Vaccine, 1996, 14: 1019-1027.
[8]李雪翔, 邬嘉生, 刘建福, 等. 小学生接种乙型肝炎血源疫苗后七年效果观察. 中华预防医学杂志, 1996, 30:151-153.
收稿日期:1999-04-01, http://www.100md.com
单位:710061 西安医科大学流行病学教研室
关键词:肝炎疫苗,乙型;接种;免疫记忆
中华预防医学杂志000217 摘 要:目的 观察乙型肝炎疫苗接种10年后远期效果,为确定复种时间提供依据。方法 按随机、双盲、安慰剂对照严格设计,对乙型肝炎疫苗接种11年后效果及免疫记忆进行观察。结果 11年疫苗免疫原性和保护率仍好,对HBV感染保护率73.5%,但9~11年观察时段HBV感染率疫苗组和安慰剂组差异已无显著性(7.89%与13.25%);11年有免疫记忆存在,但较10年内明显减弱。结论 接种后11年疫苗效果已开始下降,应继续追踪观察,以期得出确切结论。
Efficacy and immune memory of plasma-derived hepatitis B vaccine 11 years after primary immunization
, 百拇医药
XU Huiwen, ZHUANG Guihua, WANG Xueliang, et al.
Department of Epidemiology, Xi′an Medical University, Xi′an 710061,China
Abstract:Objective To evaluate the long-term efficacy of hepatitis B vaccine 10 years after primary immunization to provide scientific basis for the time of revaccination. Methods The study was strictly designed with randomization, double-blinding, and placebo-controlled method to observe the efficacy and immune memory 11 years following hepatitis B vaccination. Results Immunogenicity and protective rate of vaccine were still kept well 11 years after immunization with a protective rate against HBV infection of 73.5%. But, there was no significant difference in HBV infection rates between vaccine group and placebo-controlled group (7.89% vs. 13.25%, P>0.1) nine to 11 years following immunization. There still existed immune memeory 11 years after immunization, but it was significantly weaker than that within the first 10 years after immunization. Conclusion The efficacy of the vaccine had begun to drop 11years after immunization, which should be followed up further to reach a clear conclusion.
, 百拇医药
Key words:Hepatitis B vaccines;Vaccination;Immunologic memory
1986年,采用随机、双盲、安慰剂对照方法进行了乙型肝炎(乙肝)疫苗现场实验研究,9年结果显示疫苗效果良好[1]。在此基础上,1997年4月继续对疫苗接种11年效果进行了观察;同年9月,同时观察初种后11年免疫记忆情况。试图对乙肝疫苗接种10年后的远期效果作深入、全面地评价。
对象与方法
1.1997年4月,对原疫苗组126人、安慰剂组135人进行初种后第11年(T132)随访采血,方法参见文献[1]。同年9月,对疫苗组T132时抗-HBs S/N值降至10以下、且HBsAg阴性者36人注射一针5 μg重组乙肝疫苗(北京生物制品研究所,批号97054)。分别于注射后第1、4周采血检测HBV 3项指标。
, http://www.100md.com
2.血清检测按密码双盲原则进行[1]。HBsAg S/N值在2.1~10者重测1次,仍≥2.1者判为阳性。HBsAg阳性者6个月后再采血检测1次,判断HBsAg慢性携带。用ELISA法检测抗-HBc,先用上海科华试剂,再用北京四环试剂复测,两次同为阳性者判为阳性。
3.回忆应答的判断:于接种后第1、4周2次采血检测抗-HBs,S/N值4倍增长,且≥10者为有应答。其他指标的定义参见文献[1]。
结果
1.资料完整性:应查261人,实查184人,失访率29.5%。疫苗组、安慰剂组失访率分别为33.3%(42/126)和25.9%(35/135),差异无显著性(P>0.1)。无因病失访者,失访原因两组差异无显著性。
2.疫苗免疫原性:T132时疫苗组抗-HBs S/N≥2.1、≥10的阳性率和GMT仍显著高于安慰剂组,分别为72.7%、52.3%、9.7和26.0%、15.0%、1.2(P<0.01);与第9年(T108)比较差异无显著性(P>0.05);较第6年(T72)各项指标均明显下降(P<0.05,图1)。
 图1 疫苗组与安慰剂组各期抗-HBs阳性率和GMT
图1 疫苗组与安慰剂组各期抗-HBs阳性率和GMT, 百拇医药
3.疫苗长期保护效果:疫苗组、安慰剂组各期人年HBV感染率如图2所示,均显示安慰剂组显著高于疫苗组。11年来,疫苗组共发生28例HBV感染,安慰剂组发生84例,相应人年HBV感染率为2.58%(28/1 083.7)和9.75%(84/861.5),保护率为73.5%。与第9年81.6%相比,略有下降。若仅以HBsAg阳转作为评价指标,疫苗组发生1例,安慰剂组发生10例,均为一过性阳转,无慢性携带,人年感染率分别为0.09%(1/1 169.2)和0.81%(10/1 231.0),保护率为88.9%。与第9年87.0%相比,保持一致。疫苗组未见显性乙肝病例,安慰剂组于T108时发生1例。
 图2 疫苗组与安慰剂组各期人年HBV感染率
图2 疫苗组与安慰剂组各期人年HBV感染率11年来共进行了12次随访采血。比较不同观察时段两组人年HBV感染率(图3)。在T108以前,除T18~T24外各时段安慰剂组显著高于疫苗组,T108~T132时段两组差异不显著,疫苗组为7.89%(12/152.0),安慰剂组13.25%(11/83.0,P>0.1)。此时段疫苗组发生的12例单项抗-HBc阳转者中,原应答良好者10人,无弱应答者2人,经分析均与T108和T12抗体水平低下有关。
 图3 疫苗组与安慰剂组各观察时段人年HBV感染率
图3 疫苗组与安慰剂组各观察时段人年HBV感染率, 百拇医药
11年中,无弱应答11人中6例HBV感染,应答良好115人中发生22例,两组人年HBV感染率分别为8.75%(6/68.6)和2.17%(22/1 015.3),P<0.05。
4.初种11年后的免疫记忆: 第1周时随访到31人,6人出现回忆应答,发生率为19.4%。未出现回忆应答的25人中,第4周随访到21人,15人出现回忆应答,发生率为71.4%。抗体GMT注射前为2.1,注射后1周为8.9,注射后4周为26.0,分别增加4.2和12.4倍。
讨论
11年来,为使失访率降到最低限度,并能获得可靠的第一手资料,科研人员多次追访每例研究对象。11年随访率为70%,两组失访率和失访原因无明显差异。国外9~10年观察的随访率40%~60%[2,3]。
11年保护率虽为73.5%,但T108~T132时段两组HBV感染率差异却无显著性。国外10年内的研究多认为[3,4],疫苗组HBV感染者多为初种时无、弱应答者。本研究的12例HBV感染者中,10例为原应答良好者,说明应答良好者抗体下降到保护水平以下时,虽有自然加强在调整抗体水平,但亦难以避免受感染。
, http://www.100md.com
本研究所见的HBV感染者,多数为单项抗-HBc 阳转。本研究11年观察结果说明[5,6],单项抗-HBc阳性者多数与HBV感染有关。本研究是在有严格安慰剂对照下进行的,因假阳性而产生的偏倚在对比观察中已得到控制。
11年的免疫记忆与国外报道5~7年抗体上升26~147倍[7]、国内7年抗体上升57倍相比[8],有明显减弱。
本研究提示,接种后11年乙肝疫苗预防效果已开始下降,复种问题是否应提到议事日程?应作进一步追踪观察。
参考文献
[1]徐慧文, 左弘, 庄贵华, 等. 国产血源性乙型肝炎疫苗接种后九年效果评价. 中华预防医学杂志, 1998, 32:205-207.
[2]Chen HL, Chang MH, Ni YH, et al. Seroepidemiology of hepatitis B virus infection in children: ten years of mass vaccination in Taiwan. JAMA, 1996, 276:906-908.
, http://www.100md.com
[3]Wainwright RB, Bulkow LR, Parkinson AJ, et al. Protection provided by hepatitis B vaccine in a Yupik Eskimo population- results of a 10-year study. J Infect Dis, 1997, 175:674-677.
[4]Hadler SC, Judson FN, O′Malley PM, et al. Studies of hepatitis B vaccine in homosexual men. Vol 194. London:John Libbey Eurotext Ltd,1990. 165-175.
[5]徐慧文, 王学良, 庄贵华, 等. 乙肝疫苗接种无弱应答与遗传关系的研究. 解放军预防医学杂志, 1998, 16:104-108.
, http://www.100md.com
[6]Jilg W, Sieger E, Zachoval R, et al. Individuals with antibodies hepatitis B core antigen as the only serological marker for hepatitis B infection: high percentage of carriers of hepatitis B and C virus. J Hepatol, 1995, 23:14-20.
[7]West DJ, Calandra GB. Vaccine induced immunologic memory for hepatitis B surface antigen: implications for policy on booster vaccination. Vaccine, 1996, 14: 1019-1027.
[8]李雪翔, 邬嘉生, 刘建福, 等. 小学生接种乙型肝炎血源疫苗后七年效果观察. 中华预防医学杂志, 1996, 30:151-153.
收稿日期:1999-04-01, http://www.100md.com