抑制肠蠕动的小鼠模型的建立
作者:崔生辉 李业鹏 李玉伟 韩春卉 李燕俊 刘红蕾 张靖 江涛
单位:卫生部食品卫生监督检验所,北京 100021
关键词:复方地芬诺酯;抑制肠蠕动的小鼠模型
卫生研究000611 摘要:针对检验保健食品润肠通便功能的实验要求,用5mg/kg BW复方地芬诺酯即可建立稳定的抑制肠蠕动的小鼠模型,在灌服墨汁25min后,计算小鼠小肠墨汁推进距离。
中图分类号:TS207.3 文献标识码:B
文章编号:1000-8020(2000)06-0385-02
Development of a peristaltic inhibition model in mice
, 百拇医药
Cui Shenghui Li Yepeng Li Yuwei Han Chunhui et al
(Institute of Food Safety Control and Inspection, Ministry of Health, Beijing 100021, China)
Abstract:Diphenoxylate was administered to mice at the dose of 5mg/kg BW for the development of peristaltic inhibition model for formulating the examination procedure of health foods. An ink solution containing 5% charcoal was then administered 30 minutes later. The length of ink progradation of the small intestine of mice was calculated 25 minutes after the administration of ink. The results in this model was stable and reliable, and it was recommended to use this model to verify the function of health foods.
, 百拇医药
Key words:diphenoxylate, peristaltic in inhibition model of mice
公认具有润肠通便功能的保健食品有药食同源类中药制剂、食用纤维素、活菌制剂及双歧因子等产品。保健食品与药品的区别在于不能有任何毒副作用。目前,药理学 评价中用50 mg/kg BW复方地芬诺酯建立小鼠便秘模型[1]。而活菌、双歧因子及纤维素等产品的润肠通便作用较温和,故此药效评价中使用的小鼠小肠蠕动抑制模型不适合保健食品的功能检测,作者针对保健食品润肠通便功能检测要求,对小鼠小肠蠕动抑制模型进行了研究,初步提出了适合保健食品润肠通便功能检验 的小鼠蠕动抑制模型的建立方法。
1 材料和方法
1.1 造模药物
复方地芬诺酯片,为止泻药,每片含盐酸地芬诺酯2.37~2.63mg,含硫酸阿托品20.0~30.0μg[2],由江苏国营武进制药厂制造,人体使用剂量为每日3~4次,每次1~2片,即人体的推荐使用剂量为0.125~0.333mg/(kg.d)BW。
, http://www.100md.com
1.2 实验动物
中国医学科学院肿瘤研究所实验动物中心提供的二级昆明种(批准号为京动字8910M050)健康雄性小鼠,体重20~23g,实验前24h各组动物禁食,自由饮水,模型组灌胃给予复方地芬诺酯,对照组给水,小鼠灌胃量为20ml/kg BW。
1.3 仪器与试剂
1.3.1 仪器 分析天平、动物天平、秒表、手术剪、眼科镊、灌胃针及注射器。
1.3.2 试剂 墨汁的配制:准确称取阿拉伯树胶100g,加水800ml,煮沸至溶液透明,称取活性炭粉50g加入上述溶液中煮沸3次,待溶液凉后加水定容到1000ml。
复方地芬诺酯混悬液的配制:取复方地芬诺酯片,用研钵研碎后加水配制成所需浓度的复方地芬诺酯混悬液。
, http://www.100md.com
1.4 实验方法
对照组及模型组小鼠禁食24h(期间自由饮水)。模型组灌胃给予相应浓度的复方地芬诺酯混 悬液,对照组给水,灌胃量20ml/kg BW。给复方地芬诺酯30min后,模型组和对照组均给予墨汁(含5%的活性炭粉、10%阿拉伯树胶),25min后脱颈椎处死动物,立即打开腹腔分离肠系膜,剪取上端自幽门、下端至回盲部的肠管,置于托盘上,轻轻将小肠拉成直线,测量肠管长度为“小肠总长度”,从幽门至墨汁前沿为“墨汁推进长度”,计算墨汁推进率[3]: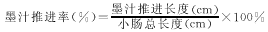
2 实验结果
2.1 复方地芬诺酯药物剂量的筛选
取小鼠70只,随机分为7组,每组10只,分别设为摄入复方地芬诺酯1、3、5、7、10和25 mg /kg BW和空白对照组,模型组按剂量分别给予复方地芬诺酯,测定小鼠小肠墨汁推进率依次为0.67±0.10、0.52±0.07、0.45±0.09、0.37±0.10、0.35±0.08、0.34 ±0.08和0.30±0.05;用方差分析方法进行统计分析,结果与对照组比较均差异具有极 显著性,P<0.01。
, 百拇医药
当复方地芬诺酯给药量达到1mg/kg BW时,模型组小鼠的小肠墨汁推进率与对照组间差异有极显著性(P<0.01),随着给药量的增加小鼠小肠墨汁推进率不断降低,存在剂量-效应关系,当复方地芬诺酯给药量大于5mg/kg BW,墨汁推进率降低速率减慢,在5~25mg/kg BW之间存在一个平台,给药剂量与小肠墨汁推进率的敏感变化范围在0~5mg/kg BW间。
2.2 复方地芬诺酯造模剂量的确定
取小鼠80只,随机分为8组,每组10只,分别设为摄入复方地芬诺酯0.3、1、3、4、5、6和7 mg/kg BW模型组和对照组,模型组按剂量分别给与复方地芬诺酯 ,测定小鼠小肠墨汁推进率依次为0.74±0.10、0.70±0.11、0.53±0.12、0.46±0.12、0.46±0.07、0.40±0.07、0.38±0.10、0.40±0.09,用方差分析方法进行统计分析,结果除0.3mg /kg组外,其余模型对照组与对照组相比差别均有极显著性,P<0.01。
, http://www.100md.com
当复方地芬诺酯给药量达到1mg/kg BW时,模型组小鼠的小肠墨汁推进率与对照组间出现极显著性差异(P<0.01),随着给药量的增加小鼠小肠墨汁推进率不断降低,存在剂量-反应关系,当给药量达到5mg/kg BW时,随着给药量的增加,墨汁推进率的降低幅度超缓,存在一个平台,故5mg/kg BW为小鼠小肠蠕动模型较合适的造模剂量。
2.3 解剖时间的确定
取小鼠30只,分为3组,每组10只,摄入复方地芬诺酯量均为5mg/kg BW,分别在灌胃墨汁15min、20min和25min测定小肠墨汁推进率(%),分别为0.32±0.12、0.41±0.05和0.4 1±0.09。20min与25min墨汁推进率基本一致,在时间上较易控制,建议在灌胃墨汁后25min解剖小鼠,量取小肠墨汁推进长度,计算墨汁推进率。
2.4 实验模型的验证
, http://www.100md.com
以5mg/kg BW的复方地芬诺酯造模进行了3次重复实验,对用t-test方法进行了统计分析,结果见表1。
表1 实验模型墨汁推进率的重复实验 组别
第1次
第2次
第3次
对照组
0.61±0.17
0.79±0.13
0.57±0.18
模型对照组
0.38±0.08(1)
, http://www.100md.com
0.48±0.11(1)
0.33±0.05 (1)
注:(1)与空白对照组比较P<0.01 附表表明,通过多次实验验证,用5mg/kg BW复方地芬诺酯和墨汁指示剂建立的小鼠蠕动抑制模型稳定,变异系数小于30%。
2.5 样品验证
对某保健食品样品用上述模型进行了润肠通便功能检测,结果见表2。
表2 某样品对小鼠小肠推进运动的影响 组别
动物数(只)
墨汁推进率
(%)
, 百拇医药
P
对照组
15
0.61±0.17
模型对照组
15
0.38±0.08(1)
0.000
低剂量
15
0.33±0.05
0.259
, http://www.100md.com 中剂量
14
0.38±0.05
0.844
高剂量
15
0.51±0.09(2)
0.001
注:(1)与对照组比较 P<0.01
(2) 与模型对照组比较 P<0.01
通过统计学处理,经口给予复方地芬诺酯5mg/kg BW小鼠肠蠕动抑制模型成立(P<0.01);其便秘模型小鼠小肠墨汁推进率在高剂量组与模型对照组间比较差异有极显著性(P<0.01),在低、中剂量组与模型对照组间比较差异均无显著性(P>0.05),即高剂量的样品能增加便秘模型小鼠小肠墨汁推进率。
, 百拇医药
3 讨论
复方地芬诺酯的给药量选择:造模药物给药量是造模的关键,选择药物剂量过高会掩盖保健 食品功能的体现,而药物剂量过低其模型稳定,故此在本实验中选择5mg/kg BW复方地芬诺 酯作为造模剂量,对评价保健食品的润肠通便功能较敏感。
墨汁的配制:灌胃墨汁必须按配方自行配制,笔者用市售印度墨汁实验发现,空白对照组在给墨汁2~3min后,墨汁推进率即达80%以上,严重影响实验结果,其原因是普通墨汁中胶体成分较少,而本实验中配制的墨汁,其阿拉伯胶浓度为10%,此墨汁在小鼠小肠内蠕动速度较易掌握。配制墨汁时,应将阿拉伯胶煮沸至透明后再加入炭粉反复煮沸。
作者简介:崔生辉,男,硕士
4 参考文献
1,万锦州.一种简易的小鼠便 秘模型.中国药理学通报,1994,10(1):71-72
2,中华人民共和国卫生部药典委员会编.中华人民共和国药典.北京:化学工业出版社,1995
3,陈奇.中药药理研究方法.北京:人民卫生出版社,1993,333-334
(2000-02-28收稿), 百拇医药
单位:卫生部食品卫生监督检验所,北京 100021
关键词:复方地芬诺酯;抑制肠蠕动的小鼠模型
卫生研究000611 摘要:针对检验保健食品润肠通便功能的实验要求,用5mg/kg BW复方地芬诺酯即可建立稳定的抑制肠蠕动的小鼠模型,在灌服墨汁25min后,计算小鼠小肠墨汁推进距离。
中图分类号:TS207.3 文献标识码:B
文章编号:1000-8020(2000)06-0385-02
Development of a peristaltic inhibition model in mice
, 百拇医药
Cui Shenghui Li Yepeng Li Yuwei Han Chunhui et al
(Institute of Food Safety Control and Inspection, Ministry of Health, Beijing 100021, China)
Abstract:Diphenoxylate was administered to mice at the dose of 5mg/kg BW for the development of peristaltic inhibition model for formulating the examination procedure of health foods. An ink solution containing 5% charcoal was then administered 30 minutes later. The length of ink progradation of the small intestine of mice was calculated 25 minutes after the administration of ink. The results in this model was stable and reliable, and it was recommended to use this model to verify the function of health foods.
, 百拇医药
Key words:diphenoxylate, peristaltic in inhibition model of mice
公认具有润肠通便功能的保健食品有药食同源类中药制剂、食用纤维素、活菌制剂及双歧因子等产品。保健食品与药品的区别在于不能有任何毒副作用。目前,药理学 评价中用50 mg/kg BW复方地芬诺酯建立小鼠便秘模型[1]。而活菌、双歧因子及纤维素等产品的润肠通便作用较温和,故此药效评价中使用的小鼠小肠蠕动抑制模型不适合保健食品的功能检测,作者针对保健食品润肠通便功能检测要求,对小鼠小肠蠕动抑制模型进行了研究,初步提出了适合保健食品润肠通便功能检验 的小鼠蠕动抑制模型的建立方法。
1 材料和方法
1.1 造模药物
复方地芬诺酯片,为止泻药,每片含盐酸地芬诺酯2.37~2.63mg,含硫酸阿托品20.0~30.0μg[2],由江苏国营武进制药厂制造,人体使用剂量为每日3~4次,每次1~2片,即人体的推荐使用剂量为0.125~0.333mg/(kg.d)BW。
, http://www.100md.com
1.2 实验动物
中国医学科学院肿瘤研究所实验动物中心提供的二级昆明种(批准号为京动字8910M050)健康雄性小鼠,体重20~23g,实验前24h各组动物禁食,自由饮水,模型组灌胃给予复方地芬诺酯,对照组给水,小鼠灌胃量为20ml/kg BW。
1.3 仪器与试剂
1.3.1 仪器 分析天平、动物天平、秒表、手术剪、眼科镊、灌胃针及注射器。
1.3.2 试剂 墨汁的配制:准确称取阿拉伯树胶100g,加水800ml,煮沸至溶液透明,称取活性炭粉50g加入上述溶液中煮沸3次,待溶液凉后加水定容到1000ml。
复方地芬诺酯混悬液的配制:取复方地芬诺酯片,用研钵研碎后加水配制成所需浓度的复方地芬诺酯混悬液。
, http://www.100md.com
1.4 实验方法
对照组及模型组小鼠禁食24h(期间自由饮水)。模型组灌胃给予相应浓度的复方地芬诺酯混 悬液,对照组给水,灌胃量20ml/kg BW。给复方地芬诺酯30min后,模型组和对照组均给予墨汁(含5%的活性炭粉、10%阿拉伯树胶),25min后脱颈椎处死动物,立即打开腹腔分离肠系膜,剪取上端自幽门、下端至回盲部的肠管,置于托盘上,轻轻将小肠拉成直线,测量肠管长度为“小肠总长度”,从幽门至墨汁前沿为“墨汁推进长度”,计算墨汁推进率[3]:
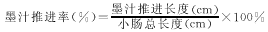
2 实验结果
2.1 复方地芬诺酯药物剂量的筛选
取小鼠70只,随机分为7组,每组10只,分别设为摄入复方地芬诺酯1、3、5、7、10和25 mg /kg BW和空白对照组,模型组按剂量分别给予复方地芬诺酯,测定小鼠小肠墨汁推进率依次为0.67±0.10、0.52±0.07、0.45±0.09、0.37±0.10、0.35±0.08、0.34 ±0.08和0.30±0.05;用方差分析方法进行统计分析,结果与对照组比较均差异具有极 显著性,P<0.01。
, 百拇医药
当复方地芬诺酯给药量达到1mg/kg BW时,模型组小鼠的小肠墨汁推进率与对照组间差异有极显著性(P<0.01),随着给药量的增加小鼠小肠墨汁推进率不断降低,存在剂量-效应关系,当复方地芬诺酯给药量大于5mg/kg BW,墨汁推进率降低速率减慢,在5~25mg/kg BW之间存在一个平台,给药剂量与小肠墨汁推进率的敏感变化范围在0~5mg/kg BW间。
2.2 复方地芬诺酯造模剂量的确定
取小鼠80只,随机分为8组,每组10只,分别设为摄入复方地芬诺酯0.3、1、3、4、5、6和7 mg/kg BW模型组和对照组,模型组按剂量分别给与复方地芬诺酯 ,测定小鼠小肠墨汁推进率依次为0.74±0.10、0.70±0.11、0.53±0.12、0.46±0.12、0.46±0.07、0.40±0.07、0.38±0.10、0.40±0.09,用方差分析方法进行统计分析,结果除0.3mg /kg组外,其余模型对照组与对照组相比差别均有极显著性,P<0.01。
, http://www.100md.com
当复方地芬诺酯给药量达到1mg/kg BW时,模型组小鼠的小肠墨汁推进率与对照组间出现极显著性差异(P<0.01),随着给药量的增加小鼠小肠墨汁推进率不断降低,存在剂量-反应关系,当给药量达到5mg/kg BW时,随着给药量的增加,墨汁推进率的降低幅度超缓,存在一个平台,故5mg/kg BW为小鼠小肠蠕动模型较合适的造模剂量。
2.3 解剖时间的确定
取小鼠30只,分为3组,每组10只,摄入复方地芬诺酯量均为5mg/kg BW,分别在灌胃墨汁15min、20min和25min测定小肠墨汁推进率(%),分别为0.32±0.12、0.41±0.05和0.4 1±0.09。20min与25min墨汁推进率基本一致,在时间上较易控制,建议在灌胃墨汁后25min解剖小鼠,量取小肠墨汁推进长度,计算墨汁推进率。
2.4 实验模型的验证
, http://www.100md.com
以5mg/kg BW的复方地芬诺酯造模进行了3次重复实验,对用t-test方法进行了统计分析,结果见表1。
表1 实验模型墨汁推进率的重复实验 组别
第1次
第2次
第3次
对照组
0.61±0.17
0.79±0.13
0.57±0.18
模型对照组
0.38±0.08(1)
, http://www.100md.com
0.48±0.11(1)
0.33±0.05 (1)
注:(1)与空白对照组比较P<0.01 附表表明,通过多次实验验证,用5mg/kg BW复方地芬诺酯和墨汁指示剂建立的小鼠蠕动抑制模型稳定,变异系数小于30%。
2.5 样品验证
对某保健食品样品用上述模型进行了润肠通便功能检测,结果见表2。
表2 某样品对小鼠小肠推进运动的影响 组别
动物数(只)
墨汁推进率
(%)
, 百拇医药
P
对照组
15
0.61±0.17
模型对照组
15
0.38±0.08(1)
0.000
低剂量
15
0.33±0.05
0.259
, http://www.100md.com 中剂量
14
0.38±0.05
0.844
高剂量
15
0.51±0.09(2)
0.001
注:(1)与对照组比较 P<0.01
(2) 与模型对照组比较 P<0.01
通过统计学处理,经口给予复方地芬诺酯5mg/kg BW小鼠肠蠕动抑制模型成立(P<0.01);其便秘模型小鼠小肠墨汁推进率在高剂量组与模型对照组间比较差异有极显著性(P<0.01),在低、中剂量组与模型对照组间比较差异均无显著性(P>0.05),即高剂量的样品能增加便秘模型小鼠小肠墨汁推进率。
, 百拇医药
3 讨论
复方地芬诺酯的给药量选择:造模药物给药量是造模的关键,选择药物剂量过高会掩盖保健 食品功能的体现,而药物剂量过低其模型稳定,故此在本实验中选择5mg/kg BW复方地芬诺 酯作为造模剂量,对评价保健食品的润肠通便功能较敏感。
墨汁的配制:灌胃墨汁必须按配方自行配制,笔者用市售印度墨汁实验发现,空白对照组在给墨汁2~3min后,墨汁推进率即达80%以上,严重影响实验结果,其原因是普通墨汁中胶体成分较少,而本实验中配制的墨汁,其阿拉伯胶浓度为10%,此墨汁在小鼠小肠内蠕动速度较易掌握。配制墨汁时,应将阿拉伯胶煮沸至透明后再加入炭粉反复煮沸。
作者简介:崔生辉,男,硕士
4 参考文献
1,万锦州.一种简易的小鼠便 秘模型.中国药理学通报,1994,10(1):71-72
2,中华人民共和国卫生部药典委员会编.中华人民共和国药典.北京:化学工业出版社,1995
3,陈奇.中药药理研究方法.北京:人民卫生出版社,1993,333-334
(2000-02-28收稿), 百拇医药