骨肿瘤的CT诊断
作者:余文昌 王仁法
单位:余文昌(武汉,同济医科大学附属同济医院CT室 430030); 王仁法(武汉,同济医科大学附属同济医院CT室 430030)
关键词:
临床放射学杂志000217 影像学检查方法已成为诊断骨肿瘤的主要手段。应用CT对骨肿瘤的研究,迄今有十几年历史。CT扫描以独特的密度分辨率和清晰的横断解剖关系显示了它的优越性,可以区别出组织密度差别极小的肌肉、软骨,还可进行不同平面的图像重建三维观察,并具有安全、无创、快速、准确的特点。CT检查骨肿瘤主要目的不是单一解决诊断问题,同时可显示肿瘤与周围组织的关系,侵犯骨的范围,骨髓受累情况以及病变与神经血管的关系[1](图1)。
1 检查方法
1.1 平扫
, http://www.100md.com
根据体检所获信息,先扫描获得前后位或侧位定位像,再于定位像上确定扫描范围。扫描应包括健侧同时进行,以便于对照;在肩关节和膝关节附近的恶性肿瘤,应连续扫描到髓腔表现正常时终止[2]。层厚8~10mm,或确定兴趣区后用2~3mm层厚薄层扫描。国外文献[3]报道骨盆扫描层厚5mm,四肢骨近侧扫描层厚10mm,远侧扫描层厚3mm。观察骨结构窗位100~150HU。软组织病变或骨病变的软组织部分窗宽400HU,窗位0~20HU。骨髓瘤造成骨质疏松破坏,选择窗宽窗位时要适当调整。
1.2 增强扫描
静脉注射水溶性对比剂后行增强扫描,可以提高病灶显示率。在下列情况下需作增强扫描:(1)疑有等密度软组织肿块; (2)了解主要血管受侵情况; (3)了解软组织肿块内供血情况; (4)欲根据增强扫描特点帮助定性或进行鉴别诊断。增强扫描多用一次性大剂量注射,必要时在注射对比剂后对感兴趣区层面进行连续动态扫描,扫描时间间隔为5~15秒,总时间为3~5分钟,之后绘制时间-密度曲线,良性肿瘤的曲线与正常肌肉几乎没有差别。若数秒内曲线陡峭上升且达到高峰,则可能为富血管的恶性肿瘤[4]。Hudson等[5]报道50例巨细胞瘤运用CT增强扫描,48例明确骨肿瘤扩展的范围及与主要血管的关系。国外也有学者认为骨肿瘤患者CT检查不必作平扫而直接增强扫描[6]。
, 百拇医药
2 骨关节正常CT表现
CT横断面可以显示皮质骨、松质骨、骨小梁、骨髓腔、关节腔、包绕骨关节的软组织成分。皮质连续完整,密度均匀。连续扫描层面观察可见皮质有规律变化,如由厚到薄,或由薄到厚或由薄到厚再到薄。松质骨内见骨小梁分布,表现为细束状骨质影,其排列规律由它所在部位生物力学决定。骨髓腔CT值为负值(-100~-200HU),当肿瘤侵犯骨髓腔时,即使未钙化的骨样组织(CT值约20~40HU)也可以被衬托出来。Helms等[7]认为两侧肢体骨髓腔的CT值相差20HU则属异常。扫描层面通过关节腔时,CT图像可以清晰显示相邻骨间的关节面,双侧对称,高分辨率CT可以分清皮肤、皮下脂肪、肌肉,肌肉间常有脂肪分隔。
3 良性骨肿瘤CT征象
病灶区密度减低,多呈膨胀性,边缘清楚,皮质完整或者受压破坏后形成骨壳,一般无骨外软组织肿块(图2);或皮质轻度中断,突入软组织,则形成边界清楚局限性软组织肿块,有时可见散在钙化,骨膜较少受累[8]。
, http://www.100md.com
4 恶性骨肿瘤CT征象[9~13]
4.1 骨的弥漫浸润性破坏(图3)
表现为筛孔样、虫噬样(皮质骨)、斑片状(松质骨)。这种不同形态的骨破坏主要是肿瘤对骨侵蚀程度和部位不同,不能作为肿瘤定性依据。
4.2 瘤骨
基本形态有3种:(1) 象牙状瘤骨:表现为高密度骨影呈象牙质样,无骨小梁结构,成团块状聚集于肿瘤一处,与周围组织分界清楚。(2) 棉絮状瘤骨:表现呈团片状分布于骨或软组织肿块内,密度低,边缘模糊如棉絮样。(3) 针状瘤骨:表现为位于骨皮质外,与皮质垂直,细长而直,平行排列。
4.3 瘤软骨(图4)
钙化呈环形或半环形,恶性骨肿瘤环形钙化最多见于软骨肉瘤,其次为骨肉瘤。
, 百拇医药
4.4 骨肿瘤的反应骨和残留骨
4.4.1 反应骨: 骨受到肿瘤的破坏后,骨膜或骨髓内新生骨叫反应骨。它是正常骨组织,不是肿瘤特有征象。CT表现为骨破坏灶周围产生散在片状骨化影。骨膜反应即为肿瘤刺激骨膜成骨细胞活动增强,产生新骨。恶性骨肿瘤早期可见单层骨膜反应,晚期出现多层、“葱皮”样、梳状骨膜反应。特别值得注意的是骨膜反应常为肿瘤突破、中断,形成Codman三角。Codman三角在CT表现为越远离肿瘤中心,骨膜反应越淡、越薄,越近肿瘤中心骨膜反应越明显、越厚,并在肿瘤中心突然中断,中断处被肿瘤组织填充。CT因大多数情况下只能做横断扫描,须结合上下连续多个层面才能判断骨干长轴的Codman三角,而横断上的Codman三角能在CT上直观显示[14]。
4.4.2 骨肿瘤内残留骨: 原来骨结构被肿瘤破坏后残留下来的骨组织叫残留骨(图5)。残留骨皮质表现为皮质骨残缺不齐,密度较高。残留的松质骨表现为疏松的小梁结构,边缘模糊,密度较低。
, http://www.100md.com
4.5 软组织肿块(图6)
恶性骨肿瘤生长迅速,极易突破骨皮质向软组织内浸润。CT表现为软组织肿块无明确界限,其内可见瘤骨及环形钙化。骨肿瘤尤其是恶性骨肿瘤CT征象复杂多样,缺乏可用于定性的“金标准”,正确的诊断要掌握好上述骨肿瘤的共同CT表现,并结合临床资料、X线平片进行综合分析。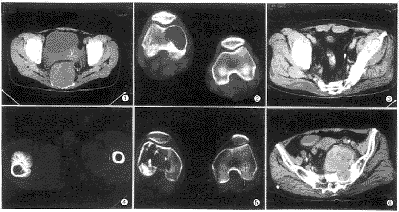
图1 骶骨骨巨细胞瘤。CT平扫示骶骨破坏,肿块推压子宫、直肠向盆腔左侧移位 图2 右股骨下端骨巨细胞瘤。CT扫描示骨质破坏区略有膨胀,边缘清楚,皮质完整 图3 左耻骨上支滑膜肉瘤术后,左髂骨转移,呈斑片状破坏,边界模糊不清 图4 右股骨小转子处骨软骨瘤恶变,瘤软骨清晰可见 图5 右股骨下端成骨肉瘤。大片状破坏区内可见点状、条状残留骨 图6 骶骨恶性肿瘤。CT扫描示骶骨破坏并见巨大软组织肿块
5 CT用于骨肿瘤诊断进展
, http://www.100md.com
5.1 技术方面
投入临床运行的CT机均具有多平面重建(MPR)功能。骨肿瘤常规轴位扫描后,利用该功能软件,可重建出冠状位和矢状位影像。现代螺旋CT装有三维重建软件,对骨肿瘤病灶扫描层厚愈薄,重建三维图像阶梯状伪影愈少。但扫描层厚变薄,意味着扫描层数增加,球管负荷加重和患者所受辐射剂量加大。国外文献报道,综合考虑图像质量和扫描层数这对矛盾因素,用4mm层厚,3mm层距扫描为宜[15]。扫描完毕后,在工作站上用最大密度投影法(MIP),重建出三维立体图像。
5.2 临床价值[16]
肿瘤的MPR可提供更多有价值的诊断信息,如进一步观察肿瘤的范围、边缘、中心、立体形态、骨膜反应的各种形式,有助于评估正常骨组织和肿瘤病灶之间的界面,有助于观察虫噬样、浸润性筛孔状等骨质破坏形式。肿瘤引起的病理性骨折,轴扫时因与扫描层面平行而未显示或模糊不清,在MPR的冠状位或矢状位得以清楚显示。医学影像医师主要对诊断感兴趣,对外科医师来说病理程度及与周围组织的关系都同样重要。3-D影像能立体显示肿瘤发源部位、骨破坏程度、肿瘤大小、密度、毗邻等多方面的信息,将MPR影像所反映的感兴趣区的细节集合装配成一幅“立体图画”,给人更加直观明朗的印象,有利于手术方案的设置和放疗方案的模拟。■
, 百拇医药
参考文献:
[1]张雪哲,王武.正确应用肌肉骨骼系统的影像学检查.中华放射学杂志, 1998, 32:437
[2]Mail JT, Cohen MD, Mirkin LD,et al. Response of osteosarcoma to preoperative intravenous high-dose methotrexate chemotherapy: CT evaluation. AJR, 1985, 144:89
[3]Schoenberg NY, Beltran J. Contrast enhancement in musculoskeletal imaging: Current status. The Radiologic Clinics of North America, 1994, 32:337
, http://www.100md.com
[4]Mass R, Heller M. Computer tomographic des skelettsystems. Roentgenpraxis, 1990, 43:293
[5]Hudson TM, Schieblerm, Springfield DS,et al. Radiology of giant cell tumors of bone: Computed tomography, artho-tomography and scintigraphy. Skeletal Radiology, 1984, 11:85
[6]Levine E, Lee K, Neff JR,et al. Comparsion of computed tomography and other imaging modalities in the evaluation of muskuloskeletal tumors. Radiology, 1979, 131:431
, 百拇医药
[7]Helms CA, Cann CC, Brunelle F,et al. Detection of bone-marrow metastasis using quantitative computed tomography. Radiology, 1981, 140:745
[8]黄兆民,孟悛非,肖官惠,等.65例骨肿瘤或瘤样病变CT错误诊分析.临床放射学杂志, 1998, 17:162
[9]Davies AM, Wellings RM. Imaging of bone tumors. Curr Opin Radiology, 1992, 4:32
[10]Tyrrell PH, Davies AM. Magnetic resonace imaging appearances of fatigue fractures of the lower limb. BJR, 1994, 67:332
, http://www.100md.com
[11]Wellings RM, Davies AM, Pynsent PB,et al. The value of computed tomographic measurements in osteosarcoma as a predictor of response to adjuvant chemotherapy. Clin Radiology, 1994, 49:19
[12]Alonsodesantos L, Goldstein H, Murray JA,et al. Computed tomography in the evaluation of musculoskeletal neoplasms. Radiology, 1978, 128:89
[13]Simon MA, Finn HA, Chicago,et al. Diagnostic strategy for bone and soft-tissue tumors. The Journal of Bone and Joint Surgey, 1993, 75:622
, 百拇医药
[14]孟悛非,陈应明.骨肉瘤的CT征象.中华放射学杂志, 1999, 33:196
[15]Magid D. Two-dimensional and three-dimensional computed tomographic imaging in musculoskeletal tumors. Radiologic Clinics of North America, 1993, 31:425
[16]Logan PM, Connell DG, Connell J,et al. Imaging-guided percutaneous biopsy of musculoskeletal tumors: An algorithm for selection of specific biopsy techniques. AJR, 1996, 166:137
收稿日期:1999-01-11
修稿日期:1999-06-17, 百拇医药
单位:余文昌(武汉,同济医科大学附属同济医院CT室 430030); 王仁法(武汉,同济医科大学附属同济医院CT室 430030)
关键词:
临床放射学杂志000217 影像学检查方法已成为诊断骨肿瘤的主要手段。应用CT对骨肿瘤的研究,迄今有十几年历史。CT扫描以独特的密度分辨率和清晰的横断解剖关系显示了它的优越性,可以区别出组织密度差别极小的肌肉、软骨,还可进行不同平面的图像重建三维观察,并具有安全、无创、快速、准确的特点。CT检查骨肿瘤主要目的不是单一解决诊断问题,同时可显示肿瘤与周围组织的关系,侵犯骨的范围,骨髓受累情况以及病变与神经血管的关系[1](图1)。
1 检查方法
1.1 平扫
, http://www.100md.com
根据体检所获信息,先扫描获得前后位或侧位定位像,再于定位像上确定扫描范围。扫描应包括健侧同时进行,以便于对照;在肩关节和膝关节附近的恶性肿瘤,应连续扫描到髓腔表现正常时终止[2]。层厚8~10mm,或确定兴趣区后用2~3mm层厚薄层扫描。国外文献[3]报道骨盆扫描层厚5mm,四肢骨近侧扫描层厚10mm,远侧扫描层厚3mm。观察骨结构窗位100~150HU。软组织病变或骨病变的软组织部分窗宽400HU,窗位0~20HU。骨髓瘤造成骨质疏松破坏,选择窗宽窗位时要适当调整。
1.2 增强扫描
静脉注射水溶性对比剂后行增强扫描,可以提高病灶显示率。在下列情况下需作增强扫描:(1)疑有等密度软组织肿块; (2)了解主要血管受侵情况; (3)了解软组织肿块内供血情况; (4)欲根据增强扫描特点帮助定性或进行鉴别诊断。增强扫描多用一次性大剂量注射,必要时在注射对比剂后对感兴趣区层面进行连续动态扫描,扫描时间间隔为5~15秒,总时间为3~5分钟,之后绘制时间-密度曲线,良性肿瘤的曲线与正常肌肉几乎没有差别。若数秒内曲线陡峭上升且达到高峰,则可能为富血管的恶性肿瘤[4]。Hudson等[5]报道50例巨细胞瘤运用CT增强扫描,48例明确骨肿瘤扩展的范围及与主要血管的关系。国外也有学者认为骨肿瘤患者CT检查不必作平扫而直接增强扫描[6]。
, 百拇医药
2 骨关节正常CT表现
CT横断面可以显示皮质骨、松质骨、骨小梁、骨髓腔、关节腔、包绕骨关节的软组织成分。皮质连续完整,密度均匀。连续扫描层面观察可见皮质有规律变化,如由厚到薄,或由薄到厚或由薄到厚再到薄。松质骨内见骨小梁分布,表现为细束状骨质影,其排列规律由它所在部位生物力学决定。骨髓腔CT值为负值(-100~-200HU),当肿瘤侵犯骨髓腔时,即使未钙化的骨样组织(CT值约20~40HU)也可以被衬托出来。Helms等[7]认为两侧肢体骨髓腔的CT值相差20HU则属异常。扫描层面通过关节腔时,CT图像可以清晰显示相邻骨间的关节面,双侧对称,高分辨率CT可以分清皮肤、皮下脂肪、肌肉,肌肉间常有脂肪分隔。
3 良性骨肿瘤CT征象
病灶区密度减低,多呈膨胀性,边缘清楚,皮质完整或者受压破坏后形成骨壳,一般无骨外软组织肿块(图2);或皮质轻度中断,突入软组织,则形成边界清楚局限性软组织肿块,有时可见散在钙化,骨膜较少受累[8]。
, http://www.100md.com
4 恶性骨肿瘤CT征象[9~13]
4.1 骨的弥漫浸润性破坏(图3)
表现为筛孔样、虫噬样(皮质骨)、斑片状(松质骨)。这种不同形态的骨破坏主要是肿瘤对骨侵蚀程度和部位不同,不能作为肿瘤定性依据。
4.2 瘤骨
基本形态有3种:(1) 象牙状瘤骨:表现为高密度骨影呈象牙质样,无骨小梁结构,成团块状聚集于肿瘤一处,与周围组织分界清楚。(2) 棉絮状瘤骨:表现呈团片状分布于骨或软组织肿块内,密度低,边缘模糊如棉絮样。(3) 针状瘤骨:表现为位于骨皮质外,与皮质垂直,细长而直,平行排列。
4.3 瘤软骨(图4)
钙化呈环形或半环形,恶性骨肿瘤环形钙化最多见于软骨肉瘤,其次为骨肉瘤。
, 百拇医药
4.4 骨肿瘤的反应骨和残留骨
4.4.1 反应骨: 骨受到肿瘤的破坏后,骨膜或骨髓内新生骨叫反应骨。它是正常骨组织,不是肿瘤特有征象。CT表现为骨破坏灶周围产生散在片状骨化影。骨膜反应即为肿瘤刺激骨膜成骨细胞活动增强,产生新骨。恶性骨肿瘤早期可见单层骨膜反应,晚期出现多层、“葱皮”样、梳状骨膜反应。特别值得注意的是骨膜反应常为肿瘤突破、中断,形成Codman三角。Codman三角在CT表现为越远离肿瘤中心,骨膜反应越淡、越薄,越近肿瘤中心骨膜反应越明显、越厚,并在肿瘤中心突然中断,中断处被肿瘤组织填充。CT因大多数情况下只能做横断扫描,须结合上下连续多个层面才能判断骨干长轴的Codman三角,而横断上的Codman三角能在CT上直观显示[14]。
4.4.2 骨肿瘤内残留骨: 原来骨结构被肿瘤破坏后残留下来的骨组织叫残留骨(图5)。残留骨皮质表现为皮质骨残缺不齐,密度较高。残留的松质骨表现为疏松的小梁结构,边缘模糊,密度较低。
, http://www.100md.com
4.5 软组织肿块(图6)
恶性骨肿瘤生长迅速,极易突破骨皮质向软组织内浸润。CT表现为软组织肿块无明确界限,其内可见瘤骨及环形钙化。骨肿瘤尤其是恶性骨肿瘤CT征象复杂多样,缺乏可用于定性的“金标准”,正确的诊断要掌握好上述骨肿瘤的共同CT表现,并结合临床资料、X线平片进行综合分析。

图1 骶骨骨巨细胞瘤。CT平扫示骶骨破坏,肿块推压子宫、直肠向盆腔左侧移位 图2 右股骨下端骨巨细胞瘤。CT扫描示骨质破坏区略有膨胀,边缘清楚,皮质完整 图3 左耻骨上支滑膜肉瘤术后,左髂骨转移,呈斑片状破坏,边界模糊不清 图4 右股骨小转子处骨软骨瘤恶变,瘤软骨清晰可见 图5 右股骨下端成骨肉瘤。大片状破坏区内可见点状、条状残留骨 图6 骶骨恶性肿瘤。CT扫描示骶骨破坏并见巨大软组织肿块
5 CT用于骨肿瘤诊断进展
, http://www.100md.com
5.1 技术方面
投入临床运行的CT机均具有多平面重建(MPR)功能。骨肿瘤常规轴位扫描后,利用该功能软件,可重建出冠状位和矢状位影像。现代螺旋CT装有三维重建软件,对骨肿瘤病灶扫描层厚愈薄,重建三维图像阶梯状伪影愈少。但扫描层厚变薄,意味着扫描层数增加,球管负荷加重和患者所受辐射剂量加大。国外文献报道,综合考虑图像质量和扫描层数这对矛盾因素,用4mm层厚,3mm层距扫描为宜[15]。扫描完毕后,在工作站上用最大密度投影法(MIP),重建出三维立体图像。
5.2 临床价值[16]
肿瘤的MPR可提供更多有价值的诊断信息,如进一步观察肿瘤的范围、边缘、中心、立体形态、骨膜反应的各种形式,有助于评估正常骨组织和肿瘤病灶之间的界面,有助于观察虫噬样、浸润性筛孔状等骨质破坏形式。肿瘤引起的病理性骨折,轴扫时因与扫描层面平行而未显示或模糊不清,在MPR的冠状位或矢状位得以清楚显示。医学影像医师主要对诊断感兴趣,对外科医师来说病理程度及与周围组织的关系都同样重要。3-D影像能立体显示肿瘤发源部位、骨破坏程度、肿瘤大小、密度、毗邻等多方面的信息,将MPR影像所反映的感兴趣区的细节集合装配成一幅“立体图画”,给人更加直观明朗的印象,有利于手术方案的设置和放疗方案的模拟。■
, 百拇医药
参考文献:
[1]张雪哲,王武.正确应用肌肉骨骼系统的影像学检查.中华放射学杂志, 1998, 32:437
[2]Mail JT, Cohen MD, Mirkin LD,et al. Response of osteosarcoma to preoperative intravenous high-dose methotrexate chemotherapy: CT evaluation. AJR, 1985, 144:89
[3]Schoenberg NY, Beltran J. Contrast enhancement in musculoskeletal imaging: Current status. The Radiologic Clinics of North America, 1994, 32:337
, http://www.100md.com
[4]Mass R, Heller M. Computer tomographic des skelettsystems. Roentgenpraxis, 1990, 43:293
[5]Hudson TM, Schieblerm, Springfield DS,et al. Radiology of giant cell tumors of bone: Computed tomography, artho-tomography and scintigraphy. Skeletal Radiology, 1984, 11:85
[6]Levine E, Lee K, Neff JR,et al. Comparsion of computed tomography and other imaging modalities in the evaluation of muskuloskeletal tumors. Radiology, 1979, 131:431
, 百拇医药
[7]Helms CA, Cann CC, Brunelle F,et al. Detection of bone-marrow metastasis using quantitative computed tomography. Radiology, 1981, 140:745
[8]黄兆民,孟悛非,肖官惠,等.65例骨肿瘤或瘤样病变CT错误诊分析.临床放射学杂志, 1998, 17:162
[9]Davies AM, Wellings RM. Imaging of bone tumors. Curr Opin Radiology, 1992, 4:32
[10]Tyrrell PH, Davies AM. Magnetic resonace imaging appearances of fatigue fractures of the lower limb. BJR, 1994, 67:332
, http://www.100md.com
[11]Wellings RM, Davies AM, Pynsent PB,et al. The value of computed tomographic measurements in osteosarcoma as a predictor of response to adjuvant chemotherapy. Clin Radiology, 1994, 49:19
[12]Alonsodesantos L, Goldstein H, Murray JA,et al. Computed tomography in the evaluation of musculoskeletal neoplasms. Radiology, 1978, 128:89
[13]Simon MA, Finn HA, Chicago,et al. Diagnostic strategy for bone and soft-tissue tumors. The Journal of Bone and Joint Surgey, 1993, 75:622
, 百拇医药
[14]孟悛非,陈应明.骨肉瘤的CT征象.中华放射学杂志, 1999, 33:196
[15]Magid D. Two-dimensional and three-dimensional computed tomographic imaging in musculoskeletal tumors. Radiologic Clinics of North America, 1993, 31:425
[16]Logan PM, Connell DG, Connell J,et al. Imaging-guided percutaneous biopsy of musculoskeletal tumors: An algorithm for selection of specific biopsy techniques. AJR, 1996, 166:137
收稿日期:1999-01-11
修稿日期:1999-06-17, 百拇医药