�ӳ�������K+ͨ�����˸ΰ�ϸ����ֳ�е�����
���ߣ��� �� ��Т˼ ������ ���మ ��ź�
��λ���� �� ��Т˼ ������ ����ҽ�ƴ�ѧ����ҽԺ��ͨ��ƣ����� 100083�����మ ��ź� ������ѧ����Ĥ��Ĥ���﹤�̹����ص�ʵ����
�ؼ��ʣ��ӳ�������K+ͨ���������ϸ������л����ͨ������Ƥ�������ӣ�ҩ��ѧ
����ҽ�ƴ�ѧѧ��990409 ժ Ҫ Ŀ�ģ��о��ӳ�������K+ͨ�����˸ΰ�ϸ����ֳ�е����á�����������ĤƬǯ������ȫϸ����¼��ʽ��¼�˸ΰ�ϸ���ڲ�ͬŨ��EGF���ӳ�������K+ͨ���Ŀ�Ĥ����������백�ǵ�������ऺ���(3H-TdR)���뼼���۲�EGF��K+ͨ����ϼ�(TEA)���˸ΰ�ϸ��DNA�ϳɵ�Ӱ�졣��������ֱ�Ƥ��������(EGF)�ٽ��ΰ�ϸ����ֳ��ͬʱʹ�ΰ�ϸ��Ĥ����ͨ���Ŀ�ĤK+�������ӡ�K+ͨ����ϼ����Ұ�(TEA)����������EGF�ٽ�DNA�ϳɵ����ã��������Ե���Ч��ϵ��ʱ�������ԣ�����ϸ���Ļ���������Ӱ�졣���ۣ��˸ΰ�ϸ������ֳ���Ҫ�ӳ�������K+ͨ�����롣
, ��Ĵҽҩ
�й�ͼ�����Ϸ��෨����� R735.7
The role of delayed rectifier K+ channel
in the proliferation of the human hepatocyte carcinoma cells
FU Wei��, ZHOU Xiao-Si , ZHANG Zong-Ming, ZHOU Pei-Ai, WU Cai-Hong
(#Department of General Surgery, the Third Hospital, Beijing Medical University, Beijing 100083)
ABSTRACT Objective: To study the role of the delayed rectifier K+ channel in the proliferation of the human hepatocyte carcinoma cells. Methods: The transmembrane current of human hepatocyte carcinoma cells was recorded by the whole-cell recording technique of patch clamp in different concentration of EGF. The effect of EGF and K+ channel blocker on the DNA synthesis of human hepatic carcinoma cells was observed by 3H-TdR incorporation technique. Results: EGF promoted the cell proliferatetion of the human hepatocyte carcinoma cells. At the same time, EGF made the K+ channel current of hepatocyte carcinoma cells increased. TEA of K+ channel blocker could significantly inhibited DNA synthesis induced by EGF. There was a linear relationship between the concentration of TEA and the effect of inhibition as well as time-dependence. But TEA didn't reduce the viability of hepatocyte carcinoma cells. Conclusion: K+ channel was necessary for the proliferation of the human hepatocyte carcinoma cells.
, ��Ĵҽҩ
MeSH Delayed rectifier K+ channel�� Carcinoma hepatocellular/metab Potassium channels
Endothelial growth factor/pharmacol
���ܰ�ϸ��[1]���˵��鰩ϸ��ϵMCF-2[2]���˺�ɫ����ϸ��[3]�и���K+ͨ����ϸ������ֳ�йء���ʵ���������Ƿ����˸ΰ�ϸ�������ӳ�������K+ͨ���Ļ�����[4]���о�K+ͨ�����˸ΰ�ϸ��ϵBEL-7402ϸ����ֳ�е����á�
1 �����뷽��
1.1 ϸ��ϵ
, http://www.100md.com
�˸ΰ�ϸ��ϵBEL-7402�ɱ���ҽ�ƴ�ѧҩѧ����ѧ�����������͡�
1.2 ��Ҫ����
�缫������(Narishige, PP-83, Japan)��EPC-7ĤƬǯ�Ŵ���(List, Darmstadt Co., Germany)��5.5.1��PClamp���źŲɼ��������ݲɼ�ϵͳ(Axon Instrument, Inc., USA)��
1.3 ��Ҫ�Լ�
�������Ұ�(TEA-Cl),Mg-ATP,KF��ΪSigma��Ʒ��RPMI1640������(Gibco)��EGF(Boehringer Mannheim),3H-TdR(�Ϻ�ԭ�����о���)��
1.4 ϸ����Һ�͵缫Һ�������Լ������缫���Ʊ�
, ��Ĵҽҩ
ϸ����Һ�͵缫Һ�������Լ������缫���Ʊ����ο�����[4]��
1.5 �˸ΰ�ϸ��ϵBEL-7402ϸ������
��ϸ��������ƿ�г��ɵ����ת��35 mm��10 mm����������������м�������48 h��,������Ҫ���ڸ����������зֱ����һ������EGF��TEA�������ж��ߵ�RPMI1640����Һ��������24 h�������ȫϸ����ʽ��¼ϸ���Ŀ�Ĥ������ͬʱ����ϸ���������ⶨ3H-TdR�����cpmֵ��
1.6 ȫϸ��ĤƬǯ��¼
����������,�������������£�����ȫϸ��ĤƬǯ�ļ�¼(������)��
1.7 ���ݴ�����ͳ�Ʒ���
���������� ��s��ʾ��������t�����������������Լ��飬�Զ������ݵ�����Բ���ֱ�ع�ķ����������ϵ�����м��顣
��s��ʾ��������t�����������������Լ��飬�Զ������ݵ�����Բ���ֱ�ع�ķ����������ϵ�����м��顣
, ��Ĵҽҩ
2 ���
2.1 EGF�Ըΰ�ϸ���ӳ�������K+ͨ����Ӱ��
��ͬ����Ũ�ȵ�EGF����ϸ��������Һ������24 h����ĤƬǯ��ȫϸ����¼��ʽ��¼ϸ���Ŀ�Ĥ��������ǯ�Ƶ�ѹ(holding potential, HP)=-100 mV�����Ե�ѹ(test potential,TP)=-100��90 mV�����£���ͬTP�Ŀ�Ĥ����ITP������(��1)��EGF�Ըΰ�ϸ��Ĥ���ӳ�������K+ͨ����ѹ�ſ�������Ӱ�죬ʹ��Ĥ������ǿ��
2.2 EGF�Ըΰ�ϸ��������Ӱ��
ϸ���ں���0��1��10��20 ��g.L-1 EGF������Һ�зֱ�����24 h��ϸ�������ֱ�Ϊ32��5(��104����n=4)��35��7(��104����n=4)��47��7(��104����n=4)��56��11(��104����n=4)������EGFʹϸ����Ŀ�������ӣ��ٽ�ϸ������ֳ��
, http://www.100md.com
2.3 �Ըΰ�ϸ��������Ӱ��
�ں���10 ��g.L-1 EGF������Һ��������ϸ������Ϊ2�飬�ֱ������Ũ��0��20 mmol.L-1 TEA����24 h����4 g.L-1̨����Ⱦɫ����ϸ������������TEA��ϸ�������Ϊ0.918[279(��)/304(��)]����δ��TEA��Ϊ0.946[315(��)/333(��)]�����߲�����������(��2=2.005 3��P=0.156 8)��
2.4 EGF������EGF��K+ͨ����ϼ�(TEA)�Ըΰ�ϸ��DNA�ϳɵ�Ӱ��
2.4.1 EGF�����Ըΰ�ϸ��DNA�ϳɵ�Ӱ�� ϸ���ں��в�ͬ����Ũ��EGF������Һ�зֱ�����24 h��3H-TdR�����ⶨcpm(ͼ1��Without TEA��)��EGF���Դٽ�DNA�ĺϳɡ�
, http://www.100md.com
��1 ��ͬ����Ũ�ȵ�EGF���˸ΰ�ϸ��ϵBEL-7402
ϸ����Ĥ����ITP��Ӱ��( ��s)
��s)
Table 1 The effect of different mass concentration of EGF
on the transmembrane current of carcinoma cells
of cell line BEL-7402( ��s)I/pA TP
��s)I/pA TP
(mV)
, http://www.100md.com
��(EGF)/��g.L-1
0(n=12)
1(n=11)
10(n=12)
20(n=9)
-100
-63��35
-64��30
-79��22
-82��21
-90
-46��34
, http://www.100md.com
-38��25
-49��27
-39��24
-80
-23��37
-15��23
-9��33
6��39
-70
-2��42
9��31
33��29��
, ��Ĵҽҩ 53��60��
-60
24��45
35��42
69��34��
110��78����
-50
50��49
57��53
113��42����
155��92����
, ��Ĵҽҩ
-40
82��63
86��66
154��47����
206��101����
-30
112��80
123��81
208��42����
259��112����
-20
, http://www.100md.com
142��92
164��96
264��47����
316��125����
-10
175��110
211��114
326��55����
378��128����
0
217��124
, ��Ĵҽҩ
268��131
387��67����
445��134����
10
261��143
328��146
450��78����
515��139����
20
301��166
407��154
, ��Ĵҽҩ
516��88����
606��130����
30
362��179
483��164
593��95����
689��128����
40
423��195
564��182
682��108����
, http://www.100md.com
773��123����
50
501��210
661��192
781��129����
880��122����
60
605��217
759��204
889��138����
997��138����
, ��Ĵҽҩ
70
718��230
872��233
1017��163����
1150��158����
80
838��238
887��362
1146��171����
1250��201����
90
, ��Ĵҽҩ
961��257
1128��261
1298��217����
1386��248����
There was significant difference ,the groups of 10 ��g.L-1 and 20 ��g.L-1 were compared with the group of 0 ��g.L-1 at TP=-70��90 mV level.There was not significant difference,the group of 1 ��g.L-1 was compared with the group of 0 ��g.L-1 at TP=-100��90 mV level.
, ��Ĵҽҩ
2.4.2 10 mmol.L-1��TEA�벻ͬ����Ũ�ȵ�EGF��DNA�ϳɵ�Ӱ�� 10 ��mol.L-1 TEA�뺬�в�ͬ����Ũ��EGF������Һ��ͬ����ϸ��24 h��3H-TdR�����ⶨcpmֵ(ͼ1)��
2.4.3 ��ͬŨ�ȵ�TEA��10 ��g.L-1��EGF�Ըΰ�ϸ��DNA�ϳɵ�Ӱ�� �ں���10 ��g.L-1 EGF��ϸ���������У��ټ���0��5��10��20 mmol.L-14�ֲ�ͬŨ�ȵ�TEA������24 h����3H-TdR�����ⶨ��cpmֵ(ͼ2)��
2.4.4 �ں���10 ��g.L-1 EGF���������������ĸΰ�ϸ���Ӵ�TEA(10 mmol.L-1)��ʱ���DNA�ϳɵ�Ӱ�� �ú���10 ��g.L-1 EGF������Һ�����ΰ�ϸ�����ֱ��ڽ���3H-TdR����ǰ23��18��12 h�Ͳ���ǰ���̼���TEA��ʹ��Ũ��Ϊ10 mmol.L-1��Ȼ��ⶨ��cpmֵ(ͼ3)��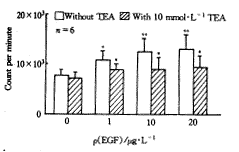
, http://www.100md.com
* the group of 10 mmol.L-1 TEA was compared with the group of without TEA, P<0.05; +, the group of 0 ��g.L-1 EGF was compared with the group of other EGF concentration, P<0.05, ++P<0.01; ��, mass concentration.
ͼ1 10 mmol.L-1 TEA�Ըΰ�ϸ���ڲ�ͬ����Ũ�ȵ�EGF��DNA�ϳɵ�Ӱ��(n=6)
Figure 1 The effect of 10 mmol.L-1 TEA on the liver
, ��Ĵҽҩ
carcinoma cells in the different mass concentration of EGF(n=6)
** P<0.01, compared with 0 mmol.L-1 TEA�� ��s in each point was the result of six paralleling samples; c, concentration.
��s in each point was the result of six paralleling samples; c, concentration.
ͼ2 TEAŨ����EGF(10 ��g.L-1)��������
�ΰ�ϸ��DNA�ϳ����Ĺ�ϵ(ͼ��ÿһ��Ϊ6��ƽ�б걾
, ��Ĵҽҩ
�ⶨ����� ��s)
��s)
Figure 2 The relationship of the concentration of EGF
with the DNA synthesis of liver carcinoma cells
in the culture medium (EGF 10 ��g.L-1)
3 ����
Ik��������ȿ��˷�����֯��ϸ������Ҫ�����������λ�ĸ����ࡢ������λ�ļ��ں�ά�ֲ�Ӧ�ڵ�����[5]��K+ͨ��������ϸ���е��������б��棬�����˵��鰩ϸ��ϵMCF-2�У����ֵ絼Ϊ23pS��K+ͨ����ϸ������ֳ�������[2]�����˺�ɫ����ϸ�����о���ͬ��������������ϸ����Ik��ϸ������ֳ�й�[3]��
, ��Ĵҽҩ
�ڱ�ʵ����EGF������ʹ�˸ΰ�ϸ��ϵBEL-7402ϸ������Ŀ(2.2)��DNA�ϳ�����(ͼ1)����������Һ�е�EGF����Ũ�����ߣ���������Ҳ�����ԡ�����EGF�ܴٽ��ΰ�ϸ��ϵBEL-7402ϸ������ֳ�����ⲻͬ����Ũ�ȵ�EGFʹϸ���Ŀ�Ĥ������������(��1)��10��20 ��g.L-1 EGF���Ըı����˸ΰ�ϸ��ϵBEL-7402ϸ��Ik�ĵ�ѹ�ſ����ԡ����ϱ���EGF�ڴٽ�ϸ����ֳ��ͬʱ��K+ͨ�����ţ�IkҲ������ʾ�ΰ�ϸ����ֳ�Ĺ�������ҪK+ͨ���Ŀ��š�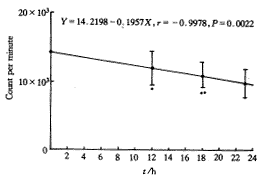
* P<0.05, ** P<0.01, compared with 0 hour; t, contacting 10 mmol.L-1 TEA time�� each point was ��s of six paralleling samples.
��s of six paralleling samples.
, ��Ĵҽҩ
ͼ3 ϸ���ں���10 ��g.L-1 EGF����������
��10 mmol.L-1 TEA�Ӵ���ʱ���DNA�ϳɵ�
Ӱ��(ͼ��ÿһ��Ϊ6��ƽ�б걾�ⶨ����� ��s)
��s)
Figure 3 The effect of 10 ��g.L-1 EGF culture medium
with 10 mmol.L-1 TEA on DNA synthesis of liver
carcinoma cells in at different contacting time
, ��Ĵҽҩ
�ڼ��벻ͬ����Ũ��EGF������Һ�У�10 mmol.L-1��K+ͨ����������ϼ�TEA������������DNA�ĺϳɣ�ʹ3H-TdR�����cpmֵ�½�����δ����TEA�Ķ�������Ȳ�����������(ͼ1)����TEA��ϸ���Ĵ������Ӱ��(���2.3)��˵��TEA����DNA�ĺϳɲ������ڶ�ϸ����ֱ�Ӷ������ã���������TEA�����K+ͨ�������DZ������иΰ�ϸ����ֳ��ͬʱ��ҪK+ͨ�����ŵĵ�2��֤�ݡ�
��ͼ1��EGF 0 ��g.L-1�飬TEA�����ò����ԣ�����ʾ�ڸΰ�ϸ���ķ���ֳ�ڼ䣬TEA��ֱ������DNA�ĺϳɣ�����EGF�ٽ�ϸ����ֳ�ڼ䣬��K+ͨ������������ߺ�K+ͨ����ϼ��ż���DNA�ϳɣ�ͬʱTEA�Ըΰ�ϸ���������á����DZ������иΰ�ϸ����ֳ��ҪK+ͨ�����ŵĵ�3��֤�ݡ�
, ��Ĵҽҩ
TEA�ļ���������DNA�ϳɵķ���֮�������Ե���Ч��ϵ(ͼ2)���ΰ�ϸ���ں���10 mmol.L-1 EGF������Һ����10 mmol.L-1 TEA�����ĽӴ�ʱ��������EGF�ٽ�DNA�ϳɵ����ñ����Ƶij̶�Ҳ�����ԣ�����������TEA�Ӵ�ʱ�������������DNA�ϳɵ�����Ҳ��ǿ(ͼ3)����ϸ�������ļ�����TEA�Ըΰ�ϸ����ֳ��Ӱ��Ƕ�������(���2.3)�����DZ�������Ϊ�ΰ�ϸ������ֳ���ҪK+ͨ��������һ�����ṩ�ĵ�4���������ݡ�
EGF�����Ӱ���˸ΰ�ϸ��ϵBEL-7402ϸ����K+ͨ��?Ŀǰ����ȷ�Ľ��ۣ��˸ΰ�ϸ������EGF����[6]��EGF���˸ΰ�ϸ��ϵBEL-7402ϸ��Ĥ�ϵ������Ϻ���ͨ������ø�͵��������ữϵͳ�Լ�G-����;��Ӱ��K+ͨ�������ڿ��˷���ϸ�����������о�[7]�������ӳ�������K+ͨ������Ca2+ͨ��[8]��EGFʹK+ͨ���ĵ�ѹ�ſ����Է����˸ı䣬ʹCa2+�������ӣ��༴K+ͨ������Ϊϸ����Ca2+���ӽ���ϸ�����ṩ��ͨ����
, ��Ĵҽҩ
�� ���ɴʡ�
�����
1 Lewis R, Cahalan M. Ion channels and signal transduction in lymphocytes. Annu Physiol, 1990,52:415-430
2 Wangman EA, Young JA, Cook DI.A 23-PS Ca2+-activated K+ channel in MCF-7 human breast carcinoma cells: an apparent correlation of channel incidence proliferation. Pflugers Arch, 1991,417:562-570
3 Lepple-Wienhuesk A, Berweck S, Bohming M, et al. K+ channels and the intracellular calcium signal in melanoma cell proliferation. J Membr Biol, 1996��151:149-157
, ��Ĵҽҩ
4 �� ���������������మ����.�˸ΰ�ϸ��Ĥ����ͨ�������о�. ����ҽ�ƴ�ѧѧ��. 1998��30:115
5 Rudy B. Diversity and ubiquity of K channels. Neuroscience, 1988��25:729-749
6 ����������������ط�. �˸ΰ�ϸ������EGFR�ı����EGF�Ըΰ�ϸ�������Ĵٽ�����. ʵ������ѧ��, 1989,22:445-453
7 Brown AM. Membrance-delimited cell signaling complexes:direct ion channel regulation by G proteins. J Membrance Biol, 1993,131:93-104
8 Inoue ISAO. Activation-inactivation of potassium channels and development of the potassium channel spile in internally perfused squid giant axon. J Gen Physiol, 1987,78:43-61
(1998-08-26�ո�), ��Ĵҽҩ
��λ���� �� ��Т˼ ������ ����ҽ�ƴ�ѧ����ҽԺ��ͨ��ƣ����� 100083�����మ ��ź� ������ѧ����Ĥ��Ĥ���﹤�̹����ص�ʵ����
�ؼ��ʣ��ӳ�������K+ͨ���������ϸ������л����ͨ������Ƥ�������ӣ�ҩ��ѧ
����ҽ�ƴ�ѧѧ��990409 ժ Ҫ Ŀ�ģ��о��ӳ�������K+ͨ�����˸ΰ�ϸ����ֳ�е����á�����������ĤƬǯ������ȫϸ����¼��ʽ��¼�˸ΰ�ϸ���ڲ�ͬŨ��EGF���ӳ�������K+ͨ���Ŀ�Ĥ����������백�ǵ�������ऺ���(3H-TdR)���뼼���۲�EGF��K+ͨ����ϼ�(TEA)���˸ΰ�ϸ��DNA�ϳɵ�Ӱ�졣��������ֱ�Ƥ��������(EGF)�ٽ��ΰ�ϸ����ֳ��ͬʱʹ�ΰ�ϸ��Ĥ����ͨ���Ŀ�ĤK+�������ӡ�K+ͨ����ϼ����Ұ�(TEA)����������EGF�ٽ�DNA�ϳɵ����ã��������Ե���Ч��ϵ��ʱ�������ԣ�����ϸ���Ļ���������Ӱ�졣���ۣ��˸ΰ�ϸ������ֳ���Ҫ�ӳ�������K+ͨ�����롣
, ��Ĵҽҩ
�й�ͼ�����Ϸ��෨����� R735.7
The role of delayed rectifier K+ channel
in the proliferation of the human hepatocyte carcinoma cells
FU Wei��, ZHOU Xiao-Si , ZHANG Zong-Ming, ZHOU Pei-Ai, WU Cai-Hong
(#Department of General Surgery, the Third Hospital, Beijing Medical University, Beijing 100083)
ABSTRACT Objective: To study the role of the delayed rectifier K+ channel in the proliferation of the human hepatocyte carcinoma cells. Methods: The transmembrane current of human hepatocyte carcinoma cells was recorded by the whole-cell recording technique of patch clamp in different concentration of EGF. The effect of EGF and K+ channel blocker on the DNA synthesis of human hepatic carcinoma cells was observed by 3H-TdR incorporation technique. Results: EGF promoted the cell proliferatetion of the human hepatocyte carcinoma cells. At the same time, EGF made the K+ channel current of hepatocyte carcinoma cells increased. TEA of K+ channel blocker could significantly inhibited DNA synthesis induced by EGF. There was a linear relationship between the concentration of TEA and the effect of inhibition as well as time-dependence. But TEA didn't reduce the viability of hepatocyte carcinoma cells. Conclusion: K+ channel was necessary for the proliferation of the human hepatocyte carcinoma cells.
, ��Ĵҽҩ
MeSH Delayed rectifier K+ channel�� Carcinoma hepatocellular/metab Potassium channels
Endothelial growth factor/pharmacol
���ܰ�ϸ��[1]���˵��鰩ϸ��ϵMCF-2[2]���˺�ɫ����ϸ��[3]�и���K+ͨ����ϸ������ֳ�йء���ʵ���������Ƿ����˸ΰ�ϸ�������ӳ�������K+ͨ���Ļ�����[4]���о�K+ͨ�����˸ΰ�ϸ��ϵBEL-7402ϸ����ֳ�е����á�
1 �����뷽��
1.1 ϸ��ϵ
, http://www.100md.com
�˸ΰ�ϸ��ϵBEL-7402�ɱ���ҽ�ƴ�ѧҩѧ����ѧ�����������͡�
1.2 ��Ҫ����
�缫������(Narishige, PP-83, Japan)��EPC-7ĤƬǯ�Ŵ���(List, Darmstadt Co., Germany)��5.5.1��PClamp���źŲɼ��������ݲɼ�ϵͳ(Axon Instrument, Inc., USA)��
1.3 ��Ҫ�Լ�
�������Ұ�(TEA-Cl),Mg-ATP,KF��ΪSigma��Ʒ��RPMI1640������(Gibco)��EGF(Boehringer Mannheim),3H-TdR(�Ϻ�ԭ�����о���)��
1.4 ϸ����Һ�͵缫Һ�������Լ������缫���Ʊ�
, ��Ĵҽҩ
ϸ����Һ�͵缫Һ�������Լ������缫���Ʊ����ο�����[4]��
1.5 �˸ΰ�ϸ��ϵBEL-7402ϸ������
��ϸ��������ƿ�г��ɵ����ת��35 mm��10 mm����������������м�������48 h��,������Ҫ���ڸ����������зֱ����һ������EGF��TEA�������ж��ߵ�RPMI1640����Һ��������24 h�������ȫϸ����ʽ��¼ϸ���Ŀ�Ĥ������ͬʱ����ϸ���������ⶨ3H-TdR�����cpmֵ��
1.6 ȫϸ��ĤƬǯ��¼
����������,�������������£�����ȫϸ��ĤƬǯ�ļ�¼(������)��
1.7 ���ݴ�����ͳ�Ʒ���
����������
 ��s��ʾ��������t�����������������Լ��飬�Զ������ݵ�����Բ���ֱ�ع�ķ����������ϵ�����м��顣
��s��ʾ��������t�����������������Լ��飬�Զ������ݵ�����Բ���ֱ�ع�ķ����������ϵ�����м��顣, ��Ĵҽҩ
2 ���
2.1 EGF�Ըΰ�ϸ���ӳ�������K+ͨ����Ӱ��
��ͬ����Ũ�ȵ�EGF����ϸ��������Һ������24 h����ĤƬǯ��ȫϸ����¼��ʽ��¼ϸ���Ŀ�Ĥ��������ǯ�Ƶ�ѹ(holding potential, HP)=-100 mV�����Ե�ѹ(test potential,TP)=-100��90 mV�����£���ͬTP�Ŀ�Ĥ����ITP������(��1)��EGF�Ըΰ�ϸ��Ĥ���ӳ�������K+ͨ����ѹ�ſ�������Ӱ�죬ʹ��Ĥ������ǿ��
2.2 EGF�Ըΰ�ϸ��������Ӱ��
ϸ���ں���0��1��10��20 ��g.L-1 EGF������Һ�зֱ�����24 h��ϸ�������ֱ�Ϊ32��5(��104����n=4)��35��7(��104����n=4)��47��7(��104����n=4)��56��11(��104����n=4)������EGFʹϸ����Ŀ�������ӣ��ٽ�ϸ������ֳ��
, http://www.100md.com
2.3 �Ըΰ�ϸ��������Ӱ��
�ں���10 ��g.L-1 EGF������Һ��������ϸ������Ϊ2�飬�ֱ������Ũ��0��20 mmol.L-1 TEA����24 h����4 g.L-1̨����Ⱦɫ����ϸ������������TEA��ϸ�������Ϊ0.918[279(��)/304(��)]����δ��TEA��Ϊ0.946[315(��)/333(��)]�����߲�����������(��2=2.005 3��P=0.156 8)��
2.4 EGF������EGF��K+ͨ����ϼ�(TEA)�Ըΰ�ϸ��DNA�ϳɵ�Ӱ��
2.4.1 EGF�����Ըΰ�ϸ��DNA�ϳɵ�Ӱ�� ϸ���ں��в�ͬ����Ũ��EGF������Һ�зֱ�����24 h��3H-TdR�����ⶨcpm(ͼ1��Without TEA��)��EGF���Դٽ�DNA�ĺϳɡ�
, http://www.100md.com
��1 ��ͬ����Ũ�ȵ�EGF���˸ΰ�ϸ��ϵBEL-7402
ϸ����Ĥ����ITP��Ӱ��(
 ��s)
��s)Table 1 The effect of different mass concentration of EGF
on the transmembrane current of carcinoma cells
of cell line BEL-7402(
 ��s)I/pA TP
��s)I/pA TP(mV)
, http://www.100md.com
��(EGF)/��g.L-1
0(n=12)
1(n=11)
10(n=12)
20(n=9)
-100
-63��35
-64��30
-79��22
-82��21
-90
-46��34
, http://www.100md.com
-38��25
-49��27
-39��24
-80
-23��37
-15��23
-9��33
6��39
-70
-2��42
9��31
33��29��
, ��Ĵҽҩ 53��60��
-60
24��45
35��42
69��34��
110��78����
-50
50��49
57��53
113��42����
155��92����
, ��Ĵҽҩ
-40
82��63
86��66
154��47����
206��101����
-30
112��80
123��81
208��42����
259��112����
-20
, http://www.100md.com
142��92
164��96
264��47����
316��125����
-10
175��110
211��114
326��55����
378��128����
0
217��124
, ��Ĵҽҩ
268��131
387��67����
445��134����
10
261��143
328��146
450��78����
515��139����
20
301��166
407��154
, ��Ĵҽҩ
516��88����
606��130����
30
362��179
483��164
593��95����
689��128����
40
423��195
564��182
682��108����
, http://www.100md.com
773��123����
50
501��210
661��192
781��129����
880��122����
60
605��217
759��204
889��138����
997��138����
, ��Ĵҽҩ
70
718��230
872��233
1017��163����
1150��158����
80
838��238
887��362
1146��171����
1250��201����
90
, ��Ĵҽҩ
961��257
1128��261
1298��217����
1386��248����
There was significant difference ,the groups of 10 ��g.L-1 and 20 ��g.L-1 were compared with the group of 0 ��g.L-1 at TP=-70��90 mV level.There was not significant difference,the group of 1 ��g.L-1 was compared with the group of 0 ��g.L-1 at TP=-100��90 mV level.
, ��Ĵҽҩ
2.4.2 10 mmol.L-1��TEA�벻ͬ����Ũ�ȵ�EGF��DNA�ϳɵ�Ӱ�� 10 ��mol.L-1 TEA�뺬�в�ͬ����Ũ��EGF������Һ��ͬ����ϸ��24 h��3H-TdR�����ⶨcpmֵ(ͼ1)��
2.4.3 ��ͬŨ�ȵ�TEA��10 ��g.L-1��EGF�Ըΰ�ϸ��DNA�ϳɵ�Ӱ�� �ں���10 ��g.L-1 EGF��ϸ���������У��ټ���0��5��10��20 mmol.L-14�ֲ�ͬŨ�ȵ�TEA������24 h����3H-TdR�����ⶨ��cpmֵ(ͼ2)��
2.4.4 �ں���10 ��g.L-1 EGF���������������ĸΰ�ϸ���Ӵ�TEA(10 mmol.L-1)��ʱ���DNA�ϳɵ�Ӱ�� �ú���10 ��g.L-1 EGF������Һ�����ΰ�ϸ�����ֱ��ڽ���3H-TdR����ǰ23��18��12 h�Ͳ���ǰ���̼���TEA��ʹ��Ũ��Ϊ10 mmol.L-1��Ȼ��ⶨ��cpmֵ(ͼ3)��

, http://www.100md.com
* the group of 10 mmol.L-1 TEA was compared with the group of without TEA, P<0.05; +, the group of 0 ��g.L-1 EGF was compared with the group of other EGF concentration, P<0.05, ++P<0.01; ��, mass concentration.
ͼ1 10 mmol.L-1 TEA�Ըΰ�ϸ���ڲ�ͬ����Ũ�ȵ�EGF��DNA�ϳɵ�Ӱ��(n=6)
Figure 1 The effect of 10 mmol.L-1 TEA on the liver
, ��Ĵҽҩ
carcinoma cells in the different mass concentration of EGF(n=6)

** P<0.01, compared with 0 mmol.L-1 TEA��
 ��s in each point was the result of six paralleling samples; c, concentration.
��s in each point was the result of six paralleling samples; c, concentration.ͼ2 TEAŨ����EGF(10 ��g.L-1)��������
�ΰ�ϸ��DNA�ϳ����Ĺ�ϵ(ͼ��ÿһ��Ϊ6��ƽ�б걾
, ��Ĵҽҩ
�ⶨ�����
 ��s)
��s)Figure 2 The relationship of the concentration of EGF
with the DNA synthesis of liver carcinoma cells
in the culture medium (EGF 10 ��g.L-1)
3 ����
Ik��������ȿ��˷�����֯��ϸ������Ҫ�����������λ�ĸ����ࡢ������λ�ļ��ں�ά�ֲ�Ӧ�ڵ�����[5]��K+ͨ��������ϸ���е��������б��棬�����˵��鰩ϸ��ϵMCF-2�У����ֵ絼Ϊ23pS��K+ͨ����ϸ������ֳ�������[2]�����˺�ɫ����ϸ�����о���ͬ��������������ϸ����Ik��ϸ������ֳ�й�[3]��
, ��Ĵҽҩ
�ڱ�ʵ����EGF������ʹ�˸ΰ�ϸ��ϵBEL-7402ϸ������Ŀ(2.2)��DNA�ϳ�����(ͼ1)����������Һ�е�EGF����Ũ�����ߣ���������Ҳ�����ԡ�����EGF�ܴٽ��ΰ�ϸ��ϵBEL-7402ϸ������ֳ�����ⲻͬ����Ũ�ȵ�EGFʹϸ���Ŀ�Ĥ������������(��1)��10��20 ��g.L-1 EGF���Ըı����˸ΰ�ϸ��ϵBEL-7402ϸ��Ik�ĵ�ѹ�ſ����ԡ����ϱ���EGF�ڴٽ�ϸ����ֳ��ͬʱ��K+ͨ�����ţ�IkҲ������ʾ�ΰ�ϸ����ֳ�Ĺ�������ҪK+ͨ���Ŀ��š�

* P<0.05, ** P<0.01, compared with 0 hour; t, contacting 10 mmol.L-1 TEA time�� each point was
 ��s of six paralleling samples.
��s of six paralleling samples., ��Ĵҽҩ
ͼ3 ϸ���ں���10 ��g.L-1 EGF����������
��10 mmol.L-1 TEA�Ӵ���ʱ���DNA�ϳɵ�
Ӱ��(ͼ��ÿһ��Ϊ6��ƽ�б걾�ⶨ�����
 ��s)
��s)Figure 3 The effect of 10 ��g.L-1 EGF culture medium
with 10 mmol.L-1 TEA on DNA synthesis of liver
carcinoma cells in at different contacting time
, ��Ĵҽҩ
�ڼ��벻ͬ����Ũ��EGF������Һ�У�10 mmol.L-1��K+ͨ����������ϼ�TEA������������DNA�ĺϳɣ�ʹ3H-TdR�����cpmֵ�½�����δ����TEA�Ķ�������Ȳ�����������(ͼ1)����TEA��ϸ���Ĵ������Ӱ��(���2.3)��˵��TEA����DNA�ĺϳɲ������ڶ�ϸ����ֱ�Ӷ������ã���������TEA�����K+ͨ�������DZ������иΰ�ϸ����ֳ��ͬʱ��ҪK+ͨ�����ŵĵ�2��֤�ݡ�
��ͼ1��EGF 0 ��g.L-1�飬TEA�����ò����ԣ�����ʾ�ڸΰ�ϸ���ķ���ֳ�ڼ䣬TEA��ֱ������DNA�ĺϳɣ�����EGF�ٽ�ϸ����ֳ�ڼ䣬��K+ͨ������������ߺ�K+ͨ����ϼ��ż���DNA�ϳɣ�ͬʱTEA�Ըΰ�ϸ���������á����DZ������иΰ�ϸ����ֳ��ҪK+ͨ�����ŵĵ�3��֤�ݡ�
, ��Ĵҽҩ
TEA�ļ���������DNA�ϳɵķ���֮�������Ե���Ч��ϵ(ͼ2)���ΰ�ϸ���ں���10 mmol.L-1 EGF������Һ����10 mmol.L-1 TEA�����ĽӴ�ʱ��������EGF�ٽ�DNA�ϳɵ����ñ����Ƶij̶�Ҳ�����ԣ�����������TEA�Ӵ�ʱ�������������DNA�ϳɵ�����Ҳ��ǿ(ͼ3)����ϸ�������ļ�����TEA�Ըΰ�ϸ����ֳ��Ӱ��Ƕ�������(���2.3)�����DZ�������Ϊ�ΰ�ϸ������ֳ���ҪK+ͨ��������һ�����ṩ�ĵ�4���������ݡ�
EGF�����Ӱ���˸ΰ�ϸ��ϵBEL-7402ϸ����K+ͨ��?Ŀǰ����ȷ�Ľ��ۣ��˸ΰ�ϸ������EGF����[6]��EGF���˸ΰ�ϸ��ϵBEL-7402ϸ��Ĥ�ϵ������Ϻ���ͨ������ø�͵��������ữϵͳ�Լ�G-����;��Ӱ��K+ͨ�������ڿ��˷���ϸ�����������о�[7]�������ӳ�������K+ͨ������Ca2+ͨ��[8]��EGFʹK+ͨ���ĵ�ѹ�ſ����Է����˸ı䣬ʹCa2+�������ӣ��༴K+ͨ������Ϊϸ����Ca2+���ӽ���ϸ�����ṩ��ͨ����
, ��Ĵҽҩ
�� ���ɴʡ�
�����
1 Lewis R, Cahalan M. Ion channels and signal transduction in lymphocytes. Annu Physiol, 1990,52:415-430
2 Wangman EA, Young JA, Cook DI.A 23-PS Ca2+-activated K+ channel in MCF-7 human breast carcinoma cells: an apparent correlation of channel incidence proliferation. Pflugers Arch, 1991,417:562-570
3 Lepple-Wienhuesk A, Berweck S, Bohming M, et al. K+ channels and the intracellular calcium signal in melanoma cell proliferation. J Membr Biol, 1996��151:149-157
, ��Ĵҽҩ
4 �� ���������������మ����.�˸ΰ�ϸ��Ĥ����ͨ�������о�. ����ҽ�ƴ�ѧѧ��. 1998��30:115
5 Rudy B. Diversity and ubiquity of K channels. Neuroscience, 1988��25:729-749
6 ����������������ط�. �˸ΰ�ϸ������EGFR�ı����EGF�Ըΰ�ϸ�������Ĵٽ�����. ʵ������ѧ��, 1989,22:445-453
7 Brown AM. Membrance-delimited cell signaling complexes:direct ion channel regulation by G proteins. J Membrance Biol, 1993,131:93-104
8 Inoue ISAO. Activation-inactivation of potassium channels and development of the potassium channel spile in internally perfused squid giant axon. J Gen Physiol, 1987,78:43-61
(1998-08-26�ո�), ��Ĵҽҩ