»±―θ–‘ΖΈΕ·¬ωΗΏ―Ι¥σ σΖΈΕ·¬ω“Μ―θΜ·ΒΣΚœΟΗΒΡ Β―ι―–ΨΩ*
Ής’ΏΘΚ¥ό―ύΡœ ¬μ”τΈΡ Ε≈Ψϋ±Θ
ΒΞΈΜΘΚ±±Ψ©“ΫΩΤ¥σ―ßΒΎ“Μ“Ϋ‘ΚΕυΩΤ,±±Ψ© 100034
ΙΊΦϋ¥ ΘΚΗΏ―Σ―ΙΘΜΖΈ–‘ΘΜΝς––≤Γ―ßΘΜ“Μ―θΜ·ΒΣΚœΟΗΓνΘΜΖΈΕ·¬ωΘΜΟΗ―ßΘΜ“Μ―θΜ·ΒΣΘΜ―Σ“Κ
±±Ψ©“ΫΩΤ¥σ―ß―ß±®990619 ’Σ “Σ ΡΩΒΡΘΚ―–ΨΩ¥σ σΖΈΕ·¬ω÷–“Μ―θΜ·ΒΣΚœΟΗ(nitric oxide synthase, NOS)ΒΡΚ§ΝΩΦΑΖ÷≤Φ±δΜ·”κ¬ΐ–‘»±―θ–‘ΖΈΕ·¬ωΗΏ―Ι(hypoxic pulmonary hypertension, HPH)ΖΔ…ζΒΡΙΊœΒΓΘΖΫΖ®ΘΚ≤…”ΟeNOSΕύΩΥ¬ΓΩΙΧεΘ§Ε‘¬ΐ–‘HPH¥σ σΒΡΖΈΉι÷·Ϋχ––Οβ“ΏΉι÷·Μ·―ßΖ÷ΈωΘ§Ιέ≤λ»±―θΉιΦΑΕ‘’’Ήι¥σ σΗςΦΕΖΈΕ·¬ω÷–eNOSΚ§ΝΩΦΑΕ®ΈΜΘΜΆ§ ±”Π”ΟΖ÷ΙβΙβΕ»ΦΤ≤βΕ®»±―θΉιΦΑΕ‘’’Ήι¥σ σ―ΣΫ§÷–NOΒΡΦδΫ”≈®Ε»ΓΘΫαΙϊΘΚ’ΐ≥Θ¥σ σΖΈΕ·¬ωΡΎΤΛœΗΑϊΦΑΤΫΜ§ΦΓœΗΑϊΨυΚ§”–ΫœΗΏΒΡeNOS±μ¥οΘ§«“ΗςΦΕΖΈΕ·¬ω÷–eNOSΚ§ΝΩ≤ν“λΈόœ‘÷χ–‘ΘΜ»±―θΉι¥σ σΗςΦΕΖΈΕ·¬ωΡΎΤΛœΗΑϊΦΑΤΫΜ§ΦΓœΗΑϊeNOSΚ§ΝΩΨυΫœΕ‘’’Ήιœ‘÷χΦθ…ΌΘΜ»±―θΉι¥σ σ―ΣΫ§NOΦδΫ”≈®Ε»ΫœΕ‘’’ΉιΟςœ‘ΫΒΒΆΓΘΫα¬έΘΚ¥σ σΖΈΕ·¬ωΡΎΤΛœΗΑϊΚΆΤΫΜ§ΦΓœΗΑϊeNOSΚ§ΝΩœ¬ΫΒΦΑ―ΣΫ§NO≈®Ε»œ¬ΫΒ≤Έ”κ¬ΐ–‘HPHΒΡ–Έ≥…ΓΘ
, ΑΌΡ¥“Ϋ“©
÷–ΙζΆΦ ιΉ ΝœΖ÷άύΖ®Ζ÷άύΚ≈ R563-332
A study on endothelial nitric oxide synthase in pulmonary arteries
of hypoxic pulmonary hypertensive rats
CUI Yan-Nan, MA Yu-Wenȧ DU Jun-Bao
(Department of Pediatrics, the First Hospital, Beijing Medical University, Beijing 100034)
MeSH Hypertension, pulmonary/epidemiol Nitric oxide synthaseΓν Pulmonary artery/enzymol Nitric oxide/blood
, ΑΌΡ¥“Ϋ“©
ABSTRACT Objective: To study the abundance and localization of nitric oxide synthase (NOS) in pulmonary arteries of rats and to explore the relationship between their changes and chronic hypoxic pulmonary hypertension (HPH). Methods: Immunohistochemistry technique was performed on the lung tissues of the HPH rats with eNOS multiclonal antibody to assay the abundance and localization of eNOS in different segments of pulmonary arteries of the hypoxic and control rats. At the same time, the plasma concentration of nitric oxide (NO) metabolite, nitrite, was measured by spectrophotometry. Results: eNOS expression was found in pulmonary artery endothelial cells and smooth muscle cells, and there was no significant difference among the different segments of pulmonary arteries, whereas the eNOS expression was inhibited in endothelial cells and smooth muscle cells of pulmonary arteries in hypoxia group; The plasma concentration of nitrite in hypoxia group was significantly decreased compared with that of control rats. Conclusion: The results suggest that the decrease in eNOS in pulmonary artery endothelial cells and smooth muscle cells by hypoxia as well as the decrease in plasma concentration of NO may play a role in the development of chronic HPH.
, ΑΌΡ¥“Ϋ“©
(J Beijing Med Univ, 1999,31:552-554)
»±―θ–‘ΖΈΕ·¬ωΗΏ―Ι( hypoxic pulmonary hypertension, HPH) «Εύ÷÷–ΡΖΈΦ≤≤ΓΖΔ’ΙΙΐ≥Χ÷–ΒΡ≤Γάμ…ζάμΜΖΫΎΘ§ΤδΖΔ…ζΜζ÷Τ…–Έ¥Άξ»Ϊ«ε≥ΰΓΘ―–ΨΩΖΔœ÷―ΣΙήΡΎΤΛœΗΑϊ≤ζ…ζΒΡ“Μ―θΜ·ΒΣ(nitric oxide, NO)‘ΎHPHΒΡΖΔ…ζΜζ÷Τ÷–Τπ÷Ί“ΣΒςΫΎΉς”ΟΓΘΕ·Έο Β―ι±μΟςΆβ‘¥–‘L-ΨΪΑ±Υα(L-Arginine, L-Arg)Θ§Ω… ΙNOΚœ≥…‘ωΕύΘ§¥”ΕχΫΒΒΆΖΈΕ·¬ω―ΙΝΠ;Ζ¥÷°Ηχ”ηNOΚœΟΗ(nitric oxide synthase, NOS)“÷÷ΤΦΝ»γL-ΨΪΑ±ΥαΦΉ÷§(NΠΊ-L-Arginine methyl ester, L-NAME)ΉΔ…δΘ§‘ρΩ… ΙNOΚœ≥…Φθ…ΌΘ§÷¬ΖΈΕ·¬ω―ΙΝΠΫχ“Μ≤Ϋ…ΐΗΏΓΘNOS «NOΚœ≥…÷–÷Ί“ΣΒΡœόΥΌΟΗΓΘΤυΫώΈΣ÷ΙΙΊ”Ύ¬ΐ–‘HPH ±ΖΈΕ·¬ω÷–NOΧεœΒΘ§ΧΊ±π «ΖΈΕ·¬ωΡΎΤΛœΗΑϊΦΑΤΫΜ§ΦΓœΗΑϊΡΎΡΎΤΛ‘¥–‘NOS (endothelial NOS, eNOS)Κ§ΝΩΦΑΕ®ΈΜΒΡ―–ΨΩΫœ…ΌΓΘΈ“Ο«”Π”ΟeNOSΕύΩΥ¬ΓΩΙΧεΘ§Ε‘¬ΐ–‘HPH¥σ σΒΡΖΈΉι÷·Ϋχ––Οβ“ΏΉι÷·Μ·―ßΖ÷ΈωΘ§”κ’ΐ≥Θ«ιΩωœ¬ΖΈΕ·¬ωeNOSΒΡΚ§ΝΩΦΑΕ®ΈΜœύΕ‘±»Θ§―–ΨΩHPH ±Θ§ΖΈΕ·¬ωeNOSΚ§ΝΩ±δΜ·ΦΑΤδΕ®ΈΜΘ§ΧΫΧ÷NOSΕ‘HPHΒΡΒςΫΎΉς”ΟΓΘ
, ΑΌΡ¥“Ϋ“©
1 ≤ΡΝœ”κΖΫΖ®
1.1 Ϋ®ΝΔ»±―θ–‘ΖΈΕ·¬ωΗΏ―ΙΡΘ–Ά
–έ–‘Wistar¥σ σΙ≤12÷ΜΘ§Χε÷Ί200ΓΪ300gΘ§ΥφΜζΖ÷ΈΣ»±―θΉιΦΑΕ‘’’ΉιΘ§Ης6÷ΜΓΘΫΪ»±―θΉι¥σ σ÷Ο”ΎCG1–Ά≥Θ―ΙΒΆ―θœδΡΎ(÷–Ιζ“Ϋ―ßΩΤ―ß‘ΚΜυ¥Γ“Ϋ―ß―–ΨΩΥυ)Θ§Ά®»κΒΣΤχΘ§ ΙœδΡΎ―θΧεΜΐΖ÷ ΐ‘Ύ30minΉσ”“¥ο(10.0Γά0.5)%Θ§ΟΩΧλ»±―θ6hΘ§Ι≤»±―θ1÷ήΓΘΕ‘’’Ήι¥σ σΚτΈϋ “ΡΎΩ’ΤχΓΘ Β―ιΤΎΦδΝΫΉι¥σ σ‘ΎœύΆ§ “Έ¬œ¬Θ§Υ«―χΧθΦΰœύΆ§ΓΘ
1.2 ΖΈΕ·¬ω―ΙΝΠ≤βΕ®
ΫΪ¥σ σ¬ιΉμΚσΘ§Ψ≠…œ«ΜΨ≤¬ω≤ε»κ”“–ΡΒΦΙήΘ§Ψ≠”“–ΡΖΩΓΔ”“–Ρ “¥οΖΈΕ·¬ωΓΘ”ΟP50―ΙΝΠ¥ΪΗ–ΤςΝ§Ϋ”RM-6000–ΆΕύΒΦ…ζάμΦ«¬Φ“«Φ«¬ΦΖΈΕ·¬ω ’Υθ―Ι(pulmonary artery systolic pressure, PASP)ΓΔΖΈΕ·¬ω φ’≈―Ι(pulmonary artery diastolic pressure, PADP)ΦΑΖΈΕ·¬ωΤΫΨυ―Ι(pulmonary artery mean pressure, PAMP)ΓΘ
, http://www.100md.com
1.3 ―ΣΫ§NOΒΡGreissΖ¥”ΠΖ®≤βΕ®
ΫΪ―Σ“Κάκ–ΡΚσΘ§”ΟΗ…‘οΩΙΡΐ≤ΘΝßΙή ’»Γ―ΣΫ§0.1 mlΘ§Φ”1.5 g.L-1ΝρΥα–Ω0.6mlΘ§Φ”ΥΪ’τΥ°0.4mlΜλ‘»Θ§Φ”40g.L-1«β―θΜ·ΡΤ0.1mlΜλ‘»Θ§±υ…œΖθ”ΐ60minΘ§10000ΓΝgάκ–Ρ2minΘ§»Γ…œ«ε0.6mlΘ§Φ”ΥΪ’τΥ°0.4mlΦΑ3g.L-1Μ«ΑΖ0.1mlΘ§±υ…œΖθ”ΐ15minΘ§÷°ΚσΦ”6mmol.L-1ίΝ““œ©ΕΰΑΖ―ΈΥα―Έ0.1mlΘ§ “Έ¬Ζ≈÷Ο1hΘ§545nm±»…ΪΕΝΙβΟήΕ»÷ΒΘ§ΗυΨί―υΤΖΙβΟήΕ»÷ΒΘ§Α¥±ξΉΦ«ζœΏΦΤΥψNOΦδΫ”≈®Ε»ΓΘ‘Ύ―«œθΥαΡΤΥυΉς±ξΉΦ«ζœΏ…œΘ§ΙβΟήΕ»÷Β(545nm±»…Ϊ)Ω…≤βΖΕΈßΈΣ0.02ΓΪ0.14(NOΦδΫ”≈®Ε»œύ”ΠΈΣ0ΓΪ100ΠΧmol.L-1)[1]ΓΘ
1.4 Οβ“ΏΉι÷·Μ·―ßΖ÷Έω
, ΑΌΡ¥“Ϋ“©
±ξ±Ψ÷Τ±Η:»Γ“Μ≤ύΖΈ“ΕΉι÷·Θ§‘ΎΚψάδ«–Τ§ΜζΡΎΘ§Ν§–χ±υΕ≥«–Τ§Θ§Τ§Κώ8ΓΪ10 ΠΧmΘ§ώ―Χυ”ΎΨ≠5g.L-1ΟςΫΚΜ·ΒΡ‘Ί≤ΘΤ§…œΓΘ»Γ±υΕ≥«–Τ§ “Έ¬Η…‘ο1hΘ§¥Ω±ϊΆΣ÷–Φ”0.3%(ΧεΜΐΖ÷ ΐ)H2O2 “Έ¬ΙΧΕ®10ΓΪ20minΘ§PBS«εœ¥2minΓΝ3¥ΈΓΘ1ΓΟ50(ΧεΜΐ±»)’ΐ≥Θ―Σ«εΖβ±’20minΘ§ΒΈΦ”ΧεΜΐ±»ΈΣ1ΓΟ50œΓ ΆΒΡ“ΜΩΙ,4ΓψCΙΐ“Ι, PBSœ¥2minΓΝ3¥ΈΘ§ΒΈΦ”1ΓΟ100(ΧεΜΐ±»)œΓ ΆΒΡ…ζΈοΥΊΜ·ΕΰΩΙΘ§37ΓψC Θ§20minΘ§PBS≥εœ¥Θ§ΒΈΦ”1ΓΟ100(ΧεΜΐ±»)œΓ ΆΒΡSABC“ΚΘ§37ΓψC, 20min,PBS≥εœ¥Θ§DABœ‘…Ϊ3ΓΪ5minΘ§Υ’ΡΨΥΊΗ¥»ΨΘ§ΧίΕ»ΨΤΨΪΆ―Υ°Θ§ΕΰΦΉ±ΫΆΗΟςΘ§ΖβΤ§ΨΒΦλΓΘΙβΨΒœ¬Θ§ΖΈΕ·¬ω÷–eNOSΒΡΖ÷≤Φ≥ ΉΊΜΤ…ΪΩ≈ΝΘΈΣΤδ―τ–‘–≈Κ≈ΓΘ
1.5 ΖΈΕ·¬ωΉι÷·÷–eNOSΒΡΟβ“ΏΜν–‘±μ¥οΖ÷Έω
”ΟΑκΕ®ΝΩΖ®Ζ÷ΈωeNOSΒΡΚ§ΝΩΓΘ Ήœ»ΗυΨίΖΈΕ·¬ω‘ΎΖΈΡΎΒΡΈΜ÷ΟΫΪΤδΖ÷ΈΣ3ΦΕ:ΔώΦΕΖΈΕ·¬ω, ΑιΚτΈϋ–‘÷ßΤχΙήΒΡΕ·¬ω;ΔρΦΕΖΈΕ·¬ω, Αι÷’Ρ©÷ßΤχΙήΒΡΕ·¬ω; ΔσΦΕΖΈΕ·¬ω,ΑιœΗ÷ßΤχΙήΒΡΕ·¬ωΓΘ‘ΎΙβ―ßœ‘ΈΔΨΒœ¬Θ§ΗυΨίΟΩΧθΖΈΕ·¬ωΡΎΤΛœΗΑϊΜρΤΫΜ§ΦΓœΗΑϊ≥ œ÷eNOS―τ–‘±μ¥οΒΡΑΌΖ÷±»Θ§ΫΪΤδΟβ“ΏΜν–‘Ζ÷ΈΣ3ΗωΒ»ΦΕΓΘΖΈΕ·¬ωΡΎΤΛœΗΑϊΜρΤΫΜ§ΦΓœΗΑϊ÷–ΈόeNOS―τ–‘±μ¥ο’ΏΈΣ(-);ΖΈΕ·¬ω0ΓΪ50%ΒΡΡΎΤΛœΗΑϊΜρΤΫΜ§ΦΓœΗΑϊ÷–eNOS≥ œ÷―τ–‘±μ¥ο’ΏΈΣ(+);ΖΈΕ·¬ω51%ΓΪ100%ΒΡΡΎΤΛœΗΑϊΜρΤΫΜ§ΦΓœΗΑϊ÷–eNOS≥ œ÷―τ–‘±μ¥ο’ΏΈΣ(++)ΓΘΟΩΖί±ξ±ΨΗςΦΕ―ΣΙή÷Ν…ΌΦλ≤β10ΧθΓΘΈΣ±ψ”ΎάμΫβΘ§ΖΈΕ·¬ω÷–eNOSΚ§ΝΩ”ΟΜΐΖ÷±μ ΨΘ§Φ¥:“‘ΖΈΕ·¬ωΒΡΑΌΖ÷±»≥Υ“‘Ζ¥”Π«ΩΕ»Φ”»®÷Β(ΓΑ-Γ±’ΏΘ§ΤδΖ¥”Π«ΩΕ»Φ”»®÷ΒΈΣ0;ΓΑ+Γ±’ΏΘ§ΤδΖ¥”Π«ΩΕ»Φ”»®÷ΒΈΣ0.5;ΓΑ++Γ±’ΏΘ§ΤδΖ¥”Π«ΩΕ»Φ”»®÷ΒΈΣ1)[2]ΓΘ
, ΑΌΡ¥“Ϋ“©
1.6 Ά≥ΦΤ―ß¥Πάμ
≤…”ΟΉιΦδtΦλ―ιΕ‘ΖΈΕ·¬ω―ΙΝΠ‘ΎΝΫΉιΦδΒΡ≤ν“λΫχ––Ά≥ΦΤ―ß¥ΠάμΘΜ≤…”ΟΩ®ΖΫΦλ―ιΕ‘ΝΫΉι≤ΜΆ§ΫΎΕΈΖΈΕ·¬ωeNOS±μ¥ο«ΩΕ»÷°ΖΈΕ·¬ωΑΌΖ÷±»Ϋχ––Ά≥ΦΤ―ßΖ÷ΈωΓΘ”…”ΎΕΰΉι¥σ σΖΈΕ·¬ω÷–eNOS±μ¥οΒΡΜΐΖ÷÷Βά¥‘¥”ΎΖ¥”Π«ΩΕ»Φ”»®÷Β”κΗΟ±μ¥ο«ΩΕ»ΒΡΖΈΕ·¬ω÷°ΑΌΖ÷±»÷°≥ΥΜΐ(ΦδΫ”ΦΤΥψ)Θ§“ρ¥ΥΕ‘¥Υ÷Η±ξΈ¥––Ά≥ΦΤ―ß¥Πάμ[2]ΓΘ
2 ΫαΙϊ
2.1 ΖΈΕ·¬ω―ΙΝΠΒΡ±δΜ·
»±―θΉι¥σ σΒΡPASPΓΔPAMPΦΑPADPΨυΫœΕ‘’’ΉιΟςœ‘…ΐΗΏ(P÷ΒΨυ<0.01, ±μ1)ΓΘ
±μ1 ΕΰΉι¥σ σΖΈΕ·¬ω―ΙΝΠΒΡ±δΜ·(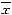 Γάs
Γάs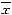 )
)
, ΑΌΡ¥“Ϋ“©
Table 1 Changes in pulmonary artery pressure in hypoxic rats(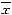 Γάs
Γάs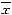 ) Groups
) Groups
n
p/kPa
PASP
PAMP
PADP
Control
6
3.14Γά0.13
, http://www.100md.com
2.23Γά0.16
1.55Γά0.22
Hypoxia
6
6.74Γά0.22**
4.75Γά0.27**
3.33Γά0.38**
PASP, pulmonary artery systolic pressure; PAMP, pulmonary artery mean pressure; PADP, pulmonary artery diastolic pressure; **P<0.01, compared with the control group.2.2 ―ΣΫ§NOΦδΫ”≈®Ε»ΒΡ±δΜ·
, http://www.100md.com
»±―θΉι¥σ σ―ΣΫ§NOΦδΫ”≈®Ε»[(2.2Γά0.3)ΠΧmol.L-1)]ΫœΕ‘’’Ήι[(10.0Γά3.0) ΠΧmol.L-1]Οςœ‘ΫΒΒΆ(t'=2.940Θ§P<0.05)ΓΘ
2.3 ΖΈΕ·¬ωΉι÷·÷–eNOSΒΡΟβ“ΏΜν–‘±μ¥ο(±μ2)
2.3.1 ΖΈΕ·¬ωΡΎΤΛœΗΑϊ÷–eNOSΒΡΟβ“ΏΜν–‘±μ¥ο Ε‘’’Ήι¥σ σΗςΦΕΖΈΕ·¬ωΡΎΤΛœΗΑϊeNOSΟβ“ΏΜν–‘±μ¥οΨυΈΣ―τ–‘(+Μρ++)Θ§Τδ÷–(58Γά20)%ΔώΦΕΖΈΕ·¬ωΓΔ(52Γά15)%ΔρΦΕΖΈΕ·¬ωΓΔ(83Γά9)%ΔσΦΕΖΈΕ·¬ωΤδΡΎΤΛœΗΑϊeNOSΟβ“ΏΜν–‘±μ¥οΈΣ++ΘΜ»±―θΉι¥σ σ(100Γά0)%ΔώΦΕΖΈΕ·¬ωΓΔ(92Γά5)%ΔρΦΕΖΈΕ·¬ωΦΑ(83Γά14)%ΔσΦΕΖΈΕ·¬ωΤδΡΎΤΛœΗΑϊeNOSΟβ“ΏΜν–‘±μ¥οΈΣ-Θ§ΝΫΉι±»Ϋœ≤ν“λ”–œ‘÷χ–‘ (PΨυ<0.01)ΓΘ
±μ2 ≤ΜΆ§eNOS±μ¥ο«ΩΕ»÷°ΖΈΕ·¬ωΑΌΖ÷±»(%)(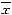 Γάs
Γάs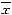 )
)
, ΑΌΡ¥“Ϋ“©
Table 2 The percentage of pulmonary arteries expressing
the different strength of signals of eNOS(%)(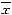 Γάs
Γάs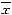 ) Strength of
) Strength of
signals
Control
Hypoxia group
EC
SMC
, ΑΌΡ¥“Ϋ“©
EC
SMC
PA segment Δώ
-
9Γά8
11Γά5
100Γά0
94Γά6
+
33Γά17
42Γά20
0
6Γά6
, ΑΌΡ¥“Ϋ“©
++
58Γά20
47Γά18
0
0
PA segment Δρ
-
8Γά8
0
92Γά5
74Γά16
+
40Γά10
, ΑΌΡ¥“Ϋ“©
38Γά14
8Γά5
26Γά16
++
52Γά15
62Γά14
0
0
PA segment Δσ
-
5Γά6
0
83Γά14
, http://www.100md.com
72Γά20
+
12Γά8
21Γά12
17Γά14
28Γά18
++
83Γά9
79Γά12
0
0
ECΘ§ endothelial cell; SMCΘ§ smooth muscle cell; PAΘ§ pulmonary artery. Comparison of the percentages of PA expressing different signals(-Θ§+Θ§++) between control and hypoxia groups: EC of segment Δώ:Π÷2=166.0, P<0.01; EC of segment Δρ: Π÷2=143.9, P<0.01; EC of segment Δσ: Π÷2=152.9, P<0.01; SMC of segment Δώ: Π÷2=139.6, P<0.01; SMC of segment Δρ: Π÷2=59.9, P<0.01; SMC of segment Δσ: Π÷2=152.0, P<0.01.
, http://www.100md.com
2.3.2 ΖΈΕ·¬ωΤΫΜ§ΦΓœΗΑϊ÷–eNOSΒΡΟβ“ΏΜν–‘±μ¥ο Ε‘’’Ήι¥σ σΗςΦΕΖΈΕ·¬ωΤΫΜ§ΦΓœΗΑϊeNOSΟβ“ΏΜν–‘±μ¥οΨυΈΣ―τ–‘(+Μρ++)Θ§Τδ÷–(47Γά18)%ΔώΦΕΖΈΕ·¬ωΓΔ(62Γά14)%ΔρΦΕΖΈΕ·¬ωΦΑ(79Γά12)%ΔσΦΕΖΈΕ·¬ωΤδΤΫΜ§ΦΓœΗΑϊ÷–eNOSΟβ“ΏΜν–‘±μ¥οΈΣ++ΘΜ»±―θΉι¥σ σ(94Γά6)%ΔώΦΕΖΈΕ·¬ωΓΔ(74Γά16)%ΔρΦΕΖΈΕ·¬ωΦΑ(39Γά20)%ΔσΦΕΖΈΕ·¬ωΤδΤΫΜ§ΦΓœΗΑϊ÷–eNOSΒΡΟβ“ΏΜν–‘±μ¥οΈΣ-ΓΘ
2.3.3 ΕΰΉι¥σ σΖΈΕ·¬ω÷–eNOS±μ¥οΜΐΖ÷«ιΩωΦϊ±μ3ΓΘ
±μ3 ΕΰΉι¥σ σΖΈΕ·¬ω÷–eNOS±μ¥οΒΡΜΐΖ÷÷Β(Ζ÷)
Table 3 The expressing score of eNOS in pulmonary arteries of rats PA segment
Control
, ΑΌΡ¥“Ϋ“©
Hypoxia group
SMC
EC
SMC
EC
Δώ
68.05
74.50
2.78
0
Δρ
81.22
71.83
, ΑΌΡ¥“Ϋ“©
12.92
3.75
Δσ
89.44
88.62
13.89
8.56
ECȧ endothelial cell; SMCȧ smooth muscle cell; PAȧ pulmonary artery. Satistical analysis was not performed because the above scores were indirectly derived data.
3 Χ÷¬έ
, ΑΌΡ¥“Ϋ“©
ΖΈ―ΣΙή¥≤ΒΡΡΎΤΛœΗΑϊΕ‘ΖΈ―≠ΜΖΒΡΒςΫΎΨΏ”–÷Ί“ΣΉς”Ο[3]ΓΘ–μΕύ―ΣΙήΜν–‘“ρΉ”Ής”Ο”ΎΡΎΤΛœΗΑϊΘ§Ά®ΙΐΡΎΤΛœΗΑϊ―ήΜ· φ’≈“ρΉ”(endothelium-derived relaxing factor, EDRF)“ΐΤπ―ΣΙή φ’≈Θ§ΜρΆ®ΙΐΡΎΤΛœΗΑϊ―ήΜ· ’Υθ“ρΉ”(endothelium-derived contracting factors, EDCFs)“ΐΤπ―ΣΙή ’Υθ[4]ΓΘHPH ±…œ ωΝΫ’Ώ÷°ΦδΒΡΙΊœΒ“λ≥ΘΘ§Αϋά®EDRF”κEDCFs÷°ΦδΒΡΉς”Ο ßΚβΘ§’β“ΜΙέΒψ“―‘Ϋά¥‘ΫΈΣ»ΥΟ«ΥυΫ” ήΓΘ
»ΥΟ«“―»œ ΕΒΫNO «ΒςΫΎΖΈ―ΣΙήΒ·–‘ΒΡ÷Ί“ΣΫι÷ ÷°“ΜΘ§ΕχNOS «NO–Έ≥…Υυ±Ί–ηΒΡΟΗΘ§NOS“‘L-ΨΪΑ±ΥαΚΆΖ÷Ή”―θΈΣΒΉΈοΘ§–Έ≥…NOΚΆL-ΙœΑ±ΥαΘ§NOS «NO…ζ≥…ΒΡœόΥΌ“ρΉ”ΓΘNOS”–3÷÷Ά§ΙΠΟΗΘ§Φ¥ΡΎΤΛœΗΑϊ–ΆNOS(eNOS)ΓΔΡ‘–ΆNOS(bNOS)ΦΑ”’ΒΦ–ΆNOS(iNOS),“―”…Ζ÷Ή”ΩΥ¬ΓΚΆΜυ“ρ±μ¥οΥυ÷Λ ΒΓΘJenniferΒ»[5]ΒΎ“Μ¥Έ”ΟΕύΩΥ¬ΓΩΙΧεΟβ“ΏΉι÷·Μ·―ßΖΫΖ®÷ΛΟςΘ§eNOS¥φ‘Ύ”ΎΦΗΗω÷÷ τ(Αϋά®»Υ)ΒΡΗς÷÷―ΣΙήΡΎΤΛœΗΑϊΘ§’β÷÷ΕύΩΥ¬ΓΩΙΧε «ΧΊ“λΒΡΘ§”κά¥Ή‘Ρ‘ΚΆΨό …œΗΑϊΒΡbNOSΚΆiNOSΨυΈόΫΜ≤φΖ¥”ΠΓΘ
, ΑΌΡ¥“Ϋ“©
Β―ι÷ΛΟςΘ§NO÷ς“Σ≤ζ…ζ”Ύ―ΣΙήΡΎΤΛœΗΑϊ[6]Θ§eNOSΫω¥φ‘Ύ”ΎΡΎΤΛœΗΑϊ÷–ΓΘΥφΉ≈―–ΨΩΒΡΫχ’ΙΘ§»ΥΟ«ΖΔœ÷eNOS≤ΜΫω¥φ‘Ύ”ΎΖΈΕ·¬ωΡΎΤΛœΗΑϊ,Ά§ ±“ύ¥φ‘Ύ”ΎΤΫΜ§ΦΓœΗΑϊ[7]ΓΘ±Ψ Β―ι”ΟΟβ“ΏΉι÷·Μ·―ßΖΫΖ®÷Λ ΒΘ§eNOS≤ΜΫω¥φ‘Ύ”ΎΖΈΕ·¬ωΡΎΤΛœΗΑϊΘ§Ά§ ±“ύ¥σΝΩ¥φ‘Ύ”ΎΖΈΕ·¬ωΒΡΤΫΜ§ΦΓœΗΑϊ÷–Θ§Εΰ’ΏΚ§ΝΩΨυΈόœ‘÷χ≤ν“λΘ§ΆΤ≤βNO“≤Ά§ ±≤ζ…ζ”ΎΡΎΤΛœΗΑϊΦΑΤΫΜ§ΦΓœΗΑϊΓΘ
Έ“Ο«ΜΙΙέ≤λΒΫΕ‘’’Ήι¥σ σΗςΦΕΖΈΕ·¬ω÷–eNOSΚ§ΝΩΫœΗΏΘ§NOΦδΫ”Κ§ΝΩΫœΗΏΘ§ΤδΖΈΕ·¬ω―ΙΝΠ‘Ύ’ΐ≥ΘΖΕΈß;»±―θΚσΗςΦΕΖΈΕ·¬ω÷–eNOSΚ§ΝΩœ‘÷χœ¬ΫΒΘ§NOΦδΫ”Κ§ΝΩΟςœ‘œ¬ΫΒΘ§ΕχΤδPAPΟςœ‘…ΐΗΏΘ§Χα Ψ»±―θΉ¥Χ§œ¬ΖΈΕ·¬ωeNOSΒΡ±μ¥οΦθ…ΌΘ§Υφ÷°NO…ζ≥…”κ ΆΖ≈Φθ…ΌΘ§ φ’≈―ΣΙήΉς”ΟΦθ»θΘ§±μΟςΖΈΕ·¬ω÷–eNOS»Ζ Β≤Έ”κΝΥHPHΒΡΖΔ…ζΙΐ≥ΧΓΘΆ§ ±Θ§ΫαΚœ“‘Άυ Β―ι÷Λ ΒΘ§»±―θ¥ΧΦΛETmRNA±μ¥ο‘ωΦ”[8]Θ§ ΙETΚœ≥…”κ ΆΖ≈‘ωΦ”Θ§Υθ―ΣΙήΉς”Ο‘ω«ΩΘ§Εΰ’ΏΙ≤Ά§Ής”ΟΒΡΫαΙϊ «¥ΌΫχ―ΣΙή―ΙΝΠ‘ωΗΏΘ§―ΣΙήΉηΝΠ‘ω¥σΘ§¥”Εχ–Έ≥…ΖΈΕ·¬ωΗΏ―ΙΓΘ
, ΑΌΡ¥“Ϋ“©
Ήέ…œΥυ ωΘ§Έ“Ο«ΒΡ―–ΨΩΫαΙϊΈΣ’ΐ≥ΘΖΈΕ·¬ωΉι÷·÷–Έό¬έΡΎΤΛœΗΑϊΜρΤΫΜ§ΦΓœΗΑϊΨυΚ§”–eNOSΘ§HPH¥σ σΗςΦΕΖΈΕ·¬ωΡΎΤΛœΗΑϊΚΆΤΫΜ§ΦΓœΗΑϊ÷–eNOSΚ§ΝΩΨυΫœΕ‘’’ΉιΟςœ‘ΫΒΒΆΘ§»±―θ“÷÷ΤΝΥeNOSΒΡ±μ¥οΘ§NO≤ζ…ζ”κ ΆΖ≈œ¬ΫΒΘ§ φ’≈―ΣΙήΉς”ΟΦθ»θΘ§–Έ≥…ΖΈΕ·¬ωΗΏ―ΙΓΘ
±ΨΈΡ‘ΎΖ÷Έω¥σ σΖΈΕ·¬ωΉι÷·NOS±μ¥ο ±Θ§ΜΙ≤…”ΟΝΥ±μ¥ο«ΩΕ»ΜΐΖ÷’β“Μ÷Η±ξΓΘΦ¥ΖΈΕ·¬ω÷–eNOSΚ§ΝΩ”ΟΜΐΖ÷±μ Ψ[2]ΓΘ“‘ΖΈΕ·¬ωΒΡΑΌΖ÷±»≥Υ“‘Ζ¥”Π«ΩΕ»Φ”»®÷ΒΦ¥ΈΣ±μ¥ο«ΩΕ»ΜΐΖ÷ΓΘΗΟΖ÷ΈωΖΫΖ®ΒΡ”≈Βψ‘Ύ”Ύ±ψ”Ύ¥”¥σ σ’ϊΧεΖΈΉι÷·Ϋ«Ε»»œ ΕΤδΖΈΕ·¬ω÷–ΡΎΤΛœΗΑϊΜρΤΫΜ§ΦΓœΗΑϊNOS±μ¥ο«ΩΕ»Θ§Ϋœ¥”ΒΞ“ΜΖΈΕ·¬ωΉι÷·ΥυΒΟ≥ωΒΡΡ≥“Μ±μ¥ο«ΩΕ»ΗϋΦ”»ΪΟφΓΘ
*ΙζΦ“Ή‘»ΜΩΤ―ßΜυΫπ(39870844)”κΈά…ζ≤ΩΩΤ―–ΜυΫπΉ ÷ζΩΈΧβΘΜ
≤ΈΩΦΈΡœΉ
1 ΤκΫ®ΙβΘ§Ε≈Ψϋ±ΘΘ§Φ÷Ϋ®ΖφΘ§Β».ΒΆ―θ–‘ΖΈΕ·¬ωΗΏ―Ι¥σ σΖΈ―ΣΙήΫαΙΙΦΑ―ΣΫ§“Μ―θΜ·ΒΣΒΡ±δΜ·.±±Ψ©“ΫΩΤ¥σ―ß―ß±®Θ§1999Θ§4ΘΚ324-327
, ΑΌΡ¥“Ϋ“©
2 Hislop AA, Springgall DR, Buttery LDK, et al. Aboundance of endothelial nitric oxide synthase in newborn intrapulmonary arteries. Arch Dis Child, 1995, 73: F17-F21
3 Loesch A, Burnstock G. Ultrastructural localization of nitric oxide synthase and endothelin in rat pulmonary artery and vein during postnatal development and aging. Cell Tissue Res, 1996,283:355-365
4 Shepherd JT, Vanhontte PM. Endothelium derived relaxing factor (EDRF) and contracting factors (EDCF) in the control of cardiovascular homeostasis: the pioneering observations. In:Rubanyi Gȧ ed. Cardiovascular significance of endothelium derived vasoactive factors. New York: Futara, 1991.39-64
, ΑΌΡ¥“Ϋ“©
5 Jennifer SP, Nakane M, Buttery LDK, et al. Characterization and localization of endothelial nitric oxide synthase using specific monoclonal antibodies. Am J Physiol,1993,265:C1379-1387
6 Clive JL, Barry AB. What is the relationship between the endothelium derived relaxant factor and nitric oxide? Life Sci, 1989,45(1):1-14
7 Loesch A, Burnstock G. Ultrastructural localization of nitric oxide synthase and endothelin in coronary and pulmonary arteries of newborn rats. Cell Tissue Res, 1995,279:475-483
8 Ε≈Ψϋ±Θ,άνΆρ’ρ,άη ΈΡ,Β».¬ΐ–‘ΒΆ―θ¥σ σΖΈΕ·¬ωΡΎΤΛΥΊmRNAΒΡ±μ¥οΦΑΕ®ΈΜ.±±Ψ©“ΫΩΤ¥σ―ß―ß±®Θ§ 1997,29(1):15-17
(1999-04-21 ’Ηε), ΑΌΡ¥“Ϋ“©
ΒΞΈΜΘΚ±±Ψ©“ΫΩΤ¥σ―ßΒΎ“Μ“Ϋ‘ΚΕυΩΤ,±±Ψ© 100034
ΙΊΦϋ¥ ΘΚΗΏ―Σ―ΙΘΜΖΈ–‘ΘΜΝς––≤Γ―ßΘΜ“Μ―θΜ·ΒΣΚœΟΗΓνΘΜΖΈΕ·¬ωΘΜΟΗ―ßΘΜ“Μ―θΜ·ΒΣΘΜ―Σ“Κ
±±Ψ©“ΫΩΤ¥σ―ß―ß±®990619 ’Σ “Σ ΡΩΒΡΘΚ―–ΨΩ¥σ σΖΈΕ·¬ω÷–“Μ―θΜ·ΒΣΚœΟΗ(nitric oxide synthase, NOS)ΒΡΚ§ΝΩΦΑΖ÷≤Φ±δΜ·”κ¬ΐ–‘»±―θ–‘ΖΈΕ·¬ωΗΏ―Ι(hypoxic pulmonary hypertension, HPH)ΖΔ…ζΒΡΙΊœΒΓΘΖΫΖ®ΘΚ≤…”ΟeNOSΕύΩΥ¬ΓΩΙΧεΘ§Ε‘¬ΐ–‘HPH¥σ σΒΡΖΈΉι÷·Ϋχ––Οβ“ΏΉι÷·Μ·―ßΖ÷ΈωΘ§Ιέ≤λ»±―θΉιΦΑΕ‘’’Ήι¥σ σΗςΦΕΖΈΕ·¬ω÷–eNOSΚ§ΝΩΦΑΕ®ΈΜΘΜΆ§ ±”Π”ΟΖ÷ΙβΙβΕ»ΦΤ≤βΕ®»±―θΉιΦΑΕ‘’’Ήι¥σ σ―ΣΫ§÷–NOΒΡΦδΫ”≈®Ε»ΓΘΫαΙϊΘΚ’ΐ≥Θ¥σ σΖΈΕ·¬ωΡΎΤΛœΗΑϊΦΑΤΫΜ§ΦΓœΗΑϊΨυΚ§”–ΫœΗΏΒΡeNOS±μ¥οΘ§«“ΗςΦΕΖΈΕ·¬ω÷–eNOSΚ§ΝΩ≤ν“λΈόœ‘÷χ–‘ΘΜ»±―θΉι¥σ σΗςΦΕΖΈΕ·¬ωΡΎΤΛœΗΑϊΦΑΤΫΜ§ΦΓœΗΑϊeNOSΚ§ΝΩΨυΫœΕ‘’’Ήιœ‘÷χΦθ…ΌΘΜ»±―θΉι¥σ σ―ΣΫ§NOΦδΫ”≈®Ε»ΫœΕ‘’’ΉιΟςœ‘ΫΒΒΆΓΘΫα¬έΘΚ¥σ σΖΈΕ·¬ωΡΎΤΛœΗΑϊΚΆΤΫΜ§ΦΓœΗΑϊeNOSΚ§ΝΩœ¬ΫΒΦΑ―ΣΫ§NO≈®Ε»œ¬ΫΒ≤Έ”κ¬ΐ–‘HPHΒΡ–Έ≥…ΓΘ
, ΑΌΡ¥“Ϋ“©
÷–ΙζΆΦ ιΉ ΝœΖ÷άύΖ®Ζ÷άύΚ≈ R563-332
A study on endothelial nitric oxide synthase in pulmonary arteries
of hypoxic pulmonary hypertensive rats
CUI Yan-Nan, MA Yu-Wenȧ DU Jun-Bao
(Department of Pediatrics, the First Hospital, Beijing Medical University, Beijing 100034)
MeSH Hypertension, pulmonary/epidemiol Nitric oxide synthaseΓν Pulmonary artery/enzymol Nitric oxide/blood
, ΑΌΡ¥“Ϋ“©
ABSTRACT Objective: To study the abundance and localization of nitric oxide synthase (NOS) in pulmonary arteries of rats and to explore the relationship between their changes and chronic hypoxic pulmonary hypertension (HPH). Methods: Immunohistochemistry technique was performed on the lung tissues of the HPH rats with eNOS multiclonal antibody to assay the abundance and localization of eNOS in different segments of pulmonary arteries of the hypoxic and control rats. At the same time, the plasma concentration of nitric oxide (NO) metabolite, nitrite, was measured by spectrophotometry. Results: eNOS expression was found in pulmonary artery endothelial cells and smooth muscle cells, and there was no significant difference among the different segments of pulmonary arteries, whereas the eNOS expression was inhibited in endothelial cells and smooth muscle cells of pulmonary arteries in hypoxia group; The plasma concentration of nitrite in hypoxia group was significantly decreased compared with that of control rats. Conclusion: The results suggest that the decrease in eNOS in pulmonary artery endothelial cells and smooth muscle cells by hypoxia as well as the decrease in plasma concentration of NO may play a role in the development of chronic HPH.
, ΑΌΡ¥“Ϋ“©
(J Beijing Med Univ, 1999,31:552-554)
»±―θ–‘ΖΈΕ·¬ωΗΏ―Ι( hypoxic pulmonary hypertension, HPH) «Εύ÷÷–ΡΖΈΦ≤≤ΓΖΔ’ΙΙΐ≥Χ÷–ΒΡ≤Γάμ…ζάμΜΖΫΎΘ§ΤδΖΔ…ζΜζ÷Τ…–Έ¥Άξ»Ϊ«ε≥ΰΓΘ―–ΨΩΖΔœ÷―ΣΙήΡΎΤΛœΗΑϊ≤ζ…ζΒΡ“Μ―θΜ·ΒΣ(nitric oxide, NO)‘ΎHPHΒΡΖΔ…ζΜζ÷Τ÷–Τπ÷Ί“ΣΒςΫΎΉς”ΟΓΘΕ·Έο Β―ι±μΟςΆβ‘¥–‘L-ΨΪΑ±Υα(L-Arginine, L-Arg)Θ§Ω… ΙNOΚœ≥…‘ωΕύΘ§¥”ΕχΫΒΒΆΖΈΕ·¬ω―ΙΝΠ;Ζ¥÷°Ηχ”ηNOΚœΟΗ(nitric oxide synthase, NOS)“÷÷ΤΦΝ»γL-ΨΪΑ±ΥαΦΉ÷§(NΠΊ-L-Arginine methyl ester, L-NAME)ΉΔ…δΘ§‘ρΩ… ΙNOΚœ≥…Φθ…ΌΘ§÷¬ΖΈΕ·¬ω―ΙΝΠΫχ“Μ≤Ϋ…ΐΗΏΓΘNOS «NOΚœ≥…÷–÷Ί“ΣΒΡœόΥΌΟΗΓΘΤυΫώΈΣ÷ΙΙΊ”Ύ¬ΐ–‘HPH ±ΖΈΕ·¬ω÷–NOΧεœΒΘ§ΧΊ±π «ΖΈΕ·¬ωΡΎΤΛœΗΑϊΦΑΤΫΜ§ΦΓœΗΑϊΡΎΡΎΤΛ‘¥–‘NOS (endothelial NOS, eNOS)Κ§ΝΩΦΑΕ®ΈΜΒΡ―–ΨΩΫœ…ΌΓΘΈ“Ο«”Π”ΟeNOSΕύΩΥ¬ΓΩΙΧεΘ§Ε‘¬ΐ–‘HPH¥σ σΒΡΖΈΉι÷·Ϋχ––Οβ“ΏΉι÷·Μ·―ßΖ÷ΈωΘ§”κ’ΐ≥Θ«ιΩωœ¬ΖΈΕ·¬ωeNOSΒΡΚ§ΝΩΦΑΕ®ΈΜœύΕ‘±»Θ§―–ΨΩHPH ±Θ§ΖΈΕ·¬ωeNOSΚ§ΝΩ±δΜ·ΦΑΤδΕ®ΈΜΘ§ΧΫΧ÷NOSΕ‘HPHΒΡΒςΫΎΉς”ΟΓΘ
, ΑΌΡ¥“Ϋ“©
1 ≤ΡΝœ”κΖΫΖ®
1.1 Ϋ®ΝΔ»±―θ–‘ΖΈΕ·¬ωΗΏ―ΙΡΘ–Ά
–έ–‘Wistar¥σ σΙ≤12÷ΜΘ§Χε÷Ί200ΓΪ300gΘ§ΥφΜζΖ÷ΈΣ»±―θΉιΦΑΕ‘’’ΉιΘ§Ης6÷ΜΓΘΫΪ»±―θΉι¥σ σ÷Ο”ΎCG1–Ά≥Θ―ΙΒΆ―θœδΡΎ(÷–Ιζ“Ϋ―ßΩΤ―ß‘ΚΜυ¥Γ“Ϋ―ß―–ΨΩΥυ)Θ§Ά®»κΒΣΤχΘ§ ΙœδΡΎ―θΧεΜΐΖ÷ ΐ‘Ύ30minΉσ”“¥ο(10.0Γά0.5)%Θ§ΟΩΧλ»±―θ6hΘ§Ι≤»±―θ1÷ήΓΘΕ‘’’Ήι¥σ σΚτΈϋ “ΡΎΩ’ΤχΓΘ Β―ιΤΎΦδΝΫΉι¥σ σ‘ΎœύΆ§ “Έ¬œ¬Θ§Υ«―χΧθΦΰœύΆ§ΓΘ
1.2 ΖΈΕ·¬ω―ΙΝΠ≤βΕ®
ΫΪ¥σ σ¬ιΉμΚσΘ§Ψ≠…œ«ΜΨ≤¬ω≤ε»κ”“–ΡΒΦΙήΘ§Ψ≠”“–ΡΖΩΓΔ”“–Ρ “¥οΖΈΕ·¬ωΓΘ”ΟP50―ΙΝΠ¥ΪΗ–ΤςΝ§Ϋ”RM-6000–ΆΕύΒΦ…ζάμΦ«¬Φ“«Φ«¬ΦΖΈΕ·¬ω ’Υθ―Ι(pulmonary artery systolic pressure, PASP)ΓΔΖΈΕ·¬ω φ’≈―Ι(pulmonary artery diastolic pressure, PADP)ΦΑΖΈΕ·¬ωΤΫΨυ―Ι(pulmonary artery mean pressure, PAMP)ΓΘ
, http://www.100md.com
1.3 ―ΣΫ§NOΒΡGreissΖ¥”ΠΖ®≤βΕ®
ΫΪ―Σ“Κάκ–ΡΚσΘ§”ΟΗ…‘οΩΙΡΐ≤ΘΝßΙή ’»Γ―ΣΫ§0.1 mlΘ§Φ”1.5 g.L-1ΝρΥα–Ω0.6mlΘ§Φ”ΥΪ’τΥ°0.4mlΜλ‘»Θ§Φ”40g.L-1«β―θΜ·ΡΤ0.1mlΜλ‘»Θ§±υ…œΖθ”ΐ60minΘ§10000ΓΝgάκ–Ρ2minΘ§»Γ…œ«ε0.6mlΘ§Φ”ΥΪ’τΥ°0.4mlΦΑ3g.L-1Μ«ΑΖ0.1mlΘ§±υ…œΖθ”ΐ15minΘ§÷°ΚσΦ”6mmol.L-1ίΝ““œ©ΕΰΑΖ―ΈΥα―Έ0.1mlΘ§ “Έ¬Ζ≈÷Ο1hΘ§545nm±»…ΪΕΝΙβΟήΕ»÷ΒΘ§ΗυΨί―υΤΖΙβΟήΕ»÷ΒΘ§Α¥±ξΉΦ«ζœΏΦΤΥψNOΦδΫ”≈®Ε»ΓΘ‘Ύ―«œθΥαΡΤΥυΉς±ξΉΦ«ζœΏ…œΘ§ΙβΟήΕ»÷Β(545nm±»…Ϊ)Ω…≤βΖΕΈßΈΣ0.02ΓΪ0.14(NOΦδΫ”≈®Ε»œύ”ΠΈΣ0ΓΪ100ΠΧmol.L-1)[1]ΓΘ
1.4 Οβ“ΏΉι÷·Μ·―ßΖ÷Έω
, ΑΌΡ¥“Ϋ“©
±ξ±Ψ÷Τ±Η:»Γ“Μ≤ύΖΈ“ΕΉι÷·Θ§‘ΎΚψάδ«–Τ§ΜζΡΎΘ§Ν§–χ±υΕ≥«–Τ§Θ§Τ§Κώ8ΓΪ10 ΠΧmΘ§ώ―Χυ”ΎΨ≠5g.L-1ΟςΫΚΜ·ΒΡ‘Ί≤ΘΤ§…œΓΘ»Γ±υΕ≥«–Τ§ “Έ¬Η…‘ο1hΘ§¥Ω±ϊΆΣ÷–Φ”0.3%(ΧεΜΐΖ÷ ΐ)H2O2 “Έ¬ΙΧΕ®10ΓΪ20minΘ§PBS«εœ¥2minΓΝ3¥ΈΓΘ1ΓΟ50(ΧεΜΐ±»)’ΐ≥Θ―Σ«εΖβ±’20minΘ§ΒΈΦ”ΧεΜΐ±»ΈΣ1ΓΟ50œΓ ΆΒΡ“ΜΩΙ,4ΓψCΙΐ“Ι, PBSœ¥2minΓΝ3¥ΈΘ§ΒΈΦ”1ΓΟ100(ΧεΜΐ±»)œΓ ΆΒΡ…ζΈοΥΊΜ·ΕΰΩΙΘ§37ΓψC Θ§20minΘ§PBS≥εœ¥Θ§ΒΈΦ”1ΓΟ100(ΧεΜΐ±»)œΓ ΆΒΡSABC“ΚΘ§37ΓψC, 20min,PBS≥εœ¥Θ§DABœ‘…Ϊ3ΓΪ5minΘ§Υ’ΡΨΥΊΗ¥»ΨΘ§ΧίΕ»ΨΤΨΪΆ―Υ°Θ§ΕΰΦΉ±ΫΆΗΟςΘ§ΖβΤ§ΨΒΦλΓΘΙβΨΒœ¬Θ§ΖΈΕ·¬ω÷–eNOSΒΡΖ÷≤Φ≥ ΉΊΜΤ…ΪΩ≈ΝΘΈΣΤδ―τ–‘–≈Κ≈ΓΘ
1.5 ΖΈΕ·¬ωΉι÷·÷–eNOSΒΡΟβ“ΏΜν–‘±μ¥οΖ÷Έω
”ΟΑκΕ®ΝΩΖ®Ζ÷ΈωeNOSΒΡΚ§ΝΩΓΘ Ήœ»ΗυΨίΖΈΕ·¬ω‘ΎΖΈΡΎΒΡΈΜ÷ΟΫΪΤδΖ÷ΈΣ3ΦΕ:ΔώΦΕΖΈΕ·¬ω, ΑιΚτΈϋ–‘÷ßΤχΙήΒΡΕ·¬ω;ΔρΦΕΖΈΕ·¬ω, Αι÷’Ρ©÷ßΤχΙήΒΡΕ·¬ω; ΔσΦΕΖΈΕ·¬ω,ΑιœΗ÷ßΤχΙήΒΡΕ·¬ωΓΘ‘ΎΙβ―ßœ‘ΈΔΨΒœ¬Θ§ΗυΨίΟΩΧθΖΈΕ·¬ωΡΎΤΛœΗΑϊΜρΤΫΜ§ΦΓœΗΑϊ≥ œ÷eNOS―τ–‘±μ¥οΒΡΑΌΖ÷±»Θ§ΫΪΤδΟβ“ΏΜν–‘Ζ÷ΈΣ3ΗωΒ»ΦΕΓΘΖΈΕ·¬ωΡΎΤΛœΗΑϊΜρΤΫΜ§ΦΓœΗΑϊ÷–ΈόeNOS―τ–‘±μ¥ο’ΏΈΣ(-);ΖΈΕ·¬ω0ΓΪ50%ΒΡΡΎΤΛœΗΑϊΜρΤΫΜ§ΦΓœΗΑϊ÷–eNOS≥ œ÷―τ–‘±μ¥ο’ΏΈΣ(+);ΖΈΕ·¬ω51%ΓΪ100%ΒΡΡΎΤΛœΗΑϊΜρΤΫΜ§ΦΓœΗΑϊ÷–eNOS≥ œ÷―τ–‘±μ¥ο’ΏΈΣ(++)ΓΘΟΩΖί±ξ±ΨΗςΦΕ―ΣΙή÷Ν…ΌΦλ≤β10ΧθΓΘΈΣ±ψ”ΎάμΫβΘ§ΖΈΕ·¬ω÷–eNOSΚ§ΝΩ”ΟΜΐΖ÷±μ ΨΘ§Φ¥:“‘ΖΈΕ·¬ωΒΡΑΌΖ÷±»≥Υ“‘Ζ¥”Π«ΩΕ»Φ”»®÷Β(ΓΑ-Γ±’ΏΘ§ΤδΖ¥”Π«ΩΕ»Φ”»®÷ΒΈΣ0;ΓΑ+Γ±’ΏΘ§ΤδΖ¥”Π«ΩΕ»Φ”»®÷ΒΈΣ0.5;ΓΑ++Γ±’ΏΘ§ΤδΖ¥”Π«ΩΕ»Φ”»®÷ΒΈΣ1)[2]ΓΘ
, ΑΌΡ¥“Ϋ“©
1.6 Ά≥ΦΤ―ß¥Πάμ
≤…”ΟΉιΦδtΦλ―ιΕ‘ΖΈΕ·¬ω―ΙΝΠ‘ΎΝΫΉιΦδΒΡ≤ν“λΫχ––Ά≥ΦΤ―ß¥ΠάμΘΜ≤…”ΟΩ®ΖΫΦλ―ιΕ‘ΝΫΉι≤ΜΆ§ΫΎΕΈΖΈΕ·¬ωeNOS±μ¥ο«ΩΕ»÷°ΖΈΕ·¬ωΑΌΖ÷±»Ϋχ––Ά≥ΦΤ―ßΖ÷ΈωΓΘ”…”ΎΕΰΉι¥σ σΖΈΕ·¬ω÷–eNOS±μ¥οΒΡΜΐΖ÷÷Βά¥‘¥”ΎΖ¥”Π«ΩΕ»Φ”»®÷Β”κΗΟ±μ¥ο«ΩΕ»ΒΡΖΈΕ·¬ω÷°ΑΌΖ÷±»÷°≥ΥΜΐ(ΦδΫ”ΦΤΥψ)Θ§“ρ¥ΥΕ‘¥Υ÷Η±ξΈ¥––Ά≥ΦΤ―ß¥Πάμ[2]ΓΘ
2 ΫαΙϊ
2.1 ΖΈΕ·¬ω―ΙΝΠΒΡ±δΜ·
»±―θΉι¥σ σΒΡPASPΓΔPAMPΦΑPADPΨυΫœΕ‘’’ΉιΟςœ‘…ΐΗΏ(P÷ΒΨυ<0.01, ±μ1)ΓΘ
±μ1 ΕΰΉι¥σ σΖΈΕ·¬ω―ΙΝΠΒΡ±δΜ·(
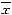 Γάs
Γάs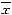 )
), ΑΌΡ¥“Ϋ“©
Table 1 Changes in pulmonary artery pressure in hypoxic rats(
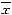 Γάs
Γάs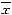 ) Groups
) Groupsn
p/kPa
PASP
PAMP
PADP
Control
6
3.14Γά0.13
, http://www.100md.com
2.23Γά0.16
1.55Γά0.22
Hypoxia
6
6.74Γά0.22**
4.75Γά0.27**
3.33Γά0.38**
PASP, pulmonary artery systolic pressure; PAMP, pulmonary artery mean pressure; PADP, pulmonary artery diastolic pressure; **P<0.01, compared with the control group.2.2 ―ΣΫ§NOΦδΫ”≈®Ε»ΒΡ±δΜ·
, http://www.100md.com
»±―θΉι¥σ σ―ΣΫ§NOΦδΫ”≈®Ε»[(2.2Γά0.3)ΠΧmol.L-1)]ΫœΕ‘’’Ήι[(10.0Γά3.0) ΠΧmol.L-1]Οςœ‘ΫΒΒΆ(t'=2.940Θ§P<0.05)ΓΘ
2.3 ΖΈΕ·¬ωΉι÷·÷–eNOSΒΡΟβ“ΏΜν–‘±μ¥ο(±μ2)
2.3.1 ΖΈΕ·¬ωΡΎΤΛœΗΑϊ÷–eNOSΒΡΟβ“ΏΜν–‘±μ¥ο Ε‘’’Ήι¥σ σΗςΦΕΖΈΕ·¬ωΡΎΤΛœΗΑϊeNOSΟβ“ΏΜν–‘±μ¥οΨυΈΣ―τ–‘(+Μρ++)Θ§Τδ÷–(58Γά20)%ΔώΦΕΖΈΕ·¬ωΓΔ(52Γά15)%ΔρΦΕΖΈΕ·¬ωΓΔ(83Γά9)%ΔσΦΕΖΈΕ·¬ωΤδΡΎΤΛœΗΑϊeNOSΟβ“ΏΜν–‘±μ¥οΈΣ++ΘΜ»±―θΉι¥σ σ(100Γά0)%ΔώΦΕΖΈΕ·¬ωΓΔ(92Γά5)%ΔρΦΕΖΈΕ·¬ωΦΑ(83Γά14)%ΔσΦΕΖΈΕ·¬ωΤδΡΎΤΛœΗΑϊeNOSΟβ“ΏΜν–‘±μ¥οΈΣ-Θ§ΝΫΉι±»Ϋœ≤ν“λ”–œ‘÷χ–‘ (PΨυ<0.01)ΓΘ
±μ2 ≤ΜΆ§eNOS±μ¥ο«ΩΕ»÷°ΖΈΕ·¬ωΑΌΖ÷±»(%)(
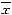 Γάs
Γάs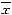 )
), ΑΌΡ¥“Ϋ“©
Table 2 The percentage of pulmonary arteries expressing
the different strength of signals of eNOS(%)(
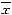 Γάs
Γάs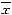 ) Strength of
) Strength ofsignals
Control
Hypoxia group
EC
SMC
, ΑΌΡ¥“Ϋ“©
EC
SMC
PA segment Δώ
-
9Γά8
11Γά5
100Γά0
94Γά6
+
33Γά17
42Γά20
0
6Γά6
, ΑΌΡ¥“Ϋ“©
++
58Γά20
47Γά18
0
0
PA segment Δρ
-
8Γά8
0
92Γά5
74Γά16
+
40Γά10
, ΑΌΡ¥“Ϋ“©
38Γά14
8Γά5
26Γά16
++
52Γά15
62Γά14
0
0
PA segment Δσ
-
5Γά6
0
83Γά14
, http://www.100md.com
72Γά20
+
12Γά8
21Γά12
17Γά14
28Γά18
++
83Γά9
79Γά12
0
0
ECΘ§ endothelial cell; SMCΘ§ smooth muscle cell; PAΘ§ pulmonary artery. Comparison of the percentages of PA expressing different signals(-Θ§+Θ§++) between control and hypoxia groups: EC of segment Δώ:Π÷2=166.0, P<0.01; EC of segment Δρ: Π÷2=143.9, P<0.01; EC of segment Δσ: Π÷2=152.9, P<0.01; SMC of segment Δώ: Π÷2=139.6, P<0.01; SMC of segment Δρ: Π÷2=59.9, P<0.01; SMC of segment Δσ: Π÷2=152.0, P<0.01.
, http://www.100md.com
2.3.2 ΖΈΕ·¬ωΤΫΜ§ΦΓœΗΑϊ÷–eNOSΒΡΟβ“ΏΜν–‘±μ¥ο Ε‘’’Ήι¥σ σΗςΦΕΖΈΕ·¬ωΤΫΜ§ΦΓœΗΑϊeNOSΟβ“ΏΜν–‘±μ¥οΨυΈΣ―τ–‘(+Μρ++)Θ§Τδ÷–(47Γά18)%ΔώΦΕΖΈΕ·¬ωΓΔ(62Γά14)%ΔρΦΕΖΈΕ·¬ωΦΑ(79Γά12)%ΔσΦΕΖΈΕ·¬ωΤδΤΫΜ§ΦΓœΗΑϊ÷–eNOSΟβ“ΏΜν–‘±μ¥οΈΣ++ΘΜ»±―θΉι¥σ σ(94Γά6)%ΔώΦΕΖΈΕ·¬ωΓΔ(74Γά16)%ΔρΦΕΖΈΕ·¬ωΦΑ(39Γά20)%ΔσΦΕΖΈΕ·¬ωΤδΤΫΜ§ΦΓœΗΑϊ÷–eNOSΒΡΟβ“ΏΜν–‘±μ¥οΈΣ-ΓΘ
2.3.3 ΕΰΉι¥σ σΖΈΕ·¬ω÷–eNOS±μ¥οΜΐΖ÷«ιΩωΦϊ±μ3ΓΘ
±μ3 ΕΰΉι¥σ σΖΈΕ·¬ω÷–eNOS±μ¥οΒΡΜΐΖ÷÷Β(Ζ÷)
Table 3 The expressing score of eNOS in pulmonary arteries of rats PA segment
Control
, ΑΌΡ¥“Ϋ“©
Hypoxia group
SMC
EC
SMC
EC
Δώ
68.05
74.50
2.78
0
Δρ
81.22
71.83
, ΑΌΡ¥“Ϋ“©
12.92
3.75
Δσ
89.44
88.62
13.89
8.56
ECȧ endothelial cell; SMCȧ smooth muscle cell; PAȧ pulmonary artery. Satistical analysis was not performed because the above scores were indirectly derived data.
3 Χ÷¬έ
, ΑΌΡ¥“Ϋ“©
ΖΈ―ΣΙή¥≤ΒΡΡΎΤΛœΗΑϊΕ‘ΖΈ―≠ΜΖΒΡΒςΫΎΨΏ”–÷Ί“ΣΉς”Ο[3]ΓΘ–μΕύ―ΣΙήΜν–‘“ρΉ”Ής”Ο”ΎΡΎΤΛœΗΑϊΘ§Ά®ΙΐΡΎΤΛœΗΑϊ―ήΜ· φ’≈“ρΉ”(endothelium-derived relaxing factor, EDRF)“ΐΤπ―ΣΙή φ’≈Θ§ΜρΆ®ΙΐΡΎΤΛœΗΑϊ―ήΜ· ’Υθ“ρΉ”(endothelium-derived contracting factors, EDCFs)“ΐΤπ―ΣΙή ’Υθ[4]ΓΘHPH ±…œ ωΝΫ’Ώ÷°ΦδΒΡΙΊœΒ“λ≥ΘΘ§Αϋά®EDRF”κEDCFs÷°ΦδΒΡΉς”Ο ßΚβΘ§’β“ΜΙέΒψ“―‘Ϋά¥‘ΫΈΣ»ΥΟ«ΥυΫ” ήΓΘ
»ΥΟ«“―»œ ΕΒΫNO «ΒςΫΎΖΈ―ΣΙήΒ·–‘ΒΡ÷Ί“ΣΫι÷ ÷°“ΜΘ§ΕχNOS «NO–Έ≥…Υυ±Ί–ηΒΡΟΗΘ§NOS“‘L-ΨΪΑ±ΥαΚΆΖ÷Ή”―θΈΣΒΉΈοΘ§–Έ≥…NOΚΆL-ΙœΑ±ΥαΘ§NOS «NO…ζ≥…ΒΡœόΥΌ“ρΉ”ΓΘNOS”–3÷÷Ά§ΙΠΟΗΘ§Φ¥ΡΎΤΛœΗΑϊ–ΆNOS(eNOS)ΓΔΡ‘–ΆNOS(bNOS)ΦΑ”’ΒΦ–ΆNOS(iNOS),“―”…Ζ÷Ή”ΩΥ¬ΓΚΆΜυ“ρ±μ¥οΥυ÷Λ ΒΓΘJenniferΒ»[5]ΒΎ“Μ¥Έ”ΟΕύΩΥ¬ΓΩΙΧεΟβ“ΏΉι÷·Μ·―ßΖΫΖ®÷ΛΟςΘ§eNOS¥φ‘Ύ”ΎΦΗΗω÷÷ τ(Αϋά®»Υ)ΒΡΗς÷÷―ΣΙήΡΎΤΛœΗΑϊΘ§’β÷÷ΕύΩΥ¬ΓΩΙΧε «ΧΊ“λΒΡΘ§”κά¥Ή‘Ρ‘ΚΆΨό …œΗΑϊΒΡbNOSΚΆiNOSΨυΈόΫΜ≤φΖ¥”ΠΓΘ
, ΑΌΡ¥“Ϋ“©
Β―ι÷ΛΟςΘ§NO÷ς“Σ≤ζ…ζ”Ύ―ΣΙήΡΎΤΛœΗΑϊ[6]Θ§eNOSΫω¥φ‘Ύ”ΎΡΎΤΛœΗΑϊ÷–ΓΘΥφΉ≈―–ΨΩΒΡΫχ’ΙΘ§»ΥΟ«ΖΔœ÷eNOS≤ΜΫω¥φ‘Ύ”ΎΖΈΕ·¬ωΡΎΤΛœΗΑϊ,Ά§ ±“ύ¥φ‘Ύ”ΎΤΫΜ§ΦΓœΗΑϊ[7]ΓΘ±Ψ Β―ι”ΟΟβ“ΏΉι÷·Μ·―ßΖΫΖ®÷Λ ΒΘ§eNOS≤ΜΫω¥φ‘Ύ”ΎΖΈΕ·¬ωΡΎΤΛœΗΑϊΘ§Ά§ ±“ύ¥σΝΩ¥φ‘Ύ”ΎΖΈΕ·¬ωΒΡΤΫΜ§ΦΓœΗΑϊ÷–Θ§Εΰ’ΏΚ§ΝΩΨυΈόœ‘÷χ≤ν“λΘ§ΆΤ≤βNO“≤Ά§ ±≤ζ…ζ”ΎΡΎΤΛœΗΑϊΦΑΤΫΜ§ΦΓœΗΑϊΓΘ
Έ“Ο«ΜΙΙέ≤λΒΫΕ‘’’Ήι¥σ σΗςΦΕΖΈΕ·¬ω÷–eNOSΚ§ΝΩΫœΗΏΘ§NOΦδΫ”Κ§ΝΩΫœΗΏΘ§ΤδΖΈΕ·¬ω―ΙΝΠ‘Ύ’ΐ≥ΘΖΕΈß;»±―θΚσΗςΦΕΖΈΕ·¬ω÷–eNOSΚ§ΝΩœ‘÷χœ¬ΫΒΘ§NOΦδΫ”Κ§ΝΩΟςœ‘œ¬ΫΒΘ§ΕχΤδPAPΟςœ‘…ΐΗΏΘ§Χα Ψ»±―θΉ¥Χ§œ¬ΖΈΕ·¬ωeNOSΒΡ±μ¥οΦθ…ΌΘ§Υφ÷°NO…ζ≥…”κ ΆΖ≈Φθ…ΌΘ§ φ’≈―ΣΙήΉς”ΟΦθ»θΘ§±μΟςΖΈΕ·¬ω÷–eNOS»Ζ Β≤Έ”κΝΥHPHΒΡΖΔ…ζΙΐ≥ΧΓΘΆ§ ±Θ§ΫαΚœ“‘Άυ Β―ι÷Λ ΒΘ§»±―θ¥ΧΦΛETmRNA±μ¥ο‘ωΦ”[8]Θ§ ΙETΚœ≥…”κ ΆΖ≈‘ωΦ”Θ§Υθ―ΣΙήΉς”Ο‘ω«ΩΘ§Εΰ’ΏΙ≤Ά§Ής”ΟΒΡΫαΙϊ «¥ΌΫχ―ΣΙή―ΙΝΠ‘ωΗΏΘ§―ΣΙήΉηΝΠ‘ω¥σΘ§¥”Εχ–Έ≥…ΖΈΕ·¬ωΗΏ―ΙΓΘ
, ΑΌΡ¥“Ϋ“©
Ήέ…œΥυ ωΘ§Έ“Ο«ΒΡ―–ΨΩΫαΙϊΈΣ’ΐ≥ΘΖΈΕ·¬ωΉι÷·÷–Έό¬έΡΎΤΛœΗΑϊΜρΤΫΜ§ΦΓœΗΑϊΨυΚ§”–eNOSΘ§HPH¥σ σΗςΦΕΖΈΕ·¬ωΡΎΤΛœΗΑϊΚΆΤΫΜ§ΦΓœΗΑϊ÷–eNOSΚ§ΝΩΨυΫœΕ‘’’ΉιΟςœ‘ΫΒΒΆΘ§»±―θ“÷÷ΤΝΥeNOSΒΡ±μ¥οΘ§NO≤ζ…ζ”κ ΆΖ≈œ¬ΫΒΘ§ φ’≈―ΣΙήΉς”ΟΦθ»θΘ§–Έ≥…ΖΈΕ·¬ωΗΏ―ΙΓΘ
±ΨΈΡ‘ΎΖ÷Έω¥σ σΖΈΕ·¬ωΉι÷·NOS±μ¥ο ±Θ§ΜΙ≤…”ΟΝΥ±μ¥ο«ΩΕ»ΜΐΖ÷’β“Μ÷Η±ξΓΘΦ¥ΖΈΕ·¬ω÷–eNOSΚ§ΝΩ”ΟΜΐΖ÷±μ Ψ[2]ΓΘ“‘ΖΈΕ·¬ωΒΡΑΌΖ÷±»≥Υ“‘Ζ¥”Π«ΩΕ»Φ”»®÷ΒΦ¥ΈΣ±μ¥ο«ΩΕ»ΜΐΖ÷ΓΘΗΟΖ÷ΈωΖΫΖ®ΒΡ”≈Βψ‘Ύ”Ύ±ψ”Ύ¥”¥σ σ’ϊΧεΖΈΉι÷·Ϋ«Ε»»œ ΕΤδΖΈΕ·¬ω÷–ΡΎΤΛœΗΑϊΜρΤΫΜ§ΦΓœΗΑϊNOS±μ¥ο«ΩΕ»Θ§Ϋœ¥”ΒΞ“ΜΖΈΕ·¬ωΉι÷·ΥυΒΟ≥ωΒΡΡ≥“Μ±μ¥ο«ΩΕ»ΗϋΦ”»ΪΟφΓΘ
*ΙζΦ“Ή‘»ΜΩΤ―ßΜυΫπ(39870844)”κΈά…ζ≤ΩΩΤ―–ΜυΫπΉ ÷ζΩΈΧβΘΜ
≤ΈΩΦΈΡœΉ
1 ΤκΫ®ΙβΘ§Ε≈Ψϋ±ΘΘ§Φ÷Ϋ®ΖφΘ§Β».ΒΆ―θ–‘ΖΈΕ·¬ωΗΏ―Ι¥σ σΖΈ―ΣΙήΫαΙΙΦΑ―ΣΫ§“Μ―θΜ·ΒΣΒΡ±δΜ·.±±Ψ©“ΫΩΤ¥σ―ß―ß±®Θ§1999Θ§4ΘΚ324-327
, ΑΌΡ¥“Ϋ“©
2 Hislop AA, Springgall DR, Buttery LDK, et al. Aboundance of endothelial nitric oxide synthase in newborn intrapulmonary arteries. Arch Dis Child, 1995, 73: F17-F21
3 Loesch A, Burnstock G. Ultrastructural localization of nitric oxide synthase and endothelin in rat pulmonary artery and vein during postnatal development and aging. Cell Tissue Res, 1996,283:355-365
4 Shepherd JT, Vanhontte PM. Endothelium derived relaxing factor (EDRF) and contracting factors (EDCF) in the control of cardiovascular homeostasis: the pioneering observations. In:Rubanyi Gȧ ed. Cardiovascular significance of endothelium derived vasoactive factors. New York: Futara, 1991.39-64
, ΑΌΡ¥“Ϋ“©
5 Jennifer SP, Nakane M, Buttery LDK, et al. Characterization and localization of endothelial nitric oxide synthase using specific monoclonal antibodies. Am J Physiol,1993,265:C1379-1387
6 Clive JL, Barry AB. What is the relationship between the endothelium derived relaxant factor and nitric oxide? Life Sci, 1989,45(1):1-14
7 Loesch A, Burnstock G. Ultrastructural localization of nitric oxide synthase and endothelin in coronary and pulmonary arteries of newborn rats. Cell Tissue Res, 1995,279:475-483
8 Ε≈Ψϋ±Θ,άνΆρ’ρ,άη ΈΡ,Β».¬ΐ–‘ΒΆ―θ¥σ σΖΈΕ·¬ωΡΎΤΛΥΊmRNAΒΡ±μ¥οΦΑΕ®ΈΜ.±±Ψ©“ΫΩΤ¥σ―ß―ß±®Θ§ 1997,29(1):15-17
(1999-04-21 ’Ηε), ΑΌΡ¥“Ϋ“©