���ú˴ż���ȷ�������ǻ�̼�յĽṹ����
���ߣ������� ������ ������
��λ��������ѧҩѧԺ��ѧ����ѧϵ������ 100083
�ؼ��ʣ������ǻ�̼�գ����ӽṹ���˴Ź���
����ҽ�ƴ�ѧѧ��000324 [ժ Ҫ] Ŀ�ģ�ȷ�������ǻ�̼�յĽṹ���ռ��Ĺ��͡��������Ժ˴Ź�����(���ף�̼�ף����������)Ϊ���������������������ƶϡ������֤ʵ�����ϳɵ���������ǻ�̼��a��e��Ϊ��-��ૹ��͡����ۣ�������Ʒ������²��ö��ֲ�������ֱ��ȷ֤�����ǻ�̼�յĽṹ�����ǿ��еġ�
[��ͼ�����] Q74 [���ױ�ʶ��] B
[���±��] 1000-1530(2000)03-0277-03
Affirming structure and configuration of free hydroxyl C-glycosides by NMR
, http://www.100md.com
WANG Wen-Zhong, LU Yi-Xian, ZHANG Pei-Ying
(Department of Chemical Biology, School of Pharmaceutical Sciences,Peking University,Beijing 100083, China)
ABSTRACT Objective�� To affirm structure and glycosidic bond configuration of free hydroxyl C-glycosides. Methods�� NMR (1HNMR, 13CNMR, 1H- 1HCOSY, NOESY , etc.) were used as dominant factors, assisted by other spectrum data. Results�� All free hydroxyl C-glycosides synthesized were ��-C-pyranglycosides. Conclusion�� It is possible to directly determine the structure and configuration of free hydroxyl C-glycosides with many kinds of spectrum data, which particularly suits circumstance of no contrast product.
, ��Ĵҽҩ
KEY WORDS Free hydroxyl C-glycosides; Molecular structure; Nuclear magnetic resonance��
���ž����������Ե���Ȼ̼�ջ�����(������showdomycin��vienomycin[1])���ϱ����֣�̼�ջ������Ϊ����Ѱ���½ṹҩ�����Ҫ��Դ֮һ���ر��ǽ����������ǻ�ѧ��ø��ѧ���л��ϳ��о���̼�ճ�Ϊ������֮�����ǹ�ע����һ�ȵ�֮һ�������о�����ø���Ƽ�����Ҫ������̼������������ǻ����Ա�֤�нϺõ�ˮ���Լ������ṹ�����̶ȵ������ԡ��������������ȩ�Ǻͼ�ȩ�ǿ�ʼ������һ��������רһ�Եغϳɳ�5�������-����DZ���ͪ��̼��(a��e��ͼ1)������������������(a��e)δ��������Ϊ�������Ժ˴���Ϊ�����������������ȷ֤�����ǵĽṹ���ռ��Ĺ��͡�
1 �����뷽��
1.1 �������Լ�
, http://www.100md.com
Ԫ�ط����ͺ�ΪPE-240C���˴Ź������� INOVA-500 �˴Ź����Dzⶨ�� TMS��Ϊ�ڱꡣ���¡��ܼ��� DMSO-d6,5 mm��Ʒ�ܣ� 1H 90������8.6 ��s�� 13C 90������16 ��s��̽ͷ��ID-PFG(����-�ݶ�̽ͷ)��NOESY���ʱ��0.8 s��������AEI MS-50 SD90(EIMS)��VG ZabspecE�����Dzⶨ(HMS)������������ͺ�ΪPE-983���������ͺ�AA-10R���۵�ⶨ��Ϊ�������۵�ⶨ�ǡ� �Լ���δע���ľ�Ϊ����CP��AR����Ʒ����������ֱ��ʹ�á�������Ʒͨ�� Wittig-Horner ��Ӧһ�����ϳɵõ���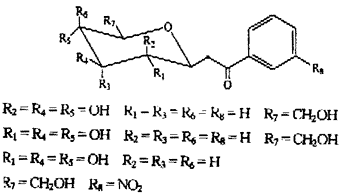
ͼ1 ̼��a��e
Figure 1 Structures of C-glycosides a-e
, ��Ĵҽҩ
1.2 ���Է���
ͨ��������ף�Ԫ�ط������߷ֱ�����a��e��Ʒ���ж��Լ������Ļ����ϣ���������Ʒ���������Ҫ����1HNMR��13CNMR��NOESY��1H-1H COSY�Ⱥ˴���ȷ֤�ǻ��Ĵ�С���ռ��Ĺ��͡�
2 ���
̼��a��e����Ҫ�������ݼ���1�����·�����̼��aΪ��������ṹ��C��H ������ͼ2����2��NOESY��ͼ3��
�����������ݱ���������̼��a��e�ǻ����־�Ϊ��ૻ����ռ�Ϊ��- ���͡�
��1 ̼��a��e����Ҫ��������
Table 1 Major determined data of C-glycosides a-e C-glycosides
, http://www.100md.com
m.p(��)
[��]26D
0
IR (cm-1)
13CNMR ��
1HNMR
�� H1
Element analysis
��C��0
��pH-H
, ��Ĵҽҩ
��C-NO2
C��O
C1
C6
CO��CH2
C
H
a
163
dep.
-17.39
C 0.46
, ��Ĵҽҩ
1 686
1 589
694
-
197.90
81.24
61.51
39.97
3.94
59.57
59.35
6.43��
6.73����
, ��Ĵҽҩ
b
203
-204
-20.00
C 0.60
1 671
1 590
684
-
198.20
80.75
61.08
41.30
, ��Ĵҽҩ
3.71
59.57
59.28
6.43��
6.15����
c
149.5
-151
+19.05
C 0.84
1 692
1 609
, http://www.100md.com
690
1 529
1 347
-
-
-
-
4.30
328.290 2����
328.102 7����
d
101
, http://www.100md.com -102
-49.12
C 0.57
1 672
1 591
687
-
198.90
78.18
65.16
41.16
3.94
253.266 4����
, ��Ĵҽҩ
253.106 9����
e
syrup
-40.00
C 0.40
1 673
1 593
687
-
198.40
81.75
59.77
, http://www.100md.com 42.86
4.10
-
��, HMS(M+H)+; ��,calculated data; ����, found data.��2 ̼��a NMR����(ԭ�ӱ�ż�ͼ2)
Table 2 1H and 13CNMR data of C-glycoside a(atomes positions see figure 2) ��H
7.95
7.65
7.54
4.72
, http://www.100md.com
4.69
4.52
4.32
3.94
3.65
3.63
3.41
3.35
3.28
3.05
H numbers
2
1
, http://www.100md.com
2
1
1
1
1
1
1
1
1
2
2
1
H positions
10
, http://www.100md.com
12
11
C4-
C3-
C2-
C6-
1
2
6
6��
3
7
, ��Ĵҽҩ
5
14
13
OH
OH
OH
OH
4
7��
��C
197.9
136.9
133.2
, http://www.100md.com
128.7
127.9
81.2
74.8
74.1
70.2
67.1
61.5
39.9
��C numbers
1
1
1
, ��Ĵҽҩ
2
2
1
1
3
1
1
C positions
8
9
12
10
11
1
, http://www.100md.com
5
2-4
6
7
14
13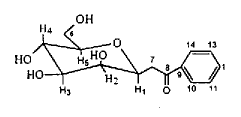
ͼ2 ̼��a�ṹʾ��ͼ
Figure 2 Structure of C-glycoside a
3 ����
Railton����[2]��Wittig ��Wittig-Horner��Ӧ����̼�յĺϳ�ʱ�����γ�ૻ���Ȼ����ת����ૻ�[3]�õ���-�ͦ�-��Ļ������ת�ɵ�һ�Ħ�-�塣�����Ǻϳɹ����У����ۺ�����Ϊԭ�ϣ�������Ӧ���̵�TLC����ֻ����һ��������㡣������̼��a(��-D-��¶�ǻ�����ͪ)Ϊ��˵��ȷ�����ﻷϵ��С���ռ����͵ķ�����
, ��Ĵҽҩ
�������Ͻ�����1HNMR����̼�յ�C1-HӦΪ���ط壬��ʵ����ֻ���������ط壬�����Ͳ���������ͨ����3JH1-H2���ж�C1����(ʵ�������ڸ�¶�ǵ�H1��H2�Ķ�����ڦ�-�ͦ�-���м��������������Ʒ������£�����3JH1-H2�ж�C1���Ϳɿ���Ҳ����)����Ȼ�ڦ�-�ͦ�-���1H��13C���У�H1��C1��λ��ֵ��һ�����죬����������Ӧ�����Ҳ�����жϡ���������NOESY��ȷ֤�˹��͡���������1�Ԧ������ʱ(ͼ2)��H1��H3��H5֮��Ӧ��NOEЧӦ[4]�����Ԧ�-��������˹�ϵ��������(ͼ3)����������ǰ�ߣ��˽��ͬ����˵����Ϊ��ૻ�������ૻ���
, http://www.100md.com
������̼���γɵ�̼��d��e���ӱ�1�г���
13 CNMR��C1�Ħ�ֵ�ɿ�������������̼�ǵ�̼�վ���ͬ�����͡����⣬��1H��ȷ���ǻ��Ĵ�С�������̼��(d)��1HNMR�ױ�����3��OH�е�H��Ϊd�壬˵����-OH������̼��ֻ��һ����ԭ�ӣ�������HOCH2-���ţ���ֻ������ૻ�(ͼ4��d-1)��������ૻ�(ͼ4��d-2)��e��1HNMR����֮���ơ�
ͼ3 ̼��a��NOESY��
Figure 3 NOESY spectra of C-glycoside a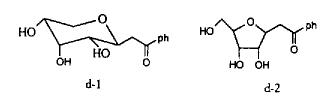
, ��Ĵҽҩ
ͼ4 ̼��d�����ֿ��ܽṹ
Figure 4 Two possible structures of C-glycoside d
�ڷ�������̼�յ������ѽ����ʱ���֣�̼��d��e û���ѵ��״�����Ƭ���ӡ����ѵ��״�����Ƭ���ӵĴ������ǻ���HO-CH2-���ŵ���Ҫ֤�ݣ������һ���Ƕ�Ҳ˵����̼��dΪ��ૻ�����
�����ң����ڻ���ú̿ҽѧԺ��
������Ŀ��������Ȼ��ѧ����(29472034)������Ŀ��
�����
[1]Imamura N, Kakinuma N, Ikekawa N, et al. The structure of vineomycin B2 [J]. Antibiot�� 1981, 34: 1517
, ��Ĵҽҩ
[2]Railton CJ, Clive DLJ. Wittig chain extension of unprotected carbohydrates: formation of carbohydrate-derived ��,��-unsaturated esters [J]. Carbohydrate Res, 1996��281: 69-77
[3]Davidson AH, Hughes LR, Qureshi SS, et al. Wittig reactions on unprotected aldohexoses: formation of optically active tetrahydrofurans and tetrahydropyrans [J]. Tetrahedron Lett, 1988��29: 693-669
[4]�ŵ¿� H���������W.�����˴Ź����ײ����ṹ[M].�ڵ�Ȫ��.����: ����ҽ�ƴ�ѧ�й�Э��ҽ�ƴ�ѧ���ϳ�����, 1991. 10-13
�ո����ڣ�2000-01-12, ��Ĵҽҩ
��λ��������ѧҩѧԺ��ѧ����ѧϵ������ 100083
�ؼ��ʣ������ǻ�̼�գ����ӽṹ���˴Ź���
����ҽ�ƴ�ѧѧ��000324 [ժ Ҫ] Ŀ�ģ�ȷ�������ǻ�̼�յĽṹ���ռ��Ĺ��͡��������Ժ˴Ź�����(���ף�̼�ף����������)Ϊ���������������������ƶϡ������֤ʵ�����ϳɵ���������ǻ�̼��a��e��Ϊ��-��ૹ��͡����ۣ�������Ʒ������²��ö��ֲ�������ֱ��ȷ֤�����ǻ�̼�յĽṹ�����ǿ��еġ�
[��ͼ�����] Q74 [���ױ�ʶ��] B
[���±��] 1000-1530(2000)03-0277-03
Affirming structure and configuration of free hydroxyl C-glycosides by NMR
, http://www.100md.com
WANG Wen-Zhong, LU Yi-Xian, ZHANG Pei-Ying
(Department of Chemical Biology, School of Pharmaceutical Sciences,Peking University,Beijing 100083, China)
ABSTRACT Objective�� To affirm structure and glycosidic bond configuration of free hydroxyl C-glycosides. Methods�� NMR (1HNMR, 13CNMR, 1H- 1HCOSY, NOESY , etc.) were used as dominant factors, assisted by other spectrum data. Results�� All free hydroxyl C-glycosides synthesized were ��-C-pyranglycosides. Conclusion�� It is possible to directly determine the structure and configuration of free hydroxyl C-glycosides with many kinds of spectrum data, which particularly suits circumstance of no contrast product.
, ��Ĵҽҩ
KEY WORDS Free hydroxyl C-glycosides; Molecular structure; Nuclear magnetic resonance��
���ž����������Ե���Ȼ̼�ջ�����(������showdomycin��vienomycin[1])���ϱ����֣�̼�ջ������Ϊ����Ѱ���½ṹҩ�����Ҫ��Դ֮һ���ر��ǽ����������ǻ�ѧ��ø��ѧ���л��ϳ��о���̼�ճ�Ϊ������֮�����ǹ�ע����һ�ȵ�֮һ�������о�����ø���Ƽ�����Ҫ������̼������������ǻ����Ա�֤�нϺõ�ˮ���Լ������ṹ�����̶ȵ������ԡ��������������ȩ�Ǻͼ�ȩ�ǿ�ʼ������һ��������רһ�Եغϳɳ�5�������-����DZ���ͪ��̼��(a��e��ͼ1)������������������(a��e)δ��������Ϊ�������Ժ˴���Ϊ�����������������ȷ֤�����ǵĽṹ���ռ��Ĺ��͡�
1 �����뷽��
1.1 �������Լ�
, http://www.100md.com
Ԫ�ط����ͺ�ΪPE-240C���˴Ź������� INOVA-500 �˴Ź����Dzⶨ�� TMS��Ϊ�ڱꡣ���¡��ܼ��� DMSO-d6,5 mm��Ʒ�ܣ� 1H 90������8.6 ��s�� 13C 90������16 ��s��̽ͷ��ID-PFG(����-�ݶ�̽ͷ)��NOESY���ʱ��0.8 s��������AEI MS-50 SD90(EIMS)��VG ZabspecE�����Dzⶨ(HMS)������������ͺ�ΪPE-983���������ͺ�AA-10R���۵�ⶨ��Ϊ�������۵�ⶨ�ǡ� �Լ���δע���ľ�Ϊ����CP��AR����Ʒ����������ֱ��ʹ�á�������Ʒͨ�� Wittig-Horner ��Ӧһ�����ϳɵõ���

ͼ1 ̼��a��e
Figure 1 Structures of C-glycosides a-e
, ��Ĵҽҩ
1.2 ���Է���
ͨ��������ף�Ԫ�ط������߷ֱ�����a��e��Ʒ���ж��Լ������Ļ����ϣ���������Ʒ���������Ҫ����1HNMR��13CNMR��NOESY��1H-1H COSY�Ⱥ˴���ȷ֤�ǻ��Ĵ�С���ռ��Ĺ��͡�
2 ���
̼��a��e����Ҫ�������ݼ���1�����·�����̼��aΪ��������ṹ��C��H ������ͼ2����2��NOESY��ͼ3��
�����������ݱ���������̼��a��e�ǻ����־�Ϊ��ૻ����ռ�Ϊ��- ���͡�
��1 ̼��a��e����Ҫ��������
Table 1 Major determined data of C-glycosides a-e C-glycosides
, http://www.100md.com
m.p(��)
[��]26D
0
IR (cm-1)
13CNMR ��
1HNMR
�� H1
Element analysis
��C��0
��pH-H
, ��Ĵҽҩ
��C-NO2
C��O
C1
C6
CO��CH2
C
H
a
163
dep.
-17.39
C 0.46
, ��Ĵҽҩ
1 686
1 589
694
-
197.90
81.24
61.51
39.97
3.94
59.57
59.35
6.43��
6.73����
, ��Ĵҽҩ
b
203
-204
-20.00
C 0.60
1 671
1 590
684
-
198.20
80.75
61.08
41.30
, ��Ĵҽҩ
3.71
59.57
59.28
6.43��
6.15����
c
149.5
-151
+19.05
C 0.84
1 692
1 609
, http://www.100md.com
690
1 529
1 347
-
-
-
-
4.30
328.290 2����
328.102 7����
d
101
, http://www.100md.com -102
-49.12
C 0.57
1 672
1 591
687
-
198.90
78.18
65.16
41.16
3.94
253.266 4����
, ��Ĵҽҩ
253.106 9����
e
syrup
-40.00
C 0.40
1 673
1 593
687
-
198.40
81.75
59.77
, http://www.100md.com 42.86
4.10
-
��, HMS(M+H)+; ��,calculated data; ����, found data.��2 ̼��a NMR����(ԭ�ӱ�ż�ͼ2)
Table 2 1H and 13CNMR data of C-glycoside a(atomes positions see figure 2) ��H
7.95
7.65
7.54
4.72
, http://www.100md.com
4.69
4.52
4.32
3.94
3.65
3.63
3.41
3.35
3.28
3.05
H numbers
2
1
, http://www.100md.com
2
1
1
1
1
1
1
1
1
2
2
1
H positions
10
, http://www.100md.com
12
11
C4-
C3-
C2-
C6-
1
2
6
6��
3
7
, ��Ĵҽҩ
5
14
13
OH
OH
OH
OH
4
7��
��C
197.9
136.9
133.2
, http://www.100md.com
128.7
127.9
81.2
74.8
74.1
70.2
67.1
61.5
39.9
��C numbers
1
1
1
, ��Ĵҽҩ
2
2
1
1
3
1
1
C positions
8
9
12
10
11
1
, http://www.100md.com
5
2-4
6
7
14
13

ͼ2 ̼��a�ṹʾ��ͼ
Figure 2 Structure of C-glycoside a
3 ����
Railton����[2]��Wittig ��Wittig-Horner��Ӧ����̼�յĺϳ�ʱ�����γ�ૻ���Ȼ����ת����ૻ�[3]�õ���-�ͦ�-��Ļ������ת�ɵ�һ�Ħ�-�塣�����Ǻϳɹ����У����ۺ�����Ϊԭ�ϣ�������Ӧ���̵�TLC����ֻ����һ��������㡣������̼��a(��-D-��¶�ǻ�����ͪ)Ϊ��˵��ȷ�����ﻷϵ��С���ռ����͵ķ�����
, ��Ĵҽҩ
�������Ͻ�����1HNMR����̼�յ�C1-HӦΪ���ط壬��ʵ����ֻ���������ط壬�����Ͳ���������ͨ����3JH1-H2���ж�C1����(ʵ�������ڸ�¶�ǵ�H1��H2�Ķ�����ڦ�-�ͦ�-���м��������������Ʒ������£�����3JH1-H2�ж�C1���Ϳɿ���Ҳ����)����Ȼ�ڦ�-�ͦ�-���1H��13C���У�H1��C1��λ��ֵ��һ�����죬����������Ӧ�����Ҳ�����жϡ���������NOESY��ȷ֤�˹��͡���������1�Ԧ������ʱ(ͼ2)��H1��H3��H5֮��Ӧ��NOEЧӦ[4]�����Ԧ�-��������˹�ϵ��������(ͼ3)����������ǰ�ߣ��˽��ͬ����˵����Ϊ��ૻ�������ૻ���
, http://www.100md.com
������̼���γɵ�̼��d��e���ӱ�1�г���
13 CNMR��C1�Ħ�ֵ�ɿ�������������̼�ǵ�̼�վ���ͬ�����͡����⣬��1H��ȷ���ǻ��Ĵ�С�������̼��(d)��1HNMR�ױ�����3��OH�е�H��Ϊd�壬˵����-OH������̼��ֻ��һ����ԭ�ӣ�������HOCH2-���ţ���ֻ������ૻ�(ͼ4��d-1)��������ૻ�(ͼ4��d-2)��e��1HNMR����֮���ơ�

ͼ3 ̼��a��NOESY��
Figure 3 NOESY spectra of C-glycoside a

, ��Ĵҽҩ
ͼ4 ̼��d�����ֿ��ܽṹ
Figure 4 Two possible structures of C-glycoside d
�ڷ�������̼�յ������ѽ����ʱ���֣�̼��d��e û���ѵ��״�����Ƭ���ӡ����ѵ��״�����Ƭ���ӵĴ������ǻ���HO-CH2-���ŵ���Ҫ֤�ݣ������һ���Ƕ�Ҳ˵����̼��dΪ��ૻ�����
�����ң����ڻ���ú̿ҽѧԺ��
������Ŀ��������Ȼ��ѧ����(29472034)������Ŀ��
�����
[1]Imamura N, Kakinuma N, Ikekawa N, et al. The structure of vineomycin B2 [J]. Antibiot�� 1981, 34: 1517
, ��Ĵҽҩ
[2]Railton CJ, Clive DLJ. Wittig chain extension of unprotected carbohydrates: formation of carbohydrate-derived ��,��-unsaturated esters [J]. Carbohydrate Res, 1996��281: 69-77
[3]Davidson AH, Hughes LR, Qureshi SS, et al. Wittig reactions on unprotected aldohexoses: formation of optically active tetrahydrofurans and tetrahydropyrans [J]. Tetrahedron Lett, 1988��29: 693-669
[4]�ŵ¿� H���������W.�����˴Ź����ײ����ṹ[M].�ڵ�Ȫ��.����: ����ҽ�ƴ�ѧ�й�Э��ҽ�ƴ�ѧ���ϳ�����, 1991. 10-13
�ո����ڣ�2000-01-12, ��Ĵҽҩ