人硫氧还蛋白及其变异体对TF-1和NFS60细胞的凋亡抑制和促增殖效应
作者:王应 狄春辉 张颖妹 宋泉声 马大龙
单位:北京大学基础医学院免疫学系,北京 100083
关键词:硫氧还蛋白;药理学;hTRXδ3;凋亡;肿瘤细胞;培养的;药物作用
北京医科大学学报000413 [摘 要] 目的:比较rhTRX与rhTRXδ3对细胞因子依赖株TF-1细胞、NFS60细胞撤除细胞因子所诱导凋亡的抑制及促细胞增殖作用。方法:在大肠杆菌中克隆并表达重组hTRX和hTRXδ3,纯化rhTRX与rhTRXδ3蛋白,FACS检测凋亡细胞,MTT法检测细胞增殖。结果:在依赖IL-3、GM-CSF生长的TF-1细胞(人红白血病细胞)和依赖G-CSF生长的NFS60细胞(小鼠白血病细胞)撤除细胞因子后,加入rhTRXδ3比加入rhTRX能更有效地抑制这两种细胞的凋亡并有促增殖的作用。结论:重组hTRX和hTRXδ3有着不同的生物活性,rhTRXδ3有着更强的抑制这两种细胞的凋亡和促增殖的作用。
, 百拇医药
[中图分类号] Q251 [文献标识码] A [文章编号] 1000-1530(2000)04-0328-04
Human thioredoxin and its isoform inhibit apoptosis
and stimulate growth in TF-1 and NFS60 cells
WANG Ying
(Department of Immunology, Peking University, Beijing 100083, China)
DI Chun-Hui
(Department of Immunology, Peking University, Beijing 100083, China)
, http://www.100md.com
ZHANG Ying-Mei
(Department of Immunology, Peking University, Beijing 100083, China)
SONG Quan-Sheng
(Department of Immunology, Peking University, Beijing 100083, China)
MA Da-Long
(Department of Immunology, Peking University, Beijing 100083, China)
ABSTRACT Objective:
, 百拇医药
To compare cytoprotective activity against cytokine withdrawal-induced apoptosis and a growth-promoting effect between rhTRX and rhTRXδ3 in GM-CSF-dependent cell line TF-1 and G-CSF-dependent cell line NFS60. Methods: rhTRX and rhTRXδ3 are purified after cloning and expressing in E.coli., analysing apoptotic cells by fluorescence activated cell sorting(FACS), mesuring cellular proliferation by MTT assay. Results: rhTRXδ3 shows a more potently cytoprotective activity against cytokine withdrawal-induced apoptosis and a growth-promoting effect than that of rhTRX in GM-CSF-dependent cell line TF-1 and G-CSF-dependent cell line NFS60. Conclusion: Recombinant hTRX and hTRXδ3, expressed in E.coli, possess varions bioactivities.
, 百拇医药
KEY WORDS Thioredoxin/pharmacol; hTRXδ3; Apoptosis; Tumor cells, cultured/drug eff
(J Beijing Med Univ, 2000,32:328-331)
人硫氧还蛋白(human thioredoxin,hTRX)是一种硫氧化还原酶,与多种生物反应过程紧密相关,是一些细胞重要的生长调节因子[1]。已证实成人T白血病细胞的自分泌生长因子――成人T细胞衍生因子(adult T-cell derived factor ,ADF)即为hTRX[2]。在细胞内,hTRX调节细胞内信号分子、蛋白与蛋白、蛋白与核酸的相互作用,最终影响基因的表达[3]。在DNA与糖皮质激素受体结合、铁反应性结合蛋白与转铁蛋白受体mRNA的相互作用中TRX都是必不可少的。TRX可通过调节Ref-1/APEX而增强Jun/Fos复合物与转录因子AP-1位点的结合,还调节转录因子NF-κB与它的Cis位点结合及与DNA结合。最近,发现细胞内TRX可抑制凋亡信号调节激酶I(apoptosis signal-regulating kinase 1, ASK1)和CASPASE-3样蛋白酶的活性而抑制细胞凋亡[4,5]。TRX与2-含氧酸脱氢酶相互作用,不仅与TRX活性位点有关,还与活性区以外氨基酸残基的极性有关[6]。
, 百拇医药
本室在构建hTRX表达克隆中,在国际上首次发现在人胎肝细胞中存在一种hTRXδ3――hTRX的不同剪切形式(GenBank登记号为AF065241)[7],它缺少hTRX的第3外显子,活性部位Trp-Cys-Gly-Pro-Cys仍然存在,其它编码区域序列没有改变。为了研究hTRXδ3与hTRX在功能上的区别,我们表达和纯化成功重组hTRXδ3蛋白,首次发现在依赖IL-3、GM-CSF生长的TF-1细胞(人红白血病细胞)和依赖G-CSF生长的NFS60细胞(小鼠白血病细胞)撤除细胞因子后,加入rhTRXδ3比加入rhTRX能更有效地抑制这两种细胞的凋亡并有促增殖的作用。
1 材料与方法
1.1 材料
菌株:大肠杆菌pop2136(C600衍生株,含CI857基因,编码温度敏感的λ阻遏蛋白),由Raidaud博士惠赠。DH5αF'IQTM购自GIBCO-BRL公司。
, 百拇医药
质粒: pMT-hIL-3质粒由本室构建[8]。pGEM-3zf(±)质粒和pUC19质粒购自Promega公司。
组织和细胞:TF-1(来自红白血病病人的前髓系细胞株),NFS60细胞(小鼠白血病细胞):本室常规培养。
试剂:各种限制性内切酶、DNA修饰酶、核苷酸dNTP、ATP购自Boehring Mannheim、GIBCO-BRL、Promega、华美、Stratagene等公司。DEAE-Fast Flow柱填料购自Pharmacia公司。测序样品处理试剂盒:Auto Cycle TM Sequencing Kit,购自Pharmacia公司。ANNEXIN V-FITC由本室提供。
1.2 方法
pMT-hTRX和pMT-hTRXδ3原核表达质粒的构建:在获得的人胎肝PCR产物中加入Klenow酶30℃15 min以切去3′突起A,65℃灭活10 min,用Promega公司的Magic Minipres柱纯化PCR产物。然后将纯化的PCR产物用XbaI酶切,pMT-hIL-3质粒经HpaI、XbaI酶切,选用T4连接酶在14℃过夜连接。
, 百拇医药
核酸序列测定:将pMT-hTRX和pMT-hTRXδ3用EcoRI和XbaI酶切后释放的含有全部目的基因的片段克隆到pGEM-3zf(±)或pUC19质粒载体中,提取质粒用试剂盒Auto CycleTM Seguencing Kit处理质粒样品后,在ALF DNA自动序列分析仪上测序。
质粒转化、诱导及细菌裂解:按本室方法进行[9]。
蛋白分离纯化:经凝血酶切的蛋白样品,上DEAE Fast Flow柱,收集NaCl梯度洗脱的各样品峰。
细胞增殖测定:在依赖IL-3、GM-CSF生长的TF-1细胞(人红白血病细胞)和依赖G-CSF生长的NFS60细胞(小鼠白血病细胞)的培养基中,撤除细胞因子后,加入rhTRXδ3和rhTRX蛋白,48~72 h后,加MTT,4~6 h后加入裂解液,12~24 h后用酶联免疫检测仪测定540 nm吸光度(D540nm),以不加因子细胞孔作为空白对照。
, 百拇医药
细胞凋亡检测:在依赖IL-3、GM-CSF生长的TF-1细胞(人红白血病细胞)和依赖G-CSF生长的NFS60细胞(小鼠白血病细胞)的培养基中,撤除细胞因子后,加入rhTRXδ3和rhTRX蛋白,18 h后,用PBS洗细胞1次,用200 μl Binding Buffer悬起,加入ANNEXIN V-FITC(终质量浓度1 mg.L-1)、PI(终质量浓度2.5mg.L-1),室温避光保存15 min,用流式细胞仪进行检测。
2 结果
2.1 原核表达质粒pMT-hTRX和pMT-hTRXδ3的构建
将人胎肝RT-PCR产物用XbaI酶切与pMT-hIL-3质粒HpaI、XbaI酶切产物连接,转化pop2136菌,涂LA板,37℃过夜。挑细菌克隆,经30℃增菌,42℃诱导表达后,125g.L-1 SDS-PAGE分析,筛选出两种不同蛋白相对分子质量的阳性克隆。这两种克隆的质粒分别经StyI、PstI、VspI酶切,10g.L-1琼脂糖凝胶电泳分析鉴定,与理论计算的酶切片段大小相符。同时,我们以构建的质粒为模板进行PCR,经80g.L-1丙烯酰胺凝胶电泳鉴定为带目的基因的目的克隆。因此,初步确定,我们获得了pMT-hTRX和pMT-hTRXδ3原核表达质粒。
, 百拇医药
2.2 核酸序列分析
测序结果与文献[2,10]报道的hTRX cDNA序列比较,核酸序列完全无误,证明我们同时获得了pMT-hTRXδ3和pMT-hTRX 两种表达克隆。
2.3 大肠杆菌中原核表达蛋白的分析
150 g.L-1 SDS-PAGE结果表明,pMT-hTRX克隆表达约25 000左右的融合蛋白,经超声裂解细菌后,超声上清中含有可溶性的pMT-hTRX表达蛋白。pMT-hTRXδ3克隆表达约23 000左右的融合蛋白,以包涵体形式存在,其超声上清中无可溶性的pMT-hTRXδ3表达蛋白。pMT-hTRX表达的融合蛋白MS2-hTRX和pMT-hTRXδ3表达的融合蛋白MS2-hTRXδ3经凝血酶消化,切下MS2,再经DEAE Fast Flow柱分离,得到纯化的蛋白(图1),纯度达95%,并用于活性测定。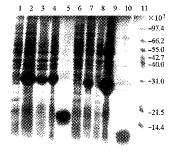
, http://www.100md.com
1, negative control of E.coli lysate; 2, rhTRX expressed in E.coli;
3, sonic supernatant of rhTRX expressed in E.coli; 4, Inclusion body of rhTRX;
5, purified rhTRX protein; 6, negative control of E.coli lysate;
7, rhTRXδ3 expressed in E.coli; 8, sonic supernatant of rhTRXδ3
expressed in E.coli; 9, inclusion body of rhTRXδ3; 10, purified rhTRXδ3
, 百拇医药
protein; 11, molecularmarker(Promega).
图1 SDS-PAGE分析 pMT-hTRX和pMT-hTRXδ3
质粒所表达的融合蛋白及纯化蛋白
Figure 1 Analysis by SDS-PAGE on rhTRX
and rhTRXδ3 from E.coli
2.4 重组的hTRX和hTRXδ3活性比较
MTT法检测结果显示,在依赖IL-3、GM-CSF生长的TF-1细胞(人红白血病细胞)和依赖G-CSF生长的NFS60细胞(小鼠白血病细胞)的培养基中,撤除细胞因子后,加入rhTRXδ3比加入rhTRX能更有效地促细胞增殖(图2)。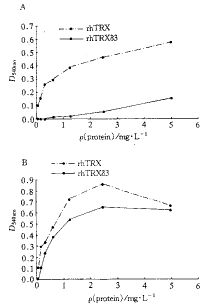
, 百拇医药
图2 rhTRX和rhTRXδ3在TF-1(A)、NFS(B)细胞上的活性
Figure 2 The effect of rhTRX and rhTRXδ3
on TF-1(A), NFS(B) cells
FACS检测结果显示,在依赖IL-3、GM-CSF生长的TF-1细胞(人红白血病细胞)中,撤除细胞因子,加入rhTRXδ3的ANNEXIN V-FITC标记细胞率为10.06%,而加入rhTRX的ANNEXIN V-FITC标记细胞率为18.22%。在依赖G-CSF生长的NFS60细胞(小鼠白血病细胞)的培养基中,撤除细胞因子,加入rhTRXδ3的ANNEXIN V-FITC标记细胞率为8.80%,而加入rhTRX的ANNEXIN V-FITC标记细胞率为11.55%。因此,加入rhTRXδ3比加入rhTRX能更有效地抑制细胞早期凋亡(图3,4)。
, 百拇医药
A, the effect on cytokine withdrawal TF-1 cells for 18h;
B, negative control of TF-1 cells; C, the effect of rhTRX(1 mg.L-1)
on TF-1 cells for 18h after cytokine withdrawal; D, the effect of
rhTRXδ3 (1mg.L-1) on TF-1 cells for 18 h after cytokine withdrawal.
图3 rhTRX和rhTRXδ3作用于TF-1细胞的
, 百拇医药
AnnexinV流式细胞仪检测结果
Figure 3 The effect of rhTRX and rhTRXδ3 on TF-1 cells
and analysing apoptotic cells by FACS
A, the effect on cytokine withdrawal NFS60 cells for 18h;
B, negative control of NFS60 cells; C, the effect of rhTRX(1 mg.L-1)
on NFS60 cells for 18h after cytokine withdrawal; D, the effect of
, http://www.100md.com
rhTRXδ3 (1mg.L-1) on NFS60 cells for 18 h after cytokine withdrawal
图4 rhTRX和rhTRXδ3作用于NFS60细胞的
AnnexinV流式细胞仪检测结果
Figure 4 The effect of rhTRX and rhTRXδ3 on NFS60 cells and
analysing apoptotic cells by FACS
3 讨论
生物的选择性剪切机制导致了同种蛋白多样性的产生,这些同种异型蛋白可能产生自不同的组织,表达在不同分化状态的细胞,表现出不同的功能和位于细胞的不同的部位。
, 百拇医药
蛋白水平生物活性分析证明,虽然hTRXδ3缺少第3外显子,酶活性位点仍然存在,但它依赖DTT催化胰岛素还原的活性明显低于完整的hTRX。这说明,第3外显子所表达的氨基酸对蛋白空间构型有影响,是充分发挥hTRX酶活性所必不可少的[7]。
而在依赖IL-3、GM-CSF生长的TF-1细胞(人红白血病细胞)和依赖G-CSF生长的NFS60细胞(小鼠白血病细胞)的培养基中,撤除细胞因子后,我们首次发现,加入rhTRXδ3比加入rhTRX能更有效地抑制这两种细胞的凋亡并有促增殖的作用,进一步说明hTRXδ3缺失第3外显子编码的20个氨基酸,可能使其蛋白空间构型与hTRX的不同,从而承担着不同的生物学功能。
TRX与2-含氧酸脱氢酶相互作用,不仅与TRX活性位点有关,还与活性区以外氨基酸残基的极性有关[6],提示我们第3外显子所表达的氨基酸还可能对蛋白的极性有影响,从而导致了rhTRXδ3与rhTRX功能的差异。文献报道细胞内TRX可调节NF-κB、 AP-1的活性,抑制凋亡信号调节激酶I和CASPASE-3样蛋白酶的活性而抑制细胞凋亡[4,5]。我们的实验结果说明细胞外的rhTRX也可抑制细胞凋亡,而rhTRXδ3可能有着更强的抑制凋亡信号调节激酶I(ASK1)和CASPASE-3样蛋白酶的活性,或者可能具有新的调控功能和信号转导的途径。进一步深入拓展这一新发现可能具有重要的理论意义和应用前景。
, 百拇医药
(感谢我校陶家平、马士良和韩梅老师帮助进行流式细胞仪检测和数据分析。)
参考文献
1,Anna R, Neris B, Roberto S. High rates of thioredoxin secretion correlate with growth arrest[J]. Cancer Res, 1995,55:675-680
2,Pamela Y, John E O , Ian A C, et al. The predicted amino acid sequence of human thioredoxin is identical to that of the autocrine growth factor human adult T-cell derived factor (ADF): thioredoxin mRNA is elevated in some human tumors[J]. Biochim Biophys Acta, 1994,1218:292-296
, http://www.100md.com
3,Nakamura H. Redox regulation of cellular activation[J]. Annu Rev Immunol. 1997,15:351-369
4,Saitoh M. Mammalian thioredoxin is a direct inhibitor of apoptosis signal-regulating kinase(ASK)1[J]. EMBO J. 1998,17:2596-2606
5,Ueda S. Redox regulation of caspase-3(-like) protease activity: regulatory roles of thioredoxin and cytochrome C[J]. J Immunol. 1998,161:6689-6695
6,Bunik V. Interaction of thioredoxins with target proteins: role of particular structural elements and electrostatic properties of thioredoxins in their interplay with 2-oxoacid dehydrogenase complexes[J]. Protein Sci, 1999,8:65-74
, 百拇医药
7,王 应,王玉刚,张颖妹,等.人硫氧还蛋白存在不同的选择性剪切形式[J].科学通报,1998,43:63-66
8,马大龙,狄春辉,宋泉生,等.人白细胞IL-9 cDNA的PCR扩增及其在大肠杆菌的表达[J].北京医科大学学报,1994,26(4):243-247
9,刘 洁,马大龙,狄春辉,等.重组白细胞IL-3同源双体分子基因在大肠杆菌的表达[J].中华血液学杂志,1993,14(9):475-480
10,Wollman EE, d'Auriol, Rimsky L, et al. Cloning and expression of a cDNA for human thioredoxin[J]. J Biol Chem, 1988, 263:15506-15512
(2000-03-31收稿), 百拇医药
单位:北京大学基础医学院免疫学系,北京 100083
关键词:硫氧还蛋白;药理学;hTRXδ3;凋亡;肿瘤细胞;培养的;药物作用
北京医科大学学报000413 [摘 要] 目的:比较rhTRX与rhTRXδ3对细胞因子依赖株TF-1细胞、NFS60细胞撤除细胞因子所诱导凋亡的抑制及促细胞增殖作用。方法:在大肠杆菌中克隆并表达重组hTRX和hTRXδ3,纯化rhTRX与rhTRXδ3蛋白,FACS检测凋亡细胞,MTT法检测细胞增殖。结果:在依赖IL-3、GM-CSF生长的TF-1细胞(人红白血病细胞)和依赖G-CSF生长的NFS60细胞(小鼠白血病细胞)撤除细胞因子后,加入rhTRXδ3比加入rhTRX能更有效地抑制这两种细胞的凋亡并有促增殖的作用。结论:重组hTRX和hTRXδ3有着不同的生物活性,rhTRXδ3有着更强的抑制这两种细胞的凋亡和促增殖的作用。
, 百拇医药
[中图分类号] Q251 [文献标识码] A [文章编号] 1000-1530(2000)04-0328-04
Human thioredoxin and its isoform inhibit apoptosis
and stimulate growth in TF-1 and NFS60 cells
WANG Ying
(Department of Immunology, Peking University, Beijing 100083, China)
DI Chun-Hui
(Department of Immunology, Peking University, Beijing 100083, China)
, http://www.100md.com
ZHANG Ying-Mei
(Department of Immunology, Peking University, Beijing 100083, China)
SONG Quan-Sheng
(Department of Immunology, Peking University, Beijing 100083, China)
MA Da-Long
(Department of Immunology, Peking University, Beijing 100083, China)
ABSTRACT Objective:
, 百拇医药
To compare cytoprotective activity against cytokine withdrawal-induced apoptosis and a growth-promoting effect between rhTRX and rhTRXδ3 in GM-CSF-dependent cell line TF-1 and G-CSF-dependent cell line NFS60. Methods: rhTRX and rhTRXδ3 are purified after cloning and expressing in E.coli., analysing apoptotic cells by fluorescence activated cell sorting(FACS), mesuring cellular proliferation by MTT assay. Results: rhTRXδ3 shows a more potently cytoprotective activity against cytokine withdrawal-induced apoptosis and a growth-promoting effect than that of rhTRX in GM-CSF-dependent cell line TF-1 and G-CSF-dependent cell line NFS60. Conclusion: Recombinant hTRX and hTRXδ3, expressed in E.coli, possess varions bioactivities.
, 百拇医药
KEY WORDS Thioredoxin/pharmacol; hTRXδ3; Apoptosis; Tumor cells, cultured/drug eff
(J Beijing Med Univ, 2000,32:328-331)
人硫氧还蛋白(human thioredoxin,hTRX)是一种硫氧化还原酶,与多种生物反应过程紧密相关,是一些细胞重要的生长调节因子[1]。已证实成人T白血病细胞的自分泌生长因子――成人T细胞衍生因子(adult T-cell derived factor ,ADF)即为hTRX[2]。在细胞内,hTRX调节细胞内信号分子、蛋白与蛋白、蛋白与核酸的相互作用,最终影响基因的表达[3]。在DNA与糖皮质激素受体结合、铁反应性结合蛋白与转铁蛋白受体mRNA的相互作用中TRX都是必不可少的。TRX可通过调节Ref-1/APEX而增强Jun/Fos复合物与转录因子AP-1位点的结合,还调节转录因子NF-κB与它的Cis位点结合及与DNA结合。最近,发现细胞内TRX可抑制凋亡信号调节激酶I(apoptosis signal-regulating kinase 1, ASK1)和CASPASE-3样蛋白酶的活性而抑制细胞凋亡[4,5]。TRX与2-含氧酸脱氢酶相互作用,不仅与TRX活性位点有关,还与活性区以外氨基酸残基的极性有关[6]。
, 百拇医药
本室在构建hTRX表达克隆中,在国际上首次发现在人胎肝细胞中存在一种hTRXδ3――hTRX的不同剪切形式(GenBank登记号为AF065241)[7],它缺少hTRX的第3外显子,活性部位Trp-Cys-Gly-Pro-Cys仍然存在,其它编码区域序列没有改变。为了研究hTRXδ3与hTRX在功能上的区别,我们表达和纯化成功重组hTRXδ3蛋白,首次发现在依赖IL-3、GM-CSF生长的TF-1细胞(人红白血病细胞)和依赖G-CSF生长的NFS60细胞(小鼠白血病细胞)撤除细胞因子后,加入rhTRXδ3比加入rhTRX能更有效地抑制这两种细胞的凋亡并有促增殖的作用。
1 材料与方法
1.1 材料
菌株:大肠杆菌pop2136(C600衍生株,含CI857基因,编码温度敏感的λ阻遏蛋白),由Raidaud博士惠赠。DH5αF'IQTM购自GIBCO-BRL公司。
, 百拇医药
质粒: pMT-hIL-3质粒由本室构建[8]。pGEM-3zf(±)质粒和pUC19质粒购自Promega公司。
组织和细胞:TF-1(来自红白血病病人的前髓系细胞株),NFS60细胞(小鼠白血病细胞):本室常规培养。
试剂:各种限制性内切酶、DNA修饰酶、核苷酸dNTP、ATP购自Boehring Mannheim、GIBCO-BRL、Promega、华美、Stratagene等公司。DEAE-Fast Flow柱填料购自Pharmacia公司。测序样品处理试剂盒:Auto Cycle TM Sequencing Kit,购自Pharmacia公司。ANNEXIN V-FITC由本室提供。
1.2 方法
pMT-hTRX和pMT-hTRXδ3原核表达质粒的构建:在获得的人胎肝PCR产物中加入Klenow酶30℃15 min以切去3′突起A,65℃灭活10 min,用Promega公司的Magic Minipres柱纯化PCR产物。然后将纯化的PCR产物用XbaI酶切,pMT-hIL-3质粒经HpaI、XbaI酶切,选用T4连接酶在14℃过夜连接。
, 百拇医药
核酸序列测定:将pMT-hTRX和pMT-hTRXδ3用EcoRI和XbaI酶切后释放的含有全部目的基因的片段克隆到pGEM-3zf(±)或pUC19质粒载体中,提取质粒用试剂盒Auto CycleTM Seguencing Kit处理质粒样品后,在ALF DNA自动序列分析仪上测序。
质粒转化、诱导及细菌裂解:按本室方法进行[9]。
蛋白分离纯化:经凝血酶切的蛋白样品,上DEAE Fast Flow柱,收集NaCl梯度洗脱的各样品峰。
细胞增殖测定:在依赖IL-3、GM-CSF生长的TF-1细胞(人红白血病细胞)和依赖G-CSF生长的NFS60细胞(小鼠白血病细胞)的培养基中,撤除细胞因子后,加入rhTRXδ3和rhTRX蛋白,48~72 h后,加MTT,4~6 h后加入裂解液,12~24 h后用酶联免疫检测仪测定540 nm吸光度(D540nm),以不加因子细胞孔作为空白对照。
, 百拇医药
细胞凋亡检测:在依赖IL-3、GM-CSF生长的TF-1细胞(人红白血病细胞)和依赖G-CSF生长的NFS60细胞(小鼠白血病细胞)的培养基中,撤除细胞因子后,加入rhTRXδ3和rhTRX蛋白,18 h后,用PBS洗细胞1次,用200 μl Binding Buffer悬起,加入ANNEXIN V-FITC(终质量浓度1 mg.L-1)、PI(终质量浓度2.5mg.L-1),室温避光保存15 min,用流式细胞仪进行检测。
2 结果
2.1 原核表达质粒pMT-hTRX和pMT-hTRXδ3的构建
将人胎肝RT-PCR产物用XbaI酶切与pMT-hIL-3质粒HpaI、XbaI酶切产物连接,转化pop2136菌,涂LA板,37℃过夜。挑细菌克隆,经30℃增菌,42℃诱导表达后,125g.L-1 SDS-PAGE分析,筛选出两种不同蛋白相对分子质量的阳性克隆。这两种克隆的质粒分别经StyI、PstI、VspI酶切,10g.L-1琼脂糖凝胶电泳分析鉴定,与理论计算的酶切片段大小相符。同时,我们以构建的质粒为模板进行PCR,经80g.L-1丙烯酰胺凝胶电泳鉴定为带目的基因的目的克隆。因此,初步确定,我们获得了pMT-hTRX和pMT-hTRXδ3原核表达质粒。
, 百拇医药
2.2 核酸序列分析
测序结果与文献[2,10]报道的hTRX cDNA序列比较,核酸序列完全无误,证明我们同时获得了pMT-hTRXδ3和pMT-hTRX 两种表达克隆。
2.3 大肠杆菌中原核表达蛋白的分析
150 g.L-1 SDS-PAGE结果表明,pMT-hTRX克隆表达约25 000左右的融合蛋白,经超声裂解细菌后,超声上清中含有可溶性的pMT-hTRX表达蛋白。pMT-hTRXδ3克隆表达约23 000左右的融合蛋白,以包涵体形式存在,其超声上清中无可溶性的pMT-hTRXδ3表达蛋白。pMT-hTRX表达的融合蛋白MS2-hTRX和pMT-hTRXδ3表达的融合蛋白MS2-hTRXδ3经凝血酶消化,切下MS2,再经DEAE Fast Flow柱分离,得到纯化的蛋白(图1),纯度达95%,并用于活性测定。

, http://www.100md.com
1, negative control of E.coli lysate; 2, rhTRX expressed in E.coli;
3, sonic supernatant of rhTRX expressed in E.coli; 4, Inclusion body of rhTRX;
5, purified rhTRX protein; 6, negative control of E.coli lysate;
7, rhTRXδ3 expressed in E.coli; 8, sonic supernatant of rhTRXδ3
expressed in E.coli; 9, inclusion body of rhTRXδ3; 10, purified rhTRXδ3
, 百拇医药
protein; 11, molecularmarker(Promega).
图1 SDS-PAGE分析 pMT-hTRX和pMT-hTRXδ3
质粒所表达的融合蛋白及纯化蛋白
Figure 1 Analysis by SDS-PAGE on rhTRX
and rhTRXδ3 from E.coli
2.4 重组的hTRX和hTRXδ3活性比较
MTT法检测结果显示,在依赖IL-3、GM-CSF生长的TF-1细胞(人红白血病细胞)和依赖G-CSF生长的NFS60细胞(小鼠白血病细胞)的培养基中,撤除细胞因子后,加入rhTRXδ3比加入rhTRX能更有效地促细胞增殖(图2)。

, 百拇医药
图2 rhTRX和rhTRXδ3在TF-1(A)、NFS(B)细胞上的活性
Figure 2 The effect of rhTRX and rhTRXδ3
on TF-1(A), NFS(B) cells
FACS检测结果显示,在依赖IL-3、GM-CSF生长的TF-1细胞(人红白血病细胞)中,撤除细胞因子,加入rhTRXδ3的ANNEXIN V-FITC标记细胞率为10.06%,而加入rhTRX的ANNEXIN V-FITC标记细胞率为18.22%。在依赖G-CSF生长的NFS60细胞(小鼠白血病细胞)的培养基中,撤除细胞因子,加入rhTRXδ3的ANNEXIN V-FITC标记细胞率为8.80%,而加入rhTRX的ANNEXIN V-FITC标记细胞率为11.55%。因此,加入rhTRXδ3比加入rhTRX能更有效地抑制细胞早期凋亡(图3,4)。

, 百拇医药
A, the effect on cytokine withdrawal TF-1 cells for 18h;
B, negative control of TF-1 cells; C, the effect of rhTRX(1 mg.L-1)
on TF-1 cells for 18h after cytokine withdrawal; D, the effect of
rhTRXδ3 (1mg.L-1) on TF-1 cells for 18 h after cytokine withdrawal.
图3 rhTRX和rhTRXδ3作用于TF-1细胞的
, 百拇医药
AnnexinV流式细胞仪检测结果
Figure 3 The effect of rhTRX and rhTRXδ3 on TF-1 cells
and analysing apoptotic cells by FACS

A, the effect on cytokine withdrawal NFS60 cells for 18h;
B, negative control of NFS60 cells; C, the effect of rhTRX(1 mg.L-1)
on NFS60 cells for 18h after cytokine withdrawal; D, the effect of
, http://www.100md.com
rhTRXδ3 (1mg.L-1) on NFS60 cells for 18 h after cytokine withdrawal
图4 rhTRX和rhTRXδ3作用于NFS60细胞的
AnnexinV流式细胞仪检测结果
Figure 4 The effect of rhTRX and rhTRXδ3 on NFS60 cells and
analysing apoptotic cells by FACS
3 讨论
生物的选择性剪切机制导致了同种蛋白多样性的产生,这些同种异型蛋白可能产生自不同的组织,表达在不同分化状态的细胞,表现出不同的功能和位于细胞的不同的部位。
, 百拇医药
蛋白水平生物活性分析证明,虽然hTRXδ3缺少第3外显子,酶活性位点仍然存在,但它依赖DTT催化胰岛素还原的活性明显低于完整的hTRX。这说明,第3外显子所表达的氨基酸对蛋白空间构型有影响,是充分发挥hTRX酶活性所必不可少的[7]。
而在依赖IL-3、GM-CSF生长的TF-1细胞(人红白血病细胞)和依赖G-CSF生长的NFS60细胞(小鼠白血病细胞)的培养基中,撤除细胞因子后,我们首次发现,加入rhTRXδ3比加入rhTRX能更有效地抑制这两种细胞的凋亡并有促增殖的作用,进一步说明hTRXδ3缺失第3外显子编码的20个氨基酸,可能使其蛋白空间构型与hTRX的不同,从而承担着不同的生物学功能。
TRX与2-含氧酸脱氢酶相互作用,不仅与TRX活性位点有关,还与活性区以外氨基酸残基的极性有关[6],提示我们第3外显子所表达的氨基酸还可能对蛋白的极性有影响,从而导致了rhTRXδ3与rhTRX功能的差异。文献报道细胞内TRX可调节NF-κB、 AP-1的活性,抑制凋亡信号调节激酶I和CASPASE-3样蛋白酶的活性而抑制细胞凋亡[4,5]。我们的实验结果说明细胞外的rhTRX也可抑制细胞凋亡,而rhTRXδ3可能有着更强的抑制凋亡信号调节激酶I(ASK1)和CASPASE-3样蛋白酶的活性,或者可能具有新的调控功能和信号转导的途径。进一步深入拓展这一新发现可能具有重要的理论意义和应用前景。
, 百拇医药
(感谢我校陶家平、马士良和韩梅老师帮助进行流式细胞仪检测和数据分析。)
参考文献
1,Anna R, Neris B, Roberto S. High rates of thioredoxin secretion correlate with growth arrest[J]. Cancer Res, 1995,55:675-680
2,Pamela Y, John E O , Ian A C, et al. The predicted amino acid sequence of human thioredoxin is identical to that of the autocrine growth factor human adult T-cell derived factor (ADF): thioredoxin mRNA is elevated in some human tumors[J]. Biochim Biophys Acta, 1994,1218:292-296
, http://www.100md.com
3,Nakamura H. Redox regulation of cellular activation[J]. Annu Rev Immunol. 1997,15:351-369
4,Saitoh M. Mammalian thioredoxin is a direct inhibitor of apoptosis signal-regulating kinase(ASK)1[J]. EMBO J. 1998,17:2596-2606
5,Ueda S. Redox regulation of caspase-3(-like) protease activity: regulatory roles of thioredoxin and cytochrome C[J]. J Immunol. 1998,161:6689-6695
6,Bunik V. Interaction of thioredoxins with target proteins: role of particular structural elements and electrostatic properties of thioredoxins in their interplay with 2-oxoacid dehydrogenase complexes[J]. Protein Sci, 1999,8:65-74
, 百拇医药
7,王 应,王玉刚,张颖妹,等.人硫氧还蛋白存在不同的选择性剪切形式[J].科学通报,1998,43:63-66
8,马大龙,狄春辉,宋泉生,等.人白细胞IL-9 cDNA的PCR扩增及其在大肠杆菌的表达[J].北京医科大学学报,1994,26(4):243-247
9,刘 洁,马大龙,狄春辉,等.重组白细胞IL-3同源双体分子基因在大肠杆菌的表达[J].中华血液学杂志,1993,14(9):475-480
10,Wollman EE, d'Auriol, Rimsky L, et al. Cloning and expression of a cDNA for human thioredoxin[J]. J Biol Chem, 1988, 263:15506-15512
(2000-03-31收稿), 百拇医药