分次小剂量131I-C50抑制肿瘤转移机制初探
作者:丁勇 田嘉禾 张锦明 曹丽敏 李清 陈英茂 张书文 冯惠茹 关志伟
单位:丁勇 田嘉禾 张锦明 曹丽敏 陈英茂 张书文 冯惠茹 关志伟(北京,解放军总医院核医学科 100853);李清(解放军307医院病理科)
关键词:
中华核医学杂志000414 在以往的实验中发现,分次小剂量放射免疫治疗(RIT)对荷瘤小鼠实验动物模型肿瘤的抑制和控制转移与单次大剂量RIT、单纯化疗、手术比较,作用更明显。本研究探讨了小剂量RIT的抑瘤机制,现报道如下。
材料与方法
1. 动物模型。T739近交系小鼠,6~8周龄,体重22~25 g,雌雄不限(中国医学科学院肿瘤研究所提供)。小鼠右下肢后臀部皮下接种LA-795小鼠肺腺癌细胞瘤株(中国医学科学院肿瘤研究所提供),建立实验动物模型。
, http://www.100md.com
2. 抗体及标记。单克隆抗体C50(北京医科大学肿瘤研究所提供),以小鼠肺腺癌LA-795细胞为免疫原。用氯胺T法进行131I标记,标记后免疫活性为标记前85%(ELISA法测定);用纸层析法测定标记率,展开剂为生理盐水,C50标记率为50%~80%,分离后放化纯大于95%,比活度为18.5~370 MBq/mg。
3. 化疗药物。阿糖胞苷(Arc)。
4. 实验分组。对照组,腹腔注射生理盐水0.2 mL,1次/d,共14次;化疗组:腹腔注射Arc,0.8 mg/d,共14次;分次小剂量RIT组,尾静脉注射131I-C50 1.85 MBq,1次/3 d,共5次;冷抗体组:尾静脉注射0.05 mg(0.2 L)C50,1次/3 d,共5次;131I组,尾静脉注射131I 1.85 MBq,1次/3 d,共5次。
, 百拇医药
5. 实验方案。疗效观察:在小鼠接种后第7 d随机分成5组(每组10只)。各组按上述给药方法给药,实验结束(第21 d)处死动物,称瘤重及体重,记录小鼠全肺表面的转移结节数,并作病理切片检查。小剂量RIT对免疫系统的影响:分2组(每组8只),给药24 h后眼眶取血,肝素抗凝,进行小鼠外周血T淋巴细胞亚群分类,数50个细胞分别计量CD3+,L3T4+,Lyt-2+,T细胞数。小剂量RIT对小鼠胸腺淋巴细胞、肿瘤细胞增殖周期的影响:分2组(每组4只),24 h后杀死小鼠,取胸腺、肿瘤组织,机械法制成单细胞悬液,用流式细胞仪测定细胞周期分布。
6. 观察指标。观察小鼠体重变化、瘤灶生长(瘤重)、肺及其他器官内转移数量,采用碱性磷酸酶-抗碱性磷酸酶法测量小鼠外周血T淋巴细胞亚群的变化,采用流式细胞仪测定胸腺淋巴细胞和肿瘤细胞的细胞周期分布的改变。
7. 统计学处理。采用SAS统计软件行组间方差分析及t检验。
, http://www.100md.com
结 果
1. 不同治疗方法结果比较。各组给药后小鼠体重、瘤重、转移数的变化结果见表1。以放免组疗效最佳,化疗组次之,131I组再次之,冷抗体组与对照组比较无明显治疗作用。病理观察:对照组、冷抗体组、131I组小鼠肺组织内可见肿瘤广泛转移及心脏转移。化疗组肺组织病理切片镜下观察肺转移未见明显减少,但不侵犯心脏。放免组肺转移数较少,转移灶多孤立,未见心脏受累。
2. 小剂量放射性核素内照射的免疫“兴奋效应"。小剂量RIT组与对照组比较,小鼠T淋巴细胞亚群CD3+和L3T4+(CD4+)增加,差异有显著性(t分别为2.42和2.29,P均<0.05),Lyt-2+(CD8+)减少,差异有显著性(t=3.14,P<0.01)。CD4+(Th)/CD8+(Ts)值升高。表明给药组荷瘤小鼠的机体免疫抑制状态被解除。
, 百拇医药
3. 小剂量RIT引起的小鼠胸腺淋巴细胞、肿瘤细胞增殖周期的改变。小剂量RIT后,小鼠的胸腺淋巴细胞及肿瘤细胞与对照组比较均呈现G0G1期细胞百分数的增加(G0G1期阻滞),G2M期细胞百分数、S期细胞百分数相对减少(表2)。
讨 论
小剂量RIT抑制和杀伤肿瘤细胞的
表1 各组用药后小鼠肺转移数、瘤重及体重变化(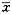 ±s) 组 别
±s) 组 别
肺转移数
瘤重(g)
体重变化(g)
, 百拇医药
对照组
26.4±3.9
5.7±0.7
-2.4±0.6
冷抗组
24.8±4.1
5.9±0.4
-1.9±0.7
化疗组
13.6±4.3△
3.1±0.5△
-0.8±0.3△
, 百拇医药
放免组
8.4±3.5*
3.1±0.7*
-0.5±0.2*
131 I组
17.6±3.7#
4.2±0.4#
-1.7±0.8#
注:与其他各组比较,*P均<0.05;与冷抗组、131I组、对照组比较,△P均<0.05;与对照组比较,#P<0.05表2 小鼠胸腺淋巴细胞和肿瘤细胞周期变化(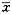 ±s)% 组 别
±s)% 组 别
, 百拇医药
G0G1
G2M
S
胸腺细胞
对照组
给药组
60.25±9.13
76.53±5.94(2.99)*
10.54±3.52
4.10±2.94(2.81)*
27.50±5.08
, 百拇医药
19.20±5.55
肿瘤细胞
对照组
给药组
63.60±6.68
84.16±3.91(5.31)*
11.27±2.63
4.94±3.61(2.83)*
25.02±5.18
10.88±3.42(4.21)*
注:括号内为t值;与对照组相比,*P<0.05机制为:①放射性核素所产生的核射线(主要是β射线)通过电离辐射的直接和间接作用,物理和化学作用杀灭肿瘤细胞;②通过直接相遇、渗透相遇、引力键定位3种定位机制使标记抗体能够特异性与肿瘤细胞结合;③小剂量放射性核素引入,虽机体吸收剂量低,但可刺激免疫系统,调动其自身的免疫机制,抑制或杀伤肿瘤细胞。
, 百拇医药
从RIT和131I治疗的结果看,前者抑制肿瘤肺转移的作用明显较后者强,但后者仍有一定的肿瘤抑制效果,可能是131I与血中蛋白质结合对肿瘤非特异性照射,但因未与抗体结合,故在体内不能有效地定位于瘤细胞,以至对瘤细胞的杀伤作用有限。小剂量内照射对机体免疫系统的刺激作用,可能是131I在实验动物中肿瘤抑制作用的机制之一。本研究结果示冷抗体对荷瘤小鼠无治疗作用,与文献[1]报道单纯抗体有抑瘤作用不符,可能与本实验所用抗体量偏小有关,但也表明实验时小剂量RIT的抑瘤效应不是单纯的131I或抗体作用,而是通过抗体与肿瘤细胞特异性亲和力把核素载带到肿瘤组织中,由于放射性核素在组织内射程较短,故主要聚集在肿瘤组织,而非瘤组织的吸收剂量很小,有利于保护正常组织。
射线主要是通过对细胞的敏感部位即“靶"的作用来损伤肿瘤细胞[2],同时细胞也经过自身的修复功能恢复其正常生理功能。两者的相互作用决定细胞的转归。分次RIT由于前次治疗杀伤部分肿瘤细胞,缓解了肿瘤组织内的高压,改善了血运, 使肿瘤内原来的乏氧细胞再充氧,恢复对射线的敏感性,有利于肿瘤细胞的杀伤[3]。射线对肿瘤细胞的作用还表现在改变细胞周期:实验中给予小剂量的放射性核素标记单克隆抗体后,小鼠胸腺淋巴细胞、肿瘤细胞明显出现G1期停滞,S期细胞减少。Palayoor等[4]报道G1期停滞和S期细胞减少,G2M阻滞时相缩短能使肿瘤细胞放射敏感性增加,加速肿瘤细胞死亡。
, 百拇医药
本研究结果显示,荷瘤小鼠给予低剂量RIT后,小鼠外周血T淋巴细胞亚群中CD3+细胞有所增加,L3T4+(CD4+,Th)细胞增加,而Lyt-2+(CD8+,TS)细胞相对减少,明显抑制肿瘤转移。可以认为低剂量辐射使抑制性T细胞(TS)遭到破坏而下降,辅助性T细胞(Th)增高并与TS的比值相应升高,导致免疫上调, 从而提高机体的免疫功能和抗肿瘤能力。 参 考 文 献
1,Jessy D, Siegal GP, Aberez RD, et al. Targeted tumor killing via an intracellular antibody against erb-b. J Clin Invest, 1995, 96:2980-2989.
, 百拇医药
2,Radford IR, George SH, Matthews PJ, et al. Critical DNA target size model of ionizing radiation-induced mammalian cell death. Int J Radiat Biol, 1998, 54:63-76.
3,Muschel RJ, Oernhard EJ, Garza L. Induction of apoptosis at different oxygen tention: evidence that oxygen radicals do not mediate apoptotic signaling. Cancer Res, 1995, 55:995-1003.
4,Palayoor ST, Macklis RM, Bump EA, et al. Modulation of radiation-induced apoptosis and G2/M block in murine T-lymphoma cell. Radiat Res, 1995, 141:235-243B.
(收稿日期:1999-08-09), 百拇医药
单位:丁勇 田嘉禾 张锦明 曹丽敏 陈英茂 张书文 冯惠茹 关志伟(北京,解放军总医院核医学科 100853);李清(解放军307医院病理科)
关键词:
中华核医学杂志000414 在以往的实验中发现,分次小剂量放射免疫治疗(RIT)对荷瘤小鼠实验动物模型肿瘤的抑制和控制转移与单次大剂量RIT、单纯化疗、手术比较,作用更明显。本研究探讨了小剂量RIT的抑瘤机制,现报道如下。
材料与方法
1. 动物模型。T739近交系小鼠,6~8周龄,体重22~25 g,雌雄不限(中国医学科学院肿瘤研究所提供)。小鼠右下肢后臀部皮下接种LA-795小鼠肺腺癌细胞瘤株(中国医学科学院肿瘤研究所提供),建立实验动物模型。
, http://www.100md.com
2. 抗体及标记。单克隆抗体C50(北京医科大学肿瘤研究所提供),以小鼠肺腺癌LA-795细胞为免疫原。用氯胺T法进行131I标记,标记后免疫活性为标记前85%(ELISA法测定);用纸层析法测定标记率,展开剂为生理盐水,C50标记率为50%~80%,分离后放化纯大于95%,比活度为18.5~370 MBq/mg。
3. 化疗药物。阿糖胞苷(Arc)。
4. 实验分组。对照组,腹腔注射生理盐水0.2 mL,1次/d,共14次;化疗组:腹腔注射Arc,0.8 mg/d,共14次;分次小剂量RIT组,尾静脉注射131I-C50 1.85 MBq,1次/3 d,共5次;冷抗体组:尾静脉注射0.05 mg(0.2 L)C50,1次/3 d,共5次;131I组,尾静脉注射131I 1.85 MBq,1次/3 d,共5次。
, 百拇医药
5. 实验方案。疗效观察:在小鼠接种后第7 d随机分成5组(每组10只)。各组按上述给药方法给药,实验结束(第21 d)处死动物,称瘤重及体重,记录小鼠全肺表面的转移结节数,并作病理切片检查。小剂量RIT对免疫系统的影响:分2组(每组8只),给药24 h后眼眶取血,肝素抗凝,进行小鼠外周血T淋巴细胞亚群分类,数50个细胞分别计量CD3+,L3T4+,Lyt-2+,T细胞数。小剂量RIT对小鼠胸腺淋巴细胞、肿瘤细胞增殖周期的影响:分2组(每组4只),24 h后杀死小鼠,取胸腺、肿瘤组织,机械法制成单细胞悬液,用流式细胞仪测定细胞周期分布。
6. 观察指标。观察小鼠体重变化、瘤灶生长(瘤重)、肺及其他器官内转移数量,采用碱性磷酸酶-抗碱性磷酸酶法测量小鼠外周血T淋巴细胞亚群的变化,采用流式细胞仪测定胸腺淋巴细胞和肿瘤细胞的细胞周期分布的改变。
7. 统计学处理。采用SAS统计软件行组间方差分析及t检验。
, http://www.100md.com
结 果
1. 不同治疗方法结果比较。各组给药后小鼠体重、瘤重、转移数的变化结果见表1。以放免组疗效最佳,化疗组次之,131I组再次之,冷抗体组与对照组比较无明显治疗作用。病理观察:对照组、冷抗体组、131I组小鼠肺组织内可见肿瘤广泛转移及心脏转移。化疗组肺组织病理切片镜下观察肺转移未见明显减少,但不侵犯心脏。放免组肺转移数较少,转移灶多孤立,未见心脏受累。
2. 小剂量放射性核素内照射的免疫“兴奋效应"。小剂量RIT组与对照组比较,小鼠T淋巴细胞亚群CD3+和L3T4+(CD4+)增加,差异有显著性(t分别为2.42和2.29,P均<0.05),Lyt-2+(CD8+)减少,差异有显著性(t=3.14,P<0.01)。CD4+(Th)/CD8+(Ts)值升高。表明给药组荷瘤小鼠的机体免疫抑制状态被解除。
, 百拇医药
3. 小剂量RIT引起的小鼠胸腺淋巴细胞、肿瘤细胞增殖周期的改变。小剂量RIT后,小鼠的胸腺淋巴细胞及肿瘤细胞与对照组比较均呈现G0G1期细胞百分数的增加(G0G1期阻滞),G2M期细胞百分数、S期细胞百分数相对减少(表2)。
讨 论
小剂量RIT抑制和杀伤肿瘤细胞的
表1 各组用药后小鼠肺转移数、瘤重及体重变化(
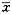 ±s) 组 别
±s) 组 别肺转移数
瘤重(g)
体重变化(g)
, 百拇医药
对照组
26.4±3.9
5.7±0.7
-2.4±0.6
冷抗组
24.8±4.1
5.9±0.4
-1.9±0.7
化疗组
13.6±4.3△
3.1±0.5△
-0.8±0.3△
, 百拇医药
放免组
8.4±3.5*
3.1±0.7*
-0.5±0.2*
131 I组
17.6±3.7#
4.2±0.4#
-1.7±0.8#
注:与其他各组比较,*P均<0.05;与冷抗组、131I组、对照组比较,△P均<0.05;与对照组比较,#P<0.05表2 小鼠胸腺淋巴细胞和肿瘤细胞周期变化(
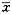 ±s)% 组 别
±s)% 组 别, 百拇医药
G0G1
G2M
S
胸腺细胞
对照组
给药组
60.25±9.13
76.53±5.94(2.99)*
10.54±3.52
4.10±2.94(2.81)*
27.50±5.08
, 百拇医药
19.20±5.55
肿瘤细胞
对照组
给药组
63.60±6.68
84.16±3.91(5.31)*
11.27±2.63
4.94±3.61(2.83)*
25.02±5.18
10.88±3.42(4.21)*
注:括号内为t值;与对照组相比,*P<0.05机制为:①放射性核素所产生的核射线(主要是β射线)通过电离辐射的直接和间接作用,物理和化学作用杀灭肿瘤细胞;②通过直接相遇、渗透相遇、引力键定位3种定位机制使标记抗体能够特异性与肿瘤细胞结合;③小剂量放射性核素引入,虽机体吸收剂量低,但可刺激免疫系统,调动其自身的免疫机制,抑制或杀伤肿瘤细胞。
, 百拇医药
从RIT和131I治疗的结果看,前者抑制肿瘤肺转移的作用明显较后者强,但后者仍有一定的肿瘤抑制效果,可能是131I与血中蛋白质结合对肿瘤非特异性照射,但因未与抗体结合,故在体内不能有效地定位于瘤细胞,以至对瘤细胞的杀伤作用有限。小剂量内照射对机体免疫系统的刺激作用,可能是131I在实验动物中肿瘤抑制作用的机制之一。本研究结果示冷抗体对荷瘤小鼠无治疗作用,与文献[1]报道单纯抗体有抑瘤作用不符,可能与本实验所用抗体量偏小有关,但也表明实验时小剂量RIT的抑瘤效应不是单纯的131I或抗体作用,而是通过抗体与肿瘤细胞特异性亲和力把核素载带到肿瘤组织中,由于放射性核素在组织内射程较短,故主要聚集在肿瘤组织,而非瘤组织的吸收剂量很小,有利于保护正常组织。
射线主要是通过对细胞的敏感部位即“靶"的作用来损伤肿瘤细胞[2],同时细胞也经过自身的修复功能恢复其正常生理功能。两者的相互作用决定细胞的转归。分次RIT由于前次治疗杀伤部分肿瘤细胞,缓解了肿瘤组织内的高压,改善了血运, 使肿瘤内原来的乏氧细胞再充氧,恢复对射线的敏感性,有利于肿瘤细胞的杀伤[3]。射线对肿瘤细胞的作用还表现在改变细胞周期:实验中给予小剂量的放射性核素标记单克隆抗体后,小鼠胸腺淋巴细胞、肿瘤细胞明显出现G1期停滞,S期细胞减少。Palayoor等[4]报道G1期停滞和S期细胞减少,G2M阻滞时相缩短能使肿瘤细胞放射敏感性增加,加速肿瘤细胞死亡。
, 百拇医药
本研究结果显示,荷瘤小鼠给予低剂量RIT后,小鼠外周血T淋巴细胞亚群中CD3+细胞有所增加,L3T4+(CD4+,Th)细胞增加,而Lyt-2+(CD8+,TS)细胞相对减少,明显抑制肿瘤转移。可以认为低剂量辐射使抑制性T细胞(TS)遭到破坏而下降,辅助性T细胞(Th)增高并与TS的比值相应升高,导致免疫上调, 从而提高机体的免疫功能和抗肿瘤能力。 参 考 文 献
1,Jessy D, Siegal GP, Aberez RD, et al. Targeted tumor killing via an intracellular antibody against erb-b. J Clin Invest, 1995, 96:2980-2989.
, 百拇医药
2,Radford IR, George SH, Matthews PJ, et al. Critical DNA target size model of ionizing radiation-induced mammalian cell death. Int J Radiat Biol, 1998, 54:63-76.
3,Muschel RJ, Oernhard EJ, Garza L. Induction of apoptosis at different oxygen tention: evidence that oxygen radicals do not mediate apoptotic signaling. Cancer Res, 1995, 55:995-1003.
4,Palayoor ST, Macklis RM, Bump EA, et al. Modulation of radiation-induced apoptosis and G2/M block in murine T-lymphoma cell. Radiat Res, 1995, 141:235-243B.
(收稿日期:1999-08-09), 百拇医药