扩散加权平面回波成像在肝占位性病变中的应用探讨
作者:徐海波 孔祥泉 肖学宏 杨炼 杨帆 江利 梁波 刘定西 熊茵 于群 彭振军
单位:430022 武汉,同济医科大学附属协和医院放射科
关键词:肝肿瘤;磁共振成像;血管瘤;囊肿
中华放射学杂志991112
【摘要】 目的 探讨扩散加权平面回波成像在肝占位性病变中的应用,以及表面扩散系数(ADC)评估肝占位病变的价值。方法 对48例共有58个肝占位病灶患者进行了扩散加权平面回波成像。58个肝占位病灶中肝癌30个,肝血管瘤16个,肝囊肿12个。应用不同梯度因子b值的扩散图像拟合出ADC图,并获取ADC值。结果 肝癌、肝血管瘤和肝囊肿的平均ADC值分别为:(1.25±0.51)×10-3 mm2/s、(1.75±0.60)×10-3 mm2/s和(3.15±0.43)×10-3 mm2/s,三者存在着显著性差异(P<0.01)。结论 扩散加权平面回波成像对肝癌、肝血管瘤和肝囊肿的鉴别诊断具有一定的价值,但不适宜对小病灶作定性诊断。
, http://www.100md.com
Diffusion-weighted echo-planar imaging:applications in evaluation of hepatic masses
XU Haibo, KONG Xiangquan, XIAO Xuehong, et al.
Department of Radiology, Xiehe Hospital, Tongji Medical University, Wuhan 430022
【Abstract】 Objective To evaluate the application of diffusion-weighted echo-planar imaging(EPI) and apparent diffusion coefficient(ADC) in hepatic masses. Methods Forty-eight patients with 58 liver masses had diffusion-weighted EPI. Among the 58 cases, 30 were hepatomas, 16 hemangiomas,and 12 hepatic cysts. Multi-diffusion weighted images with different b values were integrated to ADC map, and the average ADC values were obtained. Results Average ADC values of hepatoma, liver hemangioma and liver cysts were (1.25±0.51)×10-3、(1.75±0.6)×10-3, and (3.15±0.43)×10-3 mm2/s, respectively. The difference between the average ADC values was significant (P<0.01). Conclusion Diffusion-weighted EPI is useful in differentiation among hepatoma, liver hemangioma and liver cysts. It is, however, difficult to detect or identify small liver lesions with diffusion-weighted EPI.
, 百拇医药
【Key words】 Liver neoplasms Magnetic resonance imaging Hemangioma Cysts
扩散加权磁共振成像(diffusion-weighted MR imaging,DWMRI)是一种对分子运动敏感的成像技术,是唯一无创反映活体组织扩散的检查方法[1]。在脑部应用DWMRI,可早期预示脑中风,以及鉴别脑囊肿、富含水分的脑肿瘤与实体肿瘤[2,3]。因而,促使人们探讨此法在其他脏器的应用。然而早期的扩散成像多用于高场,成像时间长,对运动伪影非常敏感,不适于受生理运动影响大的脏器,如肝、脾、肾等。随着平面回波成像(echo-planar imaging,EPI)技术──超快速成像技术的出现,抑制或减弱了运动伪影,使扩散加权平面回波成像(DW-EPI)技术在上腹部脏器的应用成为可能[4-6]。现将DW-EPI技术在肝局灶占位性病变的应用分析如下。
, http://www.100md.com
材料与方法
1.对象:对48例共有58个肝占位病变的病人进行了DWMRI,年龄28~67岁,平均47.5岁。男40例,女8例。58个肝占位病变中,30个肝癌,16个肝血管瘤,12个肝囊肿。所有肝癌根据甲胎蛋白、临床资料、超声和(或)CT及常规MRI综合诊断,肝血管瘤和肝囊肿根据临床资料、超声和(或)CT及常规MRI综合诊断,并随访6~8个月。7例肝癌和4例肝血管瘤行 DSA检查,结果支持上述诊断;6例肝癌和2 例血管瘤经手术证实。所有病人均在1.5 T超导磁共振仪(Magnetom Vision,Siemens)上检查,采用体部阵列(body phased-array)线圈。
2.肝脏常规MR扫描:采用轴面、冠状面,T1WI快速小角度激发(fast low-angle shot,FLASH)序列,TR 174.9毫秒,TE 4.1毫秒,翻转角70°;T2WI半傅立叶转换单次激发快速自旋回波(half fourier acquisition single shot turbo spin echo,HASTE)序列,TR 4.4毫秒,TE 90毫秒,此处TR为回波链上相邻回波之间的间隔。层厚8 mm,间隔2 mm,视野(FOV)为32~38 cm,矩阵128~192×256。均屏气采集。
, 百拇医药
3.DW-EPI:采用平面回波SE类型的扩散加权成像法。TE 118~123毫秒,矩阵96~120×200,FOV 35~45 cm,回波间隔0.8毫秒,层厚5 mm,间距1 mm,采集10层。分别在SE序列180°脉冲前后施加不同扩散梯度因子(gradient factor),用b值表示,分别为0 s/mm2、30 s/mm2、1000 s/mm2。
4.图像分析:在不同b值的扩散加权图像上,测量感兴趣区(ROI)的信号强度值,然后计算出表面扩散系数(apparent diffusion coefficient,ADC),并拟合出ADC图。计算ADC公式如下:
ADC=-(1/b)In(S/S0)
式中S、S0为不同b值扩散图像上的感兴趣区的信号强度,In 为自然对数,b为两种不同扩散梯度因子的差值。肝囊肿、肝血管瘤和肝癌的三者ADC平均值的差异采用单因子方差分析。
, 百拇医药
结果
应用Excel软件中单因子方差分析统计法获得肝癌、肝血管瘤和肝囊肿三者的平均ADC值,分别为(1.25±0.51)×10-3 mm2/s、(1.75±0.6)×10-3 mm2/s和 (3.15±0.43)×10-3 mm2/s,三者组间方差之差F=215.5, P<0.01。在b=0 s/mm2或30 s/mm2的扩散加权图像上,肝囊肿、血管瘤和肝癌呈高信号强度;随b值增大(b≥1000 s/mm2),上述病灶在扩散加权图像上信号强度不同程度减低,肝囊肿明显减低直至消失,肝血管瘤亦有降低但不如囊肿明显,实体肝癌信号降低程度较小且高于脾信号,但富含血管和坏死囊变的肝癌信号降低明显(图1~9)。此外,我们发现EPI产生视野1/2或N/2 (N为阅读的原始数据行数) 重叠伪影,即在施加b值梯度场方向上产生的前后或左右影像重叠。这可能与EPI摆动阅读方式或局部涡流电流有关,但这种伪影不影响ADC值计算或ADC图拟合。在48例病人中,有2例出现严重影像变形,未用于ADC值计算。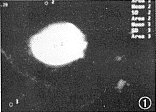
, http://www.100md.com
图1 肝右叶巨大囊肿。图1示b=0 s/mm2,T2WI(TR 3000毫秒,TE 118毫秒)示肝右叶边界清晰的高信号囊肿。当b=1000 s/mm2时,囊肿信号消失
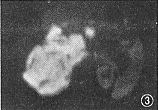
图2,3 肝右叶巨块型肝癌。图2示b=0 s/mm2,T2WI(TR 3000毫秒,TE 118毫秒)显示肝右叶稍高信号肿块。图3示b=1000 s/mm2,肝癌信号强度减低不明显且高于脾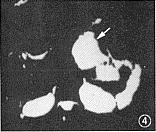


, 百拇医药
图4~6 肝左叶血管瘤。图4示b=30 s/mm2,T2WI(TR 3000毫秒,TE 118毫秒)显示肝左叶稍高信号血管瘤(↑)。图5示b=1000 s/mm2,肝血管瘤信号明显降低(↑)。图6为表面扩散系数(ADC)图像,示肝左叶血管瘤(↑),ADC值为1.95×10-3 mm2/s
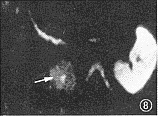
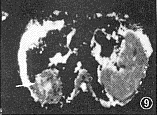
图7~9 肝右叶巨块型肝癌。图7示b=30 s/mm2,T2WI(TR 3000毫秒,TE 118毫秒)显示肝右叶稍高信号肿块(↑)和半月形高信号腹水。图8示b=1000 s/mm2,肝癌信号减低和腹水信号消失。图9为ADC图,示肝右叶肝癌(↑)为低ADC值(1.04×10-3 mm2/s)
, http://www.100md.com
讨论
一、扩散成像原理及ADC的应用
磁共振扩散加权成像利用MR对运动检测敏感的基本特性,对活体水分子扩散(diffusion)进行了测定,是将宏观流动相位位移成像原理应用于显微水平扩散成像。在梯度磁场下,扩散运动的水分子中的质子横向磁化发生相位位移,可产生MR信号,构成扩散图像的对比。但这种相位位移在常规MR成像序列中呈广泛扩散,相互干扰致MR信号衰减,扩散效应非常小,可忽略不计。其中信号衰减取决于分子运动的幅度及磁场梯度强度,前者与ADC相关[7]。
在成像序列中若加入强磁场梯度即扩散梯度,即可获取扩散加权成像。扩散梯度的程度由梯度脉冲的强度和持续时间即所谓的梯度因子(gradient factor)决定,用b值表示。由于扩散成像受到微循环的干扰,如毛细血管灌注,产生类似于真正的扩散效应,这种扩散图像实际上包含一些体素不相干运动(intravoxel incoherent motion,IVIM)的图像,以及细胞壁、温度、非单一扩散媒介等因素影响获取真正的扩散系数。因而,在实际工作中用ADC代替扩散系数(DC)评估扩散成像的结果[8,9]。
, 百拇医药
活体组织的ADC值受细胞内外水的黏滞度、比例、膜通透性、方向和温度的影响。在扩散加权图像上扩散快的组织信号衰减大,呈暗色;而在ADC图像上相反,呈亮色,表示ADC值大;扩散慢的组织信号衰减小,呈亮色,ADC值小。不难理解,肝囊肿随着b值增大,扩散加权图像上信号变暗,甚至消失,其ADC值较肝血管瘤和肝癌大,原因是肝囊肿内水分含量多和相对游离。而肝癌的ADC值小于肝血管瘤,可能是肝癌内血液黏滞度较高,以及其内间隔、出血坏死等因素限制分子扩散运动所致。三者的ADC值显著性差异在临床鉴别诊断中可能有一定的参考价值。
尽管本研究和国外研究结果反映了实体肝癌、血管瘤、囊肿的ADC值有显著性差异,但ADC的统计值目前并非完全一样[4-6],这可能与采样数、插入b值多少和数值大小以及灌注影响程度有关。在理论上,使用2种不同b值即可获取ADC值或拟合出ADC图像,但b值愈多,ADC值愈精确、愈接近真实的ADC值。在本研究中,一次扩散加权序列只能使用2种不同b值。现在,我们的一次扩散加权图像序列已可使用3种不同b值,并自动拟合出ADC图,将对上述问题作进一步研究。
, 百拇医药
二、扩散加权平面回波成像局限性
扩散加权平面回波成像对肝局灶占位性病变的评估存在着以下一些局限性或缺陷:(1)小病灶漏诊或ADC值不准。为了计算出ADC值或拟合出ADC图像,必须使用至少2种不同b值采样成像,2次成像时若位置匹配不良或EPI产生严重的化学位移,将影响小病灶的ADC值准确测定或造成小病灶漏诊。(2)严重图像扭曲变形。EPI对磁场不均匀极为敏感,在肝组织与含气的胃、肠界面易产生严重图形扭曲变形,尤以肝左叶为重,导致无法获取理想的ADC图像。(3)富含血管、囊变的转移癌与肝血管瘤在ADC值上有部分重叠,故无法鉴别[5]。
通过本研究的初步结果,我们认为DWMRI可用于鉴别诊断肝囊肿、肝血管瘤和实体肝癌,但不适宜于小病灶的诊断,有关灌注对ADC值的影响和部分肝癌与肝血管瘤的ADC值部分重叠的原因有待进一步研究。
参考文献
, 百拇医药
1 Turner R, Le Bihan D, Maier J, et al. Echo-planar imaging of intravoxel incoherent motion. Radiology, 1990,177: 407-414.
2 Tsuruda JS, Chew WM, Moseley ME, et al. Diffusion-weighted MR imaging of the brain: value of differentiating between extraaxial cysts and epidermoid tumors. AJR,1990,155: 1059-1068.
3 Tien RD, Felsberg GJ, Friedman H, et al. MR imaging of high-grade cerebral gliomas: value of diffusion-weighted echo-planar pulse sequence. AJR,1994,162: 671-677.
, http://www.100md.com
4 Muller MF, Prasad P, Siewert B, et al. Abdominal diffusion mapping with use of a whole-body echo-planar system. Radiology,1994,190: 475-478.
5 Namimoto T, Yamashita Y, Sumi S, et al. Focal liver masses: characterization with diffusion-weighted echo-planar MR imaging. Radiology,1997,204: 739-744.
6 Ichikawa T, Haradome H, Hachiya J, et al. Diffusion-weighted MR imaging with a single-shot echo-planar sequence detection and characterization of focal hepatic lesions. AJR,1998,170: 397-402.
, 百拇医药
7 Chenevert TL, Brunberg JA, Pipe JG. Anisotropic diffusion in human white matter: demonstration with MR techniques in vivo. Radiology,1990,177: 401-405.
8 Le Bihan D, Breton E, Lallemand D, et al. Separation of diffusion and perfusion in intravoxel incoherrent motion MR imaging. Radiology,1988,168: 497-505.
9 Le Bihan D, Broton E, Lallemand D, et al. MR imaging of intravoxel incoherent motions: application to diffusion and perfusion in neurologic disorders. Radiology,1986,161: 401-407.
收稿:1999-07-15, 百拇医药
单位:430022 武汉,同济医科大学附属协和医院放射科
关键词:肝肿瘤;磁共振成像;血管瘤;囊肿
中华放射学杂志991112
【摘要】 目的 探讨扩散加权平面回波成像在肝占位性病变中的应用,以及表面扩散系数(ADC)评估肝占位病变的价值。方法 对48例共有58个肝占位病灶患者进行了扩散加权平面回波成像。58个肝占位病灶中肝癌30个,肝血管瘤16个,肝囊肿12个。应用不同梯度因子b值的扩散图像拟合出ADC图,并获取ADC值。结果 肝癌、肝血管瘤和肝囊肿的平均ADC值分别为:(1.25±0.51)×10-3 mm2/s、(1.75±0.60)×10-3 mm2/s和(3.15±0.43)×10-3 mm2/s,三者存在着显著性差异(P<0.01)。结论 扩散加权平面回波成像对肝癌、肝血管瘤和肝囊肿的鉴别诊断具有一定的价值,但不适宜对小病灶作定性诊断。
, http://www.100md.com
Diffusion-weighted echo-planar imaging:applications in evaluation of hepatic masses
XU Haibo, KONG Xiangquan, XIAO Xuehong, et al.
Department of Radiology, Xiehe Hospital, Tongji Medical University, Wuhan 430022
【Abstract】 Objective To evaluate the application of diffusion-weighted echo-planar imaging(EPI) and apparent diffusion coefficient(ADC) in hepatic masses. Methods Forty-eight patients with 58 liver masses had diffusion-weighted EPI. Among the 58 cases, 30 were hepatomas, 16 hemangiomas,and 12 hepatic cysts. Multi-diffusion weighted images with different b values were integrated to ADC map, and the average ADC values were obtained. Results Average ADC values of hepatoma, liver hemangioma and liver cysts were (1.25±0.51)×10-3、(1.75±0.6)×10-3, and (3.15±0.43)×10-3 mm2/s, respectively. The difference between the average ADC values was significant (P<0.01). Conclusion Diffusion-weighted EPI is useful in differentiation among hepatoma, liver hemangioma and liver cysts. It is, however, difficult to detect or identify small liver lesions with diffusion-weighted EPI.
, 百拇医药
【Key words】 Liver neoplasms Magnetic resonance imaging Hemangioma Cysts
扩散加权磁共振成像(diffusion-weighted MR imaging,DWMRI)是一种对分子运动敏感的成像技术,是唯一无创反映活体组织扩散的检查方法[1]。在脑部应用DWMRI,可早期预示脑中风,以及鉴别脑囊肿、富含水分的脑肿瘤与实体肿瘤[2,3]。因而,促使人们探讨此法在其他脏器的应用。然而早期的扩散成像多用于高场,成像时间长,对运动伪影非常敏感,不适于受生理运动影响大的脏器,如肝、脾、肾等。随着平面回波成像(echo-planar imaging,EPI)技术──超快速成像技术的出现,抑制或减弱了运动伪影,使扩散加权平面回波成像(DW-EPI)技术在上腹部脏器的应用成为可能[4-6]。现将DW-EPI技术在肝局灶占位性病变的应用分析如下。
, http://www.100md.com
材料与方法
1.对象:对48例共有58个肝占位病变的病人进行了DWMRI,年龄28~67岁,平均47.5岁。男40例,女8例。58个肝占位病变中,30个肝癌,16个肝血管瘤,12个肝囊肿。所有肝癌根据甲胎蛋白、临床资料、超声和(或)CT及常规MRI综合诊断,肝血管瘤和肝囊肿根据临床资料、超声和(或)CT及常规MRI综合诊断,并随访6~8个月。7例肝癌和4例肝血管瘤行 DSA检查,结果支持上述诊断;6例肝癌和2 例血管瘤经手术证实。所有病人均在1.5 T超导磁共振仪(Magnetom Vision,Siemens)上检查,采用体部阵列(body phased-array)线圈。
2.肝脏常规MR扫描:采用轴面、冠状面,T1WI快速小角度激发(fast low-angle shot,FLASH)序列,TR 174.9毫秒,TE 4.1毫秒,翻转角70°;T2WI半傅立叶转换单次激发快速自旋回波(half fourier acquisition single shot turbo spin echo,HASTE)序列,TR 4.4毫秒,TE 90毫秒,此处TR为回波链上相邻回波之间的间隔。层厚8 mm,间隔2 mm,视野(FOV)为32~38 cm,矩阵128~192×256。均屏气采集。
, 百拇医药
3.DW-EPI:采用平面回波SE类型的扩散加权成像法。TE 118~123毫秒,矩阵96~120×200,FOV 35~45 cm,回波间隔0.8毫秒,层厚5 mm,间距1 mm,采集10层。分别在SE序列180°脉冲前后施加不同扩散梯度因子(gradient factor),用b值表示,分别为0 s/mm2、30 s/mm2、1000 s/mm2。
4.图像分析:在不同b值的扩散加权图像上,测量感兴趣区(ROI)的信号强度值,然后计算出表面扩散系数(apparent diffusion coefficient,ADC),并拟合出ADC图。计算ADC公式如下:
ADC=-(1/b)In(S/S0)
式中S、S0为不同b值扩散图像上的感兴趣区的信号强度,In 为自然对数,b为两种不同扩散梯度因子的差值。肝囊肿、肝血管瘤和肝癌的三者ADC平均值的差异采用单因子方差分析。
, 百拇医药
结果
应用Excel软件中单因子方差分析统计法获得肝癌、肝血管瘤和肝囊肿三者的平均ADC值,分别为(1.25±0.51)×10-3 mm2/s、(1.75±0.6)×10-3 mm2/s和 (3.15±0.43)×10-3 mm2/s,三者组间方差之差F=215.5, P<0.01。在b=0 s/mm2或30 s/mm2的扩散加权图像上,肝囊肿、血管瘤和肝癌呈高信号强度;随b值增大(b≥1000 s/mm2),上述病灶在扩散加权图像上信号强度不同程度减低,肝囊肿明显减低直至消失,肝血管瘤亦有降低但不如囊肿明显,实体肝癌信号降低程度较小且高于脾信号,但富含血管和坏死囊变的肝癌信号降低明显(图1~9)。此外,我们发现EPI产生视野1/2或N/2 (N为阅读的原始数据行数) 重叠伪影,即在施加b值梯度场方向上产生的前后或左右影像重叠。这可能与EPI摆动阅读方式或局部涡流电流有关,但这种伪影不影响ADC值计算或ADC图拟合。在48例病人中,有2例出现严重影像变形,未用于ADC值计算。

, http://www.100md.com
图1 肝右叶巨大囊肿。图1示b=0 s/mm2,T2WI(TR 3000毫秒,TE 118毫秒)示肝右叶边界清晰的高信号囊肿。当b=1000 s/mm2时,囊肿信号消失


图2,3 肝右叶巨块型肝癌。图2示b=0 s/mm2,T2WI(TR 3000毫秒,TE 118毫秒)显示肝右叶稍高信号肿块。图3示b=1000 s/mm2,肝癌信号强度减低不明显且高于脾



, 百拇医药
图4~6 肝左叶血管瘤。图4示b=30 s/mm2,T2WI(TR 3000毫秒,TE 118毫秒)显示肝左叶稍高信号血管瘤(↑)。图5示b=1000 s/mm2,肝血管瘤信号明显降低(↑)。图6为表面扩散系数(ADC)图像,示肝左叶血管瘤(↑),ADC值为1.95×10-3 mm2/s



图7~9 肝右叶巨块型肝癌。图7示b=30 s/mm2,T2WI(TR 3000毫秒,TE 118毫秒)显示肝右叶稍高信号肿块(↑)和半月形高信号腹水。图8示b=1000 s/mm2,肝癌信号减低和腹水信号消失。图9为ADC图,示肝右叶肝癌(↑)为低ADC值(1.04×10-3 mm2/s)
, http://www.100md.com
讨论
一、扩散成像原理及ADC的应用
磁共振扩散加权成像利用MR对运动检测敏感的基本特性,对活体水分子扩散(diffusion)进行了测定,是将宏观流动相位位移成像原理应用于显微水平扩散成像。在梯度磁场下,扩散运动的水分子中的质子横向磁化发生相位位移,可产生MR信号,构成扩散图像的对比。但这种相位位移在常规MR成像序列中呈广泛扩散,相互干扰致MR信号衰减,扩散效应非常小,可忽略不计。其中信号衰减取决于分子运动的幅度及磁场梯度强度,前者与ADC相关[7]。
在成像序列中若加入强磁场梯度即扩散梯度,即可获取扩散加权成像。扩散梯度的程度由梯度脉冲的强度和持续时间即所谓的梯度因子(gradient factor)决定,用b值表示。由于扩散成像受到微循环的干扰,如毛细血管灌注,产生类似于真正的扩散效应,这种扩散图像实际上包含一些体素不相干运动(intravoxel incoherent motion,IVIM)的图像,以及细胞壁、温度、非单一扩散媒介等因素影响获取真正的扩散系数。因而,在实际工作中用ADC代替扩散系数(DC)评估扩散成像的结果[8,9]。
, 百拇医药
活体组织的ADC值受细胞内外水的黏滞度、比例、膜通透性、方向和温度的影响。在扩散加权图像上扩散快的组织信号衰减大,呈暗色;而在ADC图像上相反,呈亮色,表示ADC值大;扩散慢的组织信号衰减小,呈亮色,ADC值小。不难理解,肝囊肿随着b值增大,扩散加权图像上信号变暗,甚至消失,其ADC值较肝血管瘤和肝癌大,原因是肝囊肿内水分含量多和相对游离。而肝癌的ADC值小于肝血管瘤,可能是肝癌内血液黏滞度较高,以及其内间隔、出血坏死等因素限制分子扩散运动所致。三者的ADC值显著性差异在临床鉴别诊断中可能有一定的参考价值。
尽管本研究和国外研究结果反映了实体肝癌、血管瘤、囊肿的ADC值有显著性差异,但ADC的统计值目前并非完全一样[4-6],这可能与采样数、插入b值多少和数值大小以及灌注影响程度有关。在理论上,使用2种不同b值即可获取ADC值或拟合出ADC图像,但b值愈多,ADC值愈精确、愈接近真实的ADC值。在本研究中,一次扩散加权序列只能使用2种不同b值。现在,我们的一次扩散加权图像序列已可使用3种不同b值,并自动拟合出ADC图,将对上述问题作进一步研究。
, 百拇医药
二、扩散加权平面回波成像局限性
扩散加权平面回波成像对肝局灶占位性病变的评估存在着以下一些局限性或缺陷:(1)小病灶漏诊或ADC值不准。为了计算出ADC值或拟合出ADC图像,必须使用至少2种不同b值采样成像,2次成像时若位置匹配不良或EPI产生严重的化学位移,将影响小病灶的ADC值准确测定或造成小病灶漏诊。(2)严重图像扭曲变形。EPI对磁场不均匀极为敏感,在肝组织与含气的胃、肠界面易产生严重图形扭曲变形,尤以肝左叶为重,导致无法获取理想的ADC图像。(3)富含血管、囊变的转移癌与肝血管瘤在ADC值上有部分重叠,故无法鉴别[5]。
通过本研究的初步结果,我们认为DWMRI可用于鉴别诊断肝囊肿、肝血管瘤和实体肝癌,但不适宜于小病灶的诊断,有关灌注对ADC值的影响和部分肝癌与肝血管瘤的ADC值部分重叠的原因有待进一步研究。
参考文献
, 百拇医药
1 Turner R, Le Bihan D, Maier J, et al. Echo-planar imaging of intravoxel incoherent motion. Radiology, 1990,177: 407-414.
2 Tsuruda JS, Chew WM, Moseley ME, et al. Diffusion-weighted MR imaging of the brain: value of differentiating between extraaxial cysts and epidermoid tumors. AJR,1990,155: 1059-1068.
3 Tien RD, Felsberg GJ, Friedman H, et al. MR imaging of high-grade cerebral gliomas: value of diffusion-weighted echo-planar pulse sequence. AJR,1994,162: 671-677.
, http://www.100md.com
4 Muller MF, Prasad P, Siewert B, et al. Abdominal diffusion mapping with use of a whole-body echo-planar system. Radiology,1994,190: 475-478.
5 Namimoto T, Yamashita Y, Sumi S, et al. Focal liver masses: characterization with diffusion-weighted echo-planar MR imaging. Radiology,1997,204: 739-744.
6 Ichikawa T, Haradome H, Hachiya J, et al. Diffusion-weighted MR imaging with a single-shot echo-planar sequence detection and characterization of focal hepatic lesions. AJR,1998,170: 397-402.
, 百拇医药
7 Chenevert TL, Brunberg JA, Pipe JG. Anisotropic diffusion in human white matter: demonstration with MR techniques in vivo. Radiology,1990,177: 401-405.
8 Le Bihan D, Breton E, Lallemand D, et al. Separation of diffusion and perfusion in intravoxel incoherrent motion MR imaging. Radiology,1988,168: 497-505.
9 Le Bihan D, Broton E, Lallemand D, et al. MR imaging of intravoxel incoherent motions: application to diffusion and perfusion in neurologic disorders. Radiology,1986,161: 401-407.
收稿:1999-07-15, 百拇医药