1H磁共振波谱在新生儿缺氧缺血性脑病中的应用
作者:范国光 陈丽英 吴振华 叶滨滨 景奉东 毛健 潘诗农
单位:范国光、陈丽英、吴振华、叶滨滨、潘诗农 沈阳,中国医科大学第二临床学院放射科 110003,毛健 儿科;景奉东 沈阳医学院附属中心医院放射科
关键词:核磁共振;脑缺氧;脑疾病;婴儿,新生
中华放射学杂志991214摘要:目的 结合MRI探讨1H磁共振波谱(1H MRS)在新生儿缺氧缺血脑病(HIE)中的应用价值。方法 选择38例经临床确诊为HIE的足月新生儿进行MRI及1H MRS检查。年龄5~17天,平均8.2天。对其中的26例患儿于6个月以后分别进行随访和(或)复查MRI。同时选择8例无窒息史的健康足月新生儿做对照研究。MRI检查采用Elscint 2.0超导型磁共振扫描系统,应用SE序列进行常规扫描,1H MRS采用定点分辨波谱序列(TR 2 000毫秒,TE 135 毫秒)。所测定的代谢产物包括N-乙酰基天门冬氨酸(NAA)、胆碱复合物(Cho)、肌酸复合物(Cr)、肌醇(MI)、乳酸(LAC)、谷氨酸及谷氨酰胺(Glu-Gln)等。结果 (1)正常足月新生儿的1H MRS表现:8例正常新生儿Cho、NAA 、CR波峰高耸;MI波峰略低;Glu-Gln及LAC波峰低平或测不出。波幅从高至低的顺序为Cho、NAA、CR、MI、Glu-Gln及LAC。(2)HIE患儿的1H MRS表现:36例NAA波峰高耸,2例降低;26例LAC波峰增高呈典型的双峰状;9例Glu-Gln波峰呈多个增大的锯齿状波;11例CR波峰降低;7例MI波峰增高。其中LAC与CR之比<0.5者12例,MRI呈轻度表现;LAC与CR之比为0.5~1.5者15例,MRI呈中重度表现;LAC与CR之比>1.5者11例,9例呈重度表现,2例呈中度表现。6个月以后随访和(或)复查MRI,26例中有12例出现脑后遗改变。其中,LAC与CR之比>1.5的9例中有8例(占88.9%)。结论 1H MRS在本病的诊断及预后判定方面有重要的价值。
, 百拇医药
1H magnetic resonance spectroscopy in the diagnosis of hypoxia-ischemic encephalopathy in the neonates
FAN Guoguang, CHEN Liying, WU Zhenhua, et al.
Department of Radiology, the Second Affiliated Hospital, China Medical University, Shenyang 110003
Abstract Objective To evaluate 1H magnetic resonance spectroscopy (1H MRS) in the diagnosis of hypoxia-ischemic encephalopathy (HIE) of full-term neonates combined with magnetic resonance imaging (MRI). Methods Thirty-eight cases of full-term neonates diagnosed as HIE clinically had MRI and 1H MRS examination done on 2.0 T Elscint scanner. The age ranged from 5 to 17 days, with median age of 8.2 days. 26 cases were followed up and/or reexamined with MRI at 6 months of age or later. In the meantime, eight healthy neonates, with no evidence of birth asphyxia, also underwent 1H MRS for comparison.SE sequences were used for routine examination; point resolved spectroscopy sequence (TR 2 000 ms,TE 135 ms) was used for 1H MRS.The metabolites in the spectra included: N-acetylaspartate (NAA)、choline compounds (Cho)、creatine compounds (CR)、myo-inositol (MI)、lactate (LAC)、glutamate and glutamine (Glu-Gln) and so on. Results (1) 1H MRS manifestations of normal full-term neonates (8 cases): The peaks of Cho、NAA 、CR were elevated; and those of MI were slightly decreased; while peaks of Glu-Gln and LAC were flattened or undetectable. The amplitudes in high-to-low order were as follows: Cho、NAA、CR、MI、Glu-Gln and LAC. (2) 1H MRS manifestations of full-term neonates suffering from HIE (38 cases): The peaks of NAA were elevated in 36 cases, and decreased in 2 cases. The peaks of LAC, which were elevated, presented typical double-peak appearance in 26 cases; the peaks of Glu-Gln, which were also elevated, exhibited zigzag appearance in 9 cases; the peak of CR was decreased in 11 cases, while that of MI was increased in 7 cases. Mild type of lesions was present on MRI in 12 cases in which LAC/CR ratio was lower than 0.5; mild and moderate types of lesions were present in 15 cases whose LAC/CR ratio was between 0.5 and 1.5; while 9 cases of severe lesions and 2 cases of moderate lesions were present on MRI in 11 cases with LAC/CR ratio greater than 1.5. 26 of 38 cases were followed up and/or reexamined with MRI after six months, in which, sequelae were present in 12 cases. Of 9 cases with LAC/CR ratio greater than 1.5 8 cases (88.9%) had sequelae. Conclusion 1H MRS plays an important role to diagnose and predict the outcome of HIE.
, 百拇医药
Key words:Nuclear magnetic resonance Cerebral anoxia Brain diseases Infant,newborn
缺氧缺血脑病(HIE)是围产期新生儿期的常见疾病,也是引起日后脑瘫、智力低下及癫痫等疾病的重要原因。对其病因、疾病的严重程度及其预后进行合理的评估将对本病的临床治疗有一定的指导意义。MRI的应用使得本病的诊断更为客观和直接;磁共振波谱(MRS)是随着MR发展起来的一门新技术,是一种研究活体组织代谢与生化指标测定的非侵袭技术[1]。MRI与MRS的综合应用,会对本病的疾病分度及预后作出较为客观的评价。现将我院新近对38例HIE患儿的研究结果报告如下。
材料与方法
1.检查对象:对38例临床确诊为HIE的足月新生儿进行MRI及1H MRS检查。其中男16例,女22例。年龄5~17天,平均8.2天。有产钳助产及胎头吸引史者11例;因滞产而行剖宫术者6例;脐带绕颈者8例;有窒息史者33例,伴青紫者10例;生后抽搐者8例。38例HIE患儿中,有11例5分钟Apgar评分≤6分。对其中的26例患儿分别于6个月以后进行随访和(或)复查MRI,其中15例MRI复查的HIE患儿中,有9例分别合并脑外积液、髓鞘发育延迟、脑室旁白质软化、胼胝体发育不良等;11例随访的HIE患儿中,有3例运动及体能发育落后。
, http://www.100md.com
选择无窒息史的健康足月新生儿8例进行对照研究。其中男3例,女5例,年龄6~15天,平均8.4天。
2. 检查方法: MRI检查采用Elscint 2.0 T超导型磁共振扫描系统,应用SE序列头线圈T1WI (TR 620毫秒,TE 25毫秒), T2WI(TR 3 600毫秒,TE 96毫秒),常规行矢状面及轴面扫描,层厚5~10 mm。1H MRS采用SE T1WI(TR 620毫秒,TE 25毫秒),轴面确定感兴趣区(ROI,体积元大小为2 cm×2 cm×2 cm)。采用定点分辨波谱序列(point resolved spectroscopy,TR 2 000毫秒,TE 135毫秒)定位于基底节区及放射冠区。所测定的代谢产物包括N-乙酰基天门冬氨酸(NAA)、肌酸复合物(Cr)、胆碱复合物(Cho)、肌醇(MI)、乳酸(LAC)、谷氨酸及谷氨酰胺(Glu-Gln)等。波谱的后期处理包括:相位校正、基线校正、ppm(10-6)转换等。各代谢物水平的测定以波谱覆盖的面积为准。
, 百拇医药
3.统计学分析:对测量结果进行中位数的计算及秩和检验。
结果
一、正常足月新生儿的1H MRS表现
8例正常新生儿Cho、NAA、Cr的波峰高耸;MI的波峰略低;Glu-Gln及LAC波峰低平或测不出。波幅从高至低的顺序为Cho、NAA、Cr、MI、Glu-Gln及LAC(图1)。其中,NAA位于2.0 ppm;Cr位于3.0 ppm;Cho位于3.25 ppm;MI位于3.5 ppm;Glu-Gln位于2.3~2.5 ppm范围内(呈多个锯齿状波形);LAC位于1.3 ppm附近。以Cr为参照峰,分别计算出代谢物波峰面积与Cr波面积的比值。其中,NAA与Cr的比值为1.88±0.62,Cho与Cr的比值为1.21±0.35,MI与Cr的比值为0.62±0.13,LAC与Cr的比值为0.23±0.29,Glu-Gln与Cr的比值为0.55±0.31。
, 百拇医药
图1 正常新生儿的1H磁共振波谱。N-乙酰基天门冬氨酸(NAA)、肌酸复合物(Cr)、胆碱复合物(Cho)波峰高耸,肌醇(MI)波略低,谷氨酸-谷氨酰胺(Glu-Gln)及乳酸波低平
二、HIE患儿的1H MRS表现
1.本组36例NAA波峰高耸,2例NAA波峰降低,提示有神经元缺失;7例MI波峰增高(图2);9例Glu-Gln波峰增高,表现为多个增大的锯齿状波(图3);26例LAC波峰增高呈典型的双峰状,提示脑内乳酸的积聚;11例Cr波峰降低(图4);Cho与正常新生儿无显著性差异(表1)。
图2 缺氧缺血脑病患儿的1H磁共振波谱。N-乙酰基天门冬氨酸、肌酸复合物的波峰降低,肌醇波、乳酸波增高
, http://www.100md.com
图3 缺氧缺血脑病(HIE)患儿的1H磁共振波谱。位于2.3~2.5 ppm的谷氨酸-谷氨酰胺(Glu-Gln)波峰呈多个增大的锯齿状波,乳酸(LAC)波明显增高,肌酸复合物(Cr)的波峰略低
图4 HIE患儿的1H MRS。位于1.3附近的LAC波明显增高,LAC/Cr>1.5
表1 正常足月新生儿与HIE患儿脑代谢化合物相对浓度比较( ±s) 分组
±s) 分组
例数
NAA/Cr
Cho/Cr
, http://www.100md.com
MI/Cr
Glu-Gln/Cr
LAC/Cr
正常组
8
1.88±0.62
1.21±0.35
0.62±0.13
0.55±0.31
0.23±0.29
HIE组
38
, http://www.100md.com
4.22±3.56
1.96±1.92
1.37±0.84
1.35±0.95
3.35±2.86
t值
5.401
2.521
3.740
3.986
4.105
P值
, 百拇医药
<0.01
<0.05
<0.01
<0.01
<0.01
注:HIE为缺氧缺血脑病;NAA/Cr为N-乙酰基天门冬氨酸与肌酸复合物的比值;Cho/Cr为胆碱复合物与肌酸复合物的比值;MI/Cr为肌醇与肌酸复合物的比值;Glu-Gln/Cr为谷氨酸及谷氨酰胺与肌酸复合物的比值;LAC/Cr为乳酸与肌酸复合物的比值
2.根据LAC与Cr比值的不同,将HIE患儿分为3组(表2)。其中LAC与Cr之比<0.5者12例,10例MRI T1WI上仅见皮层及皮层下沿脑回迂曲的条状高信号,代表毛细血管的不完全阻塞;8例同时合并幕上、幕下蛛网膜下腔少量出血;2例基底节区点状高信号及限局性脑水肿;1H MRS可见1例Cr波峰降低。LAC与Cr之比在0.5~1.5之间者15例,其中12例MRI T1WI上除上述表现外,额叶深部白质对称性点状高信号和(或)沿侧脑室白质区条带状高信号伴限局性脑水肿(图5),这是由于大脑深静脉瘀血扩张或出血性梗死所致[2];2例同时合并脑室内出血;1例仅见蛛网膜下腔少量出血;1H MRS显示3例Cr波峰降低,3例MI波峰升高,4例Glu-Gln波峰升高。LAC与Cr之比>1.5者11例,其中9例MRI T1WI除上述表现外,还合并有基底节区及丘脑高信号伴内囊前后肢低信号(图6),提示出血性梗死、神经细胞坏死以及髓鞘化发育障碍等多种疾病并存[2,3];4例合并脑室内出血及患侧脑室扩大;6例合并弥漫性脑水肿;2例仅有基底节区斑点状高信号灶及限局性脑水肿;1H MRS显示2例NAA波峰略低(1例NAA与Cr之比为0.69,1例NAA与Cr之比为0.53),7例Cr波峰降低,4例MI波峰升高,5例Glu-Gln波峰升高。
, http://www.100md.com
图5 缺氧缺血脑病患儿的T1WI,可见沿侧脑室白质区条带状高信号及额枕叶限局性脑水肿
图6 缺氧缺血脑病患儿的T1WI,与图4为同一病人。可见基底节区斑片状高信号、内囊后肢低信号以及弥漫性脑水肿
表2 正常新生儿与HIE患儿脑内乳酸相对
浓度比较( ±s) 分组
±s) 分组
例数
NAA/Cr
t值
, 百拇医药
P值
正常组
8
0.23±0.29
-
-
LAC/Cr<0.5
12
0.47±0.22
2.326
<0.05
0.5
15
, 百拇医药
1.23±0.39
2.624
<0.05
LAC/Cr>1.5
11
3.93±1.91
4.947
<0.01
注:HIE为缺氧缺血性脑病;NAA/Cr为乳酸与肌酸复合物的比值,LAC/Cr为乳酸与肌酸复合物的比值
3.分别对26例HIE患儿6个月以后进行随访和(或)MRI复查,结果如下:LAC与Cr之比<0.5的9例(3例MRI复查,6例随访)中,7例结果正常,1例合并脑外积液,1例运动及体能发育落后;LAC与Cr之比为0.5~1.5的8例(5例MRI复查,3例随访)中,6例结果正常,1例合并有脑内小的软化灶,1例合并运动及体能发育落后;LAC与Cr之比>1.5的9例(7例MRI复查,2例随访)中,脑外积液者3例(图7),脑室旁白质软化者2例,髓鞘发育延迟者1例,胼胝体发育不良者1例,运动及体能发育落后者1例,正常者1例。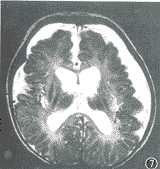
, http://www.100md.com
图7 缺氧缺血脑病患儿6个月时复查的MR图像(T2WI)。与图4、6为同一病人。可见脑外间隙增宽,合并脑外积液
讨论
新生儿HIE的发生包括一系列复杂的病理生理及生化改变。其病变发生的部位、程度与缺氧缺血持续的时间及脑内代谢物质水平的变化密切相关。基于化学位移原理的1H磁共振波谱技术能够反映出脑内主要代谢物的水平,对判断本病所引起的能量代谢障碍、细胞内酸中毒及神经元的缺失等情况能够提供有价值的信息[3]。
一、正常新生儿1H MRS中各代谢产物的水平及意义
正常新生儿1H MRS可有以下几个高峰:NAA以及不到10%的N-乙酰基天门冬氨酸盐,其波谱位于2.0 ppm处,Peden等[4]研究表明NAA主要存在于神经元内,与神经元的成熟有关。新生儿随着日龄的增长,NAA波峰也逐渐升高。Cho的波峰位于3.2 ppm处,包括磷酸甘油胆碱、磷酸胆碱和磷脂酰胆碱,反映脑内总的胆碱量。新生儿期1H MRS中,Cho波为波谱中的最高峰,NAA波峰低于Cho,1岁以后随着髓鞘化的逐渐完成而发生逆转。Cr波是总肌酸中的甲基组,包括肌酸与磷酸肌酸(Cr+PCr),是能量代谢的物质,其波谱位于3.0 ppm附近。在脑内不同代谢条件下,Cr+PCr的总量是恒定的。因此,可将Cr作为参照的波峰,得出其他代谢物质与Cr的相对比值,从而进行比较[4,5]。新生儿期NAA与Cr的比值(1.88±0.62)低于1岁以后的小儿;Cho与Cr的比值(1.21±0.35)高于其他年龄组的小儿,此种改变在3岁以前最为显著[5]。MI波位于3.5 ppm处,其功能尚不十分明确,Brian等[5]认为MI是胶质细胞存在的标志。在正常脑组织中,细胞能量代谢以有氧氧化为主,脑内乳酸水平很低,位于1.3 ppm附近的LAC波一般是不能测得的,如果出现则呈低平的波形。Glu-Gln 2个代谢物的波峰位置相近,总峰的位置在2.3~2.5 ppm处,二者作为兴奋性神经递质在脑内含量很少,但在维持线粒体的代谢中具有重要功能[5]。由于Glu-Gln波覆盖的范围较广泛,在同一共振频率内可有其他氨基酸如γ-氨基丁酸及NAA波谱的存在,精确的测量较为困难。
, 百拇医药
二、1H MRS在HIE诊断及预后评价中的应用
1.LAC升高及其LAC与Cr之比在HIE评估中的应用:HIE患儿1H MRS与正常新生儿脑组织明显不同。特征性的表现是在1.3 ppm处出现双峰状的乳酸波,乳酸波的出现是由于缺氧缺血引起继发性氧化磷酸化不足,无氧糖酵解增加所致。此波与其他代谢物的比值较正常组明显增高,尤其以LAC与Cr的比值最具特征性。因此常将LAC与Cr的比值作为衡量脑内乳酸含量相对增高的一个重要指标。脑组织在急性损伤的同时,乳酸含量就会增高。如果乳酸的积聚量不超过一定值,损伤后几周内由于局部代谢或氧的运输增加,可使脑内乳酸含量逐渐恢复到正常水平[6]。反之,如果乳酸的积聚量超过某一临界值并持续增高,就会引起细胞的酸中毒从而导致神经细胞的不可逆性损伤,最终影响患儿的预后。此临界值的测定由于实验对象、采用的技术手段及MR场强的不同而有所不同[6,7]。本研究发现LAC与Cr之比>1.5的这一组中,LAC与Cr之比为3.93±1.91,与对照组0.23±0.29比较有显著性差异。而且本组患儿MRI上病变累及的范围广、程度重(占81.8%),同时合并其他代谢物水平异常的几率高;复查的患儿中有8例出现不同程度的脑后遗症表现(占88.9%)。LAC与Cr之比在0.5~1.5之间者仅有25%的患儿出现脑后遗症改变,MRI上一般呈中等度损伤(占80.0%),合并其他代谢物水平异常的机会较前者少(占40.0%)。结合MRI的影像特征及临床资料,本组根据LAC与Cr比值的不同将HIE患儿分为轻、中、重度(即LAC与Cr之比<0.5者为轻度, LAC与Cr之比在0.5~1.5之间者为中度, LAC与Cr之比>1.5者为重度)。其中重度所致的脑损伤种类多、程度重,患儿预后多不良。
, 百拇医药
乳酸指标较敏感,常作为本病1H MRS判定的主要依据,也是本病在1H MRS上所表现的直接征象。其准确的测定取决于感兴趣区的合理选择,由于基底节和放射冠区是足月新生儿代谢活跃的区域,该区域最易受缺血缺氧的损伤[7],选择此区域作为感兴趣区,一方面可以增加生化指标检测的敏感性;另一方面也可以避免因脑边缘部脂肪波的干扰而影响乳酸波的准确测定。
2.其他代谢物水平在HIE评估中的应用:HIE的1H MRS也出现NAA波峰的改变(本组2例,占5.3%)。NAA波峰的降低提示乳酸的过多积聚引起神经元的自身溶解,也是不可逆性脑损伤的一个标志[8]。但其波峰的改变常在LAC升高数天后才出现。本组2例NAA波峰降低(NAA与Cr之比<1),复查结果显示其所出现的后遗程度最重。
HIE也可累及其他代谢物如Cr、Glu-Gln和MI等的改变。本研究中有11例Cr波降低,这与无氧糖酵解增加所导致的高能量磷酸化合物的减少有关。Glu-Gln在本病中也有参考价值。它是位于2.3~2.5 ppm之间的多个锯齿状波,呈阶梯状排列,其出现是由于缺血缺氧引起神经递质尤其是谷氨酸释放进入突触间隙所致[9]。急性缺血缺氧损伤合并能量衰竭,其波峰幅度会明显升高,在NAA波峰的左侧出现典型的“山峰状”波形(本组有5例,占13.2%)。本组同时有7例MI波峰升高,提示合并有胶质增生及髓鞘化不良[9]。
, 百拇医药
Cho在本病中无显著的波形变化,出现Cho与Cr比值的改变是由于HIE与正常脑组织间T2值的差异及Cr值的减低所致。
总之,LAC波峰的明显增高及合并其他代谢物如NAA、Cr、Glu-Gln、MI等的异常,常提示预后不良。1H MRS与MRI的综合分析,对本病的预后和临床治疗有一定的指导意义。本组复查病例数目较少,时间较短,故长期的预后如何,需进一步研究。
参考文献
1 Wang Z, Zimmerman RA,Sauter R. Proton MR spectroscopy of the brain: clinically useful information obtained in assessing CNS diseases in children.AJR, 1996,167:191-199.
, 百拇医药
2 陈丽英,王晓明,孟淑珍,等.足月新生儿缺氧缺血脑病的MRI研究. 中国医学计算机成像杂志, 1999,5:47-50.
3 Kriel RL,Krach LE,Luxenberg MG,et al. Outcome of severe anoxic/ischemic brain injury in children. Pediatr Neurol, 1994,10:207-212.
4 Peden CJ,Rutherford MA,Sargentoni J,et al. Proton spectroscopy of the neonatal brain following hypoxic-ischaemic injury. Dev Med Child Neurol,1993,35:502-510.
5 Rss B, Michaelis T. Clinical applications of magnetic resonance spectroscopy. Magn Reson Q,1994,10:191-247.
, http://www.100md.com
6 Penrice J,Lorek A,Cady EB,et al. Proton magnetic resonance spectroscopy of the brain during acute hypoxia-ischemia and delayed cerebral energy failure in the newbone piglet. Pediatr Res, 1997,41:795-802.
7 Groenendaal F, Veenhoven RH, van der Grond J, et al. Cerebral lactate and N-acetyl-aspartate/choline ratios in asphyxiated full-term neonate demonstrated in vivo using proton magnetic resonance spectroscopy. Pediatr Res ,1994,35:148-151.
, 百拇医药
8 Hanrahan JD,Sargentoni J,Azzopardi D,et al. Cerebral metabolism within 18 hours of birth asphyxia: a proton magnetic resonance spectroscopy study. Pediatr Res, 1996,39:584-590.
9 Penrice J, Cady EB, Lorek A, et al. Proton magnetic resonance spectroscopy of the brain in normal preterm and term infants, and early changes after perinatal hypoxia-ischemia. Pediar Res,1996,40:6-14.
收稿:1999-01-05
修回:1999-05-10, 百拇医药
单位:范国光、陈丽英、吴振华、叶滨滨、潘诗农 沈阳,中国医科大学第二临床学院放射科 110003,毛健 儿科;景奉东 沈阳医学院附属中心医院放射科
关键词:核磁共振;脑缺氧;脑疾病;婴儿,新生
中华放射学杂志991214摘要:目的 结合MRI探讨1H磁共振波谱(1H MRS)在新生儿缺氧缺血脑病(HIE)中的应用价值。方法 选择38例经临床确诊为HIE的足月新生儿进行MRI及1H MRS检查。年龄5~17天,平均8.2天。对其中的26例患儿于6个月以后分别进行随访和(或)复查MRI。同时选择8例无窒息史的健康足月新生儿做对照研究。MRI检查采用Elscint 2.0超导型磁共振扫描系统,应用SE序列进行常规扫描,1H MRS采用定点分辨波谱序列(TR 2 000毫秒,TE 135 毫秒)。所测定的代谢产物包括N-乙酰基天门冬氨酸(NAA)、胆碱复合物(Cho)、肌酸复合物(Cr)、肌醇(MI)、乳酸(LAC)、谷氨酸及谷氨酰胺(Glu-Gln)等。结果 (1)正常足月新生儿的1H MRS表现:8例正常新生儿Cho、NAA 、CR波峰高耸;MI波峰略低;Glu-Gln及LAC波峰低平或测不出。波幅从高至低的顺序为Cho、NAA、CR、MI、Glu-Gln及LAC。(2)HIE患儿的1H MRS表现:36例NAA波峰高耸,2例降低;26例LAC波峰增高呈典型的双峰状;9例Glu-Gln波峰呈多个增大的锯齿状波;11例CR波峰降低;7例MI波峰增高。其中LAC与CR之比<0.5者12例,MRI呈轻度表现;LAC与CR之比为0.5~1.5者15例,MRI呈中重度表现;LAC与CR之比>1.5者11例,9例呈重度表现,2例呈中度表现。6个月以后随访和(或)复查MRI,26例中有12例出现脑后遗改变。其中,LAC与CR之比>1.5的9例中有8例(占88.9%)。结论 1H MRS在本病的诊断及预后判定方面有重要的价值。
, 百拇医药
1H magnetic resonance spectroscopy in the diagnosis of hypoxia-ischemic encephalopathy in the neonates
FAN Guoguang, CHEN Liying, WU Zhenhua, et al.
Department of Radiology, the Second Affiliated Hospital, China Medical University, Shenyang 110003
Abstract Objective To evaluate 1H magnetic resonance spectroscopy (1H MRS) in the diagnosis of hypoxia-ischemic encephalopathy (HIE) of full-term neonates combined with magnetic resonance imaging (MRI). Methods Thirty-eight cases of full-term neonates diagnosed as HIE clinically had MRI and 1H MRS examination done on 2.0 T Elscint scanner. The age ranged from 5 to 17 days, with median age of 8.2 days. 26 cases were followed up and/or reexamined with MRI at 6 months of age or later. In the meantime, eight healthy neonates, with no evidence of birth asphyxia, also underwent 1H MRS for comparison.SE sequences were used for routine examination; point resolved spectroscopy sequence (TR 2 000 ms,TE 135 ms) was used for 1H MRS.The metabolites in the spectra included: N-acetylaspartate (NAA)、choline compounds (Cho)、creatine compounds (CR)、myo-inositol (MI)、lactate (LAC)、glutamate and glutamine (Glu-Gln) and so on. Results (1) 1H MRS manifestations of normal full-term neonates (8 cases): The peaks of Cho、NAA 、CR were elevated; and those of MI were slightly decreased; while peaks of Glu-Gln and LAC were flattened or undetectable. The amplitudes in high-to-low order were as follows: Cho、NAA、CR、MI、Glu-Gln and LAC. (2) 1H MRS manifestations of full-term neonates suffering from HIE (38 cases): The peaks of NAA were elevated in 36 cases, and decreased in 2 cases. The peaks of LAC, which were elevated, presented typical double-peak appearance in 26 cases; the peaks of Glu-Gln, which were also elevated, exhibited zigzag appearance in 9 cases; the peak of CR was decreased in 11 cases, while that of MI was increased in 7 cases. Mild type of lesions was present on MRI in 12 cases in which LAC/CR ratio was lower than 0.5; mild and moderate types of lesions were present in 15 cases whose LAC/CR ratio was between 0.5 and 1.5; while 9 cases of severe lesions and 2 cases of moderate lesions were present on MRI in 11 cases with LAC/CR ratio greater than 1.5. 26 of 38 cases were followed up and/or reexamined with MRI after six months, in which, sequelae were present in 12 cases. Of 9 cases with LAC/CR ratio greater than 1.5 8 cases (88.9%) had sequelae. Conclusion 1H MRS plays an important role to diagnose and predict the outcome of HIE.
, 百拇医药
Key words:Nuclear magnetic resonance Cerebral anoxia Brain diseases Infant,newborn
缺氧缺血脑病(HIE)是围产期新生儿期的常见疾病,也是引起日后脑瘫、智力低下及癫痫等疾病的重要原因。对其病因、疾病的严重程度及其预后进行合理的评估将对本病的临床治疗有一定的指导意义。MRI的应用使得本病的诊断更为客观和直接;磁共振波谱(MRS)是随着MR发展起来的一门新技术,是一种研究活体组织代谢与生化指标测定的非侵袭技术[1]。MRI与MRS的综合应用,会对本病的疾病分度及预后作出较为客观的评价。现将我院新近对38例HIE患儿的研究结果报告如下。
材料与方法
1.检查对象:对38例临床确诊为HIE的足月新生儿进行MRI及1H MRS检查。其中男16例,女22例。年龄5~17天,平均8.2天。有产钳助产及胎头吸引史者11例;因滞产而行剖宫术者6例;脐带绕颈者8例;有窒息史者33例,伴青紫者10例;生后抽搐者8例。38例HIE患儿中,有11例5分钟Apgar评分≤6分。对其中的26例患儿分别于6个月以后进行随访和(或)复查MRI,其中15例MRI复查的HIE患儿中,有9例分别合并脑外积液、髓鞘发育延迟、脑室旁白质软化、胼胝体发育不良等;11例随访的HIE患儿中,有3例运动及体能发育落后。
, http://www.100md.com
选择无窒息史的健康足月新生儿8例进行对照研究。其中男3例,女5例,年龄6~15天,平均8.4天。
2. 检查方法: MRI检查采用Elscint 2.0 T超导型磁共振扫描系统,应用SE序列头线圈T1WI (TR 620毫秒,TE 25毫秒), T2WI(TR 3 600毫秒,TE 96毫秒),常规行矢状面及轴面扫描,层厚5~10 mm。1H MRS采用SE T1WI(TR 620毫秒,TE 25毫秒),轴面确定感兴趣区(ROI,体积元大小为2 cm×2 cm×2 cm)。采用定点分辨波谱序列(point resolved spectroscopy,TR 2 000毫秒,TE 135毫秒)定位于基底节区及放射冠区。所测定的代谢产物包括N-乙酰基天门冬氨酸(NAA)、肌酸复合物(Cr)、胆碱复合物(Cho)、肌醇(MI)、乳酸(LAC)、谷氨酸及谷氨酰胺(Glu-Gln)等。波谱的后期处理包括:相位校正、基线校正、ppm(10-6)转换等。各代谢物水平的测定以波谱覆盖的面积为准。
, 百拇医药
3.统计学分析:对测量结果进行中位数的计算及秩和检验。
结果
一、正常足月新生儿的1H MRS表现
8例正常新生儿Cho、NAA、Cr的波峰高耸;MI的波峰略低;Glu-Gln及LAC波峰低平或测不出。波幅从高至低的顺序为Cho、NAA、Cr、MI、Glu-Gln及LAC(图1)。其中,NAA位于2.0 ppm;Cr位于3.0 ppm;Cho位于3.25 ppm;MI位于3.5 ppm;Glu-Gln位于2.3~2.5 ppm范围内(呈多个锯齿状波形);LAC位于1.3 ppm附近。以Cr为参照峰,分别计算出代谢物波峰面积与Cr波面积的比值。其中,NAA与Cr的比值为1.88±0.62,Cho与Cr的比值为1.21±0.35,MI与Cr的比值为0.62±0.13,LAC与Cr的比值为0.23±0.29,Glu-Gln与Cr的比值为0.55±0.31。

, 百拇医药
图1 正常新生儿的1H磁共振波谱。N-乙酰基天门冬氨酸(NAA)、肌酸复合物(Cr)、胆碱复合物(Cho)波峰高耸,肌醇(MI)波略低,谷氨酸-谷氨酰胺(Glu-Gln)及乳酸波低平
二、HIE患儿的1H MRS表现
1.本组36例NAA波峰高耸,2例NAA波峰降低,提示有神经元缺失;7例MI波峰增高(图2);9例Glu-Gln波峰增高,表现为多个增大的锯齿状波(图3);26例LAC波峰增高呈典型的双峰状,提示脑内乳酸的积聚;11例Cr波峰降低(图4);Cho与正常新生儿无显著性差异(表1)。

图2 缺氧缺血脑病患儿的1H磁共振波谱。N-乙酰基天门冬氨酸、肌酸复合物的波峰降低,肌醇波、乳酸波增高

, http://www.100md.com
图3 缺氧缺血脑病(HIE)患儿的1H磁共振波谱。位于2.3~2.5 ppm的谷氨酸-谷氨酰胺(Glu-Gln)波峰呈多个增大的锯齿状波,乳酸(LAC)波明显增高,肌酸复合物(Cr)的波峰略低

图4 HIE患儿的1H MRS。位于1.3附近的LAC波明显增高,LAC/Cr>1.5
表1 正常足月新生儿与HIE患儿脑代谢化合物相对浓度比较(
 ±s) 分组
±s) 分组例数
NAA/Cr
Cho/Cr
, http://www.100md.com
MI/Cr
Glu-Gln/Cr
LAC/Cr
正常组
8
1.88±0.62
1.21±0.35
0.62±0.13
0.55±0.31
0.23±0.29
HIE组
38
, http://www.100md.com
4.22±3.56
1.96±1.92
1.37±0.84
1.35±0.95
3.35±2.86
t值
5.401
2.521
3.740
3.986
4.105
P值
, 百拇医药
<0.01
<0.05
<0.01
<0.01
<0.01
注:HIE为缺氧缺血脑病;NAA/Cr为N-乙酰基天门冬氨酸与肌酸复合物的比值;Cho/Cr为胆碱复合物与肌酸复合物的比值;MI/Cr为肌醇与肌酸复合物的比值;Glu-Gln/Cr为谷氨酸及谷氨酰胺与肌酸复合物的比值;LAC/Cr为乳酸与肌酸复合物的比值
2.根据LAC与Cr比值的不同,将HIE患儿分为3组(表2)。其中LAC与Cr之比<0.5者12例,10例MRI T1WI上仅见皮层及皮层下沿脑回迂曲的条状高信号,代表毛细血管的不完全阻塞;8例同时合并幕上、幕下蛛网膜下腔少量出血;2例基底节区点状高信号及限局性脑水肿;1H MRS可见1例Cr波峰降低。LAC与Cr之比在0.5~1.5之间者15例,其中12例MRI T1WI上除上述表现外,额叶深部白质对称性点状高信号和(或)沿侧脑室白质区条带状高信号伴限局性脑水肿(图5),这是由于大脑深静脉瘀血扩张或出血性梗死所致[2];2例同时合并脑室内出血;1例仅见蛛网膜下腔少量出血;1H MRS显示3例Cr波峰降低,3例MI波峰升高,4例Glu-Gln波峰升高。LAC与Cr之比>1.5者11例,其中9例MRI T1WI除上述表现外,还合并有基底节区及丘脑高信号伴内囊前后肢低信号(图6),提示出血性梗死、神经细胞坏死以及髓鞘化发育障碍等多种疾病并存[2,3];4例合并脑室内出血及患侧脑室扩大;6例合并弥漫性脑水肿;2例仅有基底节区斑点状高信号灶及限局性脑水肿;1H MRS显示2例NAA波峰略低(1例NAA与Cr之比为0.69,1例NAA与Cr之比为0.53),7例Cr波峰降低,4例MI波峰升高,5例Glu-Gln波峰升高。

, http://www.100md.com
图5 缺氧缺血脑病患儿的T1WI,可见沿侧脑室白质区条带状高信号及额枕叶限局性脑水肿

图6 缺氧缺血脑病患儿的T1WI,与图4为同一病人。可见基底节区斑片状高信号、内囊后肢低信号以及弥漫性脑水肿
表2 正常新生儿与HIE患儿脑内乳酸相对
浓度比较(
 ±s) 分组
±s) 分组例数
NAA/Cr
t值
, 百拇医药
P值
正常组
8
0.23±0.29
-
-
LAC/Cr<0.5
12
0.47±0.22
2.326
<0.05
0.5
15
, 百拇医药
1.23±0.39
2.624
<0.05
LAC/Cr>1.5
11
3.93±1.91
4.947
<0.01
注:HIE为缺氧缺血性脑病;NAA/Cr为乳酸与肌酸复合物的比值,LAC/Cr为乳酸与肌酸复合物的比值
3.分别对26例HIE患儿6个月以后进行随访和(或)MRI复查,结果如下:LAC与Cr之比<0.5的9例(3例MRI复查,6例随访)中,7例结果正常,1例合并脑外积液,1例运动及体能发育落后;LAC与Cr之比为0.5~1.5的8例(5例MRI复查,3例随访)中,6例结果正常,1例合并有脑内小的软化灶,1例合并运动及体能发育落后;LAC与Cr之比>1.5的9例(7例MRI复查,2例随访)中,脑外积液者3例(图7),脑室旁白质软化者2例,髓鞘发育延迟者1例,胼胝体发育不良者1例,运动及体能发育落后者1例,正常者1例。

, http://www.100md.com
图7 缺氧缺血脑病患儿6个月时复查的MR图像(T2WI)。与图4、6为同一病人。可见脑外间隙增宽,合并脑外积液
讨论
新生儿HIE的发生包括一系列复杂的病理生理及生化改变。其病变发生的部位、程度与缺氧缺血持续的时间及脑内代谢物质水平的变化密切相关。基于化学位移原理的1H磁共振波谱技术能够反映出脑内主要代谢物的水平,对判断本病所引起的能量代谢障碍、细胞内酸中毒及神经元的缺失等情况能够提供有价值的信息[3]。
一、正常新生儿1H MRS中各代谢产物的水平及意义
正常新生儿1H MRS可有以下几个高峰:NAA以及不到10%的N-乙酰基天门冬氨酸盐,其波谱位于2.0 ppm处,Peden等[4]研究表明NAA主要存在于神经元内,与神经元的成熟有关。新生儿随着日龄的增长,NAA波峰也逐渐升高。Cho的波峰位于3.2 ppm处,包括磷酸甘油胆碱、磷酸胆碱和磷脂酰胆碱,反映脑内总的胆碱量。新生儿期1H MRS中,Cho波为波谱中的最高峰,NAA波峰低于Cho,1岁以后随着髓鞘化的逐渐完成而发生逆转。Cr波是总肌酸中的甲基组,包括肌酸与磷酸肌酸(Cr+PCr),是能量代谢的物质,其波谱位于3.0 ppm附近。在脑内不同代谢条件下,Cr+PCr的总量是恒定的。因此,可将Cr作为参照的波峰,得出其他代谢物质与Cr的相对比值,从而进行比较[4,5]。新生儿期NAA与Cr的比值(1.88±0.62)低于1岁以后的小儿;Cho与Cr的比值(1.21±0.35)高于其他年龄组的小儿,此种改变在3岁以前最为显著[5]。MI波位于3.5 ppm处,其功能尚不十分明确,Brian等[5]认为MI是胶质细胞存在的标志。在正常脑组织中,细胞能量代谢以有氧氧化为主,脑内乳酸水平很低,位于1.3 ppm附近的LAC波一般是不能测得的,如果出现则呈低平的波形。Glu-Gln 2个代谢物的波峰位置相近,总峰的位置在2.3~2.5 ppm处,二者作为兴奋性神经递质在脑内含量很少,但在维持线粒体的代谢中具有重要功能[5]。由于Glu-Gln波覆盖的范围较广泛,在同一共振频率内可有其他氨基酸如γ-氨基丁酸及NAA波谱的存在,精确的测量较为困难。
, 百拇医药
二、1H MRS在HIE诊断及预后评价中的应用
1.LAC升高及其LAC与Cr之比在HIE评估中的应用:HIE患儿1H MRS与正常新生儿脑组织明显不同。特征性的表现是在1.3 ppm处出现双峰状的乳酸波,乳酸波的出现是由于缺氧缺血引起继发性氧化磷酸化不足,无氧糖酵解增加所致。此波与其他代谢物的比值较正常组明显增高,尤其以LAC与Cr的比值最具特征性。因此常将LAC与Cr的比值作为衡量脑内乳酸含量相对增高的一个重要指标。脑组织在急性损伤的同时,乳酸含量就会增高。如果乳酸的积聚量不超过一定值,损伤后几周内由于局部代谢或氧的运输增加,可使脑内乳酸含量逐渐恢复到正常水平[6]。反之,如果乳酸的积聚量超过某一临界值并持续增高,就会引起细胞的酸中毒从而导致神经细胞的不可逆性损伤,最终影响患儿的预后。此临界值的测定由于实验对象、采用的技术手段及MR场强的不同而有所不同[6,7]。本研究发现LAC与Cr之比>1.5的这一组中,LAC与Cr之比为3.93±1.91,与对照组0.23±0.29比较有显著性差异。而且本组患儿MRI上病变累及的范围广、程度重(占81.8%),同时合并其他代谢物水平异常的几率高;复查的患儿中有8例出现不同程度的脑后遗症表现(占88.9%)。LAC与Cr之比在0.5~1.5之间者仅有25%的患儿出现脑后遗症改变,MRI上一般呈中等度损伤(占80.0%),合并其他代谢物水平异常的机会较前者少(占40.0%)。结合MRI的影像特征及临床资料,本组根据LAC与Cr比值的不同将HIE患儿分为轻、中、重度(即LAC与Cr之比<0.5者为轻度, LAC与Cr之比在0.5~1.5之间者为中度, LAC与Cr之比>1.5者为重度)。其中重度所致的脑损伤种类多、程度重,患儿预后多不良。
, 百拇医药
乳酸指标较敏感,常作为本病1H MRS判定的主要依据,也是本病在1H MRS上所表现的直接征象。其准确的测定取决于感兴趣区的合理选择,由于基底节和放射冠区是足月新生儿代谢活跃的区域,该区域最易受缺血缺氧的损伤[7],选择此区域作为感兴趣区,一方面可以增加生化指标检测的敏感性;另一方面也可以避免因脑边缘部脂肪波的干扰而影响乳酸波的准确测定。
2.其他代谢物水平在HIE评估中的应用:HIE的1H MRS也出现NAA波峰的改变(本组2例,占5.3%)。NAA波峰的降低提示乳酸的过多积聚引起神经元的自身溶解,也是不可逆性脑损伤的一个标志[8]。但其波峰的改变常在LAC升高数天后才出现。本组2例NAA波峰降低(NAA与Cr之比<1),复查结果显示其所出现的后遗程度最重。
HIE也可累及其他代谢物如Cr、Glu-Gln和MI等的改变。本研究中有11例Cr波降低,这与无氧糖酵解增加所导致的高能量磷酸化合物的减少有关。Glu-Gln在本病中也有参考价值。它是位于2.3~2.5 ppm之间的多个锯齿状波,呈阶梯状排列,其出现是由于缺血缺氧引起神经递质尤其是谷氨酸释放进入突触间隙所致[9]。急性缺血缺氧损伤合并能量衰竭,其波峰幅度会明显升高,在NAA波峰的左侧出现典型的“山峰状”波形(本组有5例,占13.2%)。本组同时有7例MI波峰升高,提示合并有胶质增生及髓鞘化不良[9]。
, 百拇医药
Cho在本病中无显著的波形变化,出现Cho与Cr比值的改变是由于HIE与正常脑组织间T2值的差异及Cr值的减低所致。
总之,LAC波峰的明显增高及合并其他代谢物如NAA、Cr、Glu-Gln、MI等的异常,常提示预后不良。1H MRS与MRI的综合分析,对本病的预后和临床治疗有一定的指导意义。本组复查病例数目较少,时间较短,故长期的预后如何,需进一步研究。
参考文献
1 Wang Z, Zimmerman RA,Sauter R. Proton MR spectroscopy of the brain: clinically useful information obtained in assessing CNS diseases in children.AJR, 1996,167:191-199.
, 百拇医药
2 陈丽英,王晓明,孟淑珍,等.足月新生儿缺氧缺血脑病的MRI研究. 中国医学计算机成像杂志, 1999,5:47-50.
3 Kriel RL,Krach LE,Luxenberg MG,et al. Outcome of severe anoxic/ischemic brain injury in children. Pediatr Neurol, 1994,10:207-212.
4 Peden CJ,Rutherford MA,Sargentoni J,et al. Proton spectroscopy of the neonatal brain following hypoxic-ischaemic injury. Dev Med Child Neurol,1993,35:502-510.
5 Rss B, Michaelis T. Clinical applications of magnetic resonance spectroscopy. Magn Reson Q,1994,10:191-247.
, http://www.100md.com
6 Penrice J,Lorek A,Cady EB,et al. Proton magnetic resonance spectroscopy of the brain during acute hypoxia-ischemia and delayed cerebral energy failure in the newbone piglet. Pediatr Res, 1997,41:795-802.
7 Groenendaal F, Veenhoven RH, van der Grond J, et al. Cerebral lactate and N-acetyl-aspartate/choline ratios in asphyxiated full-term neonate demonstrated in vivo using proton magnetic resonance spectroscopy. Pediatr Res ,1994,35:148-151.
, 百拇医药
8 Hanrahan JD,Sargentoni J,Azzopardi D,et al. Cerebral metabolism within 18 hours of birth asphyxia: a proton magnetic resonance spectroscopy study. Pediatr Res, 1996,39:584-590.
9 Penrice J, Cady EB, Lorek A, et al. Proton magnetic resonance spectroscopy of the brain in normal preterm and term infants, and early changes after perinatal hypoxia-ischemia. Pediar Res,1996,40:6-14.
收稿:1999-01-05
修回:1999-05-10, 百拇医药