不同浓度的持续性静滴葡萄糖耐量试验时老年人B细胞功能的研究1
作者:张 楚 寿晓琳
单位:杭州市第一人民医院内分泌科,杭州 310006
关键词:老年人;β细胞功能;持续静脉滴注法葡萄糖耐量试验(CIGTT);口服糖耐量试验(OGTT);快速静脉推注法葡萄糖耐量试验(IGTT);胰岛素抵抗
990214 摘 要 目的 为评价老年人胰岛B细胞功能增龄性变化。方法 应用持续静滴法葡萄糖耐量试验对20例老年人,10例老年非胰岛素依赖型糖尿病病人及20例青年人进行了研究。结果 低浓度糖负荷下老年人前30 min胰岛素释放率较两对照组无显著性统计学差异,其糖耐量介于糖尿病组与青年组之间;老年组空腹胰岛素水平高于青年组;高浓度糖负荷下120 min时血糖值老年组>青年组,相应的胰岛素分泌降低。老年组葡萄糖代谢清除率下降,仅为青年组的79%。结论 β细胞对持续高浓度的葡萄糖刺激的胰岛素分泌下降及胰岛素抵抗是老年糖耐量减退的主要原因。
, 百拇医药
传统的胰岛B细胞功能评价多采用口服75g葡萄糖耐量试验(OGTT)及相应的胰岛素释放试验(IRT)。快速静脉推注法葡萄糖耐量试验(IGTT)因其敏感性不高未获广泛应用〔1〕。为避免OGTT时胃肠道吸收不一致的干扰及糖负荷总量及糖吸收、速率不确定性影响有关参数的准确性,本文设计了持续(120min)静脉输滴注法葡萄糖耐量试验(CIGTT),观察老年人B细胞功能改变,以探讨老年人胰岛增龄性变化。
1 对象与方法
1.1 研究对象 老年组20例(男12,女8)。来源于内科非糖尿病的痊愈病人,平均年龄65岁。按输入5%或10%葡萄糖不同又分为老年高糖组、老年低糖组(各10)。青年组20例(男女各10),系本院职工,平均年龄18岁,也按上法分为青年高糖组、青年低糖组(各10)。Ⅱ型糖尿病组(NIDDM)10例,平均年龄63岁(男女各5),系本院内分泌病房住院病人,无严重并发症、夹杂症,符合WHO关于Ⅱ型糖尿病的诊断标准,该组仅输注低糖溶液。
, 百拇医药
1.2 方法 实验对象空腹于早晨8时静脉采血4 ml后开始静脉滴注5%或10%葡萄糖溶液500 ml,每分钟70滴,120min准时滴完。输液开始后分别于30,60,120min时在对侧上肢浅静脉采血4 ml送检血糖、免疫反应胰岛素(简称胰岛素)。血糖测定采用全自动生化仪葡萄糖氧化酶法,胰岛素测定采用放射免疫法。糖尿病病人均未用过胰岛素注射疗法,受试日停用口服降糖药。葡萄糖代谢清除率(MCR)计算〔2〕:MCR=M/MBG,其中M为葡萄糖摄取率,原意指OGTT中糖负荷量与2 h后仍存在于血糖池中残余负荷糖量之差。
M=糖负荷量/120+(0 min血糖-120 min血糖)×1.15×180×0.19×体重/120,单位mg/min。
MBG为实验中4次血糖均数,故MCR单位为mg.L/mmol.min-1。
, 百拇医药
本研究中将原应用于OGTT中的方法移植于持续静滴葡萄糖耐量试验中,糖负荷量按低糖组5%浓度计为25000mg。为评价老年人B细胞对葡萄糖刺激的反应性,引入胰岛素释放率(IR)〔2〕,IR=(I30-I0)/(G30-G0)(单位为mU/mmol),意为本试验前30min胰岛素面积增值与葡萄糖面积增值之比。
1.3 统计学处理 组间均数t检验。
2 结 果
青年组、老年组,糖尿病组两种浓度葡萄糖负荷后血糖、胰岛素变化见表1。
表1 青年、老年、糖尿病三组不同浓度葡萄糖输入后血糖、胰岛素变化(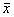 ±s)
±s)
, http://www.100md.com
(血糖(mmol/L)
(血浆胰岛素(μu/ml)
0
30
60
120(min)
0
30
60
120
(min)
5%青年组
4.02±0.24
, 百拇医药
5.76±0.73
6.62±1.15
6.20±0.85
5.62±
1.58
24.20±21.70
23.80±12.75
17.90±
9.19
5%老年组
5.60±0.72
7.62±1.49
, http://www.100md.com
8.17±1.68
8.04±2.08
25.80±25.00
43.70±45.00
54.60±54.00
46.00±45.00
5%糖尿病组
8.94±2.61
11.10±2.65
12.90±3.23
13.00±2.89
, http://www.100md.com 16.70±17.46
34.10±48.00
36.14±47.00
36.10±46.10
10%青年组
4.23±0.42
8.76±1.97
9.12±1.62
6.45±1.87
5.58±
0.92
39.90±31.47
, http://www.100md.com
71.02±41.49
73.97±43.24
10%老年组
5.23±0.44
7.89±1.49
9.01±2.28
9.35±2.56
8.45±
3.54
27.00±25.70
52.60±41.85
63.97±43.70
, 百拇医药
2.1 低糖组三组血糖反应曲线下面积为糖尿病组>老年组>青年组,其30、60、120 min血糖值三组间差异有统计学意义(P<0.005至P<0.05),相应的胰岛素释放曲线下面积为老年组>糖尿病组>青年组,但无统计学差异,仅老年组空腹胰岛素与青年组间有统计学差异(P<0.05)。
2.2 老年高糖组与青年高糖组比较,糖负荷后30、60 min时两组血糖接近,而120min时明显上扬,相应的胰岛素分泌老年组<青年组(P<0.05)。
2.3 胰岛素释放率:青年低糖组9.60±5.04,老年低糖组10.30±8.27,糖尿病组7.30±12.10,经统计学处理无显著性差异。
2.4 葡萄糖代谢清除率:青年低糖组43.31±3.37,老年低糖组34.37±3.69,糖尿病组25.27±7.89,三组有显著性差异(P<0.01)。
, http://www.100md.com
2.5 糖负荷后血糖曲线达峰时间:青年低糖组、青年高糖组、老年低糖组均为60min,老年高糖组、糖尿病组为120min。
3 讨 论
Davidson〔3〕认为老年人有糖耐量减退倾向可能与营养因素、体力活动减少、体重增加有关。而老年人易罹患Ⅱ型糖尿病的主要原因可为胰岛素分泌下降或/和对葡萄糖刺激敏感性下降及外周组织胰岛素抵抗〔4〕。以往从OGTT、IRT等手段得到的有关IR、MCR等参数肯定要受老年人胃肠道吸收不均一性的干扰,由于糖负荷总量及给糖吸收速率的不确定性,使研究结果不够可靠。快速静注法IGTT在2~3min内注射完毕,测定至30min止,显然其过高瞬间血糖不利于暴露β细胞的轻微缺陷,且持续时间亦过短。本研究中,老年人糖负荷后前30minIR值较青年组无明显下降,反映β细胞对葡萄糖刺激的胰岛素分泌功能尚正常。外周组织对葡萄糖MCR下降,仅及青年组79%,提示组织对胰岛素敏感性下降。
, http://www.100md.com
低糖组糖耐量曲线下面积糖尿病组>老年组>青年组,空腹胰岛素老年组>青年组,且糖尿病组、老年组胰岛素峰值均后移,说明老年人存在外周组织胰岛素抵抗,其高胰岛素血症与高血糖血症并存。高糖组实验显示,延长的高浓度糖刺激可暴露老年人胰岛素分泌不足,引起120min血糖上扬。可能因长时间的β细胞分泌导致分泌产物中胰岛素原/胰岛素比值上升,活性下降。Davis等〔5〕观察到在延长的静滴葡萄糖刺激后β细胞分泌有上述之改变。
在实际应用中,OGTT仍是目前诊断糖尿病的“金标准”。然而本研究采用的持续静滴法葡萄糖耐量试验因其具有精确的糖负荷总量、恒定的给糖速率、持久的糖负荷而使所得到的IR、MCR诸参数准确可信。本研究提示,β细胞对持续高浓度葡萄糖刺激的胰岛素分泌下降及外周组织胰岛素抵抗是老年糖耐量减退的主要原因。
1 本课题获杭州市卫生局科研资助
作者简介:张 楚,男,40岁,副主任医师,从事糖尿病并发症,甲状腺功能亢进免疫改变及治疗
, 百拇医药
4 参考文献
1 池芝盛.内分泌学基础与临床.北京:北京科学技术出版社,1992:586
2 Cederholm J, Wibell L.Insulin release and peripheral sensitivity at the oral glucose tolerance test.Diabetes Research and Clinical Practice,1990;10:167
3 Davidson MB.The effect of aging on carbohydrate metabolism: a review of the English literature and a practical approach to the diagnosis of diabetes mellitus in the elderly.Metabolism,1979;28:688
, http://www.100md.com
4 Taylor SI, Accili D, Imai Y.Insulin resistance or insulin deficiency:Which is the primary cause of NIDDM?Diabetes,1994;43:735
5 Davis SN, Piatti PM, Monti L et al.Proinsulin and insulin concentrations following intravenous glucose challenges in normal obese and non-insulin-dependent diabetic subjects.Metabolism,1993;42:30
〔1998-04-15收稿 1998-09-07修回〕, 百拇医药
单位:杭州市第一人民医院内分泌科,杭州 310006
关键词:老年人;β细胞功能;持续静脉滴注法葡萄糖耐量试验(CIGTT);口服糖耐量试验(OGTT);快速静脉推注法葡萄糖耐量试验(IGTT);胰岛素抵抗
990214 摘 要 目的 为评价老年人胰岛B细胞功能增龄性变化。方法 应用持续静滴法葡萄糖耐量试验对20例老年人,10例老年非胰岛素依赖型糖尿病病人及20例青年人进行了研究。结果 低浓度糖负荷下老年人前30 min胰岛素释放率较两对照组无显著性统计学差异,其糖耐量介于糖尿病组与青年组之间;老年组空腹胰岛素水平高于青年组;高浓度糖负荷下120 min时血糖值老年组>青年组,相应的胰岛素分泌降低。老年组葡萄糖代谢清除率下降,仅为青年组的79%。结论 β细胞对持续高浓度的葡萄糖刺激的胰岛素分泌下降及胰岛素抵抗是老年糖耐量减退的主要原因。
, 百拇医药
传统的胰岛B细胞功能评价多采用口服75g葡萄糖耐量试验(OGTT)及相应的胰岛素释放试验(IRT)。快速静脉推注法葡萄糖耐量试验(IGTT)因其敏感性不高未获广泛应用〔1〕。为避免OGTT时胃肠道吸收不一致的干扰及糖负荷总量及糖吸收、速率不确定性影响有关参数的准确性,本文设计了持续(120min)静脉输滴注法葡萄糖耐量试验(CIGTT),观察老年人B细胞功能改变,以探讨老年人胰岛增龄性变化。
1 对象与方法
1.1 研究对象 老年组20例(男12,女8)。来源于内科非糖尿病的痊愈病人,平均年龄65岁。按输入5%或10%葡萄糖不同又分为老年高糖组、老年低糖组(各10)。青年组20例(男女各10),系本院职工,平均年龄18岁,也按上法分为青年高糖组、青年低糖组(各10)。Ⅱ型糖尿病组(NIDDM)10例,平均年龄63岁(男女各5),系本院内分泌病房住院病人,无严重并发症、夹杂症,符合WHO关于Ⅱ型糖尿病的诊断标准,该组仅输注低糖溶液。
, 百拇医药
1.2 方法 实验对象空腹于早晨8时静脉采血4 ml后开始静脉滴注5%或10%葡萄糖溶液500 ml,每分钟70滴,120min准时滴完。输液开始后分别于30,60,120min时在对侧上肢浅静脉采血4 ml送检血糖、免疫反应胰岛素(简称胰岛素)。血糖测定采用全自动生化仪葡萄糖氧化酶法,胰岛素测定采用放射免疫法。糖尿病病人均未用过胰岛素注射疗法,受试日停用口服降糖药。葡萄糖代谢清除率(MCR)计算〔2〕:MCR=M/MBG,其中M为葡萄糖摄取率,原意指OGTT中糖负荷量与2 h后仍存在于血糖池中残余负荷糖量之差。
M=糖负荷量/120+(0 min血糖-120 min血糖)×1.15×180×0.19×体重/120,单位mg/min。
MBG为实验中4次血糖均数,故MCR单位为mg.L/mmol.min-1。
, 百拇医药
本研究中将原应用于OGTT中的方法移植于持续静滴葡萄糖耐量试验中,糖负荷量按低糖组5%浓度计为25000mg。为评价老年人B细胞对葡萄糖刺激的反应性,引入胰岛素释放率(IR)〔2〕,IR=(I30-I0)/(G30-G0)(单位为mU/mmol),意为本试验前30min胰岛素面积增值与葡萄糖面积增值之比。
1.3 统计学处理 组间均数t检验。
2 结 果
青年组、老年组,糖尿病组两种浓度葡萄糖负荷后血糖、胰岛素变化见表1。
表1 青年、老年、糖尿病三组不同浓度葡萄糖输入后血糖、胰岛素变化(
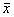 ±s)
±s), http://www.100md.com
(血糖(mmol/L)
(血浆胰岛素(μu/ml)
0
30
60
120(min)
0
30
60
120
(min)
5%青年组
4.02±0.24
, 百拇医药
5.76±0.73
6.62±1.15
6.20±0.85
5.62±
1.58
24.20±21.70
23.80±12.75
17.90±
9.19
5%老年组
5.60±0.72
7.62±1.49
, http://www.100md.com
8.17±1.68
8.04±2.08
25.80±25.00
43.70±45.00
54.60±54.00
46.00±45.00
5%糖尿病组
8.94±2.61
11.10±2.65
12.90±3.23
13.00±2.89
, http://www.100md.com 16.70±17.46
34.10±48.00
36.14±47.00
36.10±46.10
10%青年组
4.23±0.42
8.76±1.97
9.12±1.62
6.45±1.87
5.58±
0.92
39.90±31.47
, http://www.100md.com
71.02±41.49
73.97±43.24
10%老年组
5.23±0.44
7.89±1.49
9.01±2.28
9.35±2.56
8.45±
3.54
27.00±25.70
52.60±41.85
63.97±43.70
, 百拇医药
2.1 低糖组三组血糖反应曲线下面积为糖尿病组>老年组>青年组,其30、60、120 min血糖值三组间差异有统计学意义(P<0.005至P<0.05),相应的胰岛素释放曲线下面积为老年组>糖尿病组>青年组,但无统计学差异,仅老年组空腹胰岛素与青年组间有统计学差异(P<0.05)。
2.2 老年高糖组与青年高糖组比较,糖负荷后30、60 min时两组血糖接近,而120min时明显上扬,相应的胰岛素分泌老年组<青年组(P<0.05)。
2.3 胰岛素释放率:青年低糖组9.60±5.04,老年低糖组10.30±8.27,糖尿病组7.30±12.10,经统计学处理无显著性差异。
2.4 葡萄糖代谢清除率:青年低糖组43.31±3.37,老年低糖组34.37±3.69,糖尿病组25.27±7.89,三组有显著性差异(P<0.01)。
, http://www.100md.com
2.5 糖负荷后血糖曲线达峰时间:青年低糖组、青年高糖组、老年低糖组均为60min,老年高糖组、糖尿病组为120min。
3 讨 论
Davidson〔3〕认为老年人有糖耐量减退倾向可能与营养因素、体力活动减少、体重增加有关。而老年人易罹患Ⅱ型糖尿病的主要原因可为胰岛素分泌下降或/和对葡萄糖刺激敏感性下降及外周组织胰岛素抵抗〔4〕。以往从OGTT、IRT等手段得到的有关IR、MCR等参数肯定要受老年人胃肠道吸收不均一性的干扰,由于糖负荷总量及给糖吸收速率的不确定性,使研究结果不够可靠。快速静注法IGTT在2~3min内注射完毕,测定至30min止,显然其过高瞬间血糖不利于暴露β细胞的轻微缺陷,且持续时间亦过短。本研究中,老年人糖负荷后前30minIR值较青年组无明显下降,反映β细胞对葡萄糖刺激的胰岛素分泌功能尚正常。外周组织对葡萄糖MCR下降,仅及青年组79%,提示组织对胰岛素敏感性下降。
, http://www.100md.com
低糖组糖耐量曲线下面积糖尿病组>老年组>青年组,空腹胰岛素老年组>青年组,且糖尿病组、老年组胰岛素峰值均后移,说明老年人存在外周组织胰岛素抵抗,其高胰岛素血症与高血糖血症并存。高糖组实验显示,延长的高浓度糖刺激可暴露老年人胰岛素分泌不足,引起120min血糖上扬。可能因长时间的β细胞分泌导致分泌产物中胰岛素原/胰岛素比值上升,活性下降。Davis等〔5〕观察到在延长的静滴葡萄糖刺激后β细胞分泌有上述之改变。
在实际应用中,OGTT仍是目前诊断糖尿病的“金标准”。然而本研究采用的持续静滴法葡萄糖耐量试验因其具有精确的糖负荷总量、恒定的给糖速率、持久的糖负荷而使所得到的IR、MCR诸参数准确可信。本研究提示,β细胞对持续高浓度葡萄糖刺激的胰岛素分泌下降及外周组织胰岛素抵抗是老年糖耐量减退的主要原因。
1 本课题获杭州市卫生局科研资助
作者简介:张 楚,男,40岁,副主任医师,从事糖尿病并发症,甲状腺功能亢进免疫改变及治疗
, 百拇医药
4 参考文献
1 池芝盛.内分泌学基础与临床.北京:北京科学技术出版社,1992:586
2 Cederholm J, Wibell L.Insulin release and peripheral sensitivity at the oral glucose tolerance test.Diabetes Research and Clinical Practice,1990;10:167
3 Davidson MB.The effect of aging on carbohydrate metabolism: a review of the English literature and a practical approach to the diagnosis of diabetes mellitus in the elderly.Metabolism,1979;28:688
, http://www.100md.com
4 Taylor SI, Accili D, Imai Y.Insulin resistance or insulin deficiency:Which is the primary cause of NIDDM?Diabetes,1994;43:735
5 Davis SN, Piatti PM, Monti L et al.Proinsulin and insulin concentrations following intravenous glucose challenges in normal obese and non-insulin-dependent diabetic subjects.Metabolism,1993;42:30
〔1998-04-15收稿 1998-09-07修回〕, 百拇医药