ДѓЪѓаФМЁІТ-ЩіЩЯЯйЫиЪмЬхЗЂг§ЕФбаОП
зїепЃКдјКЭЦН РюЭђеђ
ЕЅЮЛЃК100034 ББОЉвНПЦДѓбЇЕквЛвНдКЖљПЦ
ЙиМќДЪЃКЪмЬхЃЛЩіЩЯЯйЫиФмІТЃЛаФМЁЃЛДѓЪѓЃЛWistar
жаЛЊЖљПЦдгжО981111 ЁОеЊвЊЁП ФПЕФ ЬНЬжЗЂг§вђЫиЖдДѓЪѓаФМЁІТ-ЩіЩЯЯйЫиЪмЬх(ІТ-AR)ЕФгАЯьЁЃЗНЗЈ гІгУХфЛљНсКЯЁЂУИЛюадВтЖЈЃЌВтЖЈВЛЭЌФъСфЖЮWistarДѓЪѓаФМЁІТ-ARУмЖШЁЂЪмЬхбЧаЭЁЂЯймеЫсЛЗЛЏУИ(AC)ЛюадКЭЖдІТ-ARМЄЖЏМСЁЊЁЊвьБћЩіЩЯЯйЫиЗДгІадвдМАЕЭМззДЯйЫиДѓЪѓаФМЁІТ-ARУмЖШЁЃНсЙћ ДѓЪѓГіЩњЪБаФМЁІТ-ARУмЖШЦНОљЮЊ14.3 fmol/mg (ЕААз)ЃЌГЩФъКѓЦНОљЮЊ31.6 fmol/mg (ЕААз)ЃЌаФМЁІТ-ARУмЖШЫцФъСфЕФдіГЄЖјдіМг(FжЕЮЊ23.46, P<0.01)ЃЛІТ1/ІТ2-ARбЧаЭЯрЖдБШжЕЃЌГіЩњЪБЮЊ51/49ЃЌГЩФъЮЊ60/40ЃЛаФМЁACЖдІТ-ARМЄЖЏМСЁЊЁЊвьБћЩіЩЯЯйЫиЕФЗДгІадЃЌГіЩњЪБЮЊ76 pmol*mg-1*min-1ЃЌГЩФъЮЊ126 pmol*mg-1*min-1 ЃЌИїФъСфЖЮЕФВювьгаЯджјвтвх(FжЕЮЊ89.00, P<0.01)ЃЛACЛљДЁЛюадКЭACЖдACМЄЖЏМСForskolinЕФЗДгІадЃЌИїФъСфЖЮУЛгаВювьЃЛІТ1-ARозПЙМСвжжЦГЩФъДѓЪѓаФМЁACЖдвьБћЩіЩЯЯйЫиЕФЗДгІадЃЌІТ2-ARозПЙМСвжжЦаТЩњКЭЗЂг§дчЦкДѓЪѓаФМЁACЖдвьБћЩіЩЯЯйЫиЕФЗДгІадЃЛбЊЧхМззДЯйЫиМѕЕЭПЩЪЙЩњКѓ1жмКЭГЩФъДѓЪѓаФМЁІТ-ARУмЖШЯТНЕЁЃНсТл ДѓЪѓаФМЁІТ-ARУмЖШЁЂІТ1/ІТ2-ARбЧаЭБШР§ЁЂІТ-ARЖдACЕФЕїНкзїгУЪмЗЂг§вђЫиЕФгАЯьЁЃ
, АйФДвНвЉ
A developmental study on myocardial ІТ -adrenergic receptor in rats Zeng Heping, Li Wanzhen. Department of Pediatrics, The First Hospital, Beijing Medical University, Beijing 100034
ЁОAbstractЁП Objective To study the effect of developmental factors on ІТ-adrenergic receptor (AR) and its regulatory role in Wistar rat myocardium. Methods With the methods of ligand-binding and enzyme activity measurement, ІТ-AR density, receptor subtypes, myocardial adenylate cyclase (AC) activity, its age-related responsiveness to ІТ-AR agonist isoprenalin, and myocardial ІТ-AR density were measured in rats at different age stages. Also, myocardial ІТ-AR density was detected in hypothyroxin rats. Results Myocardial ІТ-AR density of rats was 14.3fmol/mg protein at birth, and 31.6 fmol/mg protein in adult. It increased with age (F=23.46, P<0.01). Relative ratio of ІТ1/ІТ2-AR was 51/49 at birth, and 60/40 in adult. The responsiveness of myocardial AC to ІТ-AR agonist isoprenalin was 76 pmol*mg-1*min-1 at birth and 126 pmol*mg-1*min-1 in adult (F=89.00, P<0.01). There was no difference in basic AC activity and responsiveness to AC agonist forskolin between rats at birth and in adult. Beta 1-antagonist inhibited the responsiveness of AC to isoprenalin in adult rats, while ІТ2-AR antagonist inhibited the responsiveness of AC to isoprenalin in newborn and young rats. Serum hypothyroxin decreased myocardial ІТ-AR densities in the newborn and adult rats. Conclusion Beta-AR density, relative ratio of its subtypes and ІТ-AR regulatory effect on myocardial AC were all influenced by developmental factors.
, АйФДвНвЉ
ЁОKey wordsЁП Receptor adrenergic,beta Myocardium Rats,Wistar
аФдрІТ-ЩіЩЯЯйЫиЪмЬх(adrenergic receptor, AR)НщЕМЯИАћФкЭтаХЯЂДЋЕМЃЌВЮгыЕїНкаФМЁЪеЫѕКЭЪцеХЙІФмЃЌВЂгыаэЖраЁЖљаФдрМВВЁгаУмЧаЙиЯЕ[1]ЁЃСйДВЙлВьБэУїЃЌгЄЖљгыФъГЄЖљЖдІТ-ARМЄЖЏМСЗДгІадВЛЭЌ[2]ЁЃЮЊбаОПЗЂг§Й§ГЬаФМЁІТ-ARЕФБфЛЏЧщПіЃЌЮвУЧЖдГіЩњЪБжСГЩФъВЛЭЌФъСфЖЮWistarДѓЪѓаФМЁІТ-ARУмЖШНјааМьВтЃЌВЂЬНЬжаФМЁІТ-ARЖдЯймеЫсЛЗЛЏУИ(adenylate cyclase, AC)ЕФЕїНкзїгУвдМАМззДЯйЫиЖдІТ-ARЕФгАЯьНјаабаОПЃЌЬНЬжЗЂг§вђЫиЖдаФМЁІТ-ARЕФгАЯьЁЃ
ВФСЯМАЗНЗЈ
вЛЁЂЖЏЮя
бЁдёГіЩњЪБМАГіЩњ1ЁЂ2ЁЂ3ЁЂ4жмКЭГЩФъ6ИіФъСфЖЮЕФWistarДѓЪѓЁЃЕЭМззДЯйЫиЖЏЮяФЃаЭбЁдёГіЩњ1жмКЭГЩФъЕФДѓЪѓЁЃ
, http://www.100md.com
ЖўЁЂЪЕбщЗНЗЈ
1.аФМЁЯИАћФЄжЦБИ[3]ЃКбЁдёВЛЭЌФъСфЖЮWistarДѓЪѓЃЌЖЯЭЗЃЌШЁаФдрЃЌЩњРэбЮЫЎГхЯДЃЌПьЫйдШНЌЃЌ4ВуЩДВМЙ§ТЫЁЃ5 000ЁСg(gЮЊжиСІГЃЪ§)РыаФЃЌ4ЁцЃЌ20Зжжг,зЊвЦЩЯЧх,20 000ЁСgРыаФ,4Ёц,20 Зжжг,ЦњЩЯЧхЁЃГСЕэГхЯД2БщЃЌЯИАћФЄжќДцвКаќИЁГСЕэЃЌгУгкХфЛљВтЖЈЛђ-80ЁцБЃДцЁЃ
2.ХфЛљВтЖЈ[3]ЃКНЋаФМЁЯИАћФЄаќвКжЦГЩ1.0 mg/mlЕФХЈЖШЁЃбЁгУ5жжВЛЭЌХЈЖШ[3H]-ЫЋЧтаФЕУЪц([3H]-DHAЃЌІТ-ARХфЛљ)МД0.6ЁЋ10.0 nmol/LЃЌЗДгІЛКГхвК100 ІЬlЃЌаФМЁЯИАћФЄаќвК50 ІЬlЃЌЗДгІзмЬхЛ§ЮЊ200 ІЬlЁЃ37ЁцЫЎдЁ20 ЗжжгЃЌжежЙЗДгІЃЌОWhatman GF/CВЃСЇЯЫЮЌФЄГщТЫЃЌТЫФЄГхЯД2ДЮЃЌздШЛСРИЩЃЌВтЖЈТЫФЄЩЯЕФЗХЩфЛюадЁЃЗЧЬивьадНсКЯЪЕбщВЩгУ10 ІЬmol/LХЈЖШЕФІТ-ARозПЙМСЁЊЁЊЦеФЮТхЖћДцдкЪБ[3H]-DNAНсКЯСПБэЪОЁЃРћгУЗХЩфХфЛљНсКЯЗжЮіЗЈ(scatchard analysis)ЗжЮіаФМЁЪмЬхУмЖШКЭЧзКЭадЁЃВтЖЈІТ-ARбЧаЭЪБНЋ50 ІЬlЯИАћФЄаќвКгывЛжжХЈЖШЕФ[3H]-DNAКЭ16жжВЛЭЌХЈЖШЕФІТ1-ARозПЙМС(CGP20172A 10-10ЁЋ10-5mol/L)дк37ЁцЫЎдЁ10ЗжжгЃЌШЛКѓГщТЫЃЌНјааЗХЩфМЦЪ§ЃЌЕУГіОКељвжжЦЧњЯпЁЃЖдЧњЯпНјааМЦЫуЛњФтКЯЃЌвдЧѓЕУЪмЬхбЧаЭБШР§ЁЃЕААзЖЈСПгУLowryЗЈ[4]ЁЃ
, АйФДвНвЉ
3.УИЛюадВтЖЈ[5]ЃКЗДгІЬхЯЕжаКЌга25 mmol/LбЮЫсШ§єЧМзЛљАБЛљМзЭщЃЌ2 mmol/LТШЛЏУОЃЌ20 mmol/LМЁЫсСзЫсЃЌ20 U/mlМЁЫсМЄУИЃЌ1 mmol/LЕФІС-[32P]Ш§СзЫсЯйме(40 cpm/pmol),МгШы80ЁЋ100 ІЬgЕФаФМЁЯИАћФЄЃЌзмЬхЛ§ЮЊ100 ІЬlЃЌ30ЁцЫЎдЁ20ЗжжгЃЌМгШыжежЙЗДгІвК100 ІЬlЁЃЗДгІЮяО1 500ЁСgРыаФ5ЗжжгЃЌЩЯЧхЫГађЭЈЙ§РызгНЛЛЛЪїжЌКЭбѕЛЏТСВуЮіжљЃЌЪеМЏЗжРывКЁЃЗжБ№ВтЖЈ[32P]КЭ[3H]ЕФЗХЩфЛюадЁЃ[3H]ЛЗСзЫсЯйме([3H]-cAMP)ЕФЛиЪеТЪдМЮЊ70%ЁЋ80%ЁЃЩЯЪіЗДгІЬхЯЕжаЗжБ№МгШы10-6 mol/LЕФForskolin(вЛжжACМЄЖЏМС)ЃЌ10-7mol/LвьБћЩіЩЯЯйЫиЃЌ10-7 mol/LЕФІТ1-ARозПЙМС(CGP20712A)КЭ10-7 mol/L ІТ2-ARозПЙМС(ICI118551)ЃЌ30ЁцЫЎдЁ20ЗжжгЁЃжежЙЗДгІЃЌВтЖЈ[32P]КЭ[3H]ЕФЗХЩфЛюадЁЃ
, АйФДвНвЉ
4.ЕЭМззДЯйЫи(T4)ЖЏЮяФЃаЭжЦБИКЭбЊЧхT4ВтЖЈЃКбЁдёГіЩњКѓ1жмКЭГЩФъДѓЪѓЁЃИЙЧЛзЂЩфБћЛљСђбѕрзрЄЃЌ20 mg/kgЃЌУПЬь1ДЮЃЌСЌајИјвЉ7ЬьЁЃЖдеезщИЙЧЛзЂЩфЭЌбљМССПЕФЩњРэбЮЫЎЁЃгУЪдМСКажНЦЌНгШЁ1ЕЮДѓгк0.5 cmжБОЖДѓаЁЕФбЊбљЃЌздШЛСРИЩЁЃгУДђПзЛњМєЯТ0.5 cmжБОЖбЊбљжНЦЌКЭЫцЪдМСКаАќзАЕФБъзМжНЦЌЃЌЗХШыЪдЙмжаЁЃИїЙмМгШы200 ІЬlЕФT4ПЙЬхЃЌЗДИДеёвЁ5ЗжжгЃЌЗХШы4ЁцБљЯфжаЙ§вЙЃЌШЛКѓМгШы125I-T4100 ІЬlЁЃЪвЮТЯТЗХжУ1аЁЪБЃЌдкІУЩСЫИвЧЩЯНјааІУМЦЪ§ЁЃаФМЁІТ-ARВтЖЈЭЌЧАЁЃ
Ш§ЁЂЪ§ОнДІРэМАЭГМЦМьбщ
УПзщЪ§ОнвдОљЪ§КЭБъзМВю(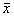 ЁРs)БэЪОЁЃЖрзщБШНЯВЩгУЗНВюЗжЮіМАNewman-KeulsМьбщЃЌСНзщБШНЯВЩгУtМьбщЛђtЁфМьбщЁЃ
ЁРs)БэЪОЁЃЖрзщБШНЯВЩгУЗНВюЗжЮіМАNewman-KeulsМьбщЃЌСНзщБШНЯВЩгУtМьбщЛђtЁфМьбщЁЃ
, http://www.100md.com
НсЙћ
вЛЁЂЗЂг§Й§ГЬжаДѓЪѓаФМЁІТ -ARУмЖШКЭЧзКЭадЕФБШНЯКЭЪмЬхбЧаЭЫљеМБШР§
ДгБэ1жаПЩПДГіЃЌаФМЁІТ-ARУмЖШГіЩњЪБНЯЕЭЃЌЫцЗЂг§ЖјдіМгЃЌжСЩњКѓ4жмГЪЯждіМгЧїЪЦЃЌГЩФъКѓТдгаЯТНЕ(FжЕ23.46, P<0.01)ЁЃГіЩњЪБЁЂЩњКѓ1жмЁЂ2жмДѓЪѓаФМЁІТ-ARУмЖШгыГЩФъДѓЪѓБШНЯВювьгаЯджјвтвхЁЃЖјЧзКЭадЮоЯджјадВювь(FжЕ1.31, P>0.05)ЁЃаФМЁІТ1-ARдкзмІТ-ARжаЫљеМЕФБШР§дкЗЂг§Й§ГЬжаГЪдіМгЧїЪЦЁЃ
Бэ1 6жЛДѓЪѓЗЂг§НзЖЮаФМЁІТ-AR
ЗХЩфХфЛљВтЖЈНсЙћ(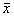 ЁРs) ЗЂг§НзЖЮ
ЁРs) ЗЂг§НзЖЮ
ІТ-ARУмЖШ
, http://www.100md.com
(fmol/mgЃЌЕААз)
ЧзКЭад
(nmol/L)
ЪмЬхбЧаЭеМІТ-AR
АйЗжБШ(%)
ІТ1
ІТ2
ГіЩњЪБ
14.3ЁР2.1*
0.45ЁР0.12
51
49
, http://www.100md.com
ГіЩњКѓ
1жм
20.1ЁР4.2*
0.57ЁР0.14
55
45
2жм
23.3ЁР1.5*
0.43ЁР0.02
55
45
3жм
, http://www.100md.com
29.3ЁР6.3
0.54ЁР0.10
58
42
4жм
39.0ЁР2.4
0.55ЁР0.12
60
40
ГЩФъ
31.6ЁР3.3
0.58ЁР0.02
60
, АйФДвНвЉ
40
зщМфБШНЯFжЕ
23.46Ёї
2.24
гыГЩФъБШНЯ * P<0.01ЃЌЁї P<0.01
ЖўЁЂЗЂг§Й§ГЬжааФМЁІТ-ARЖдACЕФЕїНкзїгУ
ДѓЪѓаФМЁACЛљДЁЛюадМАЖдACМЄЖЏМСForskolinЕФЗДгІадЃЌГіЩњжСГЩФъИїФъСфЖЮОљЮоУїЯдЕФВювьЁЃаФМЁACЖдІТ-ARМЄЖЏМСвьБћЩіЩЯЯйЫиЗДгІадЃЌГіЩњЪБКЭГіЩњ1жмНЯЕЭЃЌЫцзХЗЂг§ЃЌЗДгІадж№НЅдіМг(FжЕ89.00, P<0.01)ЃЛгУІТ1-ARозПЙМСзшЖЯаФМЁІТ1-ARЪБЃЌГЩФъДѓЪѓаФМЁACЖдвьБћЩіЩЯЯйЫиЗДгІадЪмЕНУїЯдЕФвжжЦЁЃДгБэ2ПЩПДГіЃЌвьБћЩіЩЯЯйЫиМЄЖЏГЩФъКЭаТЩњДѓЪѓаФМЁЃЌcAMPЩњГЩСПЗжБ№ЮЊ126ЁР9 pmol*mg-1*min-1КЭ76ЁР3.6 pmol*mg-1*min-1ЁЃЖјМггУІТ-ARозПЙМС(CGP)КѓЃЌГЩФъДѓЪѓаФМЁcAMPЩњГЩСПМѕЩй(73ЁР6 pmol*mg-1*min-1)ЃЌгыаТЩњДѓЪѓаФМЁcAMPЕФЩњГЩСПНќКѕЯрЕШ(68ЁР7 pmol*mg-1*min-1)ЃЛгУІТ2-ARозПЙМСзшЖЯаФМЁІТ2-ARЪБЃЌ2жмФкДѓЪѓаФМЁACЕФЗДгІадЪмЕНвжжЦНЯУїЯд(Бэ2)ЁЃ
, http://www.100md.com
Ш§ЁЂбЊЧхЕЭT4ЖдДѓЪѓаФМЁІТ-ARЕФгАЯь
ДѓЪѓМззДЯйВњЩњT4БЛБћЛљСђбѕрзрЄвжжЦЃЌT4ЫЎЦНЯТНЕгАЯь1жмСфКЭГЩФъДѓЪѓаФМЁІТ-ARЕФУмЖШЃЌЪЙЦфНЕЕЭЁЃЕЭT4ЖдаФМЁІТ-ARЕФЧзКЭадУЛгаУїЯдЕФгАЯь(Бэ3)ЁЃ
Бэ2 6жЛДѓЪѓВЛЭЌЗЂг§НзЖЮаФМЁACЛюадМАІТ-ARЖдACЕФЕїНкЧщПі(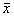 ЁРsЃЌcAMP pmol*mg-1*min-1) ЗЂг§НзЖЮ
ЁРsЃЌcAMP pmol*mg-1*min-1) ЗЂг§НзЖЮ
ЛљДЁЛюад
ЯймеЫсЛЗЛЏУИМЄЖЏМС
(ЁС10-6mol/L)
, АйФДвНвЉ
вьБћЩіЩЯЯйЫи
(ЁС10-7mol/L)
вьБћЩіЩЯЯйЫи+
ІТ1-ARозПЙМС
(ЁС10-7mol/L)
вьБћЩіЩЯЯйЫи+
ІТ2-ARозПЙМС
(ЁС10-7mol/L)
ГіЩњЪБ
20.4ЁР1.9
150ЁР5
, АйФДвНвЉ
75.8ЁР3.6
68ЁР7
38ЁР6*
ГіЩњКѓ
1жм
20.4ЁР1.7
151ЁР7
80.2ЁР2.5*
77ЁР5
42ЁР8*
2жм
20.4ЁР1.6
, АйФДвНвЉ
152ЁР5
103.7ЁР8.8*
75ЁР4
79ЁР7*
3жм
21.6ЁР2.8
151ЁР6
102.7ЁР5.8*
74ЁР3
99ЁР15*
4жм
, http://www.100md.com 22.0ЁР3.8
162ЁР12
142.0ЁР10.2
77ЁР9
137ЁР8*
ГЩФъ
19.6ЁР2.9
154ЁР9
125.6ЁР9.4
73ЁР6
116ЁР11
зщМфБШНЯFжЕ
, АйФДвНвЉ
2.13
2.07
89.00Ёї
1.88
98.72Ёї
гыГЩФъзщБШНЯ* P<0.01ЃЌзщМфБШНЯ Ёї P<0.01Бэ3 6жЛЕЭМззДЯйЫиДѓЪѓКЭЖдеезщДѓЪѓаФМЁІТ-ARУмЖШЕФБШНЯ(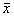 ЁРs) зщБ№
ЁРs) зщБ№
T4(nmol/L)
НзЖЮБШНЯ
tжЕ
, АйФДвНвЉ
ІТ -ARУмЖШ(fmol/mgЃЌЕААз)
НзЖЮБШНЯ
tжЕ
ЧзКЭад(nmol/L)
НзЖЮБШНЯ
tжЕ
ЩњКѓ1жм
ГЩФъ
ЩњКѓ1жм
ГЩФъ
ЩњКѓ1жм
ГЩФъ
ЕЭМззДЯйЫи
, АйФДвНвЉ
10.0ЁР 4.2
7.2ЁР 2.2
1.70
10.7ЁР0.6
20.4ЁР1.7
5.09*
0.50ЁР0.04
0.57ЁР0.05
0.86
Ждеезщ
34.4ЁР16.7
46.7ЁР13.6
, АйФДвНвЉ
3.10**
22.6ЁР2.4
32.0ЁР4.2
3.02**
0.43ЁР0.02
0.54ЁР0.04
1.27
зщМфБШНЯtжЕ
5.01*
6.45*
5.09*
, АйФДвНвЉ
3.00**
0.98
0.73
* P<0.01ЃЌ** P<0.05(СНзщЗНВюВЛЦыЃЌАДtЁфМьбщХаЖЯPжЕ)ЬжТл
ІТ-ARЖдаФдрЪеЫѕКЭЪцеХЙІФмОпгаживЊЕФЕїНкзїгУЃЌІТ-ARМЄЖЏМСКЭозПЙМСвбдкСйДВЙуЗКЪЙгУЁЃСйДВЙлВьБэУїЃЌгЄЖљгыФъГЄЖљаФдрЖдІТ-ARМЄЖЏМСЗДгІадгаУїЯдЕФВювь[2]ЁЃЮвУЧЖдWistarДѓЪѓЕФбаОПЗЂЯжЃЌЗЂг§Й§ГЬжааФМЁІТ-ARЪ§ФПГЪдіМгЧїЪЦЁЃетжжБфЛЏПЩФмЪЧгАЯьаФМЁЖдІТ-ARМЄЖЏМСЗДгІадЕФвЛИіЛЗНкЁЃЮЊНјвЛВНЬНЬжЗЂг§Й§ГЬжаІТ-ARЕФЙІФмЕїНкзїгУЃЌЮвУЧЖдІТ-ARЕїНкаФМЁACЕФзїгУНјааСЫбаОПЁЃдкЮоІТ-ARМЄЖЏМСДцдкЕФЧщПіЯТЃЌаФМЁACЕФЛљДЁЛюадКЭЖдЦфМЄЖЏМСForskolinЕФЗДгІадИїФъСфзщЮоУїЯдВювьЁЃЖдІТ-ARМЄЖЏМСвьБћЩіЩЯЯйЫиЗДгІадЃЌИїФъСфЖЮГіЯжУїЯдВювьЁЃЫЕУїЪмЬхЪ§ФПЕФБфЛЏгАЯьЖдаФМЁACЕФЕїНкЁЃ
, АйФДвНвЉ
НќФъШЫУЧдкбаОПжаШЯЪЖЕНВИШщЖЏЮяаФМЁЯИАћВЛНіДцдкІТ1-ARбЧаЭЃЌЭЌЪБЛЙДцдкІТ2-ARбЧаЭЁЃзїЮЊВЛЭЌЛљвђЕФБэДяВњЮяЃЌетСНжжЪмЬхбЧаЭЖдаФМЁЕФЕїНкзїгУФПЧАжЄЪЕгаУїЯдЕФВювь[6]ЁЃKuznetsovЕШ[5]ЖдаТЩњКЭГЩФъДѓЪѓаФМЁЯИАћІТ-ARЕФЕїНкЙІФмНјааСЫбаОПЃЌЗЂЯждкІТ2-ARМЄЖЏМСЕФзїгУЯТЃЌаТЩњДѓЪѓаФМЁЯИАћЕФЪеЫѕЗљЖШКЭACЗДгІадОљУїЯдИпгкГЩФъДѓЪѓЃЌШєгУІТ2-ARозПЙМСзшЖЯаФМЁЯИАћІТ2-ARЃЌдђІТ2-ARМЄЖЏМСЖдаФМЁЯИАћЕФМЄЖЏаЇгІЪмЕНвжжЦЃЌетдкаТЩњДѓЪѓгШЮЊУїЯдЁЃЮвУЧдкбаОПжаЗЂЯжІТ1/ІТ2-ARБШжЕЫцФъСфЖјдіМгЃЌДгГіЩњЪБЕФ51/49ж№НЅдіМгжС60/40ЃЌЗДгГСЫІТ1-ARЕФдіМгЧїЪЦЁЃЮЊСЫНтетжжБфЛЏЪЧЗёЛсЖдаФМЁACЕФЕїНкВњЩњгАЯьЃЌЮвУЧгІгУІТ-ARбЧаЭозПЙМСзшЖЯДѓЪѓаФМЁІТ1-ARКЭІТ2-ARЃЌЙлВьвьБћЩіЩЯЯйЫиЕФМЄЖЏаЇгІЁЃНсЙћБэУїЃЌзшЖЯІТ1-ARЪБЃЌГЩФъДѓЪѓаФМЁACЗДгІадЯТНЕБШЗЂг§дчЦкДѓЪѓУїЯдЃЛзшЖЯаФМЁІТ2-ARЪБЃЌГіЩњЪБКЭЩњКѓ1жмДѓЪѓаФМЁЕФACЗДгІадНЕЕЭБШГЩФъДѓЪѓУїЯдЁЃетжжІТ-ARбЧаЭЖдаФМЁACЕїНкзїгУЕФБфЛЏгыІТ-ARбЧаЭБШР§БфЛЏЪЧвЛжТЕФЁЃгабаОПБэУїЃЌаФМЁОжВПЩёОЕнжЪШЅМзЩіЩЯЯйЫижївЊЕїНкІТ1-ARЃЌбЊЩіЩЯЯйЫижївЊЕїНкІТ2-AR[7]ЁЃаФМЁзщжЏНЛИаЩёОЕФЭъШЋНЈСЂвЛАудкЩњКѓ2ЁЋ3жм[8]ЁЃетЬсЪОДгХпЬЅЁЂГіЩњжСГЩФъЃЌІТ-ARЖдаФМЁЕФЕїНкПЩФмОРњСЫвЛИіДгЩіЩЯЯйЕїНкЕННЛИаЩёОЕїНкЕФзЊЛЛЙ§ГЬЁЃ
, АйФДвНвЉ
T4ЪЧЛњЬхживЊЕФЩњГЄЗЂг§МЄЫиЁЃЦфЖдІТ-ARЕФЕїНкзїгУвбдчгабаОПЃЌЕЋДгЗЂг§ЕФНЧЖШбаОПT4ЖдаФМЁІТ-ARЕФгАЯьвдМАT4ЖдЗЂг§дчЦкКЭГЩФъаФМЁІТ-ARЕФЕїНкЃЌФПЧАбаОПЩаЩйЁЃЮвУЧгУБћЛљСђбѕрзрЄЗжБ№Жд1жмСфКЭГЩФъДѓЪѓНјааДІРэЃЌНсЙћЯдЪО1жмСфКЭГЩФъДѓЪѓбЊЧхT4ЫЎЦНЖМГіЯжУїЯдЕФЯТНЕЃЌаФМЁІТ-ARУмЖШврГіЯжЯТНЕЁЃT4ЖдЗЂг§аФМЁІТ-ARЕФгАЯьЃЌФПЧАЩаЮоЮФЯзБЈЕРЁЃЮвУЧШЯЮЊГ§СЫT4ЖдЕААзжЪКЯГЩКЭЛљвђЕФБэДягАЯьЭтЃЌгыВЛЭЌБэаЭЕФаФМЁЯИАћЖдT4ЕФЗДгІадКЭT4ЖдаФМЁІТ-ARЕїНкЕФВЛвЛжТадЁЂвдМАЬхФкЦфЫќМЄЫигыT4ЙВЭЌВЮгыЖдаФМЁІТ-ARЕФЕїНкгаЙи[9ЃЌ10]ЁЃ
ВЮПМЮФЯз
1 дјКЭЦНЃЌРюЭђеђЃЌЖХОќБЃ. аЁЖљаФбЊЙмМВВЁІТ-ЩіЩЯЯйЫиЪмЬхЕФбаОПЯжзД. жаЛЊЖљПЦдгжО, 1997ЃЌ35:611-613.
, АйФДвНвЉ
2 Friedman WF, George BL. New concept and drugs in the treatment of congestive heart failure. Pediatr Clin N Am, 1984, 31:1197-1206.
3 Tobise K, Ishikawa Y, Halmer SR, et al. Changes in types VI adenylyl cyclase isoform expresion correlation with a decrease capacity for cAMP generation in the aging ventricle. Cir Res, 1994, 74:596-603.
4 Lowry OH, Rosebrough NJ, Farr AL, et al. Protein measurement with the Folin-Phenol reagent. J Biol Chem, 1951, 193:256-275.
, АйФДвНвЉ
5 Kuznetsov V, Park E, Robinson RB, et al. Beta2-adrenergic receptor action in neonatal and adult rat ventricular myocytes. Cir Res, 1995, 76:40-52.
6 Xiao RP, Holl C, Altschuld R, et al. Beta2-adrenergic receptor-stimulated increase in cAMP in rat heart cells is not coupled to changes in Ca2+ dynamics, contractility,or phosphalamban phosphorylation. J Biol Chem, 1994, 269:19151-19156.
7 Tumer N, Houck WT, Boehm C, et al. Cardiac beta-adrenoceptor binding characteristics with age following adrenaodemodullation. Br J Pharmacol, 1990, 99:87-89.
, АйФДвНвЉ
8 Vornanen M. Postnatal development of beta-adrenergic response in ventricular muscle of the rat heart. Can J Physiol Pharmacol, 1988, 66:197-201.
9 Tejani-Butt SM, Yang J. A time course of altered thyroid states on the noradrenergic system in rat brain by quantitative autoradiagraphy. Neuroendocrinology, 1994, 59:235-244.
10 Bahouth SW. Thyroid hormones transcriptonally regulate the beta1-adrenergic receptor gene in cultured ventricular myocytes. J Biol Chem, 1991, 266: 15863-15869.
(ЪеИхЃК1998-01-22 аоЛиЃК1998-07-21), АйФДвНвЉ
ЕЅЮЛЃК100034 ББОЉвНПЦДѓбЇЕквЛвНдКЖљПЦ
ЙиМќДЪЃКЪмЬхЃЛЩіЩЯЯйЫиФмІТЃЛаФМЁЃЛДѓЪѓЃЛWistar
жаЛЊЖљПЦдгжО981111 ЁОеЊвЊЁП ФПЕФ ЬНЬжЗЂг§вђЫиЖдДѓЪѓаФМЁІТ-ЩіЩЯЯйЫиЪмЬх(ІТ-AR)ЕФгАЯьЁЃЗНЗЈ гІгУХфЛљНсКЯЁЂУИЛюадВтЖЈЃЌВтЖЈВЛЭЌФъСфЖЮWistarДѓЪѓаФМЁІТ-ARУмЖШЁЂЪмЬхбЧаЭЁЂЯймеЫсЛЗЛЏУИ(AC)ЛюадКЭЖдІТ-ARМЄЖЏМСЁЊЁЊвьБћЩіЩЯЯйЫиЗДгІадвдМАЕЭМззДЯйЫиДѓЪѓаФМЁІТ-ARУмЖШЁЃНсЙћ ДѓЪѓГіЩњЪБаФМЁІТ-ARУмЖШЦНОљЮЊ14.3 fmol/mg (ЕААз)ЃЌГЩФъКѓЦНОљЮЊ31.6 fmol/mg (ЕААз)ЃЌаФМЁІТ-ARУмЖШЫцФъСфЕФдіГЄЖјдіМг(FжЕЮЊ23.46, P<0.01)ЃЛІТ1/ІТ2-ARбЧаЭЯрЖдБШжЕЃЌГіЩњЪБЮЊ51/49ЃЌГЩФъЮЊ60/40ЃЛаФМЁACЖдІТ-ARМЄЖЏМСЁЊЁЊвьБћЩіЩЯЯйЫиЕФЗДгІадЃЌГіЩњЪБЮЊ76 pmol*mg-1*min-1ЃЌГЩФъЮЊ126 pmol*mg-1*min-1 ЃЌИїФъСфЖЮЕФВювьгаЯджјвтвх(FжЕЮЊ89.00, P<0.01)ЃЛACЛљДЁЛюадКЭACЖдACМЄЖЏМСForskolinЕФЗДгІадЃЌИїФъСфЖЮУЛгаВювьЃЛІТ1-ARозПЙМСвжжЦГЩФъДѓЪѓаФМЁACЖдвьБћЩіЩЯЯйЫиЕФЗДгІадЃЌІТ2-ARозПЙМСвжжЦаТЩњКЭЗЂг§дчЦкДѓЪѓаФМЁACЖдвьБћЩіЩЯЯйЫиЕФЗДгІадЃЛбЊЧхМззДЯйЫиМѕЕЭПЩЪЙЩњКѓ1жмКЭГЩФъДѓЪѓаФМЁІТ-ARУмЖШЯТНЕЁЃНсТл ДѓЪѓаФМЁІТ-ARУмЖШЁЂІТ1/ІТ2-ARбЧаЭБШР§ЁЂІТ-ARЖдACЕФЕїНкзїгУЪмЗЂг§вђЫиЕФгАЯьЁЃ
, АйФДвНвЉ
A developmental study on myocardial ІТ -adrenergic receptor in rats Zeng Heping, Li Wanzhen. Department of Pediatrics, The First Hospital, Beijing Medical University, Beijing 100034
ЁОAbstractЁП Objective To study the effect of developmental factors on ІТ-adrenergic receptor (AR) and its regulatory role in Wistar rat myocardium. Methods With the methods of ligand-binding and enzyme activity measurement, ІТ-AR density, receptor subtypes, myocardial adenylate cyclase (AC) activity, its age-related responsiveness to ІТ-AR agonist isoprenalin, and myocardial ІТ-AR density were measured in rats at different age stages. Also, myocardial ІТ-AR density was detected in hypothyroxin rats. Results Myocardial ІТ-AR density of rats was 14.3fmol/mg protein at birth, and 31.6 fmol/mg protein in adult. It increased with age (F=23.46, P<0.01). Relative ratio of ІТ1/ІТ2-AR was 51/49 at birth, and 60/40 in adult. The responsiveness of myocardial AC to ІТ-AR agonist isoprenalin was 76 pmol*mg-1*min-1 at birth and 126 pmol*mg-1*min-1 in adult (F=89.00, P<0.01). There was no difference in basic AC activity and responsiveness to AC agonist forskolin between rats at birth and in adult. Beta 1-antagonist inhibited the responsiveness of AC to isoprenalin in adult rats, while ІТ2-AR antagonist inhibited the responsiveness of AC to isoprenalin in newborn and young rats. Serum hypothyroxin decreased myocardial ІТ-AR densities in the newborn and adult rats. Conclusion Beta-AR density, relative ratio of its subtypes and ІТ-AR regulatory effect on myocardial AC were all influenced by developmental factors.
, АйФДвНвЉ
ЁОKey wordsЁП Receptor adrenergic,beta Myocardium Rats,Wistar
аФдрІТ-ЩіЩЯЯйЫиЪмЬх(adrenergic receptor, AR)НщЕМЯИАћФкЭтаХЯЂДЋЕМЃЌВЮгыЕїНкаФМЁЪеЫѕКЭЪцеХЙІФмЃЌВЂгыаэЖраЁЖљаФдрМВВЁгаУмЧаЙиЯЕ[1]ЁЃСйДВЙлВьБэУїЃЌгЄЖљгыФъГЄЖљЖдІТ-ARМЄЖЏМСЗДгІадВЛЭЌ[2]ЁЃЮЊбаОПЗЂг§Й§ГЬаФМЁІТ-ARЕФБфЛЏЧщПіЃЌЮвУЧЖдГіЩњЪБжСГЩФъВЛЭЌФъСфЖЮWistarДѓЪѓаФМЁІТ-ARУмЖШНјааМьВтЃЌВЂЬНЬжаФМЁІТ-ARЖдЯймеЫсЛЗЛЏУИ(adenylate cyclase, AC)ЕФЕїНкзїгУвдМАМззДЯйЫиЖдІТ-ARЕФгАЯьНјаабаОПЃЌЬНЬжЗЂг§вђЫиЖдаФМЁІТ-ARЕФгАЯьЁЃ
ВФСЯМАЗНЗЈ
вЛЁЂЖЏЮя
бЁдёГіЩњЪБМАГіЩњ1ЁЂ2ЁЂ3ЁЂ4жмКЭГЩФъ6ИіФъСфЖЮЕФWistarДѓЪѓЁЃЕЭМззДЯйЫиЖЏЮяФЃаЭбЁдёГіЩњ1жмКЭГЩФъЕФДѓЪѓЁЃ
, http://www.100md.com
ЖўЁЂЪЕбщЗНЗЈ
1.аФМЁЯИАћФЄжЦБИ[3]ЃКбЁдёВЛЭЌФъСфЖЮWistarДѓЪѓЃЌЖЯЭЗЃЌШЁаФдрЃЌЩњРэбЮЫЎГхЯДЃЌПьЫйдШНЌЃЌ4ВуЩДВМЙ§ТЫЁЃ5 000ЁСg(gЮЊжиСІГЃЪ§)РыаФЃЌ4ЁцЃЌ20Зжжг,зЊвЦЩЯЧх,20 000ЁСgРыаФ,4Ёц,20 Зжжг,ЦњЩЯЧхЁЃГСЕэГхЯД2БщЃЌЯИАћФЄжќДцвКаќИЁГСЕэЃЌгУгкХфЛљВтЖЈЛђ-80ЁцБЃДцЁЃ
2.ХфЛљВтЖЈ[3]ЃКНЋаФМЁЯИАћФЄаќвКжЦГЩ1.0 mg/mlЕФХЈЖШЁЃбЁгУ5жжВЛЭЌХЈЖШ[3H]-ЫЋЧтаФЕУЪц([3H]-DHAЃЌІТ-ARХфЛљ)МД0.6ЁЋ10.0 nmol/LЃЌЗДгІЛКГхвК100 ІЬlЃЌаФМЁЯИАћФЄаќвК50 ІЬlЃЌЗДгІзмЬхЛ§ЮЊ200 ІЬlЁЃ37ЁцЫЎдЁ20 ЗжжгЃЌжежЙЗДгІЃЌОWhatman GF/CВЃСЇЯЫЮЌФЄГщТЫЃЌТЫФЄГхЯД2ДЮЃЌздШЛСРИЩЃЌВтЖЈТЫФЄЩЯЕФЗХЩфЛюадЁЃЗЧЬивьадНсКЯЪЕбщВЩгУ10 ІЬmol/LХЈЖШЕФІТ-ARозПЙМСЁЊЁЊЦеФЮТхЖћДцдкЪБ[3H]-DNAНсКЯСПБэЪОЁЃРћгУЗХЩфХфЛљНсКЯЗжЮіЗЈ(scatchard analysis)ЗжЮіаФМЁЪмЬхУмЖШКЭЧзКЭадЁЃВтЖЈІТ-ARбЧаЭЪБНЋ50 ІЬlЯИАћФЄаќвКгывЛжжХЈЖШЕФ[3H]-DNAКЭ16жжВЛЭЌХЈЖШЕФІТ1-ARозПЙМС(CGP20172A 10-10ЁЋ10-5mol/L)дк37ЁцЫЎдЁ10ЗжжгЃЌШЛКѓГщТЫЃЌНјааЗХЩфМЦЪ§ЃЌЕУГіОКељвжжЦЧњЯпЁЃЖдЧњЯпНјааМЦЫуЛњФтКЯЃЌвдЧѓЕУЪмЬхбЧаЭБШР§ЁЃЕААзЖЈСПгУLowryЗЈ[4]ЁЃ
, АйФДвНвЉ
3.УИЛюадВтЖЈ[5]ЃКЗДгІЬхЯЕжаКЌга25 mmol/LбЮЫсШ§єЧМзЛљАБЛљМзЭщЃЌ2 mmol/LТШЛЏУОЃЌ20 mmol/LМЁЫсСзЫсЃЌ20 U/mlМЁЫсМЄУИЃЌ1 mmol/LЕФІС-[32P]Ш§СзЫсЯйме(40 cpm/pmol),МгШы80ЁЋ100 ІЬgЕФаФМЁЯИАћФЄЃЌзмЬхЛ§ЮЊ100 ІЬlЃЌ30ЁцЫЎдЁ20ЗжжгЃЌМгШыжежЙЗДгІвК100 ІЬlЁЃЗДгІЮяО1 500ЁСgРыаФ5ЗжжгЃЌЩЯЧхЫГађЭЈЙ§РызгНЛЛЛЪїжЌКЭбѕЛЏТСВуЮіжљЃЌЪеМЏЗжРывКЁЃЗжБ№ВтЖЈ[32P]КЭ[3H]ЕФЗХЩфЛюадЁЃ[3H]ЛЗСзЫсЯйме([3H]-cAMP)ЕФЛиЪеТЪдМЮЊ70%ЁЋ80%ЁЃЩЯЪіЗДгІЬхЯЕжаЗжБ№МгШы10-6 mol/LЕФForskolin(вЛжжACМЄЖЏМС)ЃЌ10-7mol/LвьБћЩіЩЯЯйЫиЃЌ10-7 mol/LЕФІТ1-ARозПЙМС(CGP20712A)КЭ10-7 mol/L ІТ2-ARозПЙМС(ICI118551)ЃЌ30ЁцЫЎдЁ20ЗжжгЁЃжежЙЗДгІЃЌВтЖЈ[32P]КЭ[3H]ЕФЗХЩфЛюадЁЃ
, АйФДвНвЉ
4.ЕЭМззДЯйЫи(T4)ЖЏЮяФЃаЭжЦБИКЭбЊЧхT4ВтЖЈЃКбЁдёГіЩњКѓ1жмКЭГЩФъДѓЪѓЁЃИЙЧЛзЂЩфБћЛљСђбѕрзрЄЃЌ20 mg/kgЃЌУПЬь1ДЮЃЌСЌајИјвЉ7ЬьЁЃЖдеезщИЙЧЛзЂЩфЭЌбљМССПЕФЩњРэбЮЫЎЁЃгУЪдМСКажНЦЌНгШЁ1ЕЮДѓгк0.5 cmжБОЖДѓаЁЕФбЊбљЃЌздШЛСРИЩЁЃгУДђПзЛњМєЯТ0.5 cmжБОЖбЊбљжНЦЌКЭЫцЪдМСКаАќзАЕФБъзМжНЦЌЃЌЗХШыЪдЙмжаЁЃИїЙмМгШы200 ІЬlЕФT4ПЙЬхЃЌЗДИДеёвЁ5ЗжжгЃЌЗХШы4ЁцБљЯфжаЙ§вЙЃЌШЛКѓМгШы125I-T4100 ІЬlЁЃЪвЮТЯТЗХжУ1аЁЪБЃЌдкІУЩСЫИвЧЩЯНјааІУМЦЪ§ЁЃаФМЁІТ-ARВтЖЈЭЌЧАЁЃ
Ш§ЁЂЪ§ОнДІРэМАЭГМЦМьбщ
УПзщЪ§ОнвдОљЪ§КЭБъзМВю(
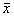 ЁРs)БэЪОЁЃЖрзщБШНЯВЩгУЗНВюЗжЮіМАNewman-KeulsМьбщЃЌСНзщБШНЯВЩгУtМьбщЛђtЁфМьбщЁЃ
ЁРs)БэЪОЁЃЖрзщБШНЯВЩгУЗНВюЗжЮіМАNewman-KeulsМьбщЃЌСНзщБШНЯВЩгУtМьбщЛђtЁфМьбщЁЃ, http://www.100md.com
НсЙћ
вЛЁЂЗЂг§Й§ГЬжаДѓЪѓаФМЁІТ -ARУмЖШКЭЧзКЭадЕФБШНЯКЭЪмЬхбЧаЭЫљеМБШР§
ДгБэ1жаПЩПДГіЃЌаФМЁІТ-ARУмЖШГіЩњЪБНЯЕЭЃЌЫцЗЂг§ЖјдіМгЃЌжСЩњКѓ4жмГЪЯждіМгЧїЪЦЃЌГЩФъКѓТдгаЯТНЕ(FжЕ23.46, P<0.01)ЁЃГіЩњЪБЁЂЩњКѓ1жмЁЂ2жмДѓЪѓаФМЁІТ-ARУмЖШгыГЩФъДѓЪѓБШНЯВювьгаЯджјвтвхЁЃЖјЧзКЭадЮоЯджјадВювь(FжЕ1.31, P>0.05)ЁЃаФМЁІТ1-ARдкзмІТ-ARжаЫљеМЕФБШР§дкЗЂг§Й§ГЬжаГЪдіМгЧїЪЦЁЃ
Бэ1 6жЛДѓЪѓЗЂг§НзЖЮаФМЁІТ-AR
ЗХЩфХфЛљВтЖЈНсЙћ(
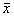 ЁРs) ЗЂг§НзЖЮ
ЁРs) ЗЂг§НзЖЮІТ-ARУмЖШ
, http://www.100md.com
(fmol/mgЃЌЕААз)
ЧзКЭад
(nmol/L)
ЪмЬхбЧаЭеМІТ-AR
АйЗжБШ(%)
ІТ1
ІТ2
ГіЩњЪБ
14.3ЁР2.1*
0.45ЁР0.12
51
49
, http://www.100md.com
ГіЩњКѓ
1жм
20.1ЁР4.2*
0.57ЁР0.14
55
45
2жм
23.3ЁР1.5*
0.43ЁР0.02
55
45
3жм
, http://www.100md.com
29.3ЁР6.3
0.54ЁР0.10
58
42
4жм
39.0ЁР2.4
0.55ЁР0.12
60
40
ГЩФъ
31.6ЁР3.3
0.58ЁР0.02
60
, АйФДвНвЉ
40
зщМфБШНЯFжЕ
23.46Ёї
2.24
гыГЩФъБШНЯ * P<0.01ЃЌЁї P<0.01
ЖўЁЂЗЂг§Й§ГЬжааФМЁІТ-ARЖдACЕФЕїНкзїгУ
ДѓЪѓаФМЁACЛљДЁЛюадМАЖдACМЄЖЏМСForskolinЕФЗДгІадЃЌГіЩњжСГЩФъИїФъСфЖЮОљЮоУїЯдЕФВювьЁЃаФМЁACЖдІТ-ARМЄЖЏМСвьБћЩіЩЯЯйЫиЗДгІадЃЌГіЩњЪБКЭГіЩњ1жмНЯЕЭЃЌЫцзХЗЂг§ЃЌЗДгІадж№НЅдіМг(FжЕ89.00, P<0.01)ЃЛгУІТ1-ARозПЙМСзшЖЯаФМЁІТ1-ARЪБЃЌГЩФъДѓЪѓаФМЁACЖдвьБћЩіЩЯЯйЫиЗДгІадЪмЕНУїЯдЕФвжжЦЁЃДгБэ2ПЩПДГіЃЌвьБћЩіЩЯЯйЫиМЄЖЏГЩФъКЭаТЩњДѓЪѓаФМЁЃЌcAMPЩњГЩСПЗжБ№ЮЊ126ЁР9 pmol*mg-1*min-1КЭ76ЁР3.6 pmol*mg-1*min-1ЁЃЖјМггУІТ-ARозПЙМС(CGP)КѓЃЌГЩФъДѓЪѓаФМЁcAMPЩњГЩСПМѕЩй(73ЁР6 pmol*mg-1*min-1)ЃЌгыаТЩњДѓЪѓаФМЁcAMPЕФЩњГЩСПНќКѕЯрЕШ(68ЁР7 pmol*mg-1*min-1)ЃЛгУІТ2-ARозПЙМСзшЖЯаФМЁІТ2-ARЪБЃЌ2жмФкДѓЪѓаФМЁACЕФЗДгІадЪмЕНвжжЦНЯУїЯд(Бэ2)ЁЃ
, http://www.100md.com
Ш§ЁЂбЊЧхЕЭT4ЖдДѓЪѓаФМЁІТ-ARЕФгАЯь
ДѓЪѓМззДЯйВњЩњT4БЛБћЛљСђбѕрзрЄвжжЦЃЌT4ЫЎЦНЯТНЕгАЯь1жмСфКЭГЩФъДѓЪѓаФМЁІТ-ARЕФУмЖШЃЌЪЙЦфНЕЕЭЁЃЕЭT4ЖдаФМЁІТ-ARЕФЧзКЭадУЛгаУїЯдЕФгАЯь(Бэ3)ЁЃ
Бэ2 6жЛДѓЪѓВЛЭЌЗЂг§НзЖЮаФМЁACЛюадМАІТ-ARЖдACЕФЕїНкЧщПі(
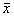 ЁРsЃЌcAMP pmol*mg-1*min-1) ЗЂг§НзЖЮ
ЁРsЃЌcAMP pmol*mg-1*min-1) ЗЂг§НзЖЮЛљДЁЛюад
ЯймеЫсЛЗЛЏУИМЄЖЏМС
(ЁС10-6mol/L)
, АйФДвНвЉ
вьБћЩіЩЯЯйЫи
(ЁС10-7mol/L)
вьБћЩіЩЯЯйЫи+
ІТ1-ARозПЙМС
(ЁС10-7mol/L)
вьБћЩіЩЯЯйЫи+
ІТ2-ARозПЙМС
(ЁС10-7mol/L)
ГіЩњЪБ
20.4ЁР1.9
150ЁР5
, АйФДвНвЉ
75.8ЁР3.6
68ЁР7
38ЁР6*
ГіЩњКѓ
1жм
20.4ЁР1.7
151ЁР7
80.2ЁР2.5*
77ЁР5
42ЁР8*
2жм
20.4ЁР1.6
, АйФДвНвЉ
152ЁР5
103.7ЁР8.8*
75ЁР4
79ЁР7*
3жм
21.6ЁР2.8
151ЁР6
102.7ЁР5.8*
74ЁР3
99ЁР15*
4жм
, http://www.100md.com 22.0ЁР3.8
162ЁР12
142.0ЁР10.2
77ЁР9
137ЁР8*
ГЩФъ
19.6ЁР2.9
154ЁР9
125.6ЁР9.4
73ЁР6
116ЁР11
зщМфБШНЯFжЕ
, АйФДвНвЉ
2.13
2.07
89.00Ёї
1.88
98.72Ёї
гыГЩФъзщБШНЯ* P<0.01ЃЌзщМфБШНЯ Ёї P<0.01Бэ3 6жЛЕЭМззДЯйЫиДѓЪѓКЭЖдеезщДѓЪѓаФМЁІТ-ARУмЖШЕФБШНЯ(
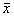 ЁРs) зщБ№
ЁРs) зщБ№T4(nmol/L)
НзЖЮБШНЯ
tжЕ
, АйФДвНвЉ
ІТ -ARУмЖШ(fmol/mgЃЌЕААз)
НзЖЮБШНЯ
tжЕ
ЧзКЭад(nmol/L)
НзЖЮБШНЯ
tжЕ
ЩњКѓ1жм
ГЩФъ
ЩњКѓ1жм
ГЩФъ
ЩњКѓ1жм
ГЩФъ
ЕЭМззДЯйЫи
, АйФДвНвЉ
10.0ЁР 4.2
7.2ЁР 2.2
1.70
10.7ЁР0.6
20.4ЁР1.7
5.09*
0.50ЁР0.04
0.57ЁР0.05
0.86
Ждеезщ
34.4ЁР16.7
46.7ЁР13.6
, АйФДвНвЉ
3.10**
22.6ЁР2.4
32.0ЁР4.2
3.02**
0.43ЁР0.02
0.54ЁР0.04
1.27
зщМфБШНЯtжЕ
5.01*
6.45*
5.09*
, АйФДвНвЉ
3.00**
0.98
0.73
* P<0.01ЃЌ** P<0.05(СНзщЗНВюВЛЦыЃЌАДtЁфМьбщХаЖЯPжЕ)ЬжТл
ІТ-ARЖдаФдрЪеЫѕКЭЪцеХЙІФмОпгаживЊЕФЕїНкзїгУЃЌІТ-ARМЄЖЏМСКЭозПЙМСвбдкСйДВЙуЗКЪЙгУЁЃСйДВЙлВьБэУїЃЌгЄЖљгыФъГЄЖљаФдрЖдІТ-ARМЄЖЏМСЗДгІадгаУїЯдЕФВювь[2]ЁЃЮвУЧЖдWistarДѓЪѓЕФбаОПЗЂЯжЃЌЗЂг§Й§ГЬжааФМЁІТ-ARЪ§ФПГЪдіМгЧїЪЦЁЃетжжБфЛЏПЩФмЪЧгАЯьаФМЁЖдІТ-ARМЄЖЏМСЗДгІадЕФвЛИіЛЗНкЁЃЮЊНјвЛВНЬНЬжЗЂг§Й§ГЬжаІТ-ARЕФЙІФмЕїНкзїгУЃЌЮвУЧЖдІТ-ARЕїНкаФМЁACЕФзїгУНјааСЫбаОПЁЃдкЮоІТ-ARМЄЖЏМСДцдкЕФЧщПіЯТЃЌаФМЁACЕФЛљДЁЛюадКЭЖдЦфМЄЖЏМСForskolinЕФЗДгІадИїФъСфзщЮоУїЯдВювьЁЃЖдІТ-ARМЄЖЏМСвьБћЩіЩЯЯйЫиЗДгІадЃЌИїФъСфЖЮГіЯжУїЯдВювьЁЃЫЕУїЪмЬхЪ§ФПЕФБфЛЏгАЯьЖдаФМЁACЕФЕїНкЁЃ
, АйФДвНвЉ
НќФъШЫУЧдкбаОПжаШЯЪЖЕНВИШщЖЏЮяаФМЁЯИАћВЛНіДцдкІТ1-ARбЧаЭЃЌЭЌЪБЛЙДцдкІТ2-ARбЧаЭЁЃзїЮЊВЛЭЌЛљвђЕФБэДяВњЮяЃЌетСНжжЪмЬхбЧаЭЖдаФМЁЕФЕїНкзїгУФПЧАжЄЪЕгаУїЯдЕФВювь[6]ЁЃKuznetsovЕШ[5]ЖдаТЩњКЭГЩФъДѓЪѓаФМЁЯИАћІТ-ARЕФЕїНкЙІФмНјааСЫбаОПЃЌЗЂЯждкІТ2-ARМЄЖЏМСЕФзїгУЯТЃЌаТЩњДѓЪѓаФМЁЯИАћЕФЪеЫѕЗљЖШКЭACЗДгІадОљУїЯдИпгкГЩФъДѓЪѓЃЌШєгУІТ2-ARозПЙМСзшЖЯаФМЁЯИАћІТ2-ARЃЌдђІТ2-ARМЄЖЏМСЖдаФМЁЯИАћЕФМЄЖЏаЇгІЪмЕНвжжЦЃЌетдкаТЩњДѓЪѓгШЮЊУїЯдЁЃЮвУЧдкбаОПжаЗЂЯжІТ1/ІТ2-ARБШжЕЫцФъСфЖјдіМгЃЌДгГіЩњЪБЕФ51/49ж№НЅдіМгжС60/40ЃЌЗДгГСЫІТ1-ARЕФдіМгЧїЪЦЁЃЮЊСЫНтетжжБфЛЏЪЧЗёЛсЖдаФМЁACЕФЕїНкВњЩњгАЯьЃЌЮвУЧгІгУІТ-ARбЧаЭозПЙМСзшЖЯДѓЪѓаФМЁІТ1-ARКЭІТ2-ARЃЌЙлВьвьБћЩіЩЯЯйЫиЕФМЄЖЏаЇгІЁЃНсЙћБэУїЃЌзшЖЯІТ1-ARЪБЃЌГЩФъДѓЪѓаФМЁACЗДгІадЯТНЕБШЗЂг§дчЦкДѓЪѓУїЯдЃЛзшЖЯаФМЁІТ2-ARЪБЃЌГіЩњЪБКЭЩњКѓ1жмДѓЪѓаФМЁЕФACЗДгІадНЕЕЭБШГЩФъДѓЪѓУїЯдЁЃетжжІТ-ARбЧаЭЖдаФМЁACЕїНкзїгУЕФБфЛЏгыІТ-ARбЧаЭБШР§БфЛЏЪЧвЛжТЕФЁЃгабаОПБэУїЃЌаФМЁОжВПЩёОЕнжЪШЅМзЩіЩЯЯйЫижївЊЕїНкІТ1-ARЃЌбЊЩіЩЯЯйЫижївЊЕїНкІТ2-AR[7]ЁЃаФМЁзщжЏНЛИаЩёОЕФЭъШЋНЈСЂвЛАудкЩњКѓ2ЁЋ3жм[8]ЁЃетЬсЪОДгХпЬЅЁЂГіЩњжСГЩФъЃЌІТ-ARЖдаФМЁЕФЕїНкПЩФмОРњСЫвЛИіДгЩіЩЯЯйЕїНкЕННЛИаЩёОЕїНкЕФзЊЛЛЙ§ГЬЁЃ
, АйФДвНвЉ
T4ЪЧЛњЬхживЊЕФЩњГЄЗЂг§МЄЫиЁЃЦфЖдІТ-ARЕФЕїНкзїгУвбдчгабаОПЃЌЕЋДгЗЂг§ЕФНЧЖШбаОПT4ЖдаФМЁІТ-ARЕФгАЯьвдМАT4ЖдЗЂг§дчЦкКЭГЩФъаФМЁІТ-ARЕФЕїНкЃЌФПЧАбаОПЩаЩйЁЃЮвУЧгУБћЛљСђбѕрзрЄЗжБ№Жд1жмСфКЭГЩФъДѓЪѓНјааДІРэЃЌНсЙћЯдЪО1жмСфКЭГЩФъДѓЪѓбЊЧхT4ЫЎЦНЖМГіЯжУїЯдЕФЯТНЕЃЌаФМЁІТ-ARУмЖШврГіЯжЯТНЕЁЃT4ЖдЗЂг§аФМЁІТ-ARЕФгАЯьЃЌФПЧАЩаЮоЮФЯзБЈЕРЁЃЮвУЧШЯЮЊГ§СЫT4ЖдЕААзжЪКЯГЩКЭЛљвђЕФБэДягАЯьЭтЃЌгыВЛЭЌБэаЭЕФаФМЁЯИАћЖдT4ЕФЗДгІадКЭT4ЖдаФМЁІТ-ARЕїНкЕФВЛвЛжТадЁЂвдМАЬхФкЦфЫќМЄЫигыT4ЙВЭЌВЮгыЖдаФМЁІТ-ARЕФЕїНкгаЙи[9ЃЌ10]ЁЃ
ВЮПМЮФЯз
1 дјКЭЦНЃЌРюЭђеђЃЌЖХОќБЃ. аЁЖљаФбЊЙмМВВЁІТ-ЩіЩЯЯйЫиЪмЬхЕФбаОПЯжзД. жаЛЊЖљПЦдгжО, 1997ЃЌ35:611-613.
, АйФДвНвЉ
2 Friedman WF, George BL. New concept and drugs in the treatment of congestive heart failure. Pediatr Clin N Am, 1984, 31:1197-1206.
3 Tobise K, Ishikawa Y, Halmer SR, et al. Changes in types VI adenylyl cyclase isoform expresion correlation with a decrease capacity for cAMP generation in the aging ventricle. Cir Res, 1994, 74:596-603.
4 Lowry OH, Rosebrough NJ, Farr AL, et al. Protein measurement with the Folin-Phenol reagent. J Biol Chem, 1951, 193:256-275.
, АйФДвНвЉ
5 Kuznetsov V, Park E, Robinson RB, et al. Beta2-adrenergic receptor action in neonatal and adult rat ventricular myocytes. Cir Res, 1995, 76:40-52.
6 Xiao RP, Holl C, Altschuld R, et al. Beta2-adrenergic receptor-stimulated increase in cAMP in rat heart cells is not coupled to changes in Ca2+ dynamics, contractility,or phosphalamban phosphorylation. J Biol Chem, 1994, 269:19151-19156.
7 Tumer N, Houck WT, Boehm C, et al. Cardiac beta-adrenoceptor binding characteristics with age following adrenaodemodullation. Br J Pharmacol, 1990, 99:87-89.
, АйФДвНвЉ
8 Vornanen M. Postnatal development of beta-adrenergic response in ventricular muscle of the rat heart. Can J Physiol Pharmacol, 1988, 66:197-201.
9 Tejani-Butt SM, Yang J. A time course of altered thyroid states on the noradrenergic system in rat brain by quantitative autoradiagraphy. Neuroendocrinology, 1994, 59:235-244.
10 Bahouth SW. Thyroid hormones transcriptonally regulate the beta1-adrenergic receptor gene in cultured ventricular myocytes. J Biol Chem, 1991, 266: 15863-15869.
(ЪеИхЃК1998-01-22 аоЛиЃК1998-07-21), АйФДвНвЉ