Φ±–‘ΗΈΙΠΡήΥΞΫΏ ±≥Π’≥ΡΛΤΝ’œΥπ…ΥΒΡ―–ΨΩ
Ής’ΏΘΚΕΈΟάάω Άθ―εΨϋ ΚΪΒ¬Έε
ΒΞΈΜΘΚΕΈΟάάω Άθ―εΨϋ :…ΫΈς“ΫΩΤ¥σ―ßΒΎ“Μ“Ϋ‘Κ(ΧΪ‘≠ 030001)ΘΜΚΪΒ¬ΈεΘΚ…ΫΈς“ΫΩΤ¥σ―ß≤Γάμ…ζάμΫΧ―– “
ΙΊΦϋ¥ ΘΚΗΈΘΜΡΎΕΨΥΊάύΘΜ≥Π’≥ΡΛΘΜ¥σΜΤ
Φ±–‘ΗΈΙΠΡήΥΞΫΏ ±≥Π’≥ΡΛΤΝ’œΥπ…ΥΒΡ―–ΨΩ ’Σ“Σ ΡΩΒΡΘΚΧΫΧ÷Φ±–‘ΗΈΙΠΡήΥΞΫΏ(Φρ≥ΤΗΈΥΞ) ±≥Π’≥ΡΛΤΝ’œΥπ…ΥΦΑΤδΜζ÷ΤΘ§≤ΔΙέ≤λ÷–“©¥σΜΤΕ‘ΥϋΒΡΖά÷ΈΉς”ΟΓΘΖΫΖ®ΘΚ≤…”ΟωΉ ‘ΦΝΖ®Ής―ΣΫ§ΡΎΕΨΥΊΕ®ΝΩΘ§Ζ”“Μ¥Έ¬»ΥαΖ®≤βΕ®Ι»Α±θΘΑΖ≈®Ε»ΦΑ”ΪΙβΖ®≤βΕ®Ι»Α±θΘΑΖΟΗΜν–‘ΚΆΉιΑΖΚ§ΝΩΘ§EvansάΕ»Ψ…ΪΖ®≤βΕ®≥Π’≥ΡΛΆ®ΆΗ–‘ΓΘΫαΙϊΘΚΝρ¥ζ““θΘΑΖ(thioacetamide,TAA)“ΐΖΔ¥σ σΦ±–‘ΗΈΥΞΘ§≤ΔΑι”–―œ÷ΊΒΡ≥Π‘¥–‘ΡΎΕΨΥΊ―Σ÷Δ(intestinal endotoxemia,IETM)ΓΘ≥ΠΙ»Α±θΘΑΖΟΗΜν–‘ΫΒΒΆΘ§≥Π’≥ΡΛΕ‘Ι»Α±θΘΑΖάϊ”ΟΦθ…ΌΘ§≥Π’≥ΡΛΆ®ΆΗ–‘‘ωΦ”ΓΘΉι÷·œΗΑϊ―ßœ‘ ΨΘ§TAAΉιΕ·ΈοΗΈœΗΑϊΖΔ…ζ―œ÷Ί±δ–‘ΜΒΥάΘΜ≥Π’≥ΡΛ”Ό―ΣΓΔΥ°÷ΉΓΔΟ”άΟΘ§≥ΠΖ ¥σœΗΑϊΆ―Ω≈ΝΘΓΘΒγΨΒ Ψ≥ΠΈΔ»όΟΪΒΙΖϋΓΔΆ―¬δΘ§œΗΑϊΦδΫτΟήΝ§Ϋ”ΤΤΜΒΓΘ¥σΜΤΉιΕ·ΈοIETM”κΗΈΉι÷·Υπ…ΥΟςœ‘Φθ«αΓΘΫα¬έΘΚΦ±–‘ΗΈΥΞΑι”–≥Π’≥ΡΛΤΝ’œΥπ…ΥΘ§ΤδΖΔ…ζΜζ÷Τ”κIETMΦΑΤδΫιΒΦΒΡΉιΑΖ‘ωΕύ”–ΙΊΓΘ¥σΜΤΕ‘Φ±–‘ΗΈΥΞ ±≥Π’≥ΡΛΤΝ’œΥπ…Υ”–“ΜΕ®Ζά÷ΈΉς”ΟΓΘ
, http://www.100md.com
Studies on intestinal mucosa barrier injuries in acute hepatic failure
DUAN Mei-Li,WANG Yan-Jun,HAN De-Wu
Shan-Xi Medical University,Taiyuan(030001)
Abstract AIMΘΚTo elucidate the mechanism of intestinal mucosa injuries,as well as the preventive and cure effect of Chinese Medicine Rheum,in acute hepatic failure (AHF) induced by thioacetamide(TAA).METHODSΘΚEndotoxin content by the Limulus test;glutamine content by phenol-hypochlorite method;glutaminase activity and histamine content by fluorescence method;intestinal mucosal permeability by Evans blue method.RESULTSΘΚAHF induced by TAA resulted in intestinal endotoxemia (IETM),reduce of glutaminase activity and glutamine utilization,increase of intestinal mucosal permeability.Histological observation showed that degeneration,necrosis of liver cells,edema,extravasated blood,erosion and degranulation of the mast cells in intestine mucosa.Electron microscope displayed intestinal microvilli fell off,the tight junction damaged.In Rheum-treated group,the last changes alleviated.CONCLUSIONΘΚIntestinal mucosa injuries were important complication in AHF,its mechanism was related to IETM and hyperhistaminemia.Rheum was effective for the prevention and therapy of intestinal mucosa injuries in AHF.
, ΑΌΡ¥“Ϋ“©
MeSH Liver;Endotoxins;Intestinal mucosa;Rhubarb
ΫϋΡξά¥Θ§Ε‘”ΎΦ±–‘ΗΈΥΞ ±IETM≤ζ…ζΜζ÷ΤΒΡ―–ΨΩΕύ≤ύ÷Ί”Ύ―–ΨΩΩίΖώœΗΑϊΙΠΡή’œΑ≠[1]ΘΜΕ‘≥Π’≥ΡΛΤΝ’œΙΠΡήΥΞΫΏ‘ΎIETMΖΔ…ζ÷–ΒΡΉς”ΟΕύœό”Ύ…’…ΥΓΔ ß―Σ–‘–ίΩΥΒ»«ιΩω[2]ΓΘΈΣ¥ΥΘ§±ΨΈΡΆ®ΙΐΕ·Έο Β―ιΧΫΧ÷Φ±–‘ΗΈΥΞ ±≥Π’≥ΡΛΤΝ’œ±δΜ·ΦΑΤδΜζ÷ΤΘ§Ά§ ±Ιέ≤λ¥σΜΤ(Rheum)ΒΡΖά÷ΈΉς”ΟΓΘ
≤ΡΝœ”κΖΫΖ®
(“Μ)Ε·ΈοΡΘ–ΆΘΚ»ΓWistar¥σ σ30÷ΜΘ§Χε÷Ί200ΓΪ240 g,¥Τ–έΗςΑκΘ§ΥφΜζΖ÷≥…3ΉιΘΚΕ‘’’ΉιΓΔTAAΉιΓΔRheum+TAAΉιΓΘ Β―ιΒΎ“Μ»’ΤπΘ§ΒΎ3ΉιΕ·ΈοΟΩ»’ΤΛœ¬ΉΔ…δ¥σΜΤ2 mL(Κ§…ζ“©1.0 g)1¥ΈΓΘΒΎ3»’ΤπΘ§ΚσΝΫΉιΕ·ΈοΤΛœ¬ΉΔ…δTAA(600mg/kg)1¥ΈΓΘΕ‘’’ΉιΆ§―υΉΔ…δ…ζάμ―ΈΥ°2 mLΓΘ24 hΚσœύΆ§ΦΝΝΩTAA÷ΊΗ¥ΉΔ…δ1¥ΈΓΘ»ΜΚσ»ΐΉιΕ·Έο»Ϊ≤ΩΫϊ ≥≤ΜΫϊΥ°Θ§¥Έ»’‘Ύ““Ο―¬ιΉμœ¬Ϋχ––…ζΜ·÷Η±ξ≤βΕ®ΚΆΉι÷·―ßΙέ≤λΓΘ
, ΑΌΡ¥“Ϋ“©
(Εΰ)≤βΕ®ΖΫΖ®ΘΚ1.ΡΎΕΨΥΊΕ®ΝΩ≤…”ΟωΉ ‘ΦΝΖ®Θ§ωΉ ‘ΦΝΚ–”……œΚΘΝΌ¥≤Φλ―ι÷––ΡΧαΙ©ΘΜ2.Ι»Α±θΘΑΖΚ§ΝΩ≤…”ΟΖ”“Μ¥Έ¬»ΥαΖ®ΘΜ3.”ΪΙβΖ®≤βΕ®Ι»Α±θΘΑΖΟΗΜν–‘ΚΆΉιΑΖΚ§ΝΩΘ§Τδ÷–Υυ”ΟL-Ι»Α±ΥαΆ―«βΟΗ”…±±Ψ©…ζΈοΜ·―ß ‘ΦΝ÷––ΡΧαΙ©ΘΜ4.≥Π’≥ΡΛΦΑ―ΣΙήΆ®ΆΗ–‘≤βΕ®≤…”ΟEvansάΕ»Ψ…ΪΖ®[3]Θ§EvansάΕ”……œΚΘΜ·―ß ‘ΦΝ≤…ΙΚΙ©”Π’ΨΧαΙ©ΘΜ5.ΗΈ‘ύΓΔ–Γ≥ΠΉι÷·––HE»Ψ…ΪΘ§–Γ≥ΠΖ ¥σœΗΑϊ––ΦΉ±ΫΑΖάΕ»Ψ…ΪΘ§«“–Γ≥Π’≥ΡΛΨ≠ΈλΕΰ»©ΙΧΕ®Ϋχ––ΆΗ…δΒγΨΒΙέ≤λΓΘ
(»ΐ)»Ϊ≤Ω ΐΨί”ΟΨυ ΐΓά±ξΉΦ≤ν( Γάs)±μ ΨΘ§≤Δ≤…”ΟΖΫ≤νΖ÷ΈωΓΔtΦλ―ιΜρtΓδΦλ―ιΫχ––Ά≥ΦΤ―ß¥ΠάμΓΘ
Γάs)±μ ΨΘ§≤Δ≤…”ΟΖΫ≤νΖ÷ΈωΓΔtΦλ―ιΜρtΓδΦλ―ιΫχ––Ά≥ΦΤ―ß¥ΠάμΓΘ
ΫαΙϊ
(“Μ)Ε·ΈοΒΡ“ΜΑψΉ¥ΩωΘΚΒΎ“Μ¥ΈΗχ“©12 hΚσΘ§TAAΉιΕ·ΈοΜνΕ·ΦΑΟΌ ≥Φθ…ΌΘΜΒΎΕΰ¥ΈΗχ“©ΚσΘ§Ε·Έο »Υ·Θ§Ε‘ΆβΫγ¥ΧΦΛΖ¥”ΠΈΔ»θΓΘ
, ΑΌΡ¥“Ϋ“©
(Εΰ)ΗςΉιΕ·Έο”–ΙΊ…ζΜ·÷Η±ξΗΡ±δΘΚΦϊ±μ1ΓΪ4ΓΘ
±μ1 ΗςΉιΕ·Έο―ΣΫ§ALT,AST,TBΚΆΡΎΕΨΥΊΒΡ±δΜ·
Tab 1 Variation of plasma ALTΓΔASTΓΔTB and endotoxin(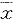 Γάs)
Γάs)
Groups
n
ALT
(U/L)
AST
, ΑΌΡ¥“Ϋ“© (U/L)
TB
(ΠΧmol/L)
Endotoxin
(ΓΝ103 EU/6L)
Normal
8
20.28Γά4.32
41.25Γά13.41
19.66Γά0.69
0.20Γά0.06
TAA
, ΑΌΡ¥“Ϋ“©
10
1473.29Γά293.74*
692.46Γά148.97*
87.72Γά53.35*
0.68Γά0.14*
Rheum+TAA
8
643.80Γά131.78**
327.34Γά208.53**
37.10Γά18.81**
, ΑΌΡ¥“Ϋ“©
0.48Γά0.10**
*P<0.01,vs normal; **P<0.01,vs group TAA ±μ2 ΗςΉιΕ·ΈοΙ»Α±θΘΑΖΚ§ΝΩΦΑΙ»Α±θΘΑΖΟΗΜν–‘±»Ϋœ
Tab 2 Comparison of glutamine content and glutaminase activity
in intestine and plasma (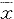 Γάs)
Γάs)
Group
n
Glutaminase
, http://www.100md.com
activity(mmol.h-1.g-1
tissue)
Glutamine
Plasma
(mg/dL)
Intestine
(mg.g-1 tissue)
Normal
7
2.25Γά0.45
, http://www.100md.com
42.73Γά23.99
2.62Γά3.17
TAA
8
1.56Γά0.25*
204.53Γά95.61*
15.80Γά8.74*
Rheum+TAA
8
1.65Γά0.28**
141.17Γά85.75**
, ΑΌΡ¥“Ϋ“©
10.75Γά6.33**
*P<0.05,vs normal; **P<0.05,vs group TAA ±μ3 ΗςΉιΕ·Έο≥ΠEvansάΕΚ§ΝΩΦΑΆ®ΆΗ÷Η ΐΠΡΒΡ±δΜ·
Tab 3 Variation of Evans blue content and permeability index
in intestine ( Γάs)
Γάs)
Groups
n
Evans blue
, http://www.100md.com
(mg/dL)
ΠΡ
Normal
8
4.49Γά1.10
1.38Γά0.64
TAA
8
12.32Γά2.82*
4.42Γά0.86*
Rheum+TAA
10
, ΑΌΡ¥“Ϋ“©
5.35Γά1.88**
2.06Γά0.90**
*P<0.05,vs Normal;P<0.01,vs group TAA ±μ4 ΗςΉιΕ·Έο―ΣΫ§ΡΎΕΨΥΊΓΔ»Ϊ―ΣΦΑ≥ΠΉιΑΖΚ§ΝΩΒΡ±δΜ·
Tab 4 Variation of plasma endotoxin and histamine in blood
and intestine ( Γάs,n=6)
Γάs,n=6)
Group
, ΑΌΡ¥“Ϋ“© Endotoxin
(ΓΝ103 EU/L)
Histamine
Blood
(ΠΧg/dL)
Intestine
(mg.g-1 tissue)
Normal
0.14Γά0.05
1.79Γά1.34
0.11Γά0.08
, ΑΌΡ¥“Ϋ“©
TAA
0.48Γά0.13*
12.52Γά2.96*
1.08Γά0.33*
Rheum+TAA
0.26Γά0.07Γς
10.80Γά2.26Γς
0.98Γά0.09Γς
*P<0.05,vs normal;ΓςP<0.05,vs group TAA
, ΑΌΡ¥“Ϋ“© (»ΐ)―ΣΫ§ΡΎΕΨΥΊΚ§ΝΩ”κ≥ΠΉιΑΖΚ§ΝΩœύΙΊΖ÷ΈωΘΚΫαΙϊ±μΟςΘ§≥ΠΉιΑΖΚ§ΝΩ”κ―ΣΫ§ΡΎΕΨΥΊΥ°ΤΫ≥ Οςœ‘’ΐœύΙΊr=0.81,P<0.01ΓΘ
(ΥΡ)Ήι÷·―ßΙέ≤λΘΚΙβΨΒœ¬Θ§TAAΉιΕ·ΈοΗΈ–Γ“Ε÷–―κΨ≤¬ω÷ήΈßΗΈœΗΑϊ±δ–‘ΓΔΜΒΥάΘ§Ω…”–≥δ―ΣΓΔ―Ή–‘œΗΑϊΫΰ»σΘ§ΤδΖΕΈßΩ…¥οΗΈ–Γ“ΕΒΡ2/3Ήσ”“ΘΜ≥Π’≥ΡΛ”Ό―ΣΓΔΥ°÷ΉΓΔΟ”άΟΓΘΕ‘’’ΉιΕ·Έο≥ΠΖ ¥σœΗΑϊΡΛΆξ’ϊΘ§ΉœΚλ…ΪΩ≈ΝΘ«εΈζΩ…ΦϊΘ§ΕχTAAΉιΕ·Έο≥ΠΖ ¥σœΗΑϊ”–Οςœ‘Ά―Ω≈ΝΘœ÷œσΓΘ
ΒγΨΒœ¬Θ§TAAΉι≥Π’≥ΡΛΈΔ»όΟΪΦθ…ΌΓΔΒΙΖϋΓΔΆ―¬δΘ§œΗΑϊΦδΫτΟήΝ§Ϋ”±ΜΤΤΜΒΘ§Ω…ΦϊœΏΝΘΧε÷Ή’ΆΓΘ¥σΜΤΉι…œ ωΉι÷·―ßΗΡ±δΦθ«αΓΘ
Χ÷¬έ
“ΜΓΔΦ±–‘ΗΈΥΞ ±≥Π’≥ΡΛΤΝ’œΥπΚΠΦΑΤδΜζ÷ΤΘΚ
≥Π’≥ΡΛΤΝ’œ÷Η≥Π’≥ΡΛΒ÷”υ≥ΠΒάœΗΨζΦΑΤδΕΨΥΊΒΡΈϋ ’ΒΡΙΠΡήΓΘΥϋ”…≥Π±μΟφ’≥“ΚΓΔ ≥Π’≥ΡΛ…œΤΛœΗΑϊΦΑΤδΦδΫτΟήΝ§Ϋ”ΓΔ ΜυΡΛΥυΉι≥…ΓΘ≥ΠΒάΡΎ¥φ‘Ύ¥σΝΩGΣ≤œΗΨζΘ§ΨζΧεΉ‘»ήΚσΖ≈≥ωΡΎΕΨΥΊΓΘ’ΐ≥Θ«ιΩωœ¬Θ§≥Π’≥ΡΛ «≥ΠΒάΡΎΕΨΥΊΒΡ”––ßΤΝ’œΓΘΦ¥±ψ”Ο–ΓΝΩΈϋ ’Θ§Ψ≠Ο≈¬ω»κΗΈ‘ύΘ§“≤ΦΗΚθ±ΜΩίΖώœΗΑϊ«ε≥ΐΓΘ
, ΑΌΡ¥“Ϋ“©
±Ψ―–ΨΩΖΔœ÷Θ§TAA“ΐΖΔΦ±–‘ΗΈΥΞ ±Ω…ΖΔ…ζ≥Π’≥ΡΛ”Ό―ΣΓΔ Υ°÷ΉΓΔ Ο”άΟΘ§≥Π’≥ΡΛΦΑΤδ―ΣΙήΆ®ΆΗ–‘‘ωΦ”Θ§¥σΝΩΡΎΕΨΥΊΨ≠Ο≈Ψ≤¬ωΜρΝήΑΆΙή»κ―ΣΘ§¥”Εχ≤ζ…ζIETMΓΘ¥ΥΆβΘ§Φ±–‘ΗΈΥΞ ±ΩίΖώœΗΑϊ«ε≥ΐΙΠΡή ήΒΫ“÷÷ΤΘΜ‘Ό”–Β®÷≠≈≈–Ι ήΉηΘ§≥ΠΒάΡΎΒ®―ΈΦθ…Ό“≤”–άϊ”ΎΡΎΕΨΥΊΈϋ ’Εχ¥ΌΫχIETM–Έ≥…ΓΘ
–μΕύ―–ΨΩ±μΟςΘ§IETM–Έ≥…ΚσΘ§―Σ÷–ΒΡΡΎΕΨΥΊΩ…Ά®ΙΐΤδ÷±Ϋ”ΜρΦδΫ”Ής”ΟΘ§ΤΤΜΒ≥Π’≥ΡΛΤΝ’œΒΡΆξ’ϊ–‘Θ§≤ζ…ζIETM[4]ΓΘΡΎΕΨΥΊΩ…Υπ…Υ≥Π’≥ΡΛ…œΤΛœΗΑϊœΏΝΘΧεΚΆ»ήΟΗΧεΡΛΘΜ“≤Ω… ’Υθ≥Π’≥ΡΛ–Γ―ΣΙήΘ§≤ΔΦΛΜνΜΤύ―Ώ ―θΜ·ΟΗ[5]Θ§≤ζ…ζ―θΉ‘”…ΜυΘ§ΒΦ÷¬≥Π’≥ΡΛ»±―Σ»±―θΓΘΡΎΕΨΥΊ“≤Ω…“‘ΦΛΜνΩίΖώœΗΑϊ ΆΖ≈–μΕύ―Ή–‘Ϋι÷ ΚΆœΗΑϊ“ρΉ”[6]Θ§»γΉιΑΖΓΔTNFΓΔIL-2ȧ»»“ΐΤπ≥Π’≥ΡΛΤΝ’œΥπ…Υ”κΤδΤΝ’œΙΠΡήΦθ»θΓΘ
–Γ≥Π «Ι»Α±θΘΑΖΈϋ ’ΒΡ÷ς“ΣΤςΙΌΘ§Ι»Α±θΘΑΖ «–Γ≥ΠΒΡ÷ς“ΣΚτΈϋ»ΦΝœΓΘ Β―ι±μΟςΘ§Φ±–‘ΗΈΥΞ ±Θ§―Σ÷–Ι»Α±θΘΑΖ≤Δ≤ΜΫΒΒΆΘ§Ζ¥Εχ…ΐΗΏΘ§’β «Φ±–‘ΗΈΥΞ ±―ΣΫ§Α±ΜυΥαΡΘ ΫΗΡ±δΒΡΫαΙϊΓΘ”…”ΎΡΎΕΨΥΊ ΙΙ»Α±θΘΑΖΟΗΜν–‘ΫΒΒΆ[7]Θ§÷¬ Ι≥Πάϊ”ΟΙ»Α±θΘΑΖΦθ…ΌΘ§‘λ≥…≥ΠΡή‘¥≤ΜΉψΓΘSoubaΒ»[7]ΒΡ Β―ι“≤ΒΟ≥ωάύΥΤΫα¬έΓΘ’βΨΆΧα ΨΦ±–‘ΗΈΥΞ ±ΖΔ…ζIETMΘ§ΥϋΩ…Η…»≈≥ΠΙ»Α±θΘΑΖ¥ζ–ΜΘ§ Ι≥ΠΉι÷·άϊ”ΟΙ»Α±θΘΑΖΦθ…ΌΓΘ¥ΥΆβΘ§–Γ≥Π¥”―Σ÷–…ψ»ΓΙ»Α±θΘΑΖ“≤Φθ…Ό[8]Θ§ΒΦ÷¬≥Π”Σ―χ’œΑ≠Θ§Φ”÷Ί≥Π’≥ΡΛΤΝ’œΙΠΡήΥΞΫΏΓΘ
, ΑΌΡ¥“Ϋ“©
±Ψ Β―ι‘Ό¥Έ÷ΛΟςΘ§IETMΒΡ–Έ≥…≥ΐΩίΖώœΗΑϊ«ε≥ΐΡήΝΠœ¬ΫΒΆβΘ§≥Π’≥ΡΛΤΝ’œΙΠΡήΥΞΫΏΥυ÷¬ΒΡ≥ΠΡΎΕΨΥΊΈϋ ’‘ωΕύ“≤ «÷Ί“Σ‘≠“ρΓΘ
ΕΰΓΔ¥σΜΤΕ‘Φ±–‘ΗΈΥΞΚœ≤Δ≥Π’≥ΡΛΥπ…ΥΒΡΖά÷ΈΉς”ΟΘΚ
“©άμ―–ΨΩ÷ΛΟςΘ§¥σΜΤΨΏ”––Κœ¬ΓΔ“÷ΨζΓΔœϊ―ΉΓΔ±ΘΗΈΒ»Ής”ΟΓΘ…œ ωΫαΙϊ±μΟςΘ§¥σΜΤΩ…Φθ«αTAAΥυ÷¬ΗΈΥπ…ΥΓΘ’βΩ…Ρή”κ¥σΜΤΦθ«αIETM”–ΙΊΓΘ
”–―ß’Ώ±®ΒάΘ§¥σΜΤΩ…ΗΡ…Τ≥ΠΒάΈΔ―≠ΜΖΘ§±ΘΜΛ≥Π’≥ΡΛΤΝ’œΘ§≤ΔΫΒΒΆ≥Π’≥ΡΛΒΡΟΪœΗ―ΣΙήΆ®ΆΗ–‘[9]Θ§¥”ΕχΦθ…Ό≥ΠΒάΡΎΕΨΥΊΒΡΈϋ ’ΘΜ¥σΜΤΒΡ–Κœ¬Ής”ΟΩ…¥ΌΫχ≥ΠΒάΡΎΕΨΥΊΒΡ≈≈≥ΐΘ§“ρΕχ÷–“©¥σΜΤΩ…Φθ«αIETMΓΘ
≤ΈΩΦΈΡœΉ
1 ΚΪΒ¬Έε.ΗΈΙΠΡήΥΞΫΏΖΔ≤ΓΜζ÷Τ―–ΨΩΫχ’Ι.÷–Ιζ≤Γάμ…ζάμ‘”÷ΨΘ§1993Θ§9ΘΚ770.
2 Deith EA,Specian RD,Berg RD.Endotoxin-induced bacterial translocation and mucosal permeability.Crit Care Med,1991,19:785.
, ΑΌΡ¥“Ϋ“©
3 ¥ςΥ≥ΝδΘ§―Π»ΪΗΘΘ§Άθ ς…ΫΘ§Β».…ΫίΙί–ΦνΦΑ¥®ήΚύΚ‘ΛΖά¥σ σΖΈΥ°÷ΉΒΡ Β―ι―–ΨΩ.÷–Ιζ≤Γάμ…ζάμ‘”÷ΨΘ§1989Θ§5ΘΚ354.
4 Saadia R,Schein M,MacFarlane C,et al.Gut barrier function and the surgeon.Br J Surg,1990,77:487.
5 Koshi R,David S,Mathan VI,et al.Enteric vascular endothelial response to bacterial endotoxin.Int J Exp Path,1993,74:539.
6 Roland CR,COSS JA,Mangino MJ,et al.Autoregulation by eicosanoids of human Kupffer cell secretory products.Ann Surg,1994,219:389.
, ΑΌΡ¥“Ϋ“©
7 Souba WW,Herskowitz K,Klimberg VS,et al.The effects of sepsis and endotoxemia on gut glutamine metabolism. Ann Surg,1990,211:543.
8 Dudricr PS,Salloum RM,Copeland EM,et al.The early response of jejounal brush border glutamine transporter to endotoxemia.J Surg Res,1992,52:372.
9 ≥¬Β¬≤ΐΘ§―νΫ®ΕΪΘ§ΨΑ±ΰΈΡΘ§Β».¥σΜΤΕ‘¥σ σ≥Π’≥ΡΛΦΑ≥Π―ΣΙήΆ®ΆΗ–‘ΒΡ”Αœλ.÷–ΙζΈΘ÷Ί≤ΓΦ±Ψ»“Ϋ―ßΘ§1997Θ§9ΘΚ385.
(1998Ρξ3‘¬17»’ ’ΗεΘ§1998Ρξ11‘¬6»’–όΜΊ), http://www.100md.com
ΒΞΈΜΘΚΕΈΟάάω Άθ―εΨϋ :…ΫΈς“ΫΩΤ¥σ―ßΒΎ“Μ“Ϋ‘Κ(ΧΪ‘≠ 030001)ΘΜΚΪΒ¬ΈεΘΚ…ΫΈς“ΫΩΤ¥σ―ß≤Γάμ…ζάμΫΧ―– “
ΙΊΦϋ¥ ΘΚΗΈΘΜΡΎΕΨΥΊάύΘΜ≥Π’≥ΡΛΘΜ¥σΜΤ
Φ±–‘ΗΈΙΠΡήΥΞΫΏ ±≥Π’≥ΡΛΤΝ’œΥπ…ΥΒΡ―–ΨΩ ’Σ“Σ ΡΩΒΡΘΚΧΫΧ÷Φ±–‘ΗΈΙΠΡήΥΞΫΏ(Φρ≥ΤΗΈΥΞ) ±≥Π’≥ΡΛΤΝ’œΥπ…ΥΦΑΤδΜζ÷ΤΘ§≤ΔΙέ≤λ÷–“©¥σΜΤΕ‘ΥϋΒΡΖά÷ΈΉς”ΟΓΘΖΫΖ®ΘΚ≤…”ΟωΉ ‘ΦΝΖ®Ής―ΣΫ§ΡΎΕΨΥΊΕ®ΝΩΘ§Ζ”“Μ¥Έ¬»ΥαΖ®≤βΕ®Ι»Α±θΘΑΖ≈®Ε»ΦΑ”ΪΙβΖ®≤βΕ®Ι»Α±θΘΑΖΟΗΜν–‘ΚΆΉιΑΖΚ§ΝΩΘ§EvansάΕ»Ψ…ΪΖ®≤βΕ®≥Π’≥ΡΛΆ®ΆΗ–‘ΓΘΫαΙϊΘΚΝρ¥ζ““θΘΑΖ(thioacetamide,TAA)“ΐΖΔ¥σ σΦ±–‘ΗΈΥΞΘ§≤ΔΑι”–―œ÷ΊΒΡ≥Π‘¥–‘ΡΎΕΨΥΊ―Σ÷Δ(intestinal endotoxemia,IETM)ΓΘ≥ΠΙ»Α±θΘΑΖΟΗΜν–‘ΫΒΒΆΘ§≥Π’≥ΡΛΕ‘Ι»Α±θΘΑΖάϊ”ΟΦθ…ΌΘ§≥Π’≥ΡΛΆ®ΆΗ–‘‘ωΦ”ΓΘΉι÷·œΗΑϊ―ßœ‘ ΨΘ§TAAΉιΕ·ΈοΗΈœΗΑϊΖΔ…ζ―œ÷Ί±δ–‘ΜΒΥάΘΜ≥Π’≥ΡΛ”Ό―ΣΓΔΥ°÷ΉΓΔΟ”άΟΘ§≥ΠΖ ¥σœΗΑϊΆ―Ω≈ΝΘΓΘΒγΨΒ Ψ≥ΠΈΔ»όΟΪΒΙΖϋΓΔΆ―¬δΘ§œΗΑϊΦδΫτΟήΝ§Ϋ”ΤΤΜΒΓΘ¥σΜΤΉιΕ·ΈοIETM”κΗΈΉι÷·Υπ…ΥΟςœ‘Φθ«αΓΘΫα¬έΘΚΦ±–‘ΗΈΥΞΑι”–≥Π’≥ΡΛΤΝ’œΥπ…ΥΘ§ΤδΖΔ…ζΜζ÷Τ”κIETMΦΑΤδΫιΒΦΒΡΉιΑΖ‘ωΕύ”–ΙΊΓΘ¥σΜΤΕ‘Φ±–‘ΗΈΥΞ ±≥Π’≥ΡΛΤΝ’œΥπ…Υ”–“ΜΕ®Ζά÷ΈΉς”ΟΓΘ
, http://www.100md.com
Studies on intestinal mucosa barrier injuries in acute hepatic failure
DUAN Mei-Li,WANG Yan-Jun,HAN De-Wu
Shan-Xi Medical University,Taiyuan(030001)
Abstract AIMΘΚTo elucidate the mechanism of intestinal mucosa injuries,as well as the preventive and cure effect of Chinese Medicine Rheum,in acute hepatic failure (AHF) induced by thioacetamide(TAA).METHODSΘΚEndotoxin content by the Limulus test;glutamine content by phenol-hypochlorite method;glutaminase activity and histamine content by fluorescence method;intestinal mucosal permeability by Evans blue method.RESULTSΘΚAHF induced by TAA resulted in intestinal endotoxemia (IETM),reduce of glutaminase activity and glutamine utilization,increase of intestinal mucosal permeability.Histological observation showed that degeneration,necrosis of liver cells,edema,extravasated blood,erosion and degranulation of the mast cells in intestine mucosa.Electron microscope displayed intestinal microvilli fell off,the tight junction damaged.In Rheum-treated group,the last changes alleviated.CONCLUSIONΘΚIntestinal mucosa injuries were important complication in AHF,its mechanism was related to IETM and hyperhistaminemia.Rheum was effective for the prevention and therapy of intestinal mucosa injuries in AHF.
, ΑΌΡ¥“Ϋ“©
MeSH Liver;Endotoxins;Intestinal mucosa;Rhubarb
ΫϋΡξά¥Θ§Ε‘”ΎΦ±–‘ΗΈΥΞ ±IETM≤ζ…ζΜζ÷ΤΒΡ―–ΨΩΕύ≤ύ÷Ί”Ύ―–ΨΩΩίΖώœΗΑϊΙΠΡή’œΑ≠[1]ΘΜΕ‘≥Π’≥ΡΛΤΝ’œΙΠΡήΥΞΫΏ‘ΎIETMΖΔ…ζ÷–ΒΡΉς”ΟΕύœό”Ύ…’…ΥΓΔ ß―Σ–‘–ίΩΥΒ»«ιΩω[2]ΓΘΈΣ¥ΥΘ§±ΨΈΡΆ®ΙΐΕ·Έο Β―ιΧΫΧ÷Φ±–‘ΗΈΥΞ ±≥Π’≥ΡΛΤΝ’œ±δΜ·ΦΑΤδΜζ÷ΤΘ§Ά§ ±Ιέ≤λ¥σΜΤ(Rheum)ΒΡΖά÷ΈΉς”ΟΓΘ
≤ΡΝœ”κΖΫΖ®
(“Μ)Ε·ΈοΡΘ–ΆΘΚ»ΓWistar¥σ σ30÷ΜΘ§Χε÷Ί200ΓΪ240 g,¥Τ–έΗςΑκΘ§ΥφΜζΖ÷≥…3ΉιΘΚΕ‘’’ΉιΓΔTAAΉιΓΔRheum+TAAΉιΓΘ Β―ιΒΎ“Μ»’ΤπΘ§ΒΎ3ΉιΕ·ΈοΟΩ»’ΤΛœ¬ΉΔ…δ¥σΜΤ2 mL(Κ§…ζ“©1.0 g)1¥ΈΓΘΒΎ3»’ΤπΘ§ΚσΝΫΉιΕ·ΈοΤΛœ¬ΉΔ…δTAA(600mg/kg)1¥ΈΓΘΕ‘’’ΉιΆ§―υΉΔ…δ…ζάμ―ΈΥ°2 mLΓΘ24 hΚσœύΆ§ΦΝΝΩTAA÷ΊΗ¥ΉΔ…δ1¥ΈΓΘ»ΜΚσ»ΐΉιΕ·Έο»Ϊ≤ΩΫϊ ≥≤ΜΫϊΥ°Θ§¥Έ»’‘Ύ““Ο―¬ιΉμœ¬Ϋχ––…ζΜ·÷Η±ξ≤βΕ®ΚΆΉι÷·―ßΙέ≤λΓΘ
, ΑΌΡ¥“Ϋ“©
(Εΰ)≤βΕ®ΖΫΖ®ΘΚ1.ΡΎΕΨΥΊΕ®ΝΩ≤…”ΟωΉ ‘ΦΝΖ®Θ§ωΉ ‘ΦΝΚ–”……œΚΘΝΌ¥≤Φλ―ι÷––ΡΧαΙ©ΘΜ2.Ι»Α±θΘΑΖΚ§ΝΩ≤…”ΟΖ”“Μ¥Έ¬»ΥαΖ®ΘΜ3.”ΪΙβΖ®≤βΕ®Ι»Α±θΘΑΖΟΗΜν–‘ΚΆΉιΑΖΚ§ΝΩΘ§Τδ÷–Υυ”ΟL-Ι»Α±ΥαΆ―«βΟΗ”…±±Ψ©…ζΈοΜ·―ß ‘ΦΝ÷––ΡΧαΙ©ΘΜ4.≥Π’≥ΡΛΦΑ―ΣΙήΆ®ΆΗ–‘≤βΕ®≤…”ΟEvansάΕ»Ψ…ΪΖ®[3]Θ§EvansάΕ”……œΚΘΜ·―ß ‘ΦΝ≤…ΙΚΙ©”Π’ΨΧαΙ©ΘΜ5.ΗΈ‘ύΓΔ–Γ≥ΠΉι÷·––HE»Ψ…ΪΘ§–Γ≥ΠΖ ¥σœΗΑϊ––ΦΉ±ΫΑΖάΕ»Ψ…ΪΘ§«“–Γ≥Π’≥ΡΛΨ≠ΈλΕΰ»©ΙΧΕ®Ϋχ––ΆΗ…δΒγΨΒΙέ≤λΓΘ
(»ΐ)»Ϊ≤Ω ΐΨί”ΟΨυ ΐΓά±ξΉΦ≤ν(
ΫαΙϊ
(“Μ)Ε·ΈοΒΡ“ΜΑψΉ¥ΩωΘΚΒΎ“Μ¥ΈΗχ“©12 hΚσΘ§TAAΉιΕ·ΈοΜνΕ·ΦΑΟΌ ≥Φθ…ΌΘΜΒΎΕΰ¥ΈΗχ“©ΚσΘ§Ε·Έο »Υ·Θ§Ε‘ΆβΫγ¥ΧΦΛΖ¥”ΠΈΔ»θΓΘ
, ΑΌΡ¥“Ϋ“©
(Εΰ)ΗςΉιΕ·Έο”–ΙΊ…ζΜ·÷Η±ξΗΡ±δΘΚΦϊ±μ1ΓΪ4ΓΘ
±μ1 ΗςΉιΕ·Έο―ΣΫ§ALT,AST,TBΚΆΡΎΕΨΥΊΒΡ±δΜ·
Tab 1 Variation of plasma ALTΓΔASTΓΔTB and endotoxin(
Groups
n
ALT
(U/L)
AST
, ΑΌΡ¥“Ϋ“© (U/L)
TB
(ΠΧmol/L)
Endotoxin
(ΓΝ103 EU/6L)
Normal
8
20.28Γά4.32
41.25Γά13.41
19.66Γά0.69
0.20Γά0.06
TAA
, ΑΌΡ¥“Ϋ“©
10
1473.29Γά293.74*
692.46Γά148.97*
87.72Γά53.35*
0.68Γά0.14*
Rheum+TAA
8
643.80Γά131.78**
327.34Γά208.53**
37.10Γά18.81**
, ΑΌΡ¥“Ϋ“©
0.48Γά0.10**
*P<0.01,vs normal; **P<0.01,vs group TAA ±μ2 ΗςΉιΕ·ΈοΙ»Α±θΘΑΖΚ§ΝΩΦΑΙ»Α±θΘΑΖΟΗΜν–‘±»Ϋœ
Tab 2 Comparison of glutamine content and glutaminase activity
in intestine and plasma (
Group
n
Glutaminase
, http://www.100md.com
activity(mmol.h-1.g-1
tissue)
Glutamine
Plasma
(mg/dL)
Intestine
(mg.g-1 tissue)
Normal
7
2.25Γά0.45
, http://www.100md.com
42.73Γά23.99
2.62Γά3.17
TAA
8
1.56Γά0.25*
204.53Γά95.61*
15.80Γά8.74*
Rheum+TAA
8
1.65Γά0.28**
141.17Γά85.75**
, ΑΌΡ¥“Ϋ“©
10.75Γά6.33**
*P<0.05,vs normal; **P<0.05,vs group TAA ±μ3 ΗςΉιΕ·Έο≥ΠEvansάΕΚ§ΝΩΦΑΆ®ΆΗ÷Η ΐΠΡΒΡ±δΜ·
Tab 3 Variation of Evans blue content and permeability index
in intestine (
Groups
n
Evans blue
, http://www.100md.com
(mg/dL)
ΠΡ
Normal
8
4.49Γά1.10
1.38Γά0.64
TAA
8
12.32Γά2.82*
4.42Γά0.86*
Rheum+TAA
10
, ΑΌΡ¥“Ϋ“©
5.35Γά1.88**
2.06Γά0.90**
*P<0.05,vs Normal;P<0.01,vs group TAA ±μ4 ΗςΉιΕ·Έο―ΣΫ§ΡΎΕΨΥΊΓΔ»Ϊ―ΣΦΑ≥ΠΉιΑΖΚ§ΝΩΒΡ±δΜ·
Tab 4 Variation of plasma endotoxin and histamine in blood
and intestine (
Group
, ΑΌΡ¥“Ϋ“© Endotoxin
(ΓΝ103 EU/L)
Histamine
Blood
(ΠΧg/dL)
Intestine
(mg.g-1 tissue)
Normal
0.14Γά0.05
1.79Γά1.34
0.11Γά0.08
, ΑΌΡ¥“Ϋ“©
TAA
0.48Γά0.13*
12.52Γά2.96*
1.08Γά0.33*
Rheum+TAA
0.26Γά0.07Γς
10.80Γά2.26Γς
0.98Γά0.09Γς
*P<0.05,vs normal;ΓςP<0.05,vs group TAA
, ΑΌΡ¥“Ϋ“© (»ΐ)―ΣΫ§ΡΎΕΨΥΊΚ§ΝΩ”κ≥ΠΉιΑΖΚ§ΝΩœύΙΊΖ÷ΈωΘΚΫαΙϊ±μΟςΘ§≥ΠΉιΑΖΚ§ΝΩ”κ―ΣΫ§ΡΎΕΨΥΊΥ°ΤΫ≥ Οςœ‘’ΐœύΙΊr=0.81,P<0.01ΓΘ
(ΥΡ)Ήι÷·―ßΙέ≤λΘΚΙβΨΒœ¬Θ§TAAΉιΕ·ΈοΗΈ–Γ“Ε÷–―κΨ≤¬ω÷ήΈßΗΈœΗΑϊ±δ–‘ΓΔΜΒΥάΘ§Ω…”–≥δ―ΣΓΔ―Ή–‘œΗΑϊΫΰ»σΘ§ΤδΖΕΈßΩ…¥οΗΈ–Γ“ΕΒΡ2/3Ήσ”“ΘΜ≥Π’≥ΡΛ”Ό―ΣΓΔΥ°÷ΉΓΔΟ”άΟΓΘΕ‘’’ΉιΕ·Έο≥ΠΖ ¥σœΗΑϊΡΛΆξ’ϊΘ§ΉœΚλ…ΪΩ≈ΝΘ«εΈζΩ…ΦϊΘ§ΕχTAAΉιΕ·Έο≥ΠΖ ¥σœΗΑϊ”–Οςœ‘Ά―Ω≈ΝΘœ÷œσΓΘ
ΒγΨΒœ¬Θ§TAAΉι≥Π’≥ΡΛΈΔ»όΟΪΦθ…ΌΓΔΒΙΖϋΓΔΆ―¬δΘ§œΗΑϊΦδΫτΟήΝ§Ϋ”±ΜΤΤΜΒΘ§Ω…ΦϊœΏΝΘΧε÷Ή’ΆΓΘ¥σΜΤΉι…œ ωΉι÷·―ßΗΡ±δΦθ«αΓΘ
Χ÷¬έ
“ΜΓΔΦ±–‘ΗΈΥΞ ±≥Π’≥ΡΛΤΝ’œΥπΚΠΦΑΤδΜζ÷ΤΘΚ
≥Π’≥ΡΛΤΝ’œ÷Η≥Π’≥ΡΛΒ÷”υ≥ΠΒάœΗΨζΦΑΤδΕΨΥΊΒΡΈϋ ’ΒΡΙΠΡήΓΘΥϋ”…≥Π±μΟφ’≥“ΚΓΔ ≥Π’≥ΡΛ…œΤΛœΗΑϊΦΑΤδΦδΫτΟήΝ§Ϋ”ΓΔ ΜυΡΛΥυΉι≥…ΓΘ≥ΠΒάΡΎ¥φ‘Ύ¥σΝΩGΣ≤œΗΨζΘ§ΨζΧεΉ‘»ήΚσΖ≈≥ωΡΎΕΨΥΊΓΘ’ΐ≥Θ«ιΩωœ¬Θ§≥Π’≥ΡΛ «≥ΠΒάΡΎΕΨΥΊΒΡ”––ßΤΝ’œΓΘΦ¥±ψ”Ο–ΓΝΩΈϋ ’Θ§Ψ≠Ο≈¬ω»κΗΈ‘ύΘ§“≤ΦΗΚθ±ΜΩίΖώœΗΑϊ«ε≥ΐΓΘ
, ΑΌΡ¥“Ϋ“©
±Ψ―–ΨΩΖΔœ÷Θ§TAA“ΐΖΔΦ±–‘ΗΈΥΞ ±Ω…ΖΔ…ζ≥Π’≥ΡΛ”Ό―ΣΓΔ Υ°÷ΉΓΔ Ο”άΟΘ§≥Π’≥ΡΛΦΑΤδ―ΣΙήΆ®ΆΗ–‘‘ωΦ”Θ§¥σΝΩΡΎΕΨΥΊΨ≠Ο≈Ψ≤¬ωΜρΝήΑΆΙή»κ―ΣΘ§¥”Εχ≤ζ…ζIETMΓΘ¥ΥΆβΘ§Φ±–‘ΗΈΥΞ ±ΩίΖώœΗΑϊ«ε≥ΐΙΠΡή ήΒΫ“÷÷ΤΘΜ‘Ό”–Β®÷≠≈≈–Ι ήΉηΘ§≥ΠΒάΡΎΒ®―ΈΦθ…Ό“≤”–άϊ”ΎΡΎΕΨΥΊΈϋ ’Εχ¥ΌΫχIETM–Έ≥…ΓΘ
–μΕύ―–ΨΩ±μΟςΘ§IETM–Έ≥…ΚσΘ§―Σ÷–ΒΡΡΎΕΨΥΊΩ…Ά®ΙΐΤδ÷±Ϋ”ΜρΦδΫ”Ής”ΟΘ§ΤΤΜΒ≥Π’≥ΡΛΤΝ’œΒΡΆξ’ϊ–‘Θ§≤ζ…ζIETM[4]ΓΘΡΎΕΨΥΊΩ…Υπ…Υ≥Π’≥ΡΛ…œΤΛœΗΑϊœΏΝΘΧεΚΆ»ήΟΗΧεΡΛΘΜ“≤Ω… ’Υθ≥Π’≥ΡΛ–Γ―ΣΙήΘ§≤ΔΦΛΜνΜΤύ―Ώ ―θΜ·ΟΗ[5]Θ§≤ζ…ζ―θΉ‘”…ΜυΘ§ΒΦ÷¬≥Π’≥ΡΛ»±―Σ»±―θΓΘΡΎΕΨΥΊ“≤Ω…“‘ΦΛΜνΩίΖώœΗΑϊ ΆΖ≈–μΕύ―Ή–‘Ϋι÷ ΚΆœΗΑϊ“ρΉ”[6]Θ§»γΉιΑΖΓΔTNFΓΔIL-2ȧ»»“ΐΤπ≥Π’≥ΡΛΤΝ’œΥπ…Υ”κΤδΤΝ’œΙΠΡήΦθ»θΓΘ
–Γ≥Π «Ι»Α±θΘΑΖΈϋ ’ΒΡ÷ς“ΣΤςΙΌΘ§Ι»Α±θΘΑΖ «–Γ≥ΠΒΡ÷ς“ΣΚτΈϋ»ΦΝœΓΘ Β―ι±μΟςΘ§Φ±–‘ΗΈΥΞ ±Θ§―Σ÷–Ι»Α±θΘΑΖ≤Δ≤ΜΫΒΒΆΘ§Ζ¥Εχ…ΐΗΏΘ§’β «Φ±–‘ΗΈΥΞ ±―ΣΫ§Α±ΜυΥαΡΘ ΫΗΡ±δΒΡΫαΙϊΓΘ”…”ΎΡΎΕΨΥΊ ΙΙ»Α±θΘΑΖΟΗΜν–‘ΫΒΒΆ[7]Θ§÷¬ Ι≥Πάϊ”ΟΙ»Α±θΘΑΖΦθ…ΌΘ§‘λ≥…≥ΠΡή‘¥≤ΜΉψΓΘSoubaΒ»[7]ΒΡ Β―ι“≤ΒΟ≥ωάύΥΤΫα¬έΓΘ’βΨΆΧα ΨΦ±–‘ΗΈΥΞ ±ΖΔ…ζIETMΘ§ΥϋΩ…Η…»≈≥ΠΙ»Α±θΘΑΖ¥ζ–ΜΘ§ Ι≥ΠΉι÷·άϊ”ΟΙ»Α±θΘΑΖΦθ…ΌΓΘ¥ΥΆβΘ§–Γ≥Π¥”―Σ÷–…ψ»ΓΙ»Α±θΘΑΖ“≤Φθ…Ό[8]Θ§ΒΦ÷¬≥Π”Σ―χ’œΑ≠Θ§Φ”÷Ί≥Π’≥ΡΛΤΝ’œΙΠΡήΥΞΫΏΓΘ
, ΑΌΡ¥“Ϋ“©
±Ψ Β―ι‘Ό¥Έ÷ΛΟςΘ§IETMΒΡ–Έ≥…≥ΐΩίΖώœΗΑϊ«ε≥ΐΡήΝΠœ¬ΫΒΆβΘ§≥Π’≥ΡΛΤΝ’œΙΠΡήΥΞΫΏΥυ÷¬ΒΡ≥ΠΡΎΕΨΥΊΈϋ ’‘ωΕύ“≤ «÷Ί“Σ‘≠“ρΓΘ
ΕΰΓΔ¥σΜΤΕ‘Φ±–‘ΗΈΥΞΚœ≤Δ≥Π’≥ΡΛΥπ…ΥΒΡΖά÷ΈΉς”ΟΘΚ
“©άμ―–ΨΩ÷ΛΟςΘ§¥σΜΤΨΏ”––Κœ¬ΓΔ“÷ΨζΓΔœϊ―ΉΓΔ±ΘΗΈΒ»Ής”ΟΓΘ…œ ωΫαΙϊ±μΟςΘ§¥σΜΤΩ…Φθ«αTAAΥυ÷¬ΗΈΥπ…ΥΓΘ’βΩ…Ρή”κ¥σΜΤΦθ«αIETM”–ΙΊΓΘ
”–―ß’Ώ±®ΒάΘ§¥σΜΤΩ…ΗΡ…Τ≥ΠΒάΈΔ―≠ΜΖΘ§±ΘΜΛ≥Π’≥ΡΛΤΝ’œΘ§≤ΔΫΒΒΆ≥Π’≥ΡΛΒΡΟΪœΗ―ΣΙήΆ®ΆΗ–‘[9]Θ§¥”ΕχΦθ…Ό≥ΠΒάΡΎΕΨΥΊΒΡΈϋ ’ΘΜ¥σΜΤΒΡ–Κœ¬Ής”ΟΩ…¥ΌΫχ≥ΠΒάΡΎΕΨΥΊΒΡ≈≈≥ΐΘ§“ρΕχ÷–“©¥σΜΤΩ…Φθ«αIETMΓΘ
≤ΈΩΦΈΡœΉ
1 ΚΪΒ¬Έε.ΗΈΙΠΡήΥΞΫΏΖΔ≤ΓΜζ÷Τ―–ΨΩΫχ’Ι.÷–Ιζ≤Γάμ…ζάμ‘”÷ΨΘ§1993Θ§9ΘΚ770.
2 Deith EA,Specian RD,Berg RD.Endotoxin-induced bacterial translocation and mucosal permeability.Crit Care Med,1991,19:785.
, ΑΌΡ¥“Ϋ“©
3 ¥ςΥ≥ΝδΘ§―Π»ΪΗΘΘ§Άθ ς…ΫΘ§Β».…ΫίΙί–ΦνΦΑ¥®ήΚύΚ‘ΛΖά¥σ σΖΈΥ°÷ΉΒΡ Β―ι―–ΨΩ.÷–Ιζ≤Γάμ…ζάμ‘”÷ΨΘ§1989Θ§5ΘΚ354.
4 Saadia R,Schein M,MacFarlane C,et al.Gut barrier function and the surgeon.Br J Surg,1990,77:487.
5 Koshi R,David S,Mathan VI,et al.Enteric vascular endothelial response to bacterial endotoxin.Int J Exp Path,1993,74:539.
6 Roland CR,COSS JA,Mangino MJ,et al.Autoregulation by eicosanoids of human Kupffer cell secretory products.Ann Surg,1994,219:389.
, ΑΌΡ¥“Ϋ“©
7 Souba WW,Herskowitz K,Klimberg VS,et al.The effects of sepsis and endotoxemia on gut glutamine metabolism. Ann Surg,1990,211:543.
8 Dudricr PS,Salloum RM,Copeland EM,et al.The early response of jejounal brush border glutamine transporter to endotoxemia.J Surg Res,1992,52:372.
9 ≥¬Β¬≤ΐΘ§―νΫ®ΕΪΘ§ΨΑ±ΰΈΡΘ§Β».¥σΜΤΕ‘¥σ σ≥Π’≥ΡΛΦΑ≥Π―ΣΙήΆ®ΆΗ–‘ΒΡ”Αœλ.÷–ΙζΈΘ÷Ί≤ΓΦ±Ψ»“Ϋ―ßΘ§1997Θ§9ΘΚ385.
(1998Ρξ3‘¬17»’ ’ΗεΘ§1998Ρξ11‘¬6»’–όΜΊ), http://www.100md.com