转化生长因子β(TGF-β)在实验性动脉粥样硬化发生中的作用
作者:李梅兰 谢作煊 郑佩娥 张爱东
单位:李梅兰 张爱东:暨南大学医学院第一附属医院心内科(广州 510632);谢作煊 郑佩娥:病理学教研室
关键词:动脉硬化;转化生长因子-β;兔;大鼠
转化生长因子β 摘要 目的:研究TGF-β与动脉粥样硬化形成的关系。方法:用10%胆固醇脂肪乳剂复制大鼠和家兔的高脂血症模型,免疫组织化学和ELISA等技术检测其动脉和周围血的TGF-β1、β2、β3及其受体,观察比较两种动物动脉粥样硬化形成的情况和血清中的脂蛋白及总胆固醇水平。结果:实验组家兔100%形成动脉粥样斑,血清高密度脂蛋白在正常范围;实验组大鼠未见动脉粥样斑形成,但其血TGF-β和高密度脂蛋白随实验时间(鼠龄)的延长而升高。结论:TGF-β可能在动脉内膜被高脂血症损伤后的炎性增生反应过程中起作用。
, 百拇医药
The role of transforming growth factors-β in the pathogenesis of
experimental atherosclerosis
LI Mei-Lan,XIE Zuo-Xuan,ZHENG Pei-Er,ZHANG Ai-Dong
Dept.of Internal Medicine,First Affilliated Hospital,JNUM ,Guangzhou(510632)
Abstract AIM: To study the effect of transforming growth factor-β(TGF-β) to atherosclerosis(AS).METHODS:Hyperlipoidemic model in SD-rats and rabbits were made by feeding with 10%cholesterol-containing lipid emulsion.TGF-β expression and its receptor in arteries and TGF-β serum level of these animals were detected by immunohistochemical and ELISA techniqes.AS and serum level of lipoproteins and total cholesterol were compared between rats and rabbits.RESULTS: 100% of the experimental rabbits resulted in AS with normal high density lipoprotein(HDL) serum level.Serum levels of TGF-β and HDL of rats were increased with prolonging of the experimental time but without developing of the AS.CONCLUSION: TGF-β may be effective only in reactive proliferation after arterial intima was injured by hyperlipoidemia.AS is a chronic inflammatory proliferative disease induced by abnormal lipometabolism.
, 百拇医药
MeSH Atherosclerosis;Transforming growth factor-beta;Rabbits;Rats
转化生长因子β(transforming growth factor-β,TGF-β)是一类功能广泛,作用复杂的生长因子。它能增强平滑肌细胞对血小板源性生长因子 (platelet-derived growth factor,PDGF)的应答性有丝分裂,促进c-fos,c-myc等原癌基因的表达而加速细胞的生长[1,2]。本文主要探讨在实验性高脂血症的特异情况下, TGF-β在动脉粥样硬化(atherosclerosis,AS)发生发展中的作用。
材料和方法
一、动物及分组:
封闭群SD大鼠40只(广东省卫生厅医用实验动物场提供,动物合格证号:94022)体重100 g,雌雄各半,随机分成实验组和对照组;新西兰家兔(广东省卫生厅医用实验动物场提供,动物合格证号:94022)16只,体重2.0~3.0 kg,随机分成实验组和对照组,分笼单独喂养。
, http://www.100md.com
二、实验方法:
大鼠实验组,参照文献[3]方法制备10%胆固醇脂肪乳剂,按1 mL/100 g体重每天灌胃1次,自由饮水,每周秤体重并调节剂量1次。对照组大鼠喂普通饲料,自由饮水。于实验的第15 d和第61 d,用2.5%硫贲妥钠0.2 mL/100 g体重,腹腔注射待麻醉后,采心血并处死动物,用Beckman CX-5型全自动生化分析仪检测血清总胆固醇(TC),HDL,LDL等,并保留血清作ELISA检测TGF-β。兔实验组,参照文献[4]方法在暨南大学医用动物所制备高脂饲料,喂养6周,对照组喂普通饲料,实验第15 d和第42 d,经耳中动脉采血,与大鼠血同批检测相同项目。第42 d处死家兔。剖开大鼠和兔各组动物的心和血管,10%福尔马林液固定,脂肪染色,在脂肪染色阳性处和在主动脉弓、上胸主动脉、下胸主动脉和腹主动脉处分别切取组织作石蜡包埋切片,做HE和TGF-β1、β2、β3和TGF-β1受体等免疫组化染色。
, http://www.100md.com
三、免疫组织化学:
组织切片厚4 μm,微波5 min,兔抗TGF-β1(SC-146)、β2(SC-90)、β3(SC-82)及兔抗TGF-βR1(SC-398)等(购自北京中山公司)1∶100,用LSAB法进行免疫染色(LSAB试剂盒为DAKO公司产品)。
四、ELISA检测:
96孔酶标板德国greiner公司产品,各组动物血清用pH 9.0碳酸钠溶液等倍稀释为1/10,1/20,1/40,1/80等4个浓度包被。一抗TGF-β1、β2、β3同免疫组化产品1∶100。二抗生物素化山羊抗兔IgG(Sigma公司产品)1∶200。三抗SABC(便用型,博士德公司产品)1∶100,TMB试剂盒北京中山公司提供。用二蒸水或分别撤消一,二,三抗和TMB等作阴性对照。各步充分洗涤,终止显色后,用酶联免疫吸附分析仪(EL311s,Bio-Tek-instrumentsINC,USA)波长450 nm,最低线0.111,测吸收值(OD)。
, 百拇医药
五、数据处理:
数据以均数±标准差(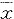 ±s)表示,各组兔给药前后比较采用配对资料比较t检验,各组鼠之间比较用两样本均数比较的t检验。
±s)表示,各组兔给药前后比较采用配对资料比较t检验,各组鼠之间比较用两样本均数比较的t检验。
结果
一、 心脏,血管的形态学观察:
实验组家兔8只的血管内膜均可见不同程度的淡黄色斑块,以主动脉弓、腹主动脉及肾主动脉分叉处较明显,脂肪染色显出明确的红色斑块,组织切片HE染色,动脉内膜弥漫增厚,有的呈丘状突向管腔,内膜下有较多泡沫细胞和少量成纤维细胞及胶原(图1)。冠状动脉和心肌内血管内膜增厚更严重并纤维化、玻璃样变、管腔闭塞(图2)。实验组大鼠20只和所有对照组家兔及大鼠的冠状血管及主动脉等的内膜光滑、未见明显异常,脂肪染色阴性,HE染色动脉各层结构清楚完好。
, http://www.100md.com
Fig 1 The AS plaque of aorta abdominalis of rabbit after 42 d with hypercholesterol feeding,The plaque had essentially monocytes/macrophages\foam cells and fibroblasts under intimal membrane,and protruded to lumen of the vellel.HE 12.6×10
图1 高脂饲料喂养42 d后家兔腹主动脉内膜的AS斑块
Fig 2 The AS plaque of arteriole inside the cardia muscle of rabbit after 42 d with hypercholesterol feeding,The vascular wall thicken seriously with fibrosis and hyaline degeneration,which occluded the lumen of vessel.HE 12.6×10
, http://www.100md.com
图2 高脂饲料喂养42 d后家兔心肌内动脉内膜的AS斑块
二、免疫组织化学检测结果:
心肌细胞、血管平滑肌细胞、血管内皮细胞、成纤维细胞、棕色脂肪细胞等的TGF-β1、β2、β3和TGF-βR1免疫染色均阳性,胶原纤维和弹力纤维则阴性。TGF-β1、β2、β3和TGF-βR1的阳性产物分布基本相同,位于核周的胞浆中(图3)。上述免疫标志的免疫染色强度,在大鼠对照组和实验组间无明显差别。
Fig 3 The positive reaction of smooth muscle cells,endothelial cells,fibroblasts and brown lipocytes in aorta thoracalis of control SD rat for TGF-βs immunostaning,the elastic fiber and collagen was negative.LSAB immunostaining 12.6×10
, http://www.100md.com
图3 对照组SD大鼠胸主动脉0的TGF-βs免疫染色
三、各组兔和大鼠血脂及脂蛋白含量比较:见表1。
表1 家兔和大鼠血脂及脂蛋白含量比较
Tab 1 Quantitative comparison of lipoidemia and lipoproteins between rats and rabbits(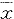 ±s)
±s)
Group
TC(nmol/L)
TG(nmol/L)
, 百拇医药
HDL(nmol/L)
AI#
Experiment rabbit (n=8,42 d)
23.33±0.47
2.12±0.26
1.46±0.08
16.40±0.88*
rat(n=10,15d)
10.90±0.60
1.51±0.12
1.94±0.12
, http://www.100md.com
5.02±0.19
rat(n=10,61d)
7.09±0.72
0.19±0.00
7.61±0.42△
0.10±0.0
Control rabbit(n=8,42 d)
1.45±0.83
0.78±0.29
0.72±0.31
1.31±0.5▲
, http://www.100md.com
rat(n=10,15d)
2.32±0.25
0.83±0.05
1.25±0.03
0.87±0.13
rat(n=10,61d)
1.75±0.12
0.34±0.05
1.26±0.37
0.85±0.2
AI=atherosclerosis index;AI=(TC-HDL)/HDL,*P<0.01,vs group of rat;▲P>0.05,vs group of rat;△P<0.01,vs group of rat in 15 d
, http://www.100md.com
从表1可见,在对照组或在实验组,家兔比大鼠均有较高的动脉粥样硬化指数(atherosclerosis,AI),尤其是在实验组,第42 d兔的AI显著高于61 d大鼠的AI(P<0.01),这主要是由于家兔的HDL相对较低,而且大鼠的血清HDL在实验第61 d反而升高(P<0.01)。
四、家兔和大鼠血清TGF-βs水平在实验过程中的变化:
TGF-β1、β2、β3的免疫显色的光密度(optical density,OD),在不同稀释倍数(1/20~1/80)的兔或大鼠血清之间无明显差异(P>0.05),它们在实验过程中的变化,以平均光密度(average of optical density,AOD)为单位,列表2进行比较。从表2的数据可见:实验组动物血清中的TGF-βs水平普遍高于对照组(P<0.05);在对照组,大鼠和家兔血清中的TGF-βs都随实验时间的增长而增高,β1和β2更为显著(P<0.05),在实验组,TGF-βs虽然随实验时间延长而升高,但是,除了β2外,均无明显差异;第61 d实验组大鼠血清中的TGF-βs与第42 d实验组家兔血清中的TGF-βs水平无显著差异。
, 百拇医药
表2 兔和大鼠在实验不同时间血清TGF-βs的AOD(ELSA法)
Tab 2 AOD of TGF-βs in serum of rabbit and rat in different time of experiment(ELISA)( ±s)
±s)
Average of optical density(AOD)
Control
Experiment
Rat
15d(n=10)
, http://www.100md.com
61d(n=10)
15d(n=10)
61d(n=10)
TGF-β1
0.257±0.049
0.777±0.252#
0.840±0.253
1.931±0.354
TGF-β2
0.460±0.249
1.110±0.297△
, http://www.100md.com
1.061±0.340
1.190±0.411
TGF-β3
0.605±0.215
0.918±0.170
0.941±0.235
1.012±0.152
Rabbit
15d(n=8)
42d(n=8)
15d(n=8)
, 百拇医药
42d(n=8)
TGF-β1
0.308±0.051
0.893±0.116▲
0.645±0.3121
0.962±0.303
TGF-β2
0.552±0.102
1.150±0.354◆
0.761±0.295
, http://www.100md.com 1.276±0.167●
TGF-β3
0.696±0.091
0.965±0.161
0.773±0.225
1.056±0.138
#P<0.01,vs 15d group;△P<0.01,vs 15d group;▲P<0.01,vs 15d group;◆P<0.05,vs 15d group;●P<0.05,vs 15d group
讨论
家兔和大鼠以高胆固醇及脂类饲料喂养数周后,均可产生明显的高脂血症,数月后就能形成早期的动脉粥样硬化病变,但大鼠则较难形成[4],而且在实验性家兔动脉粥样硬化斑块中的TGF-β mRNA较正常对照组明显增加[5]。本研究利用这两种动物的生物学特性和发病特点来进一步探究TGF-β在动脉粥样硬化发生发展中的作用。结果显示在正常大鼠的心肌、血管内皮、平滑肌等细胞内均有TGF-β1、β2、β3和TGF-β受体(TGF-βR1)的表达,而且血清中的TGF-β1、β2、β3均随鼠龄的增大而升高。虽然在实验组的大鼠成功地复制出高脂血症,血清TGF-β1、β2、β3均明显高于对照组,但未见动脉粥样斑形成,这些结果表明在高脂血症的情况下,TGF-β并不引起大鼠动脉粥样斑的形成。在实验家兔组仅6周时间则100%的动物的主动脉血管和心内血管形成了明显的粥样斑,但是,其血清中的TGF-βs水平并不比实验组大鼠的高。为什么在两动物间会有此不同从本实验两种动物的血脂结果可见家兔的TC和TG明显高于大鼠,相反,HDL则显著低于大鼠,而造成家兔的AI大于大鼠,即是说在同样饮食的情况下,家兔敏感性高、发生AS的危险性大。根据Liao F等[6]研究发现对食物诱导的动脉粥样硬化早期病变的敏感性是由于它们氧化修饰低密度脂蛋白(OLDL)形成的差异,而HDL能防止LDL的氧化修饰。大鼠随着喂养高胆固醇时间的延长其血中的HDL也随着增高(从1.95nmol/L增高至7.61nmol/L),这可能与其不易发生动脉粥样硬化早期病变有关。但是家兔血HDL并不随血总胆固醇的升高而增高或增加不明显,因此其血管内皮细胞极易受到OLDL的损害而形成AS的早期病变,即:单核细胞趋化浸润、泡沫细胞形成等,继而平滑肌细胞和成纤维细胞增生形成AS斑块,上述分析表明TGF-β在血管内皮细胞损伤后的炎性增生反应过程中才起作用,在AS斑块中TGF-β mRNA明显增加[5],可能是血管内皮损伤后的事件。近已发现TGF-β有活性和无活性两种存在形式,在炎症性纤维化的发生过程中,在蛋白裂解酶的作用下,存在于正常细胞中的无活性TGF-β转变为有活性TGF-β,并随病变的进展而增加。这些活化的TGF-β能趋化单核细胞、促进成纤维细胞的增生、移动和合成胶原及纤维粘连蛋白,后者又能抑制胶原的降解,对纤维化的发生发展起关键的作用[7]。因此可以认为,如果血管内皮细胞尚未受到OLDL损害,在正常大鼠,或即使是在实验组大鼠的心肌、血管平滑肌、棕色脂肪细胞和成纤维细胞等细胞中的TGF-β是无活性的。本结果进一步表明AS是一类脂质代谢异常引起血管内皮细胞损伤后的一种血管慢性炎症性增生性疾病。
, 百拇医药
参考文献
1 Ross R.The pathogenesis of atherosclerosis a perspective for 1990's.Nature,1993,362:801.
2 Massague J,Like B.The TGF-β family and its composite receptors.Trends in cell biology, 1994,4:172.
3 刘 明,董超仁,苏静怡.一种简便实用的大鼠高脂血症模型.中国药理学通报,1989,5(2): 121.
4 吴葆杰,张世玲.调血脂药及抗动脉硬化药筛选法.见:徐叔云主编.药理实验方法学.第1版.北京:人民卫生出版社,1985.1047~1051.
5 汤乃梅,孙士勇,柯碧波,等.转化生长因子β基因在某些疾病中的表达.生物化学杂志, 1994,10(1):30.
, http://www.100md.com
6 Liao F,Berliner JA.Minmally modified low density lipoprotein is the biologically active in vivo in mice.J Clin Invest, 1991,87:2253.
7 Mitchell NR,Cotran RS.Tissue repair:cellular growth,fibrosis,and wound healing.In: Cotran RS,Kumar V,Collins T.eds.Robbins pathologic basic of disease.6th ed.W.B.Saunders Company,1999.98.
(1999年3月31日收稿,1999年9月10日修回), 百拇医药
单位:李梅兰 张爱东:暨南大学医学院第一附属医院心内科(广州 510632);谢作煊 郑佩娥:病理学教研室
关键词:动脉硬化;转化生长因子-β;兔;大鼠
转化生长因子β 摘要 目的:研究TGF-β与动脉粥样硬化形成的关系。方法:用10%胆固醇脂肪乳剂复制大鼠和家兔的高脂血症模型,免疫组织化学和ELISA等技术检测其动脉和周围血的TGF-β1、β2、β3及其受体,观察比较两种动物动脉粥样硬化形成的情况和血清中的脂蛋白及总胆固醇水平。结果:实验组家兔100%形成动脉粥样斑,血清高密度脂蛋白在正常范围;实验组大鼠未见动脉粥样斑形成,但其血TGF-β和高密度脂蛋白随实验时间(鼠龄)的延长而升高。结论:TGF-β可能在动脉内膜被高脂血症损伤后的炎性增生反应过程中起作用。
, 百拇医药
The role of transforming growth factors-β in the pathogenesis of
experimental atherosclerosis
LI Mei-Lan,XIE Zuo-Xuan,ZHENG Pei-Er,ZHANG Ai-Dong
Dept.of Internal Medicine,First Affilliated Hospital,JNUM ,Guangzhou(510632)
Abstract AIM: To study the effect of transforming growth factor-β(TGF-β) to atherosclerosis(AS).METHODS:Hyperlipoidemic model in SD-rats and rabbits were made by feeding with 10%cholesterol-containing lipid emulsion.TGF-β expression and its receptor in arteries and TGF-β serum level of these animals were detected by immunohistochemical and ELISA techniqes.AS and serum level of lipoproteins and total cholesterol were compared between rats and rabbits.RESULTS: 100% of the experimental rabbits resulted in AS with normal high density lipoprotein(HDL) serum level.Serum levels of TGF-β and HDL of rats were increased with prolonging of the experimental time but without developing of the AS.CONCLUSION: TGF-β may be effective only in reactive proliferation after arterial intima was injured by hyperlipoidemia.AS is a chronic inflammatory proliferative disease induced by abnormal lipometabolism.
, 百拇医药
MeSH Atherosclerosis;Transforming growth factor-beta;Rabbits;Rats
转化生长因子β(transforming growth factor-β,TGF-β)是一类功能广泛,作用复杂的生长因子。它能增强平滑肌细胞对血小板源性生长因子 (platelet-derived growth factor,PDGF)的应答性有丝分裂,促进c-fos,c-myc等原癌基因的表达而加速细胞的生长[1,2]。本文主要探讨在实验性高脂血症的特异情况下, TGF-β在动脉粥样硬化(atherosclerosis,AS)发生发展中的作用。
材料和方法
一、动物及分组:
封闭群SD大鼠40只(广东省卫生厅医用实验动物场提供,动物合格证号:94022)体重100 g,雌雄各半,随机分成实验组和对照组;新西兰家兔(广东省卫生厅医用实验动物场提供,动物合格证号:94022)16只,体重2.0~3.0 kg,随机分成实验组和对照组,分笼单独喂养。
, http://www.100md.com
二、实验方法:
大鼠实验组,参照文献[3]方法制备10%胆固醇脂肪乳剂,按1 mL/100 g体重每天灌胃1次,自由饮水,每周秤体重并调节剂量1次。对照组大鼠喂普通饲料,自由饮水。于实验的第15 d和第61 d,用2.5%硫贲妥钠0.2 mL/100 g体重,腹腔注射待麻醉后,采心血并处死动物,用Beckman CX-5型全自动生化分析仪检测血清总胆固醇(TC),HDL,LDL等,并保留血清作ELISA检测TGF-β。兔实验组,参照文献[4]方法在暨南大学医用动物所制备高脂饲料,喂养6周,对照组喂普通饲料,实验第15 d和第42 d,经耳中动脉采血,与大鼠血同批检测相同项目。第42 d处死家兔。剖开大鼠和兔各组动物的心和血管,10%福尔马林液固定,脂肪染色,在脂肪染色阳性处和在主动脉弓、上胸主动脉、下胸主动脉和腹主动脉处分别切取组织作石蜡包埋切片,做HE和TGF-β1、β2、β3和TGF-β1受体等免疫组化染色。
, http://www.100md.com
三、免疫组织化学:
组织切片厚4 μm,微波5 min,兔抗TGF-β1(SC-146)、β2(SC-90)、β3(SC-82)及兔抗TGF-βR1(SC-398)等(购自北京中山公司)1∶100,用LSAB法进行免疫染色(LSAB试剂盒为DAKO公司产品)。
四、ELISA检测:
96孔酶标板德国greiner公司产品,各组动物血清用pH 9.0碳酸钠溶液等倍稀释为1/10,1/20,1/40,1/80等4个浓度包被。一抗TGF-β1、β2、β3同免疫组化产品1∶100。二抗生物素化山羊抗兔IgG(Sigma公司产品)1∶200。三抗SABC(便用型,博士德公司产品)1∶100,TMB试剂盒北京中山公司提供。用二蒸水或分别撤消一,二,三抗和TMB等作阴性对照。各步充分洗涤,终止显色后,用酶联免疫吸附分析仪(EL311s,Bio-Tek-instrumentsINC,USA)波长450 nm,最低线0.111,测吸收值(OD)。
, 百拇医药
五、数据处理:
数据以均数±标准差(
结果
一、 心脏,血管的形态学观察:
实验组家兔8只的血管内膜均可见不同程度的淡黄色斑块,以主动脉弓、腹主动脉及肾主动脉分叉处较明显,脂肪染色显出明确的红色斑块,组织切片HE染色,动脉内膜弥漫增厚,有的呈丘状突向管腔,内膜下有较多泡沫细胞和少量成纤维细胞及胶原(图1)。冠状动脉和心肌内血管内膜增厚更严重并纤维化、玻璃样变、管腔闭塞(图2)。实验组大鼠20只和所有对照组家兔及大鼠的冠状血管及主动脉等的内膜光滑、未见明显异常,脂肪染色阴性,HE染色动脉各层结构清楚完好。

, http://www.100md.com
Fig 1 The AS plaque of aorta abdominalis of rabbit after 42 d with hypercholesterol feeding,The plaque had essentially monocytes/macrophages\foam cells and fibroblasts under intimal membrane,and protruded to lumen of the vellel.HE 12.6×10
图1 高脂饲料喂养42 d后家兔腹主动脉内膜的AS斑块

Fig 2 The AS plaque of arteriole inside the cardia muscle of rabbit after 42 d with hypercholesterol feeding,The vascular wall thicken seriously with fibrosis and hyaline degeneration,which occluded the lumen of vessel.HE 12.6×10
, http://www.100md.com
图2 高脂饲料喂养42 d后家兔心肌内动脉内膜的AS斑块
二、免疫组织化学检测结果:
心肌细胞、血管平滑肌细胞、血管内皮细胞、成纤维细胞、棕色脂肪细胞等的TGF-β1、β2、β3和TGF-βR1免疫染色均阳性,胶原纤维和弹力纤维则阴性。TGF-β1、β2、β3和TGF-βR1的阳性产物分布基本相同,位于核周的胞浆中(图3)。上述免疫标志的免疫染色强度,在大鼠对照组和实验组间无明显差别。

Fig 3 The positive reaction of smooth muscle cells,endothelial cells,fibroblasts and brown lipocytes in aorta thoracalis of control SD rat for TGF-βs immunostaning,the elastic fiber and collagen was negative.LSAB immunostaining 12.6×10
, http://www.100md.com
图3 对照组SD大鼠胸主动脉0的TGF-βs免疫染色
三、各组兔和大鼠血脂及脂蛋白含量比较:见表1。
表1 家兔和大鼠血脂及脂蛋白含量比较
Tab 1 Quantitative comparison of lipoidemia and lipoproteins between rats and rabbits(
Group
TC(nmol/L)
TG(nmol/L)
, 百拇医药
HDL(nmol/L)
AI#
Experiment rabbit (n=8,42 d)
23.33±0.47
2.12±0.26
1.46±0.08
16.40±0.88*
rat(n=10,15d)
10.90±0.60
1.51±0.12
1.94±0.12
, http://www.100md.com
5.02±0.19
rat(n=10,61d)
7.09±0.72
0.19±0.00
7.61±0.42△
0.10±0.0
Control rabbit(n=8,42 d)
1.45±0.83
0.78±0.29
0.72±0.31
1.31±0.5▲
, http://www.100md.com
rat(n=10,15d)
2.32±0.25
0.83±0.05
1.25±0.03
0.87±0.13
rat(n=10,61d)
1.75±0.12
0.34±0.05
1.26±0.37
0.85±0.2
AI=atherosclerosis index;AI=(TC-HDL)/HDL,*P<0.01,vs group of rat;▲P>0.05,vs group of rat;△P<0.01,vs group of rat in 15 d
, http://www.100md.com
从表1可见,在对照组或在实验组,家兔比大鼠均有较高的动脉粥样硬化指数(atherosclerosis,AI),尤其是在实验组,第42 d兔的AI显著高于61 d大鼠的AI(P<0.01),这主要是由于家兔的HDL相对较低,而且大鼠的血清HDL在实验第61 d反而升高(P<0.01)。
四、家兔和大鼠血清TGF-βs水平在实验过程中的变化:
TGF-β1、β2、β3的免疫显色的光密度(optical density,OD),在不同稀释倍数(1/20~1/80)的兔或大鼠血清之间无明显差异(P>0.05),它们在实验过程中的变化,以平均光密度(average of optical density,AOD)为单位,列表2进行比较。从表2的数据可见:实验组动物血清中的TGF-βs水平普遍高于对照组(P<0.05);在对照组,大鼠和家兔血清中的TGF-βs都随实验时间的增长而增高,β1和β2更为显著(P<0.05),在实验组,TGF-βs虽然随实验时间延长而升高,但是,除了β2外,均无明显差异;第61 d实验组大鼠血清中的TGF-βs与第42 d实验组家兔血清中的TGF-βs水平无显著差异。
, 百拇医药
表2 兔和大鼠在实验不同时间血清TGF-βs的AOD(ELSA法)
Tab 2 AOD of TGF-βs in serum of rabbit and rat in different time of experiment(ELISA)(
Average of optical density(AOD)
Control
Experiment
Rat
15d(n=10)
, http://www.100md.com
61d(n=10)
15d(n=10)
61d(n=10)
TGF-β1
0.257±0.049
0.777±0.252#
0.840±0.253
1.931±0.354
TGF-β2
0.460±0.249
1.110±0.297△
, http://www.100md.com
1.061±0.340
1.190±0.411
TGF-β3
0.605±0.215
0.918±0.170
0.941±0.235
1.012±0.152
Rabbit
15d(n=8)
42d(n=8)
15d(n=8)
, 百拇医药
42d(n=8)
TGF-β1
0.308±0.051
0.893±0.116▲
0.645±0.3121
0.962±0.303
TGF-β2
0.552±0.102
1.150±0.354◆
0.761±0.295
, http://www.100md.com 1.276±0.167●
TGF-β3
0.696±0.091
0.965±0.161
0.773±0.225
1.056±0.138
#P<0.01,vs 15d group;△P<0.01,vs 15d group;▲P<0.01,vs 15d group;◆P<0.05,vs 15d group;●P<0.05,vs 15d group
讨论
家兔和大鼠以高胆固醇及脂类饲料喂养数周后,均可产生明显的高脂血症,数月后就能形成早期的动脉粥样硬化病变,但大鼠则较难形成[4],而且在实验性家兔动脉粥样硬化斑块中的TGF-β mRNA较正常对照组明显增加[5]。本研究利用这两种动物的生物学特性和发病特点来进一步探究TGF-β在动脉粥样硬化发生发展中的作用。结果显示在正常大鼠的心肌、血管内皮、平滑肌等细胞内均有TGF-β1、β2、β3和TGF-β受体(TGF-βR1)的表达,而且血清中的TGF-β1、β2、β3均随鼠龄的增大而升高。虽然在实验组的大鼠成功地复制出高脂血症,血清TGF-β1、β2、β3均明显高于对照组,但未见动脉粥样斑形成,这些结果表明在高脂血症的情况下,TGF-β并不引起大鼠动脉粥样斑的形成。在实验家兔组仅6周时间则100%的动物的主动脉血管和心内血管形成了明显的粥样斑,但是,其血清中的TGF-βs水平并不比实验组大鼠的高。为什么在两动物间会有此不同从本实验两种动物的血脂结果可见家兔的TC和TG明显高于大鼠,相反,HDL则显著低于大鼠,而造成家兔的AI大于大鼠,即是说在同样饮食的情况下,家兔敏感性高、发生AS的危险性大。根据Liao F等[6]研究发现对食物诱导的动脉粥样硬化早期病变的敏感性是由于它们氧化修饰低密度脂蛋白(OLDL)形成的差异,而HDL能防止LDL的氧化修饰。大鼠随着喂养高胆固醇时间的延长其血中的HDL也随着增高(从1.95nmol/L增高至7.61nmol/L),这可能与其不易发生动脉粥样硬化早期病变有关。但是家兔血HDL并不随血总胆固醇的升高而增高或增加不明显,因此其血管内皮细胞极易受到OLDL的损害而形成AS的早期病变,即:单核细胞趋化浸润、泡沫细胞形成等,继而平滑肌细胞和成纤维细胞增生形成AS斑块,上述分析表明TGF-β在血管内皮细胞损伤后的炎性增生反应过程中才起作用,在AS斑块中TGF-β mRNA明显增加[5],可能是血管内皮损伤后的事件。近已发现TGF-β有活性和无活性两种存在形式,在炎症性纤维化的发生过程中,在蛋白裂解酶的作用下,存在于正常细胞中的无活性TGF-β转变为有活性TGF-β,并随病变的进展而增加。这些活化的TGF-β能趋化单核细胞、促进成纤维细胞的增生、移动和合成胶原及纤维粘连蛋白,后者又能抑制胶原的降解,对纤维化的发生发展起关键的作用[7]。因此可以认为,如果血管内皮细胞尚未受到OLDL损害,在正常大鼠,或即使是在实验组大鼠的心肌、血管平滑肌、棕色脂肪细胞和成纤维细胞等细胞中的TGF-β是无活性的。本结果进一步表明AS是一类脂质代谢异常引起血管内皮细胞损伤后的一种血管慢性炎症性增生性疾病。
, 百拇医药
参考文献
1 Ross R.The pathogenesis of atherosclerosis a perspective for 1990's.Nature,1993,362:801.
2 Massague J,Like B.The TGF-β family and its composite receptors.Trends in cell biology, 1994,4:172.
3 刘 明,董超仁,苏静怡.一种简便实用的大鼠高脂血症模型.中国药理学通报,1989,5(2): 121.
4 吴葆杰,张世玲.调血脂药及抗动脉硬化药筛选法.见:徐叔云主编.药理实验方法学.第1版.北京:人民卫生出版社,1985.1047~1051.
5 汤乃梅,孙士勇,柯碧波,等.转化生长因子β基因在某些疾病中的表达.生物化学杂志, 1994,10(1):30.
, http://www.100md.com
6 Liao F,Berliner JA.Minmally modified low density lipoprotein is the biologically active in vivo in mice.J Clin Invest, 1991,87:2253.
7 Mitchell NR,Cotran RS.Tissue repair:cellular growth,fibrosis,and wound healing.In: Cotran RS,Kumar V,Collins T.eds.Robbins pathologic basic of disease.6th ed.W.B.Saunders Company,1999.98.
(1999年3月31日收稿,1999年9月10日修回), 百拇医药