双位点核酶对2.2.15细胞中HBV基因表达抑制作用
作者:李谨革 周永兴 连建奇 贾战生 冯志华 白宪光
单位:(第四军医大学唐都医院传染科, 陕西 西安 710038)
关键词:RNA,催化;基因治疗;肝炎病毒,乙型
中国病理生理杂志000906 [摘 要] 目的: 观察针对HBV C区双位点核酶在细胞内阻断C区基因表达的作用。方法: 采用亚克隆技术,从pGEM-Rz123(含针对HBV C区双位点核酶)上切下双位点核酶的片段,定向克隆于真核表达载体pBBS212中。利用lipofectamine介导,将重组质粒pBBS212-Rz及pBBS212转染2.2.15细胞中,采用打点杂交技术观察核酶的表达,采用ELISA、免疫荧光、免疫组化、图象分析法、Western blot分析HBe/HBcAg及HBsAg的表达。结果: 转染的2.2.15细胞经潮霉素B和G418筛选2周后,打点杂交证实可表达针对HBV C 区双位点核酶。ELISA方法检测发现核酶抑制HBeAg表达48.6%,用免疫荧光、免疫组化、图象分析法、Western blot分析证实核酶可抑制HBV细胞内表达。 结论: 该双位点核酶通过针对HBV C区基因的剪切作用,阻断C区基因表达,抑制了HBe/HBcAg的表达。
, http://www.100md.com
[中图分类号] R512.6+2 Q344+.13 [文献标识码] A
[文章编号] 1000-4718(2000)09-0792-05
Two-unit ribozyme inhibit hepatitis B virus expressed in 2.2.15 cell
LI Jin-ge, ZHOU Yong-xing, LIAN Jian-qi, JIA Zhan-sheng, FENG Zhi-hua, BAI Xian-guang
(Tangdu Infections Disease Hospital ,The Fourth Military Medical University,Xian 710038, China)
, 百拇医药
[Abstract] AIM: To observe the inhibition of HBc/HBeAg expression in the 2.2.15 cell transfected by two-unit ribozyme. METHODS: By use of subclone technique, two-unit ribozyme gene which was cutted from pGEM-Rz123 was ligated into the eukaryotic expression vector pBBS212. The recombinant plasmid was cotransfected into 2.2.15 cell using lipofectamine. Ribozyme was detected by dot-blot hybridization. The s and e/c antigen of HBV were detected by using ELISA, immunohistochemical technique, image analysis system and Western blot. RESULTS: After the transfected cell was selected two weeks by hygromycin B and G418. We found by dot-blot hybridization that ribozyme can express on 2.2.15 cell. HBeAg level can be reduced by 48.6% in the transfected 2.2.15 cell with two-ribozyme. Using immunohistochemical technique and image analysis system, Western blot, we observed that the level of HBcAg expressed in endocellular went down. CONCLUSION: All these results strongly indicate that two-unit ribozyme can inhibit hepatitis B virus expression in the cell.
, http://www.100md.com
[MeSH] RNA, catalyticl; Gene therapy; Hepatitis B virus
乙型肝炎病毒(hepatitis B virus, HBV)是乙型肝炎的病原体,HBV幼年感染后可出现机体的免疫耐受和病毒基因变异等问题,造成传统的抗病毒药物疗效欠佳,寻找新型抗病毒药物成为迫切需要。核酶(ribozyme, Rz),一种独特的RNA分子,可序列特异地与靶RNA配对,切割而使其失去生物功能[1] 。由于其长期使用对细胞无毒副作用,结构简单,易于人工合成,已成为一种新的分子生物学技术,广泛用于抗病毒,抗肿瘤治疗。本研究构建抗HBV C区2029~31及2063~65位点的双位点核酶的真核表达载体,利用脂质体转染2.2.15细胞,在细胞内观察核酶对HBV基因表达的抑制作用。
材 料 和 方 法
一、 质粒、宿主菌和细胞
, 百拇医药
2.2.15细胞购自军事医学科学院,E coli JM 109为本室保存,pBBS212由全军消化研究所郭建成博士惠赠。
二、 试剂
DMEM为GIBCO公司产品,潮霉素B(hygromycin B)为Sigma公司产品,T4DNA连接酶为Promaga公司产品,各种工具酶购自华美公司。HBsAg、HBeAg酶联检测盒为科华公司产品,鼠抗HBc为DAKO公司产品,免疫组化试剂盒购自博士德公司,进口胎牛血清为GIBCO公司产品。
三、 Ribozyme的设计与合成
根据甘人宝等发表的HBV adr亚型序列,采用上海生物化学研究所陈农安编写的ribozyme设计软件,设计两个44bp的锤头状ribozyme用pc Fold软件进行能量预测[2],用DNA合成仪合成DNA,两端分别为BamH I和 EcoR I酶切粘末端(核酶序列见图1)。
, http://www.100md.com
Fig 1 Sequencing of the ribozyme and the target mRNA of HBV gene.
图1 Rz及靶mRNA的核苷酸序列
四、 质粒构建
将两个核酶片段先后分别克隆于pGEM-7z中,构成pGEMRz123,将pGEMRz123及真核表达载体pBBS212均用EcoR I及BamH I进行双酶切,分别回收88 bp 及10535 bp片段,用双粘法进行连接[3] 。连接产物转化JM109菌,挑取克隆,用EcoR I及BamH I、Kpn I 及Hind Ⅲ对筛选重组体进行酶切鉴定,用聚丙烯酰胺凝胶电泳(见图2)。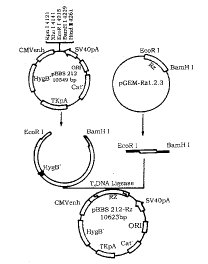
Fig 2 Diagram of the construction of expression vector of pBBS212-Rz.
, http://www.100md.com
图2 pBBS212-Rz真核表达载体构建流程图
五、 含核酶真核表达载体pBBS212-Rz的转染
2.2.15 细胞在6孔培养板中,用含10%胎牛血清的1×DMEM,在37℃ 5% CO2条件下培养至细胞密度为60%~80%。采用脂质体介导基因转染的方法(按产品说明书操作)。准备溶液A:于100 μL无血清DMEM液中加6μg pBBS212-Rz或pBBS212。准备溶液B:于85 μL无血清DMEM液中加15 μL脂质体,轻轻混匀A、B液,室温放置35 min,补足1 mL无血清DMEM,加入用DMEM洗过两次的细胞单层上,37℃ 5% CO2 条件下培养18 h。换用10%胎牛血清的培养基,37℃ 5% CO2条件下培养48 h,按1∶4传代,加含200 μL/ mL潮霉素B及170 μg/mL G418的培养基进行筛选,直到筛选出阳性克隆,再扩增培养。
, 百拇医药
六、 HBsAg 、HBeAg的测定
用科华ELISA检测试剂盒检测细胞培养上清,OD值在A450下读取,结果以阳性孔A值/阴性孔A值(P/N)表示,抑制率按下式计算:
七、 转染细胞中ribozyme的测定
ribozyme探针为人工合成的寡核苷酸,用T4多核苷酸激酶进行[32P]末端标记而成。收集培养细胞,用总RNA分离试剂盒(Promega产品)抽提细胞总RNA。采用打点杂交技术测定转染细胞中ribozyme。
八、 测定细胞中HBcAg/HBeAg的表达
转染后的2.2.15细胞爬片后经丙酮固定,常规间接免疫荧光、免疫组织化学染色,显微镜下观察拍片。
, 百拇医药
九、 Western印迹分析
2.2.15细胞经裂解、电转移、封闭、与第一抗体、与第二抗体反应。抗HBe抗体来源病人血清,第二抗体购自华美公司。按文献[4]进行。
结 果
一、含核酶真核表达载体pBBS212-Rz的构建
经酶切、连接、转化后筛选出阳性克隆pBBS212-Rz,用EcoR I及BamH I、Kpn I 及Hind Ⅲ酶切鉴定,可分别切出88及214片段。电泳可见一清晰条带(见图3)。
Fig 3 Identification of recombinant done by retriction enzyme.
, 百拇医药
1. Fragments of 214bp digested with Kpn I+Hind Ⅲ; 2. pGEM-7zf(+) /HeaⅢ Markers; 3. Fragments of 88 bp digested with BamH I + EcoR I.
图3 pBBS212-Rz重组质粒限制性内切酶酶切分析
二、转染细胞中ribozyme的表达
在转染pBBS212及pBBS212-Rz的细胞中,核酶在pBBS212-Rz组中有表达,而在pBBS212组中为阴性(见图4)。
Fig 4 Expression of ribozyme mRNA in transfected cells.
, 百拇医药
A: pBBS212-Rz group; B: pBBS212 group.
图4 转染2.2.15细胞ribozyme的mRNA 表达
三、在转染的2.2.15细胞中,核酶对HBeAg、HBsAg作用
将样品共分4组(含空载质粒转染组),每组分取4份样品。由表1及表2可以看出针对HBV C区基因的双位点核酶对细胞内的HBeAg表达有明显的抑制作用,最高为48.6%。同时发现对HBsAg无明显的抑制作用。
表1 针对HBV C区基因的双位点核酶对2.2.15
细胞内HBeAg的作用
Tab 1 Comparison of HBeAg in the transfected 2.2.15 cell ( ±s) Group
±s) Group
, 百拇医药
P/N value
Inhibition rate
PBBS212 group
15.90±0.53
PBBS212-Rz group Ⅰ
9.26±0.56
48.1%
PBBS212-Rz group Ⅱ
10.01 ±1.13
42.7%
PBBS212-Rz group Ⅲ
, 百拇医药
9.20±0.49
48.6%
表2 针对HBV C区基因的双位点核酶对2.2.15
细胞内HBsAg的作用
Tab 2 Comparison of HBsAg in the transfected 2.2.15 cell ( ±s) Group
±s) Group
P/N value
Inhibition rate
PBBS212 group
18.92±2.16
, http://www.100md.com
PBBS212-Rz group Ⅰ
18.28±2.01
3.8%
PBBS212-Rz group Ⅱ
18.52±2.16
2.4%
PBBS212-Rz group Ⅲ
18.95±2.42
-0.1%
表3 转染细胞免疫组化图象分析结果
Tab 3 Image analysis the transfected 2.2.15 cell Group
, 百拇医药
Ⅰ
Ⅱ
Ⅲ
Ⅳ
Ⅴ
pBBS212
group
177±6
173±10
161±6
180±4
176±7
pBBS212-Rz
, http://www.100md.com
group
220±10
207±4
217±10
212±6
198±6
P<0.01, pBBS212-Rz group vs pBBS212 group.
四、免疫荧光、免疫组化及图象分析结果(见图5、图6)
Fig 5 Immunofluorescence of transfected 2.2.15 cell.
, http://www.100md.com
A: pBBS212 group; B: pBBS212-Rz group.
图5 转染后2.2.15细胞免疫荧光图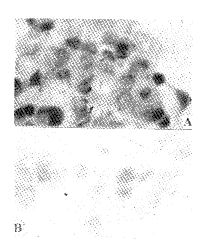
Fig 6 Immunohistochemistry of transfected 2.2.15 cell.
A: pBBS212 group; B: pBBS212-Rz group.
图6 转染后2.2.15细胞免疫组化图
pBBS212及pBBS212-Rz转染2.2.15细胞后,细胞经荧光及组化染色后发现pBBS212-Rz转染组的细胞中HBeAg/HBcAg的表达量明显下降。
, http://www.100md.com
将上两组转染细胞各取五份标本,组化染色,每份在200倍镜下随机选择50个细胞,计算胞浆所表达HBcAg染色之灰度。列表如下,结果表明转染核酶组细胞HBcAg表达受到明显抑制。
五、 Western印迹结果
将pBBS212及pBBS212-Rz转染2.2.15细胞后,用抗HBe抗体进行Western印迹分析证实(图7)转染细胞可表达HBeAg,同时核酶有抑制HBeAg表达的作用。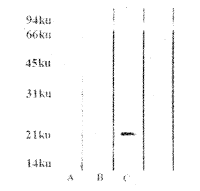
Fig 7 Western blotting of HBeAg.
A: Marker; B: pBBS212-Rz group; C: pBBS212 group.
图 7 HBeAg Western 印迹结果
, 百拇医药
讨 论
典型的乙型肝炎病毒复制过程包括病毒脱衣壳、核酸进入细胞内,经过补缺口形成双链DNA,由细胞的RNA多聚酶参与下转录成多拷贝的3.5kb RNA, 以此为模板,通过逆转录合成负链DNA[5]。其逆转录是关键环节。而且C区表达蛋白可使正常宿主细胞基因表达发生紊乱,同时是CTL作用的靶位点。由此C区mRNA成为我们研究的重点。
多位点核酶系分别针对靶RNA的不同位点设计核酶,以达到在多个不同的位点破坏靶RNA。这既可避免病毒变异造成的单一核酶切割作用的丧失,也可避免结合蛋白掩盖切割位点,从而进一步提高核酶阻断靶基因的效率。体外切割证明我们合成核酶均有切割活性,双位点核酶联合有协同作用,切割效率达80%。
1992年Weizsaker使用3个联结型核酶,离体研究结果表明对HBV的转录物切割作用明显[6]。1995年Beck等构建切割HBV中高度保守的顺式作用元件(包装信号ε)的锤头型核酶,离体切割有效,但在细胞内未能有效地抑制靶RNA水平[7]。1997年Welch则使用3个发夹状核酶,通过逆转录病毒载体导入Huh7细胞,与HBV共表达,结果使病毒颗粒下降66%-83%[8]。国内学者也有类似报道,如王平、竺来发等[9,10]。
, 百拇医药
我们于1995年设计并构建了针对HBV C区的多个核酶,离体切割达80%,进一步在细胞内应用,打点杂交证实转染细胞中有核酶表达,用ELISA方法检测发现核酶使细胞内HBeAg的表达明显下降,抑制率达48.6%。同时我们使用免疫荧光、组化、图像分析及Western blot的方法,结果均证实该双位点核酶可有效地抑制HBV C区基因表达。
由于HBV感染的动物和细胞模型建立十分困难,尤其是细胞的感染模型,于是人们就利用HBV DNA的转染细胞系代替,常见的细胞模型就是2.2.15细胞,我们的研究正是利用这模型,但是由于感染与转染之间的差别在于有逆转录过程,因为转录模型中各种抗原的表达不依赖其逆转录过程,因此我们所用核酶对HBsAg表达不受影响。只能使HBe/HBc的翻译下降。如在感染模型则可通过对前基因组mRNA的剪切,抑制逆转录过程而达到抑制病毒复制的目的。
[基金项目] 国家自然科学基金资助(No.39570652)
, 百拇医药
Tel: 029-3577595; E-mail:didthx@fmmu.edu.cn
[参 考 文 献]
[1] Haseloff J ,Gerlach WL. Simple RNA enzymes with new and highly specific endoribonuclease activites[J]. Nature ,1988, 344: 585-591.
[2] 连建奇,周永兴,金由辛. 抗乙型肝炎病毒特异联合型核酶的体外切割作用[J]. 第四军医大学学报, 1999, 20(2): 97-101.
[3] 姜 泊,张亚历,周殿元. 分子生物学常用实验方法[M].第1版. 北京:人民军医出版社, 1996. 19-33.
, 百拇医药 [4] 卢圣栋,主编. 现代分子生物学实验技术[M]. 第1版. 北京: 高等教育出版社, 1993. 403-451.
[5] 成 军, 杨守纯. 现代肝炎分子生物学[M]. 第1版. 北京:人民军医出版社, 1997. 25-37.
[6] Weizsacker FV ,Blum HE ,Wonds JR. Cleavage of hepatitis B virus RNA by three ribozymes transcribed from a single DNA template[J]. Biochem Biophy Res Commu, 1992, 189(2): 743-748.
[7] Beck J , Nassal M . Efficient hammerhead ribozyme-mediated cleavage of the structured hepatitis B virus encapsidation signal in vitro and in cell, but not in intact cells[J]. Nucleic Acids Res , 1995, 23(24): 4962.
, 百拇医药
[8] Welch PJ , Tritz R , Yei S, et al. Intracellular application of hairpin ribozyme against hepatitis B virus[J]. Gene Ther, 1997, 4(7): 736-743.
[9] 王 平, 徐 炜, 曾力宇, 等. 核酶Ripc对HBV基因体外转录物的作用[J]. 病毒学报, 1993, 9: 278-280.
[10] 竺来发, 易荣大, 陆长德, 等. 乙型肝炎病毒adr亚型核心抗原RNA片段的体外Ribozyme定量切割[J]. 生物化学与生物物理学报, 1993, 25(3): 316-317.
[收稿日期] 1999-05-19 [修回日期] 1999-10-18, 百拇医药
单位:(第四军医大学唐都医院传染科, 陕西 西安 710038)
关键词:RNA,催化;基因治疗;肝炎病毒,乙型
中国病理生理杂志000906 [摘 要] 目的: 观察针对HBV C区双位点核酶在细胞内阻断C区基因表达的作用。方法: 采用亚克隆技术,从pGEM-Rz123(含针对HBV C区双位点核酶)上切下双位点核酶的片段,定向克隆于真核表达载体pBBS212中。利用lipofectamine介导,将重组质粒pBBS212-Rz及pBBS212转染2.2.15细胞中,采用打点杂交技术观察核酶的表达,采用ELISA、免疫荧光、免疫组化、图象分析法、Western blot分析HBe/HBcAg及HBsAg的表达。结果: 转染的2.2.15细胞经潮霉素B和G418筛选2周后,打点杂交证实可表达针对HBV C 区双位点核酶。ELISA方法检测发现核酶抑制HBeAg表达48.6%,用免疫荧光、免疫组化、图象分析法、Western blot分析证实核酶可抑制HBV细胞内表达。 结论: 该双位点核酶通过针对HBV C区基因的剪切作用,阻断C区基因表达,抑制了HBe/HBcAg的表达。
, http://www.100md.com
[中图分类号] R512.6+2 Q344+.13 [文献标识码] A
[文章编号] 1000-4718(2000)09-0792-05
Two-unit ribozyme inhibit hepatitis B virus expressed in 2.2.15 cell
LI Jin-ge, ZHOU Yong-xing, LIAN Jian-qi, JIA Zhan-sheng, FENG Zhi-hua, BAI Xian-guang
(Tangdu Infections Disease Hospital ,The Fourth Military Medical University,Xian 710038, China)
, 百拇医药
[Abstract] AIM: To observe the inhibition of HBc/HBeAg expression in the 2.2.15 cell transfected by two-unit ribozyme. METHODS: By use of subclone technique, two-unit ribozyme gene which was cutted from pGEM-Rz123 was ligated into the eukaryotic expression vector pBBS212. The recombinant plasmid was cotransfected into 2.2.15 cell using lipofectamine. Ribozyme was detected by dot-blot hybridization. The s and e/c antigen of HBV were detected by using ELISA, immunohistochemical technique, image analysis system and Western blot. RESULTS: After the transfected cell was selected two weeks by hygromycin B and G418. We found by dot-blot hybridization that ribozyme can express on 2.2.15 cell. HBeAg level can be reduced by 48.6% in the transfected 2.2.15 cell with two-ribozyme. Using immunohistochemical technique and image analysis system, Western blot, we observed that the level of HBcAg expressed in endocellular went down. CONCLUSION: All these results strongly indicate that two-unit ribozyme can inhibit hepatitis B virus expression in the cell.
, http://www.100md.com
[MeSH] RNA, catalyticl; Gene therapy; Hepatitis B virus
乙型肝炎病毒(hepatitis B virus, HBV)是乙型肝炎的病原体,HBV幼年感染后可出现机体的免疫耐受和病毒基因变异等问题,造成传统的抗病毒药物疗效欠佳,寻找新型抗病毒药物成为迫切需要。核酶(ribozyme, Rz),一种独特的RNA分子,可序列特异地与靶RNA配对,切割而使其失去生物功能[1] 。由于其长期使用对细胞无毒副作用,结构简单,易于人工合成,已成为一种新的分子生物学技术,广泛用于抗病毒,抗肿瘤治疗。本研究构建抗HBV C区2029~31及2063~65位点的双位点核酶的真核表达载体,利用脂质体转染2.2.15细胞,在细胞内观察核酶对HBV基因表达的抑制作用。
材 料 和 方 法
一、 质粒、宿主菌和细胞
, 百拇医药
2.2.15细胞购自军事医学科学院,E coli JM 109为本室保存,pBBS212由全军消化研究所郭建成博士惠赠。
二、 试剂
DMEM为GIBCO公司产品,潮霉素B(hygromycin B)为Sigma公司产品,T4DNA连接酶为Promaga公司产品,各种工具酶购自华美公司。HBsAg、HBeAg酶联检测盒为科华公司产品,鼠抗HBc为DAKO公司产品,免疫组化试剂盒购自博士德公司,进口胎牛血清为GIBCO公司产品。
三、 Ribozyme的设计与合成
根据甘人宝等发表的HBV adr亚型序列,采用上海生物化学研究所陈农安编写的ribozyme设计软件,设计两个44bp的锤头状ribozyme用pc Fold软件进行能量预测[2],用DNA合成仪合成DNA,两端分别为BamH I和 EcoR I酶切粘末端(核酶序列见图1)。

, http://www.100md.com
Fig 1 Sequencing of the ribozyme and the target mRNA of HBV gene.
图1 Rz及靶mRNA的核苷酸序列
四、 质粒构建
将两个核酶片段先后分别克隆于pGEM-7z中,构成pGEMRz123,将pGEMRz123及真核表达载体pBBS212均用EcoR I及BamH I进行双酶切,分别回收88 bp 及10535 bp片段,用双粘法进行连接[3] 。连接产物转化JM109菌,挑取克隆,用EcoR I及BamH I、Kpn I 及Hind Ⅲ对筛选重组体进行酶切鉴定,用聚丙烯酰胺凝胶电泳(见图2)。

Fig 2 Diagram of the construction of expression vector of pBBS212-Rz.
, http://www.100md.com
图2 pBBS212-Rz真核表达载体构建流程图
五、 含核酶真核表达载体pBBS212-Rz的转染
2.2.15 细胞在6孔培养板中,用含10%胎牛血清的1×DMEM,在37℃ 5% CO2条件下培养至细胞密度为60%~80%。采用脂质体介导基因转染的方法(按产品说明书操作)。准备溶液A:于100 μL无血清DMEM液中加6μg pBBS212-Rz或pBBS212。准备溶液B:于85 μL无血清DMEM液中加15 μL脂质体,轻轻混匀A、B液,室温放置35 min,补足1 mL无血清DMEM,加入用DMEM洗过两次的细胞单层上,37℃ 5% CO2 条件下培养18 h。换用10%胎牛血清的培养基,37℃ 5% CO2条件下培养48 h,按1∶4传代,加含200 μL/ mL潮霉素B及170 μg/mL G418的培养基进行筛选,直到筛选出阳性克隆,再扩增培养。
, 百拇医药
六、 HBsAg 、HBeAg的测定
用科华ELISA检测试剂盒检测细胞培养上清,OD值在A450下读取,结果以阳性孔A值/阴性孔A值(P/N)表示,抑制率按下式计算:

七、 转染细胞中ribozyme的测定
ribozyme探针为人工合成的寡核苷酸,用T4多核苷酸激酶进行[32P]末端标记而成。收集培养细胞,用总RNA分离试剂盒(Promega产品)抽提细胞总RNA。采用打点杂交技术测定转染细胞中ribozyme。
八、 测定细胞中HBcAg/HBeAg的表达
转染后的2.2.15细胞爬片后经丙酮固定,常规间接免疫荧光、免疫组织化学染色,显微镜下观察拍片。
, 百拇医药
九、 Western印迹分析
2.2.15细胞经裂解、电转移、封闭、与第一抗体、与第二抗体反应。抗HBe抗体来源病人血清,第二抗体购自华美公司。按文献[4]进行。
结 果
一、含核酶真核表达载体pBBS212-Rz的构建
经酶切、连接、转化后筛选出阳性克隆pBBS212-Rz,用EcoR I及BamH I、Kpn I 及Hind Ⅲ酶切鉴定,可分别切出88及214片段。电泳可见一清晰条带(见图3)。

Fig 3 Identification of recombinant done by retriction enzyme.
, 百拇医药
1. Fragments of 214bp digested with Kpn I+Hind Ⅲ; 2. pGEM-7zf(+) /HeaⅢ Markers; 3. Fragments of 88 bp digested with BamH I + EcoR I.
图3 pBBS212-Rz重组质粒限制性内切酶酶切分析
二、转染细胞中ribozyme的表达
在转染pBBS212及pBBS212-Rz的细胞中,核酶在pBBS212-Rz组中有表达,而在pBBS212组中为阴性(见图4)。

Fig 4 Expression of ribozyme mRNA in transfected cells.
, 百拇医药
A: pBBS212-Rz group; B: pBBS212 group.
图4 转染2.2.15细胞ribozyme的mRNA 表达
三、在转染的2.2.15细胞中,核酶对HBeAg、HBsAg作用
将样品共分4组(含空载质粒转染组),每组分取4份样品。由表1及表2可以看出针对HBV C区基因的双位点核酶对细胞内的HBeAg表达有明显的抑制作用,最高为48.6%。同时发现对HBsAg无明显的抑制作用。
表1 针对HBV C区基因的双位点核酶对2.2.15
细胞内HBeAg的作用
Tab 1 Comparison of HBeAg in the transfected 2.2.15 cell (
 ±s) Group
±s) Group, 百拇医药
P/N value
Inhibition rate
PBBS212 group
15.90±0.53
PBBS212-Rz group Ⅰ
9.26±0.56
48.1%
PBBS212-Rz group Ⅱ
10.01 ±1.13
42.7%
PBBS212-Rz group Ⅲ
, 百拇医药
9.20±0.49
48.6%
表2 针对HBV C区基因的双位点核酶对2.2.15
细胞内HBsAg的作用
Tab 2 Comparison of HBsAg in the transfected 2.2.15 cell (
 ±s) Group
±s) GroupP/N value
Inhibition rate
PBBS212 group
18.92±2.16
, http://www.100md.com
PBBS212-Rz group Ⅰ
18.28±2.01
3.8%
PBBS212-Rz group Ⅱ
18.52±2.16
2.4%
PBBS212-Rz group Ⅲ
18.95±2.42
-0.1%
表3 转染细胞免疫组化图象分析结果
Tab 3 Image analysis the transfected 2.2.15 cell Group
, 百拇医药
Ⅰ
Ⅱ
Ⅲ
Ⅳ
Ⅴ
pBBS212
group
177±6
173±10
161±6
180±4
176±7
pBBS212-Rz
, http://www.100md.com
group
220±10
207±4
217±10
212±6
198±6
P<0.01, pBBS212-Rz group vs pBBS212 group.
四、免疫荧光、免疫组化及图象分析结果(见图5、图6)

Fig 5 Immunofluorescence of transfected 2.2.15 cell.
, http://www.100md.com
A: pBBS212 group; B: pBBS212-Rz group.
图5 转染后2.2.15细胞免疫荧光图

Fig 6 Immunohistochemistry of transfected 2.2.15 cell.
A: pBBS212 group; B: pBBS212-Rz group.
图6 转染后2.2.15细胞免疫组化图
pBBS212及pBBS212-Rz转染2.2.15细胞后,细胞经荧光及组化染色后发现pBBS212-Rz转染组的细胞中HBeAg/HBcAg的表达量明显下降。
, http://www.100md.com
将上两组转染细胞各取五份标本,组化染色,每份在200倍镜下随机选择50个细胞,计算胞浆所表达HBcAg染色之灰度。列表如下,结果表明转染核酶组细胞HBcAg表达受到明显抑制。
五、 Western印迹结果
将pBBS212及pBBS212-Rz转染2.2.15细胞后,用抗HBe抗体进行Western印迹分析证实(图7)转染细胞可表达HBeAg,同时核酶有抑制HBeAg表达的作用。

Fig 7 Western blotting of HBeAg.
A: Marker; B: pBBS212-Rz group; C: pBBS212 group.
图 7 HBeAg Western 印迹结果
, 百拇医药
讨 论
典型的乙型肝炎病毒复制过程包括病毒脱衣壳、核酸进入细胞内,经过补缺口形成双链DNA,由细胞的RNA多聚酶参与下转录成多拷贝的3.5kb RNA, 以此为模板,通过逆转录合成负链DNA[5]。其逆转录是关键环节。而且C区表达蛋白可使正常宿主细胞基因表达发生紊乱,同时是CTL作用的靶位点。由此C区mRNA成为我们研究的重点。
多位点核酶系分别针对靶RNA的不同位点设计核酶,以达到在多个不同的位点破坏靶RNA。这既可避免病毒变异造成的单一核酶切割作用的丧失,也可避免结合蛋白掩盖切割位点,从而进一步提高核酶阻断靶基因的效率。体外切割证明我们合成核酶均有切割活性,双位点核酶联合有协同作用,切割效率达80%。
1992年Weizsaker使用3个联结型核酶,离体研究结果表明对HBV的转录物切割作用明显[6]。1995年Beck等构建切割HBV中高度保守的顺式作用元件(包装信号ε)的锤头型核酶,离体切割有效,但在细胞内未能有效地抑制靶RNA水平[7]。1997年Welch则使用3个发夹状核酶,通过逆转录病毒载体导入Huh7细胞,与HBV共表达,结果使病毒颗粒下降66%-83%[8]。国内学者也有类似报道,如王平、竺来发等[9,10]。
, 百拇医药
我们于1995年设计并构建了针对HBV C区的多个核酶,离体切割达80%,进一步在细胞内应用,打点杂交证实转染细胞中有核酶表达,用ELISA方法检测发现核酶使细胞内HBeAg的表达明显下降,抑制率达48.6%。同时我们使用免疫荧光、组化、图像分析及Western blot的方法,结果均证实该双位点核酶可有效地抑制HBV C区基因表达。
由于HBV感染的动物和细胞模型建立十分困难,尤其是细胞的感染模型,于是人们就利用HBV DNA的转染细胞系代替,常见的细胞模型就是2.2.15细胞,我们的研究正是利用这模型,但是由于感染与转染之间的差别在于有逆转录过程,因为转录模型中各种抗原的表达不依赖其逆转录过程,因此我们所用核酶对HBsAg表达不受影响。只能使HBe/HBc的翻译下降。如在感染模型则可通过对前基因组mRNA的剪切,抑制逆转录过程而达到抑制病毒复制的目的。
[基金项目] 国家自然科学基金资助(No.39570652)
, 百拇医药
Tel: 029-3577595; E-mail:didthx@fmmu.edu.cn
[参 考 文 献]
[1] Haseloff J ,Gerlach WL. Simple RNA enzymes with new and highly specific endoribonuclease activites[J]. Nature ,1988, 344: 585-591.
[2] 连建奇,周永兴,金由辛. 抗乙型肝炎病毒特异联合型核酶的体外切割作用[J]. 第四军医大学学报, 1999, 20(2): 97-101.
[3] 姜 泊,张亚历,周殿元. 分子生物学常用实验方法[M].第1版. 北京:人民军医出版社, 1996. 19-33.
, 百拇医药 [4] 卢圣栋,主编. 现代分子生物学实验技术[M]. 第1版. 北京: 高等教育出版社, 1993. 403-451.
[5] 成 军, 杨守纯. 现代肝炎分子生物学[M]. 第1版. 北京:人民军医出版社, 1997. 25-37.
[6] Weizsacker FV ,Blum HE ,Wonds JR. Cleavage of hepatitis B virus RNA by three ribozymes transcribed from a single DNA template[J]. Biochem Biophy Res Commu, 1992, 189(2): 743-748.
[7] Beck J , Nassal M . Efficient hammerhead ribozyme-mediated cleavage of the structured hepatitis B virus encapsidation signal in vitro and in cell, but not in intact cells[J]. Nucleic Acids Res , 1995, 23(24): 4962.
, 百拇医药
[8] Welch PJ , Tritz R , Yei S, et al. Intracellular application of hairpin ribozyme against hepatitis B virus[J]. Gene Ther, 1997, 4(7): 736-743.
[9] 王 平, 徐 炜, 曾力宇, 等. 核酶Ripc对HBV基因体外转录物的作用[J]. 病毒学报, 1993, 9: 278-280.
[10] 竺来发, 易荣大, 陆长德, 等. 乙型肝炎病毒adr亚型核心抗原RNA片段的体外Ribozyme定量切割[J]. 生物化学与生物物理学报, 1993, 25(3): 316-317.
[收稿日期] 1999-05-19 [修回日期] 1999-10-18, 百拇医药