磁导向阿霉素-羧甲基葡聚糖磁性毫微粒的研究
作者:石可瑜 李朝兴 何炳林
单位:石可瑜(南开大学 化学系,天津 300071);李朝兴(南开大学 高分子化学研究所,天津 300071);何炳林(南开大学 高分子化学研究所,天津 300071)
关键词:磁导向药物;毫微粒;羧甲基葡聚糖
生物医学工程学杂志000107 摘 要:以阿霉素(ADR)为药物模型,制备了带有弱负电性的阿霉素-羧甲基葡聚糖磁性毫微粒(ADR-CMD MNPs),对比研究了静脉给药后其与电中性的ADR-dextran MNPs在小鼠肝、脾组织的富集情况,系统考察了ADR-CMD MNPs的理化性能和体内外的磁定位效果。结果表明,ADR-CMD MNPs的平均粒径为56 nm;载药量为12.4%;质量磁化率为1.06×10-4 emu.g-1,具有超顺磁性;ADR-CMD MNPs具有较好的磁导向功能,可有效定位于靶区;此外,体内分布实验证明:ADR-CMD MNPs的肝、脾被动靶向作用明显低于未经化学修饰的ADR-dextran MNPs,该研究为药物磁性毫微粒实现主动靶向提供了一种新方法。
, http://www.100md.com
Magnetic Drug Delivery System―Adriamycin-Carboxymethyl
Dextran Magnetic Nanoparticles
Shi Keyu
(Department of Chemistry, Nankai University, Tianjin 300071)
Li Chaoxing He Binglin
(Institute of Polymer Chemistry, Nankai University, Tianjin 300071)
Abstract:A novel magnetic drug carrier-carboxymethyl dextran magnetic nanoparticles(CMD MNPs) was prepared. Adriamycin(ADR) was coupled with two types of carrier-neutral dextran MNPs and anionic CMD MNPs, by periodate oxidation. The physico-chemical characteristics and the magnetic guidance effects in vitro and in vivo of ADR-CMD MNPs were studied. The distrbiution profiles of liver and spleen in mice were studied for both ADR-dextran conjugate MNPs and ADR-CMD conjuagte MNPs. The results showed ADR-CMD conjugate MNPs possessed superparamagnetism, the mean diameter was 56 nm, the mass magnetic susceptibility was 1.06×10-4 emu.g-1, and the drug loading was 12.4%. The distribution profiles in liver and spleen revealed that conjugation with neutral dextran MNPs, excessive accumulation of loaded ADR was found in liver and spleen after intravenous administration, while conjugation with CMD MNPs gave a markedly lower concentration in these organs, which indicated less uptake of ADR-CMD conjugate MNPs by reticuloendothelial system(RES) and the advantage of delivering loaded drug to sites other than the RES; thus it opens a new perspective for the active delivery of drug.
, 百拇医药
Key wrods:Magnetic drug delivery system Nanoparticles Carboxymethyl-dextran▲
磁性毫微粒是目前国内外导向药物和医用高分子材料研究领域的热门方向之一,在细胞分离、固定化酶和导向药物等研究领域均有着潜在的应用前景。磁性毫微粒在足够强的外加磁场作用下,可以引导负载药物在体内定向移动、定位浓集,从而达到提高药物治疗指数,降低药物毒副作用的目的[1,2]。然而,药物磁性毫微粒经静脉给药后,往往由于RES系统的吞噬作用而被动靶向于肝、脾,难于实现其它组织的靶向给药。研究表明,通过改善药物磁性毫微粒的表面性质可以抑制RES系统对其的吞噬作用,减少肝脾的被动靶向。一般通过在药物毫微粒表面吸附大分子表面活性剂来改善表面性能[3,4],但是这种表面修饰作用会随着载体分子的生物降解而减弱。本研究用化学修饰的方法来达到从本质上改善药物磁性毫微粒表面性能的目的,以期为实现药物磁性毫微粒主动靶向提供一种新的方法。
, http://www.100md.com
1 实验部分
1.1 主要仪器与试剂
Hitachi高速离心机(日本);Brookhaven Draft-9000AT光子相关谱仪(美国);Flexi-Dry冷冻干燥系统(美国);法拉第热磁天平(天津大学化工系);岛津RF-5000荧光分光光度计(日本);721分光光度计(上海第三分析仪器厂);高斯计(上海第四电表厂);钕铁硼磁铁(天津天磁公司);昆明种小鼠,天津药物研究院实验动物中心;注射用盐酸阿霉素(浙江海门制药厂,批号950313);葡聚糖T-40,Sephacryl 300凝胶柱(Pharmacia产品);其它试剂均为分析纯,使用前未经任何处理。
1.2 实验方法
1.2.1 载体磁性毫微粒及药物磁性毫微粒的制备 首先参照Molday等的方法[5],用共沉淀法制备葡聚糖磁性毫微粒(Dextran MNPs):将Dextran T-40水溶液和FeCl3。6H2O及FeCl2。4H2O水溶液混合均匀,搅拌下加入氨水溶液,加热至70 ℃反应1 h。反应产物冷却后经离心除去体系中的大粒子和聚集物,用Sephacryl S-300凝胶柱进行分离,弃去非磁性组分,磁性组分即Dextran MNPs用去离子水透析后冻干封存。
, 百拇医药
将所制备的Dextran MNPs进行羧甲基化处理制备羧甲基葡聚糖磁性毫微粒(CMD MNPs)。具体过程为:将Dextran MNPs冻干品分散在NaOH水溶液中并在-4 ℃的条件下保温20 min,分批加入NaOH 1/2当量的氯乙酸,升温至70 ℃反应20 min。待反应体系冷却后,用稀盐酸调节体系pH值至4左右,用甲醇沉淀反应产物,抽滤并充分洗涤后,将所得CMD MNPs置于真空条件下干燥。
Dextran MNPs和CMD MNPs分别用高碘酸钠氧化后与ADR药物分子通过Schiffs'反应偶联[6],制备ADR-Dextran MNPs和ADR-CMD MNPs。
1.2.2 载体磁性毫微粒和药物磁性毫微粒理化性能表征 磁性毫微粒平均粒径和粒径分布用光子相关谱仪进行表征。
磁性毫微粒的质量磁化率(Xm)用法拉第天平测定。
, 百拇医药
CMD MNPs羧甲基化程度用酸碱滴定法标定。
药物磁性毫微粒中药物百分含量以分光光度法测定。
1.2.3 磁导向定位实验 离体磁定位实验的装置参照Kiwada的设计[7],如图1所示。选择合适的介质流速,对比研究ADR-CMD MNPs在无外加磁场作用和附加外磁场时的流出方式。
活体磁导向定位实验选择小鼠肾脏作为磁定位器官[8]。将小鼠固定,左肾置于外加磁场中,尾静脉注射ADR-CMD MNPs。30 min后,拉断颈椎处死、解剖取出左右肾,分别测定其中药物浓度。肾组织中的阿霉素含量根据Bachur等的方法[9]测定:用20倍体积的0.3 mol。L-1的盐酸并50%乙醇溶液将组织匀浆,抽提其中的阿霉素,离心,用荧光分光光度计测定上清液中的药物浓度。对照组为同等条件下未注射药物的小鼠。
, 百拇医药
图1 离体磁导向实验装置图
Fig 1 The apparatus of magnetic guidance experiment in vitro
(A. Flow medium(Tris-HCl buffer pH8.5); B. Roller pump;C. Rubber tubing(Internal diameter 3.84 mm); D.Glass tubing(dthick10.86 mm, dthin 3.78 mm);E. Magnets; F. Eluted medium; G. Injection part of ADR-CMD MNPs)
1.2.4 组织分布实验 昆明种小鼠,18~22 g,雌雄兼用。实验动物分为3组,分别通过尾静脉注射生理盐水、ADR-Dextran MNPs或ADR-CMD MNPs,药物剂量为8 mg/kg,注射后0.5、1、4、24 h,每组各取3只,拉断颈椎处死,解剖取出小鼠肝、脾,分别测定其中药物浓度。组织器官中阿霉素的含量如前法测定。
, 百拇医药
2 结果和讨论
2.1 载体磁性毫微粒的制备
Dextran MNPs具有易于制备、磁响应性能好的特点。CMD MNPs与Dextran MNPs相比,粒子表面的羧甲基较羟基而言具有更好的亲水性能,而且通过羧甲基化处理,磁性毫微粒表面带有一定的负电性,有利于抑制血液组分对其的调理作用,从而减少RES系统的被动靶向作用,所以说,作为磁导向药物载体,CMD MNPs具有更好的表面性能。
由于多糖大分子存在碱降解反应,Dextran MNPs羧甲基化过程中所采用的碱浓度对所得CMD MNPs的理化性能具有明显影响(表1)。可以看出:随着反应体系中的碱浓度的增加,CMD MNPs的羧甲基化程度提高,但质量磁化率呈下降趋势,尤其当NaOH浓度超过4 mol。L-1时,CMD MNPs的质量磁化率显著下降,这是由于碱解作用导致粒子内部磁性微晶发生泄漏,从而使CMD MNPs磁响应性能降低。另一方面,羧甲基化反应消耗了载体粒子表面的邻羟基,所以过高的羧甲基化度也会对药物负载不利。综合考虑,选择3mol。L-1的NaOH为适宜反应浓度,在此条件下制备的CMD MNPs,不仅可以从本质上改善载体毫微粒表面性能,而且仍能保持其良好的磁响应性能和药物负载能力。
, 百拇医药
表1 碱浓度对CMD MNPs的理化性能影响
Table 1 The influence of alkali concentration on the physico-chemical characteristics of CMD MNPs CNaOH
(mol。L-1)
Carboxymethyl substitution degrees
of CMD MNPs
(mmol-CH2COOH/g CMD MNPs)
Xm
, 百拇医药 (10-4emu。g-1)
0
0
1.21
2.00
0.94
1.19
3.00
1.69
1.16
4.00
2.18
, 百拇医药
1.12
5.00
2.83
0.91
2.2 阿霉素磁性毫微粒的制备
Dextran MNPs和CMD MNPs分别用高碘酸钠氧化后与ADR药物分子通过Schiffs'反应偶联,所制备的ADR-Dextran MNPs和ADR-CMD MNPs相关理化性能如表2所示。可以看出,两种阿霉素磁性毫微粒均具有粒径小,药物负载能力较高和超顺磁性等优良的理化性能。
表2 ADR-Dextran和ADR-CMD磁性毫微粒的理化性能
Table 2 Physico-chemical characteristics of ADR-Dextran MNPs and ADR-CMD MNPs
, 百拇医药
Mean diameter
(nm)
Drug content
(%w/w)
Xm
(10-4emu。g-1)
ADR-Dextran MNPs
67
10.30
0.97
ADR-CMD MNPs
, 百拇医药
56
12.40
1.06
2.3 组织分布实验
ADR-Dextran MNPs和ADR-CMD MNPs静脉给药后,在小鼠的肝、脾中分布情况如图2所示。从中可以看出,与ADR-Dextran MNPs相比,ADR-CMD MNPs在静脉给药后,肝、脾的积累作用明显降低。这正是对载体粒子进行羧甲基化处理后,药物毫微粒表面性能改善的结果。表明通过对载体粒子进行化学修饰可以有效地改善药物磁性毫微粒表面性能。肝、脾被动靶向作用的降低为药物磁性毫微粒主动靶向的实现提供了保证。
图2 一次静脉给药(8 mg/kg)后小鼠肝(a)、脾(b)中阿霉素浓度
, 百拇医药
-●- ADR-dextran磁性毫微粒;--:ADR-CMD磁性毫微粒
Fig 2 ADR concentration in liver(a) and spleen(b) of mice after a single intravenous injection(8 mg/kg)
-●- ADR-dextran MNPs;--:ADE-CMD MNPs
2.4 ADR-CMD MNPs的磁定位实验
采用图1所示装置,测定ADR-CMD MNPs在附加或未加外磁场的条件下的流出模式。结果如图3所示。从图3的结果可以看出,在未设外加磁场时,磁性毫微粒主要随流动介质在前6 ml流出,占总量的92%,在流动介质流出21 ml后,只有1%的磁性毫微粒滞留在玻璃管中;与此截然不同,附加外磁场后,只有35%的药物磁性毫微粒随流动介质流出,65%的药物磁性毫微粒滞留在磁区。离体磁定位实验表明,是否附加外磁场对药物磁性毫微粒的流出模式有很大影响,表明所制备的ADR-CMD MNPs具有良好的磁响应性能。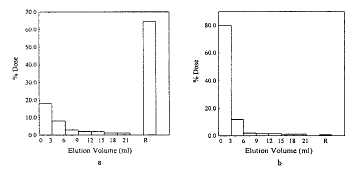
, http://www.100md.com
图3 ADR-CMD磁性毫微粒在有(a)无(b)外磁场作用时的流出模式
Fig 3 Elution pattern of the ADR-CMD MNPs with(a) or without(b) the magnet
在阿霉素磁性毫微粒活体磁定位实验中,选择小鼠肾脏作为磁定位器官,一方面是由于肾组织具有较好的可及性;另一方面,可以只在一侧肾上附加外磁场,通过对比双肾中药物含量差异来表征磁定位效果,减少了动物个体差异带来的实验误差。结果表明,当外加磁场强度较小时(约2000高斯),左右肾中阿霉素浓度没有明显差异,磁定位效果不显著;但在较高强度(约5000高斯)的外磁场的作用下,磁定位条件下的左肾中每克组织中ADR的含量达到37.8±3.3 μg,而未受外磁场作用的右肾中每克组织中阿霉素含量仅为11.9±2.1 μg,前者比后者高出2.08倍,由此可见,外加磁场对阿霉素磁性毫微粒有显著的富集作用(P<0.01),证明ADR-CMD MNPs具有明显的磁导向作用,这为进一步研究它的导向治疗效果提供了保证。
, http://www.100md.com
基金项目:国家自然科学基金资助项目(29274170)
参考文献:
[1]吴传斌,魏树礼.磁性药物微球制剂的研究进展.中国药学杂志,1993;28(6)∶330
[2]Gupta PK, Hung CT, Lam FC. Albumin Microspheres Ⅲ:Synthesis and characterization of microspheres containing adriamycin and magnetie. Int J Pharm 1988; 43∶167
[3]Illum L, Davis SS, Muller RH. The organ distribution and circulation time of intravenously injected colloidal carriers sterically stabilized with a block polymer-poloxamine 908. Life Sci, 1987; 40∶367
, 百拇医药
[4]Pimienta C, Chouinard F, Labib A. Effect of various poloxamer coating on in vitro adhesion of isohexylcyanoacrylate nanospheres to rat ileal segments under liquid flow. Int J Pharm, 1992; 80∶1
[5]Molday RS, Mackenzie D. Immunospecific ferromagnetic Iron-dextran reagents for the labeling and magnetic separation of cells. J Immunol Methods, 1982; 52∶353
[6]Brich Z, Ravel S, Kissel T. Preparation and characterization of a water soluble dextran immunoconjugate of Doxorubicin and the monoclonal antibody (ABL 364). J Controlled Rel, 1992; 19∶245
, 百拇医药
[7]Kiwada H,Sato J, Yamada S. Feasibility of magnetic liposomes as a targeting device for drugs. Chem. Pharm Bull, 1986; 34(10)∶4253
[8]Ibrahim A, Couvreur P, Roland M. New magnetic drug carrier. J Pharm Pharmacol, 1983; 35∶59
[9]Bachur NR, Moore AL, Bernstein JG. Tissue distribution and disposition of Daunomycin in mice:Fluorometric and isotopic methods. Cancer Chemother Rep, 1970; 54∶89
收稿日期:1998-10-12, 百拇医药
单位:石可瑜(南开大学 化学系,天津 300071);李朝兴(南开大学 高分子化学研究所,天津 300071);何炳林(南开大学 高分子化学研究所,天津 300071)
关键词:磁导向药物;毫微粒;羧甲基葡聚糖
生物医学工程学杂志000107 摘 要:以阿霉素(ADR)为药物模型,制备了带有弱负电性的阿霉素-羧甲基葡聚糖磁性毫微粒(ADR-CMD MNPs),对比研究了静脉给药后其与电中性的ADR-dextran MNPs在小鼠肝、脾组织的富集情况,系统考察了ADR-CMD MNPs的理化性能和体内外的磁定位效果。结果表明,ADR-CMD MNPs的平均粒径为56 nm;载药量为12.4%;质量磁化率为1.06×10-4 emu.g-1,具有超顺磁性;ADR-CMD MNPs具有较好的磁导向功能,可有效定位于靶区;此外,体内分布实验证明:ADR-CMD MNPs的肝、脾被动靶向作用明显低于未经化学修饰的ADR-dextran MNPs,该研究为药物磁性毫微粒实现主动靶向提供了一种新方法。
, http://www.100md.com
Magnetic Drug Delivery System―Adriamycin-Carboxymethyl
Dextran Magnetic Nanoparticles
Shi Keyu
(Department of Chemistry, Nankai University, Tianjin 300071)
Li Chaoxing He Binglin
(Institute of Polymer Chemistry, Nankai University, Tianjin 300071)
Abstract:A novel magnetic drug carrier-carboxymethyl dextran magnetic nanoparticles(CMD MNPs) was prepared. Adriamycin(ADR) was coupled with two types of carrier-neutral dextran MNPs and anionic CMD MNPs, by periodate oxidation. The physico-chemical characteristics and the magnetic guidance effects in vitro and in vivo of ADR-CMD MNPs were studied. The distrbiution profiles of liver and spleen in mice were studied for both ADR-dextran conjugate MNPs and ADR-CMD conjuagte MNPs. The results showed ADR-CMD conjugate MNPs possessed superparamagnetism, the mean diameter was 56 nm, the mass magnetic susceptibility was 1.06×10-4 emu.g-1, and the drug loading was 12.4%. The distribution profiles in liver and spleen revealed that conjugation with neutral dextran MNPs, excessive accumulation of loaded ADR was found in liver and spleen after intravenous administration, while conjugation with CMD MNPs gave a markedly lower concentration in these organs, which indicated less uptake of ADR-CMD conjugate MNPs by reticuloendothelial system(RES) and the advantage of delivering loaded drug to sites other than the RES; thus it opens a new perspective for the active delivery of drug.
, 百拇医药
Key wrods:Magnetic drug delivery system Nanoparticles Carboxymethyl-dextran▲
磁性毫微粒是目前国内外导向药物和医用高分子材料研究领域的热门方向之一,在细胞分离、固定化酶和导向药物等研究领域均有着潜在的应用前景。磁性毫微粒在足够强的外加磁场作用下,可以引导负载药物在体内定向移动、定位浓集,从而达到提高药物治疗指数,降低药物毒副作用的目的[1,2]。然而,药物磁性毫微粒经静脉给药后,往往由于RES系统的吞噬作用而被动靶向于肝、脾,难于实现其它组织的靶向给药。研究表明,通过改善药物磁性毫微粒的表面性质可以抑制RES系统对其的吞噬作用,减少肝脾的被动靶向。一般通过在药物毫微粒表面吸附大分子表面活性剂来改善表面性能[3,4],但是这种表面修饰作用会随着载体分子的生物降解而减弱。本研究用化学修饰的方法来达到从本质上改善药物磁性毫微粒表面性能的目的,以期为实现药物磁性毫微粒主动靶向提供一种新的方法。
, http://www.100md.com
1 实验部分
1.1 主要仪器与试剂
Hitachi高速离心机(日本);Brookhaven Draft-9000AT光子相关谱仪(美国);Flexi-Dry冷冻干燥系统(美国);法拉第热磁天平(天津大学化工系);岛津RF-5000荧光分光光度计(日本);721分光光度计(上海第三分析仪器厂);高斯计(上海第四电表厂);钕铁硼磁铁(天津天磁公司);昆明种小鼠,天津药物研究院实验动物中心;注射用盐酸阿霉素(浙江海门制药厂,批号950313);葡聚糖T-40,Sephacryl 300凝胶柱(Pharmacia产品);其它试剂均为分析纯,使用前未经任何处理。
1.2 实验方法
1.2.1 载体磁性毫微粒及药物磁性毫微粒的制备 首先参照Molday等的方法[5],用共沉淀法制备葡聚糖磁性毫微粒(Dextran MNPs):将Dextran T-40水溶液和FeCl3。6H2O及FeCl2。4H2O水溶液混合均匀,搅拌下加入氨水溶液,加热至70 ℃反应1 h。反应产物冷却后经离心除去体系中的大粒子和聚集物,用Sephacryl S-300凝胶柱进行分离,弃去非磁性组分,磁性组分即Dextran MNPs用去离子水透析后冻干封存。
, 百拇医药
将所制备的Dextran MNPs进行羧甲基化处理制备羧甲基葡聚糖磁性毫微粒(CMD MNPs)。具体过程为:将Dextran MNPs冻干品分散在NaOH水溶液中并在-4 ℃的条件下保温20 min,分批加入NaOH 1/2当量的氯乙酸,升温至70 ℃反应20 min。待反应体系冷却后,用稀盐酸调节体系pH值至4左右,用甲醇沉淀反应产物,抽滤并充分洗涤后,将所得CMD MNPs置于真空条件下干燥。
Dextran MNPs和CMD MNPs分别用高碘酸钠氧化后与ADR药物分子通过Schiffs'反应偶联[6],制备ADR-Dextran MNPs和ADR-CMD MNPs。
1.2.2 载体磁性毫微粒和药物磁性毫微粒理化性能表征 磁性毫微粒平均粒径和粒径分布用光子相关谱仪进行表征。
磁性毫微粒的质量磁化率(Xm)用法拉第天平测定。
, 百拇医药
CMD MNPs羧甲基化程度用酸碱滴定法标定。
药物磁性毫微粒中药物百分含量以分光光度法测定。
1.2.3 磁导向定位实验 离体磁定位实验的装置参照Kiwada的设计[7],如图1所示。选择合适的介质流速,对比研究ADR-CMD MNPs在无外加磁场作用和附加外磁场时的流出方式。
活体磁导向定位实验选择小鼠肾脏作为磁定位器官[8]。将小鼠固定,左肾置于外加磁场中,尾静脉注射ADR-CMD MNPs。30 min后,拉断颈椎处死、解剖取出左右肾,分别测定其中药物浓度。肾组织中的阿霉素含量根据Bachur等的方法[9]测定:用20倍体积的0.3 mol。L-1的盐酸并50%乙醇溶液将组织匀浆,抽提其中的阿霉素,离心,用荧光分光光度计测定上清液中的药物浓度。对照组为同等条件下未注射药物的小鼠。

, 百拇医药
图1 离体磁导向实验装置图
Fig 1 The apparatus of magnetic guidance experiment in vitro
(A. Flow medium(Tris-HCl buffer pH8.5); B. Roller pump;C. Rubber tubing(Internal diameter 3.84 mm); D.Glass tubing(dthick10.86 mm, dthin 3.78 mm);E. Magnets; F. Eluted medium; G. Injection part of ADR-CMD MNPs)
1.2.4 组织分布实验 昆明种小鼠,18~22 g,雌雄兼用。实验动物分为3组,分别通过尾静脉注射生理盐水、ADR-Dextran MNPs或ADR-CMD MNPs,药物剂量为8 mg/kg,注射后0.5、1、4、24 h,每组各取3只,拉断颈椎处死,解剖取出小鼠肝、脾,分别测定其中药物浓度。组织器官中阿霉素的含量如前法测定。
, 百拇医药
2 结果和讨论
2.1 载体磁性毫微粒的制备
Dextran MNPs具有易于制备、磁响应性能好的特点。CMD MNPs与Dextran MNPs相比,粒子表面的羧甲基较羟基而言具有更好的亲水性能,而且通过羧甲基化处理,磁性毫微粒表面带有一定的负电性,有利于抑制血液组分对其的调理作用,从而减少RES系统的被动靶向作用,所以说,作为磁导向药物载体,CMD MNPs具有更好的表面性能。
由于多糖大分子存在碱降解反应,Dextran MNPs羧甲基化过程中所采用的碱浓度对所得CMD MNPs的理化性能具有明显影响(表1)。可以看出:随着反应体系中的碱浓度的增加,CMD MNPs的羧甲基化程度提高,但质量磁化率呈下降趋势,尤其当NaOH浓度超过4 mol。L-1时,CMD MNPs的质量磁化率显著下降,这是由于碱解作用导致粒子内部磁性微晶发生泄漏,从而使CMD MNPs磁响应性能降低。另一方面,羧甲基化反应消耗了载体粒子表面的邻羟基,所以过高的羧甲基化度也会对药物负载不利。综合考虑,选择3mol。L-1的NaOH为适宜反应浓度,在此条件下制备的CMD MNPs,不仅可以从本质上改善载体毫微粒表面性能,而且仍能保持其良好的磁响应性能和药物负载能力。
, 百拇医药
表1 碱浓度对CMD MNPs的理化性能影响
Table 1 The influence of alkali concentration on the physico-chemical characteristics of CMD MNPs CNaOH
(mol。L-1)
Carboxymethyl substitution degrees
of CMD MNPs
(mmol-CH2COOH/g CMD MNPs)
Xm
, 百拇医药 (10-4emu。g-1)
0
0
1.21
2.00
0.94
1.19
3.00
1.69
1.16
4.00
2.18
, 百拇医药
1.12
5.00
2.83
0.91
2.2 阿霉素磁性毫微粒的制备
Dextran MNPs和CMD MNPs分别用高碘酸钠氧化后与ADR药物分子通过Schiffs'反应偶联,所制备的ADR-Dextran MNPs和ADR-CMD MNPs相关理化性能如表2所示。可以看出,两种阿霉素磁性毫微粒均具有粒径小,药物负载能力较高和超顺磁性等优良的理化性能。
表2 ADR-Dextran和ADR-CMD磁性毫微粒的理化性能
Table 2 Physico-chemical characteristics of ADR-Dextran MNPs and ADR-CMD MNPs
, 百拇医药
Mean diameter
(nm)
Drug content
(%w/w)
Xm
(10-4emu。g-1)
ADR-Dextran MNPs
67
10.30
0.97
ADR-CMD MNPs
, 百拇医药
56
12.40
1.06
2.3 组织分布实验
ADR-Dextran MNPs和ADR-CMD MNPs静脉给药后,在小鼠的肝、脾中分布情况如图2所示。从中可以看出,与ADR-Dextran MNPs相比,ADR-CMD MNPs在静脉给药后,肝、脾的积累作用明显降低。这正是对载体粒子进行羧甲基化处理后,药物毫微粒表面性能改善的结果。表明通过对载体粒子进行化学修饰可以有效地改善药物磁性毫微粒表面性能。肝、脾被动靶向作用的降低为药物磁性毫微粒主动靶向的实现提供了保证。

图2 一次静脉给药(8 mg/kg)后小鼠肝(a)、脾(b)中阿霉素浓度
, 百拇医药
-●- ADR-dextran磁性毫微粒;--:ADR-CMD磁性毫微粒
Fig 2 ADR concentration in liver(a) and spleen(b) of mice after a single intravenous injection(8 mg/kg)
-●- ADR-dextran MNPs;--:ADE-CMD MNPs
2.4 ADR-CMD MNPs的磁定位实验
采用图1所示装置,测定ADR-CMD MNPs在附加或未加外磁场的条件下的流出模式。结果如图3所示。从图3的结果可以看出,在未设外加磁场时,磁性毫微粒主要随流动介质在前6 ml流出,占总量的92%,在流动介质流出21 ml后,只有1%的磁性毫微粒滞留在玻璃管中;与此截然不同,附加外磁场后,只有35%的药物磁性毫微粒随流动介质流出,65%的药物磁性毫微粒滞留在磁区。离体磁定位实验表明,是否附加外磁场对药物磁性毫微粒的流出模式有很大影响,表明所制备的ADR-CMD MNPs具有良好的磁响应性能。

, http://www.100md.com
图3 ADR-CMD磁性毫微粒在有(a)无(b)外磁场作用时的流出模式
Fig 3 Elution pattern of the ADR-CMD MNPs with(a) or without(b) the magnet
在阿霉素磁性毫微粒活体磁定位实验中,选择小鼠肾脏作为磁定位器官,一方面是由于肾组织具有较好的可及性;另一方面,可以只在一侧肾上附加外磁场,通过对比双肾中药物含量差异来表征磁定位效果,减少了动物个体差异带来的实验误差。结果表明,当外加磁场强度较小时(约2000高斯),左右肾中阿霉素浓度没有明显差异,磁定位效果不显著;但在较高强度(约5000高斯)的外磁场的作用下,磁定位条件下的左肾中每克组织中ADR的含量达到37.8±3.3 μg,而未受外磁场作用的右肾中每克组织中阿霉素含量仅为11.9±2.1 μg,前者比后者高出2.08倍,由此可见,外加磁场对阿霉素磁性毫微粒有显著的富集作用(P<0.01),证明ADR-CMD MNPs具有明显的磁导向作用,这为进一步研究它的导向治疗效果提供了保证。
, http://www.100md.com
基金项目:国家自然科学基金资助项目(29274170)
参考文献:
[1]吴传斌,魏树礼.磁性药物微球制剂的研究进展.中国药学杂志,1993;28(6)∶330
[2]Gupta PK, Hung CT, Lam FC. Albumin Microspheres Ⅲ:Synthesis and characterization of microspheres containing adriamycin and magnetie. Int J Pharm 1988; 43∶167
[3]Illum L, Davis SS, Muller RH. The organ distribution and circulation time of intravenously injected colloidal carriers sterically stabilized with a block polymer-poloxamine 908. Life Sci, 1987; 40∶367
, 百拇医药
[4]Pimienta C, Chouinard F, Labib A. Effect of various poloxamer coating on in vitro adhesion of isohexylcyanoacrylate nanospheres to rat ileal segments under liquid flow. Int J Pharm, 1992; 80∶1
[5]Molday RS, Mackenzie D. Immunospecific ferromagnetic Iron-dextran reagents for the labeling and magnetic separation of cells. J Immunol Methods, 1982; 52∶353
[6]Brich Z, Ravel S, Kissel T. Preparation and characterization of a water soluble dextran immunoconjugate of Doxorubicin and the monoclonal antibody (ABL 364). J Controlled Rel, 1992; 19∶245
, 百拇医药
[7]Kiwada H,Sato J, Yamada S. Feasibility of magnetic liposomes as a targeting device for drugs. Chem. Pharm Bull, 1986; 34(10)∶4253
[8]Ibrahim A, Couvreur P, Roland M. New magnetic drug carrier. J Pharm Pharmacol, 1983; 35∶59
[9]Bachur NR, Moore AL, Bernstein JG. Tissue distribution and disposition of Daunomycin in mice:Fluorometric and isotopic methods. Cancer Chemother Rep, 1970; 54∶89
收稿日期:1998-10-12, 百拇医药