磁导向甲氨蝶呤缓释药物杀伤舌癌细胞的内在化过程
作者:张皖清 毛天球 吴军正 李学荣
单位:张皖清(第四军医大学口腔医学院,710032;现在304医院工作);毛天球(第四军医大学口腔医学院,710032);吴军正(第四军医大学口腔医学院,710032);李学荣(第四军医大学中心实验室)
关键词:细胞凋亡;舌癌;甲氨蝶呤;磁微球;细胞周期
实用口腔医学杂志000119 摘 要:目的:探讨磁导向甲氨蝶呤缓释药物(FM-MTX)对舌癌细胞凋亡的诱导作用,了解新药FM-MTX治疗舌癌的作用机理。方法:选用不同剂量的FM-MTX与人舌鳞癌Tca8113细胞系共同培养。按不同时间收集细胞悬液,并在透射电镜下观察细胞超微结构的变化。结果:细胞经FM-MTX药物处理组,1 h后,透射电镜下即可看到瘤细胞溶酶体大量增生,4 h后瘤细胞胞浆溶酶体开始吞噬磁性微粒,24 h吞噬颗粒明显增多,溶酶体膜开始裂解,颗粒释放到胞浆内。72 h后其内质网及线粒体内也可见颗粒沉积,溶酶体膜有消失现象,呈现胞浆空泡结构。96 h后部分瘤细胞出现凋亡。结论:甲氨蝶呤缓释药物(FM-MTX)对舌癌细胞凋亡起诱导作用,进入瘤细胞的细胞器,对肿瘤细胞有明显的杀伤作用。
, http://www.100md.com
分类号:R739.8 文献标识码:A
文章编号:1001-3733(2000)01-0058-03
Internalization of magnetic methotrexate conjugates in human tongue carcinoma Tca8113 cells
Zhang Wanqing Mao Tianqiu Wu junzheng et al.
(Stomatological Hospital,Fourth Military Medical University,Xi'an 710032)
Abstract:Objective:To investigate the internalization of FM-MTX in tongue carcinoma Tca8113 cells.Methods:A human tongue carcinoma cell line Tca8113 cells were cultured in full medium with various doses of FM-MTX for different times. The ultrastructure of the treated cells was observed under transmission electron microscope(TEM).Results:After 1 h treatment with FM-MTX, lysosomes of the cells increased. 4 h later it was found that there were ferromagnetic microspheres cytophaged in the lysosomes. By 24 h, phagocytosis incresed and parts of lysosomes membrane dissolves. Exocytosis of magnetic microspheres, cytolysis and apoptosis of the cells were observed.Conclusion:FM-MTX might be internalized into tongue carcinoma cells and induce apoptosis of the cells.
, 百拇医药
Key words:Magnetic microspheres;Apoptosis;Tongue; Carcinoma;Methotrexate; Cell cycle
细胞调亡(apoptpsis)是一种细胞生理性程序化死亡(programmed cell death),是当前肿瘤研究较活跃的领域。抗癌药物诱导肿瘤细胞发生凋亡,将成为肿瘤治疗的新焦点〔2,6〕。本文通过电镜及流式细胞术,分析了抗癌药物磁导向甲氨蝶呤缓释药FM-MTX对舌癌细胞凋亡的诱导作用,了解新药FM-MTX治疗舌癌的作用机理。
1 材料与方法
1.1 细胞系及细胞培养
人舌鳞癌细胞系Tca8113细胞由上海第二医科大学口腔医学院建株,第四军医大学口腔医学院口腔生物学教研室提供。将细胞接种于含体积分数为15%小牛血清的RPMI1640(GIBCO)培养液中、37 ℃ 的体积分数为5% CO2条件下培养。
, 百拇医药
1.2 FM-MTX进入瘤细胞后内在化过程超微结构观察
取生长旺盛的Tca8113细胞消化传代,加RPMI1640培养液,制成细胞悬液,细胞计数调至1×105个/ml。传至中号培养瓶6瓶,培养24 h后,取5瓶,每瓶加入FM-MTX 100 μg/L,继续培养,分别于1 h,4 h,24 h,72 h,96 h收获细胞,离心(1000r/min,5 min),弃上清,用0.1 mol/L PBS(pH 7.4)洗3次,弃上清,向细胞沉定内加入体积分数φ为2.5%戊二醛溶液固定1周。10 g/L锇酸后固定2 h,系列乙醇脱水后入丙酮。Epon812环氧树脂包埋。制备成超薄切片,铀-铅双染色,JEM-2000EX透射电镜观察FM-MTX药物颗粒进入瘤细胞的内在化过程。
1.3 FM-MTX对细胞周期的影响
取对数生长的Tca8113细胞,用2.5 g/L胰酶消化制成105个/ml的细胞悬液,传至中号培养瓶4瓶,继续培养24 h后,其中3瓶中分别加入FM-MTX 1000、100、10 μg/L,另一瓶不加药物作为对照组。在加热后第3 d收获细胞。各瓶细胞分别用2.5g/L胰酶消化5 min,使细胞尽可能分散成单个细胞。移入离心管中。离心(800r/min,5 min),弃上清,加预冷4 ℃ PBS 10 ml(pH7.4)吹打均匀,待细胞分散良好时,将其吹入预冷4 ℃的φ(乙醇)=70%中固定48 h,在FCM上检测细胞周期变化。对各组细胞大小、DNA含量、细胞周期G1、S、G2各期细胞数分布比例进行测定,用Multicycle软件分析并打印细胞周期分布状况〔3〕。
, 百拇医药
2 结 果
2.1 FM-MTX对瘤细胞内在化过程
在生长旺盛的Tca8113细胞中加入FM-MTX药物,1 h后,透射电镜下可见瘤细胞内溶酶体大量增生,溶酶体内尚未见到FM颗粒的沉积(图1)。4 h后可见溶酶体内有吞噬的FM超微磁粒;瘤细胞内线粒体肿胀,糖原颗粒增多(图2)。24 h则见溶酶体明显增大,FM颗粒增多(图3)。48 h溶酶体膜裂解,胞浆内可见磁微粒(图4)。72 h粗面内质网及线粒体内均可见有磁微粒沉积,溶酶体膜消失,胞浆呈空泡结构(图5)。96 h出现凋亡细胞,核固缩,可见凋亡小体(图6)。
图1 瘤细胞内溶酶体大量增生(TEM×3K)
, 百拇医药
图2 溶酶体内有吞噬的FM超微磁粒,线粒体肿胀,糖原颗粒增多(TEM×30K)
图3 溶酶体明显增大,吞噬的FM颗粒增多(TEM×60K)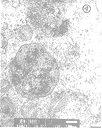
图4 溶酶体膜裂解,胞浆内可见磁微粒(TEM×60K)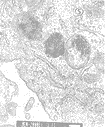
图5 溶酶体膜消失,胞浆呈空泡结构(TEM×30K)
图6 调亡细胞,核固缩,可见凋亡小体(TEM×10K)
, 百拇医药
2.2 FM-MTX对细胞周期的影响
流式细胞术处理细胞周期结果见表1,图7。FM-MTX在不同浓度时,对瘤细胞的杀伤作用不一。1000 μg/L FM-MTX对舌癌Tca8113细胞抑制作用最明显,完全阻滞细胞于G1,S期为0%。从增殖指数PI来看,随着药物浓度加大,细胞的增殖指数逐渐下降,表现为剂量依赖性特点。
图7 不同浓度的FM-MTX对舌癌Tca8113细胞周期的影响
A:0 μg/L B:10 μg/L C:100 μg/L D:1000 μg/L
表1 FM-MTX对Tca8113细胞周期的影响 FM-MTX(μg/L)
, http://www.100md.com
G0G1
S
G2/M
PI(%)
0
63.8
36.2
0.0
36.2
10
67.3
32.7
, http://www.100md.com
0.0
32.7
100
76.7
18.7
4.6
23.3
1000
98.7
0.0
1.3
01.3
3 讨 论
, 百拇医药
肿瘤的形成是基因调控的细胞增殖失控、分化异常和细胞凋亡过程受到抑制两方面共同作用所致。凋亡细胞典型的形态特征和生化改变为染色质浓缩、成块状聚集及碎裂,再由质膜包裹形成电镜下可见的凋亡小体。1972年Kerr等首次提出细胞凋亡的概念,是根据凋亡细胞所特有的形态学特征,这已成为判断细胞凋亡的经典标准〔1〕。
Tca8113细胞为低分化的人舌鳞癌细胞系,生长旺盛。不加药物对照组,细胞呈现恶性肿瘤细胞的特征,无凋亡小体形成,坏死细胞肿胀,染色质呈絮状,最终完全崩解。FM-MTX药物处理组,表现为溶酶体大量增生、膨胀增大,同时核质浓缩;药物处理96 h,核固缩成电子密度较高的凋亡小体。
FM-MTX为甲氨蝶呤缓释交联物,对裸鼠移植瘤有明显的抑制作用〔5〕,可使瘤细胞的异倍体比例降低〔7〕。本实验通过细胞周期分析,证实FM-MTX可干扰Tca8113细胞周期进程,能抑制细胞从G1期进入S期,使S期进展延缓,从而导致G1期比例增加。1 mg/L FM-MTX药物作用3 d,出现了细胞凋亡。这提示,FM-MTX主要作用在细胞周期的S期,使细胞休止于G1→S期,是细胞周期特异性抗肿瘤药物,有一定的抑制DNA合成作用。
, http://www.100md.com
由于FM-MTX药物的内核Fe3O4是电子密度较高的微粒结构,在电镜下为阻射影像。我们借助透射电镜观察了在37 ℃培养条件下FM-MTX进入瘤细胞的内在化过程。结果发现,在药物加入初期,Fe3O4主要存在于细胞外间质中,瘤细胞呈现生长活跃特征,内质网、线粒体丰富,糖原颗粒较多而集中,瘤细胞间呈现桥粒连接和紧密连接。瘤细胞内溶酶体大量增多。在药物作用4 h后,糖原颗粒分散、减少,瘤细胞内线粒体肿胀,溶酶体变大,内有少量Fe3O4吞噬颗粒,溶酶体膜尚完整。药物作用24 h后,则可见溶酶体内吞噬Fe3O4颗粒增多。48 h后,溶酶体膜溶解,Fe3O4颗粒释放于胞浆中。72 h粗面内质网及线粒体内可见Fe3O4颗粒。溶酶体呈现空泡结构,瘤细胞增殖活性下降,细胞间松解,微绒毛突起变少而短。细胞膜外可见Fe3O4释放。在药物内在化过程中,胞核未见明显异常。少数细胞呈现凋零状态,核固缩,细胞变小,表面胞膜绒毛突起消失,偶可见凋亡小体结构。这进一步说明,FM-MTX既作用于瘤细胞的胞浆,又作用于瘤细胞的胞核,达到共同杀伤肿瘤细胞的目的。
, 百拇医药
基金项目:国家自然科学基金资助项目 39070871
国家新药基金资助项目 93-(62)-N-42
参考文献:
[1]Kerr JR,Harmon BV.Apoptosis:Its significance in cancer and cancer therapy.Cancer, 1994,73:2013
[2]Ohmori T,Podack ER,Nishio K,et al.Apoptosis of lung cancer cells caused by some anticancer agents (MMC,CPT-11,ADM)is inhibited by bcl-2.Biochem Biophy Res Commun,1993,192:30
, 百拇医药
[3]Gong JP,Traganos F,Darzynkiewicz Z,et al.A selective procedure for DNA extraction from apoptotic cells applicable for gel electrophoresis and flow cytometry.Anal Biochem, 1994,218:314
[4]Fisher DE.Apoptosis in cancer therapy:crossing the threshold.Cell,1994,78:539
[5]张皖清,马定祥,毛天球,等.磁微粒负载甲氨蝶呤对舌癌移植的靶向治疗实验研究.实用口腔医学杂志,1990,6:147
[6]Korsmeyer SJ.Bcl-2 initiates a new category of oncogenes regulators of cell death.Blood,1992,80:879
[7]张皖清,马定祥,毛天球,等.DNA定量分析对甲氨喋呤磁液治疗移植性舌癌疗效估价.实用口医学杂志,1993,9(2):87
收稿日期:1998-08-24
修改日期:1999-11-01, 百拇医药
单位:张皖清(第四军医大学口腔医学院,710032;现在304医院工作);毛天球(第四军医大学口腔医学院,710032);吴军正(第四军医大学口腔医学院,710032);李学荣(第四军医大学中心实验室)
关键词:细胞凋亡;舌癌;甲氨蝶呤;磁微球;细胞周期
实用口腔医学杂志000119 摘 要:目的:探讨磁导向甲氨蝶呤缓释药物(FM-MTX)对舌癌细胞凋亡的诱导作用,了解新药FM-MTX治疗舌癌的作用机理。方法:选用不同剂量的FM-MTX与人舌鳞癌Tca8113细胞系共同培养。按不同时间收集细胞悬液,并在透射电镜下观察细胞超微结构的变化。结果:细胞经FM-MTX药物处理组,1 h后,透射电镜下即可看到瘤细胞溶酶体大量增生,4 h后瘤细胞胞浆溶酶体开始吞噬磁性微粒,24 h吞噬颗粒明显增多,溶酶体膜开始裂解,颗粒释放到胞浆内。72 h后其内质网及线粒体内也可见颗粒沉积,溶酶体膜有消失现象,呈现胞浆空泡结构。96 h后部分瘤细胞出现凋亡。结论:甲氨蝶呤缓释药物(FM-MTX)对舌癌细胞凋亡起诱导作用,进入瘤细胞的细胞器,对肿瘤细胞有明显的杀伤作用。
, http://www.100md.com
分类号:R739.8 文献标识码:A
文章编号:1001-3733(2000)01-0058-03
Internalization of magnetic methotrexate conjugates in human tongue carcinoma Tca8113 cells
Zhang Wanqing Mao Tianqiu Wu junzheng et al.
(Stomatological Hospital,Fourth Military Medical University,Xi'an 710032)
Abstract:Objective:To investigate the internalization of FM-MTX in tongue carcinoma Tca8113 cells.Methods:A human tongue carcinoma cell line Tca8113 cells were cultured in full medium with various doses of FM-MTX for different times. The ultrastructure of the treated cells was observed under transmission electron microscope(TEM).Results:After 1 h treatment with FM-MTX, lysosomes of the cells increased. 4 h later it was found that there were ferromagnetic microspheres cytophaged in the lysosomes. By 24 h, phagocytosis incresed and parts of lysosomes membrane dissolves. Exocytosis of magnetic microspheres, cytolysis and apoptosis of the cells were observed.Conclusion:FM-MTX might be internalized into tongue carcinoma cells and induce apoptosis of the cells.
, 百拇医药
Key words:Magnetic microspheres;Apoptosis;Tongue; Carcinoma;Methotrexate; Cell cycle
细胞调亡(apoptpsis)是一种细胞生理性程序化死亡(programmed cell death),是当前肿瘤研究较活跃的领域。抗癌药物诱导肿瘤细胞发生凋亡,将成为肿瘤治疗的新焦点〔2,6〕。本文通过电镜及流式细胞术,分析了抗癌药物磁导向甲氨蝶呤缓释药FM-MTX对舌癌细胞凋亡的诱导作用,了解新药FM-MTX治疗舌癌的作用机理。
1 材料与方法
1.1 细胞系及细胞培养
人舌鳞癌细胞系Tca8113细胞由上海第二医科大学口腔医学院建株,第四军医大学口腔医学院口腔生物学教研室提供。将细胞接种于含体积分数为15%小牛血清的RPMI1640(GIBCO)培养液中、37 ℃ 的体积分数为5% CO2条件下培养。
, 百拇医药
1.2 FM-MTX进入瘤细胞后内在化过程超微结构观察
取生长旺盛的Tca8113细胞消化传代,加RPMI1640培养液,制成细胞悬液,细胞计数调至1×105个/ml。传至中号培养瓶6瓶,培养24 h后,取5瓶,每瓶加入FM-MTX 100 μg/L,继续培养,分别于1 h,4 h,24 h,72 h,96 h收获细胞,离心(1000r/min,5 min),弃上清,用0.1 mol/L PBS(pH 7.4)洗3次,弃上清,向细胞沉定内加入体积分数φ为2.5%戊二醛溶液固定1周。10 g/L锇酸后固定2 h,系列乙醇脱水后入丙酮。Epon812环氧树脂包埋。制备成超薄切片,铀-铅双染色,JEM-2000EX透射电镜观察FM-MTX药物颗粒进入瘤细胞的内在化过程。
1.3 FM-MTX对细胞周期的影响
取对数生长的Tca8113细胞,用2.5 g/L胰酶消化制成105个/ml的细胞悬液,传至中号培养瓶4瓶,继续培养24 h后,其中3瓶中分别加入FM-MTX 1000、100、10 μg/L,另一瓶不加药物作为对照组。在加热后第3 d收获细胞。各瓶细胞分别用2.5g/L胰酶消化5 min,使细胞尽可能分散成单个细胞。移入离心管中。离心(800r/min,5 min),弃上清,加预冷4 ℃ PBS 10 ml(pH7.4)吹打均匀,待细胞分散良好时,将其吹入预冷4 ℃的φ(乙醇)=70%中固定48 h,在FCM上检测细胞周期变化。对各组细胞大小、DNA含量、细胞周期G1、S、G2各期细胞数分布比例进行测定,用Multicycle软件分析并打印细胞周期分布状况〔3〕。
, 百拇医药
2 结 果
2.1 FM-MTX对瘤细胞内在化过程
在生长旺盛的Tca8113细胞中加入FM-MTX药物,1 h后,透射电镜下可见瘤细胞内溶酶体大量增生,溶酶体内尚未见到FM颗粒的沉积(图1)。4 h后可见溶酶体内有吞噬的FM超微磁粒;瘤细胞内线粒体肿胀,糖原颗粒增多(图2)。24 h则见溶酶体明显增大,FM颗粒增多(图3)。48 h溶酶体膜裂解,胞浆内可见磁微粒(图4)。72 h粗面内质网及线粒体内均可见有磁微粒沉积,溶酶体膜消失,胞浆呈空泡结构(图5)。96 h出现凋亡细胞,核固缩,可见凋亡小体(图6)。

图1 瘤细胞内溶酶体大量增生(TEM×3K)

, 百拇医药
图2 溶酶体内有吞噬的FM超微磁粒,线粒体肿胀,糖原颗粒增多(TEM×30K)

图3 溶酶体明显增大,吞噬的FM颗粒增多(TEM×60K)

图4 溶酶体膜裂解,胞浆内可见磁微粒(TEM×60K)

图5 溶酶体膜消失,胞浆呈空泡结构(TEM×30K)

图6 调亡细胞,核固缩,可见凋亡小体(TEM×10K)
, 百拇医药
2.2 FM-MTX对细胞周期的影响
流式细胞术处理细胞周期结果见表1,图7。FM-MTX在不同浓度时,对瘤细胞的杀伤作用不一。1000 μg/L FM-MTX对舌癌Tca8113细胞抑制作用最明显,完全阻滞细胞于G1,S期为0%。从增殖指数PI来看,随着药物浓度加大,细胞的增殖指数逐渐下降,表现为剂量依赖性特点。

图7 不同浓度的FM-MTX对舌癌Tca8113细胞周期的影响
A:0 μg/L B:10 μg/L C:100 μg/L D:1000 μg/L
表1 FM-MTX对Tca8113细胞周期的影响 FM-MTX(μg/L)
, http://www.100md.com
G0G1
S
G2/M
PI(%)
0
63.8
36.2
0.0
36.2
10
67.3
32.7
, http://www.100md.com
0.0
32.7
100
76.7
18.7
4.6
23.3
1000
98.7
0.0
1.3
01.3
3 讨 论
, 百拇医药
肿瘤的形成是基因调控的细胞增殖失控、分化异常和细胞凋亡过程受到抑制两方面共同作用所致。凋亡细胞典型的形态特征和生化改变为染色质浓缩、成块状聚集及碎裂,再由质膜包裹形成电镜下可见的凋亡小体。1972年Kerr等首次提出细胞凋亡的概念,是根据凋亡细胞所特有的形态学特征,这已成为判断细胞凋亡的经典标准〔1〕。
Tca8113细胞为低分化的人舌鳞癌细胞系,生长旺盛。不加药物对照组,细胞呈现恶性肿瘤细胞的特征,无凋亡小体形成,坏死细胞肿胀,染色质呈絮状,最终完全崩解。FM-MTX药物处理组,表现为溶酶体大量增生、膨胀增大,同时核质浓缩;药物处理96 h,核固缩成电子密度较高的凋亡小体。
FM-MTX为甲氨蝶呤缓释交联物,对裸鼠移植瘤有明显的抑制作用〔5〕,可使瘤细胞的异倍体比例降低〔7〕。本实验通过细胞周期分析,证实FM-MTX可干扰Tca8113细胞周期进程,能抑制细胞从G1期进入S期,使S期进展延缓,从而导致G1期比例增加。1 mg/L FM-MTX药物作用3 d,出现了细胞凋亡。这提示,FM-MTX主要作用在细胞周期的S期,使细胞休止于G1→S期,是细胞周期特异性抗肿瘤药物,有一定的抑制DNA合成作用。
, http://www.100md.com
由于FM-MTX药物的内核Fe3O4是电子密度较高的微粒结构,在电镜下为阻射影像。我们借助透射电镜观察了在37 ℃培养条件下FM-MTX进入瘤细胞的内在化过程。结果发现,在药物加入初期,Fe3O4主要存在于细胞外间质中,瘤细胞呈现生长活跃特征,内质网、线粒体丰富,糖原颗粒较多而集中,瘤细胞间呈现桥粒连接和紧密连接。瘤细胞内溶酶体大量增多。在药物作用4 h后,糖原颗粒分散、减少,瘤细胞内线粒体肿胀,溶酶体变大,内有少量Fe3O4吞噬颗粒,溶酶体膜尚完整。药物作用24 h后,则可见溶酶体内吞噬Fe3O4颗粒增多。48 h后,溶酶体膜溶解,Fe3O4颗粒释放于胞浆中。72 h粗面内质网及线粒体内可见Fe3O4颗粒。溶酶体呈现空泡结构,瘤细胞增殖活性下降,细胞间松解,微绒毛突起变少而短。细胞膜外可见Fe3O4释放。在药物内在化过程中,胞核未见明显异常。少数细胞呈现凋零状态,核固缩,细胞变小,表面胞膜绒毛突起消失,偶可见凋亡小体结构。这进一步说明,FM-MTX既作用于瘤细胞的胞浆,又作用于瘤细胞的胞核,达到共同杀伤肿瘤细胞的目的。
, 百拇医药
基金项目:国家自然科学基金资助项目 39070871
国家新药基金资助项目 93-(62)-N-42
参考文献:
[1]Kerr JR,Harmon BV.Apoptosis:Its significance in cancer and cancer therapy.Cancer, 1994,73:2013
[2]Ohmori T,Podack ER,Nishio K,et al.Apoptosis of lung cancer cells caused by some anticancer agents (MMC,CPT-11,ADM)is inhibited by bcl-2.Biochem Biophy Res Commun,1993,192:30
, 百拇医药
[3]Gong JP,Traganos F,Darzynkiewicz Z,et al.A selective procedure for DNA extraction from apoptotic cells applicable for gel electrophoresis and flow cytometry.Anal Biochem, 1994,218:314
[4]Fisher DE.Apoptosis in cancer therapy:crossing the threshold.Cell,1994,78:539
[5]张皖清,马定祥,毛天球,等.磁微粒负载甲氨蝶呤对舌癌移植的靶向治疗实验研究.实用口腔医学杂志,1990,6:147
[6]Korsmeyer SJ.Bcl-2 initiates a new category of oncogenes regulators of cell death.Blood,1992,80:879
[7]张皖清,马定祥,毛天球,等.DNA定量分析对甲氨喋呤磁液治疗移植性舌癌疗效估价.实用口医学杂志,1993,9(2):87
收稿日期:1998-08-24
修改日期:1999-11-01, 百拇医药