万拉法新胶囊对健康人体不良反应试验
作者:陆 林 黄志刚 黄明生 孙学礼 李 静 杨彦春
单位:(华西医科大学第一临床医院心理卫生研究所 卫生部临床药理基地,成都 610041)
关键词:万拉法新;药物不良反应
中国新药杂志990317 摘要 目的:考察抗抑郁药国产万拉法新胶囊在健康人体的药物不良反应。方法:28名健康志愿受试者,随机分为7组,分别接受万拉法新单剂量25,75,100,125,150,175,200 mg/次空腹顿服。结果:万拉法新主要药物不良反应为恶心、头昏、出汗、厌食、口干、疲乏、呕吐、失眠等,大部分为轻度反应,未经处理,自行消失。试验中未出现谵妄、意识障碍、思维异常、人格解体等严重药物不良反应。与服药前相比,受试者服药后的体温、心率、血压等生命体征和血、小便、大便常规,肝肾功能及心电图等均在正常范围内波动。结论:国产万拉法新胶囊对健康人体耐受性较高,短期用药对人体正常生理代谢无明显影响。
, http://www.100md.com
ADRs TEST OF DOMESTIC VENLAFAXINE CAPSULES IN HEALTHY VOLUNTEERS
Lu Lin,Huang Zhigang,Huang Mingsheng,et al.
(Institute of Mental Health,West Chinal University of Medical Sciences,Chengdu 610041)
ABSTRACT OBJECTIVE:The ADRs of domestic venlafaxine capsules were tested in healthy volunteers.METHODS:28 fast healthy volunteers were equally divided into 7 groups and allocated to receive a single dose of 25,75,100,125,150,175 and 200 mg of venlafaxine respectively.RESULTS:Nausea dizziness ,sweating ,anorexia,dry mouth,asthenia,vomiting and insomnia were the main ADRs and most of them were mild and soon disappeared without treatment.There were no pro- and post-medication differences in temperature,heart rate,blood pressure,ECG,liver and renal function test,routine blood,urine and excrement tests.CONCLUSION:Venlafaxine capsules were highly tolerable in healthy volunteers and no obvious effects on physiological metabolisms were observed.
, 百拇医药
KEY WORDS Venlafaxine;ADRs
万拉法新(venlafaxine)为Ⅱ类抗抑郁新药,为一选择性的5-HT和去甲肾上腺素再摄取抑制剂(SNRI),治疗抑郁症有良好效果[1~6]。为了确定该药安全耐受的人用剂量、用法和剂量范围,我们对其进行了不良反应试验。
对象和方法
1 研究对象
28例志愿健康受试者,男女各14例,年龄20~38岁,平均(24±11.30)岁,体重46~78 kg,平均 (57.05±7.51)kg。均符合下列纳入及排除标准。
纳入标准:健康成年志愿者,年龄18~45岁,男女各半,体重为标准体重±15%;既往无严重的躯体和神经精神疾病史,近1年无任何疾病史;4周内未服用任何药物;体格和实验室(血、尿、大便、心电图、肝功、肾功)检查正常者。
, http://www.100md.com
排除标准:体检、神经、精神检查或实验室检查异常者;吸烟、嗜酒、既往药物过敏史者或4周内服用过精神药物或其他药物;妊娠、哺乳或月经期妇女;既往精神疾病、癫痫病和严重躯体疾病史,或1年内有肝、肾功能异常史。
2 研究方法
受试药物:盐酸万拉法新胶囊制剂,25 mg/粒,批号:960601,由重庆医药工业研究所提供。
给药方法:全部受试者男女各半。按随机数字表进行分组,分别接受万拉法新单剂量顿服,每人服药1次,剂量组从小到大依次从25,75,100,125,150,175,200 mg,每剂量组有4名受试者,服药前禁食12 h,服药饮温开水300 ml。
3 观察指标
3.1 不良反应 被观察的不良反应49项,包括恶心、出汗、头昏、呵欠、口干、疲乏、厌食、呕吐、嗜睡、失眠、头痛、震颤、体重改变、血压升高、畏寒、焦虑、紧张、肌张力增高、消化不良、性欲下降、尿频、月经紊乱、意识障碍、思维异常、人格解体、癫痫、自杀、皮疹等。服药后1,3,5,12,24,48,72 h记录不良反应。不良反应评分标准: 0分是指无症状;1分为轻度,指经询问有症状;2分为中度,指主动诉述症状,能忍受,无需处理;3分为重度,指有客观表现,难忍受,需要处理。
, 百拇医药
3.2 体格检查和精神检查 服药前及服药后1,3,5,12,24,72 h测量体温、脉搏、呼吸、血压。服药前及服药后12,24,72 h进行胸腹部、神经系统和精神检查。
3.3 实验室检查 服药前及服药后24,72 h检查血、尿、大便常规,肝功能,肾功能,心电图。若发现异常,则随访至正常。
4 统计分析
试验结果采用t、u、χ2检验和方差分析,应用SPSS/PC和《中国医学百科全书医学统计学》2.0版统计软件包,在AST-486微机上处理。
结 果
1 不良反应观察结果
1.1 发生的频率 28例受试者中出现与试验药物有关或可能有关的不良反应25项,主要不良反应依次为恶心26例,出汗19例,头昏19例,呵欠18例,疲乏15例,厌食15例,呕吐11例,嗜睡8例,失眠8例,头痛7例,震颤7例,体重改变6例,血压升高5例,畏寒4例,焦虑4例,紧张3例,肌张力增高3例,心动过速3例,腹胀2例,消化不良1例等。大部分为轻度反应,部分为中度反应,偶见重度反应,重度反应主要表现在恶心、呕吐、口干。另有少见不良反应如感觉异常、月经紊乱、激越各1例,试验中未出现谵妄、意识障碍、思维异常、人格解体等严重不良反应。
, 百拇医药
药物不良反应共发生217次,其中中度86次,重度14次,不良反应的总分为335分,得分较高的症状依次为恶心、呵欠、头昏等。
1.2 与服药剂量相关性 随服药剂量增加,药物不良反应增加,但各组相比,无明显差异(P>0.05),见表1。
表1 各剂量组不良反应总分比较(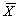 ±s) (剂量组)/((mg))
±s) (剂量组)/((mg))
n
24h
48h
72h
25
4
, http://www.100md.com
5.50±6.21
2.75±3.89
0.00±0.00
75
4
9.75±5.43
6.25±4.59
3.25±2.10
100
4
8.25±7.81
5.25±4.24
, http://www.100md.com
2.25±1.50
125
4
9.25±2.01
5.87±4.77
2.50±2.61
150
4
15.00±11.24
7.87±10.08
0.75±3.10
175
, http://www.100md.com
4
12.50±9.31
6.37±8.66
0.25±0.01
200
4
8.25±6.21
4.37±5.48
0.50±0.04
1.3 发生时间及严重程度 各剂量组服药后0.5 h即出现不良反应,在2~12 h不良反应最多,其中3~4 h不良反应最严重,得分最高,至36 h,不良反应基本消失。2 体格检查和精神检查结果
, http://www.100md.com
各剂量组服药前后血压、心率、体温均在正常范围,其差别无显著性。各剂量组服药前后体格检查无异常发现;精神检查包括一般情况、认知活动、情感活动、意志行为等,亦未发现异常。
3 实验室检查结果
各剂量组服药前后肝、肾功能、血常规、大小便常规变化无明显差异;心电图有2例轻度改变,其中1例窦性心律不齐,1例ST轻度下移,未发现中度异常。
讨 论
万拉法新对5-HT的再摄取的抑制作用弱于选择性的5-HT再摄取抑制剂(SSRI),对去甲肾上腺素再摄取的抑制作用也弱于一些三环类抗抑郁药(TCA)或SSRI,而抑制多巴胺重摄取作用则强于去甲丙咪嗪、丙咪嗪和三唑酮[6,7]。该药对于与多巴胺或苯二氮NFDA1受体结合的药物较少或几乎没有置换作用;对单胺氧化酶抑制剂(MAOI)、毒蕈碱能、胆碱能、α1-及α2-和β-肾上腺素能受体也无作用;对H1-受体作用亦较微弱[8,9]。与传统抗抑郁药相比,不良反应较少。本研究发现其主要不良反应大部分为轻度反应,未经处理自行消失,不影响服药者的正常生活;有少部分为中度到重度反应;亦未见国外文献报道的癫痫发作、自杀、肝功能障碍和皮疹等症状,说明其临床安全性较高。
, http://www.100md.com
本研究结果提示短期用药对人体正常生理代谢无明显影响。
综上所述,国产万拉法新胶囊安全剂量范围较大,重度不良反应较少,未发现自杀、意识障碍、思维异常等严重不良反应。是一种安全有效的新型抗抑郁剂。
参考文献
1 Vick L,Ellingrid,Perry PJ.Venlafaxine:a heterocyclic antidepressant.Am J Hosp Pharm,1994,51(3)∶3033
2 Derivan A,Entsuah AR,Kikta D.Venlafaxine:measuring the onset of antidepressant action.Psychopharmacol Bull,1995,45(2)∶439
, 百拇医药 3 Troy SM,Parker VD,Fruncill RS,et al.The pharmacokinetics of venlafaxine when given in a twice-daily regime.J Clin Pharmacol,1995,35(2)∶404
4 Hicks DR,Wolanink D,Russell R,et al.A high-performance liquid chromatographic method for the simultaneous determinator of venlafaxine and o-desmethylvenlafaxine in biological fluids. Ther Drug Monit,1994,16(1)∶100
5 Guelfi JD,White C,Hackett D,et al.Effectiveness of venlafaxine in patients hospitalized for major depression and melancholia.J Clin Psychiatry,1995,56(1)∶10
, 百拇医药
6 Shrivastavn RK,Cohn C,Crowder J,et al.Long-term safety and clinical acceptability of venlafaxine and imipramine in outpatients with major depression. J Clin Psychopharmacol,1994,14(3)∶322
7 Holliday SM,Benfield P.Venlafaxine:a review of its pharmacology and therapeutic potential in depression.Drugs,1995,49(2)∶282
8 Preskorn SH.Comparison of the tolerability of bupropion,fluoxetine,imipramine:nefazodone,parexetine,sertraline,and venlafaxine.J Clin Psychiatry,1995,56(Suppl 6)∶S12
9 Mentgomery SA.Rapid onset of action of venlafaxine.Inter Clin Psychopharmacol,1995,10(Suppl 2)∶S21
(收稿:1998-07-08 修回:1998-11-23), http://www.100md.com
单位:(华西医科大学第一临床医院心理卫生研究所 卫生部临床药理基地,成都 610041)
关键词:万拉法新;药物不良反应
中国新药杂志990317 摘要 目的:考察抗抑郁药国产万拉法新胶囊在健康人体的药物不良反应。方法:28名健康志愿受试者,随机分为7组,分别接受万拉法新单剂量25,75,100,125,150,175,200 mg/次空腹顿服。结果:万拉法新主要药物不良反应为恶心、头昏、出汗、厌食、口干、疲乏、呕吐、失眠等,大部分为轻度反应,未经处理,自行消失。试验中未出现谵妄、意识障碍、思维异常、人格解体等严重药物不良反应。与服药前相比,受试者服药后的体温、心率、血压等生命体征和血、小便、大便常规,肝肾功能及心电图等均在正常范围内波动。结论:国产万拉法新胶囊对健康人体耐受性较高,短期用药对人体正常生理代谢无明显影响。
, http://www.100md.com
ADRs TEST OF DOMESTIC VENLAFAXINE CAPSULES IN HEALTHY VOLUNTEERS
Lu Lin,Huang Zhigang,Huang Mingsheng,et al.
(Institute of Mental Health,West Chinal University of Medical Sciences,Chengdu 610041)
ABSTRACT OBJECTIVE:The ADRs of domestic venlafaxine capsules were tested in healthy volunteers.METHODS:28 fast healthy volunteers were equally divided into 7 groups and allocated to receive a single dose of 25,75,100,125,150,175 and 200 mg of venlafaxine respectively.RESULTS:Nausea dizziness ,sweating ,anorexia,dry mouth,asthenia,vomiting and insomnia were the main ADRs and most of them were mild and soon disappeared without treatment.There were no pro- and post-medication differences in temperature,heart rate,blood pressure,ECG,liver and renal function test,routine blood,urine and excrement tests.CONCLUSION:Venlafaxine capsules were highly tolerable in healthy volunteers and no obvious effects on physiological metabolisms were observed.
, 百拇医药
KEY WORDS Venlafaxine;ADRs
万拉法新(venlafaxine)为Ⅱ类抗抑郁新药,为一选择性的5-HT和去甲肾上腺素再摄取抑制剂(SNRI),治疗抑郁症有良好效果[1~6]。为了确定该药安全耐受的人用剂量、用法和剂量范围,我们对其进行了不良反应试验。
对象和方法
1 研究对象
28例志愿健康受试者,男女各14例,年龄20~38岁,平均(24±11.30)岁,体重46~78 kg,平均 (57.05±7.51)kg。均符合下列纳入及排除标准。
纳入标准:健康成年志愿者,年龄18~45岁,男女各半,体重为标准体重±15%;既往无严重的躯体和神经精神疾病史,近1年无任何疾病史;4周内未服用任何药物;体格和实验室(血、尿、大便、心电图、肝功、肾功)检查正常者。
, http://www.100md.com
排除标准:体检、神经、精神检查或实验室检查异常者;吸烟、嗜酒、既往药物过敏史者或4周内服用过精神药物或其他药物;妊娠、哺乳或月经期妇女;既往精神疾病、癫痫病和严重躯体疾病史,或1年内有肝、肾功能异常史。
2 研究方法
受试药物:盐酸万拉法新胶囊制剂,25 mg/粒,批号:960601,由重庆医药工业研究所提供。
给药方法:全部受试者男女各半。按随机数字表进行分组,分别接受万拉法新单剂量顿服,每人服药1次,剂量组从小到大依次从25,75,100,125,150,175,200 mg,每剂量组有4名受试者,服药前禁食12 h,服药饮温开水300 ml。
3 观察指标
3.1 不良反应 被观察的不良反应49项,包括恶心、出汗、头昏、呵欠、口干、疲乏、厌食、呕吐、嗜睡、失眠、头痛、震颤、体重改变、血压升高、畏寒、焦虑、紧张、肌张力增高、消化不良、性欲下降、尿频、月经紊乱、意识障碍、思维异常、人格解体、癫痫、自杀、皮疹等。服药后1,3,5,12,24,48,72 h记录不良反应。不良反应评分标准: 0分是指无症状;1分为轻度,指经询问有症状;2分为中度,指主动诉述症状,能忍受,无需处理;3分为重度,指有客观表现,难忍受,需要处理。
, 百拇医药
3.2 体格检查和精神检查 服药前及服药后1,3,5,12,24,72 h测量体温、脉搏、呼吸、血压。服药前及服药后12,24,72 h进行胸腹部、神经系统和精神检查。
3.3 实验室检查 服药前及服药后24,72 h检查血、尿、大便常规,肝功能,肾功能,心电图。若发现异常,则随访至正常。
4 统计分析
试验结果采用t、u、χ2检验和方差分析,应用SPSS/PC和《中国医学百科全书医学统计学》2.0版统计软件包,在AST-486微机上处理。
结 果
1 不良反应观察结果
1.1 发生的频率 28例受试者中出现与试验药物有关或可能有关的不良反应25项,主要不良反应依次为恶心26例,出汗19例,头昏19例,呵欠18例,疲乏15例,厌食15例,呕吐11例,嗜睡8例,失眠8例,头痛7例,震颤7例,体重改变6例,血压升高5例,畏寒4例,焦虑4例,紧张3例,肌张力增高3例,心动过速3例,腹胀2例,消化不良1例等。大部分为轻度反应,部分为中度反应,偶见重度反应,重度反应主要表现在恶心、呕吐、口干。另有少见不良反应如感觉异常、月经紊乱、激越各1例,试验中未出现谵妄、意识障碍、思维异常、人格解体等严重不良反应。
, 百拇医药
药物不良反应共发生217次,其中中度86次,重度14次,不良反应的总分为335分,得分较高的症状依次为恶心、呵欠、头昏等。
1.2 与服药剂量相关性 随服药剂量增加,药物不良反应增加,但各组相比,无明显差异(P>0.05),见表1。
表1 各剂量组不良反应总分比较(
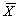 ±s) (剂量组)/((mg))
±s) (剂量组)/((mg))n
24h
48h
72h
25
4
, http://www.100md.com
5.50±6.21
2.75±3.89
0.00±0.00
75
4
9.75±5.43
6.25±4.59
3.25±2.10
100
4
8.25±7.81
5.25±4.24
, http://www.100md.com
2.25±1.50
125
4
9.25±2.01
5.87±4.77
2.50±2.61
150
4
15.00±11.24
7.87±10.08
0.75±3.10
175
, http://www.100md.com
4
12.50±9.31
6.37±8.66
0.25±0.01
200
4
8.25±6.21
4.37±5.48
0.50±0.04
1.3 发生时间及严重程度 各剂量组服药后0.5 h即出现不良反应,在2~12 h不良反应最多,其中3~4 h不良反应最严重,得分最高,至36 h,不良反应基本消失。2 体格检查和精神检查结果
, http://www.100md.com
各剂量组服药前后血压、心率、体温均在正常范围,其差别无显著性。各剂量组服药前后体格检查无异常发现;精神检查包括一般情况、认知活动、情感活动、意志行为等,亦未发现异常。
3 实验室检查结果
各剂量组服药前后肝、肾功能、血常规、大小便常规变化无明显差异;心电图有2例轻度改变,其中1例窦性心律不齐,1例ST轻度下移,未发现中度异常。
讨 论
万拉法新对5-HT的再摄取的抑制作用弱于选择性的5-HT再摄取抑制剂(SSRI),对去甲肾上腺素再摄取的抑制作用也弱于一些三环类抗抑郁药(TCA)或SSRI,而抑制多巴胺重摄取作用则强于去甲丙咪嗪、丙咪嗪和三唑酮[6,7]。该药对于与多巴胺或苯二氮NFDA1受体结合的药物较少或几乎没有置换作用;对单胺氧化酶抑制剂(MAOI)、毒蕈碱能、胆碱能、α1-及α2-和β-肾上腺素能受体也无作用;对H1-受体作用亦较微弱[8,9]。与传统抗抑郁药相比,不良反应较少。本研究发现其主要不良反应大部分为轻度反应,未经处理自行消失,不影响服药者的正常生活;有少部分为中度到重度反应;亦未见国外文献报道的癫痫发作、自杀、肝功能障碍和皮疹等症状,说明其临床安全性较高。
, http://www.100md.com
本研究结果提示短期用药对人体正常生理代谢无明显影响。
综上所述,国产万拉法新胶囊安全剂量范围较大,重度不良反应较少,未发现自杀、意识障碍、思维异常等严重不良反应。是一种安全有效的新型抗抑郁剂。
参考文献
1 Vick L,Ellingrid,Perry PJ.Venlafaxine:a heterocyclic antidepressant.Am J Hosp Pharm,1994,51(3)∶3033
2 Derivan A,Entsuah AR,Kikta D.Venlafaxine:measuring the onset of antidepressant action.Psychopharmacol Bull,1995,45(2)∶439
, 百拇医药 3 Troy SM,Parker VD,Fruncill RS,et al.The pharmacokinetics of venlafaxine when given in a twice-daily regime.J Clin Pharmacol,1995,35(2)∶404
4 Hicks DR,Wolanink D,Russell R,et al.A high-performance liquid chromatographic method for the simultaneous determinator of venlafaxine and o-desmethylvenlafaxine in biological fluids. Ther Drug Monit,1994,16(1)∶100
5 Guelfi JD,White C,Hackett D,et al.Effectiveness of venlafaxine in patients hospitalized for major depression and melancholia.J Clin Psychiatry,1995,56(1)∶10
, 百拇医药
6 Shrivastavn RK,Cohn C,Crowder J,et al.Long-term safety and clinical acceptability of venlafaxine and imipramine in outpatients with major depression. J Clin Psychopharmacol,1994,14(3)∶322
7 Holliday SM,Benfield P.Venlafaxine:a review of its pharmacology and therapeutic potential in depression.Drugs,1995,49(2)∶282
8 Preskorn SH.Comparison of the tolerability of bupropion,fluoxetine,imipramine:nefazodone,parexetine,sertraline,and venlafaxine.J Clin Psychiatry,1995,56(Suppl 6)∶S12
9 Mentgomery SA.Rapid onset of action of venlafaxine.Inter Clin Psychopharmacol,1995,10(Suppl 2)∶S21
(收稿:1998-07-08 修回:1998-11-23), http://www.100md.com