流式细胞仪全血白细胞样品制备试剂的研究
作者:曹云新 刘智广
单位:第四军医大学中心实验室,西安,710032
关键词:
细胞与分子免疫学杂志990230流式细胞仪(flow cytometer,FCM)以快速、准确、灵敏度高等优点,已广泛用于医学基础和临床研究〔1〕。特别是近年来,由于已获得多种抗白细胞膜表面抗原的单克隆抗体(mAb),以及这些mAb荧光直接标记物的出现,使FCM对外周血白细胞表面标志物的分析,已成为临床、基础研究和诊断的一项重要指标[2~4],如淋巴细胞亚群分析、白血病分型和免疫功能测定等。但由于供FCM分析的样品,一般是经荧光染色的单细胞悬液,且全血样品中除有测定的细胞外,还含有其它细胞,因此,对全血样品的制备乃是FCM分析的关键。1987年,Coulter公司已推出流式细胞仪配套的免疫学样品制备仪及其相应的全血白细胞样品制备试剂,并提供了全血样品快速、自动化的制样方法,但该制备试剂(称进口试剂)为独家生产,价格较高(不包括荧光mAb,每份样品需1.4美元)。为此,我们参照文献[5~7]的制样方法,经过反复试验,研制出了供免疫学样品制备仪用的白细胞样品制备试剂(称自制试剂),经过半年多的试用证明,自制试剂达到了进口试剂的效果,而成本却大大降低。
, http://www.100md.com
1 材料和方法
1.1 仪器和试剂 EliteESP型流式细胞仪,Q-prep型免疫学样品制备仪,全血白细胞样品制备试剂(进口试剂),抗CD3 mAb-FITC及MSIgG1-FI-TC,均为美国Coulter公司产品。
1.2 自制试剂的配制 全血白细胞样品制备试剂参照文献[5-7]略有改进。制备中全部采用国产分析纯试剂,共配制了3套不同的试剂,即自制试剂Ⅰ、自制试剂Ⅱ和自制试剂Ⅲ。其中每套试剂均由溶血剂(甲酸水溶液)、稳定剂(碳酸钠-氯化钠水溶液)、固定剂(多聚甲醛-磷酸钠缓冲液)组成,3套试剂的组成相同,但配制方法和浓度不同。
1.3 制备方法
1.3.1 荧光染色 取肝素抗凝或EDTA抗凝全血100μl,置12mm×75mm专用试管中(若全血中白细胞总数>1010/L,则用PBS调整白细胞浓度到3×109/L~1×1010/L),并小心地将样品加入试管底部(若样品碰到管壁,则必需用棉签擦干净,否则会影响测定结果),加入10μl荧光标记的mAb,小心混合,避光、室温下反应10min~15min后,上Q-prep型免疫学样品制备仪。
, 百拇医药
1.3.2 样品制备 荧光染色后的全血样品(用进口试剂和自制试剂),按照免疫学样品制备仪操作自动完成制样,进行FCM分析(若不立即分析,则将制备好的样品放于4℃~8℃保存)。
1.4 自制试剂的筛选 取同一份全血样品分为4组,每组2份。按照1.3.1的方法,1份用于MSIgG1-FITC染色(阴性对照),1份用于抗CD3 mAb-FITC染色。按照1.3.2的方法,4组样品分别用进口试剂和自制试剂(Ⅰ,Ⅱ,Ⅲ)制样,分别进行FCM分析,观察细胞在直方图中的分布,CD3+和CD3-淋巴细胞的荧光强度,以及CD3+淋巴细胞的百分率,通过比较筛选出与进口试剂结果相同的自制试剂。
1.5 白细胞分群的对比试验 取同一份全血样品分成2份,按照1.3.1的方法,进行MSIgG1-FITC染色。按照1.3.2的方法,分别用进口试剂和筛选出的自制试剂制样,进行FCM分析,于同一条件下,观察白细胞在直方图中的分群情况。
, http://www.100md.com
1.6 自制试剂的稳定性 以筛选出的自制试剂制备CD3样品,分别于4°C~8°C保存1h,4h,8h和24h,用FCM进行测定,观察用自制试剂制备的样品放置不同时间后,对CD3+淋巴细胞百分率和CD3分子表达量的影响。
1.7 自制试剂的使用期 将自制试剂在室温中放置0d,15d,30d和45d后,按照1.3的方法制备全血样品,观察自制试剂对白细胞分群的影响。
2 结果
2.1 自制试剂的筛选 用进口试剂和自制试剂制备的全血样品,经FCM分析表明:①自2制试剂Ⅱ与进口试剂制备的全血样品,细胞的分布基本相同(P>0.05),而自制试剂Ⅰ,Ⅲ制备的样品对细胞的分布略差(图1);②自制试剂Ⅱ与进口试剂的非特异性荧光也相同(P>0.05),而自制试剂Ⅰ,Ⅲ的非特异性荧光明显低于进口试剂(P<0.01);③自制试剂Ⅱ与进口试剂制备的样品CD3+淋巴细胞的百分率和CD3分子的表达量(荧光强度)高度一致(P>0.05),而自制试剂Ⅰ、Ⅲ制备的样品CD3+淋巴细胞的百分率虽然与进口试剂相同(P>0.05),但CD3+淋巴细胞上CD3分子的表达量明显降低(P<0.01)(表1)。因此,我们选用自制试剂Ⅱ作为免疫学样品制备仪全血白细胞制样试剂。
, 百拇医药
图1 进口试剂和自制试剂对MSIgG1-FITC的FCM分析
表1 自制试剂制备样品CD3+淋巴细胞的FCM测定
试剂
CD3+细胞
(%)
CD3+分子的荧光强度
(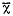 ±SD)
±SD)
进口试剂
69.4
7.04±3.72
, http://www.100md.com
自制试剂Ⅰ
68.9
3.58±2.02**
自制试剂Ⅱ
70.2
8.03±3.98
自制试剂Ⅲ
69.1
3.63±1.71**
与进口试剂相比较,**P<0.01
2.2 白细胞分群试验 用进口试剂和自制试剂Ⅱ制备的样品,经FCM分析表明:自制试剂Ⅱ与进口试剂制备的样品中淋巴细胞、单核细胞和粒细胞的分布一致(P>0.05),前向散射光和侧向散射光直方图基本相同(图2)。
, http://www.100md.com
图2 进口试剂和自制试剂Ⅱ制样的白细胞分群
2.3 自制试剂的稳定性 用自制试剂Ⅱ制备的CD3样品,于4℃~8℃放置不同时间后,测定CD3+淋巴细胞的百分率和CD3分子的表达量,结果均相同(P>0.05),表明用自制试剂制备的样品在24h内测定,不影响测定的结果(表2)。
表2 自制试剂Ⅱ制备样品CD3+淋巴细胞的稳定性
时间(h)
CD3+细胞
(%)
CD3+分子的荧光强度
(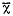 ±SD)
±SD)
, 百拇医药
1
70.2
8.03±3.98
4
69.5
8.10±3.69
8
70.4
7.97±3.82
24
69.9
8.06±4.01
2.4 自制试剂的使用期 自制试剂Ⅱ在室温下放置不同时间后制备的样品,经FCM分析表明,该试剂在室温下放置45d后,对白细胞的分群无影响(图3)。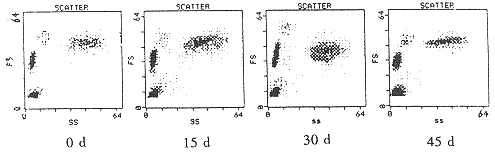
, http://www.100md.com
图3 自制试剂Ⅱ的使用期
2 讨论
在全血样品的FCM分析中,样品制备的好坏直接影响测定的结果,目前用于FCM全血样品制备的方法有3种[8]:①用荧光抗体染色全血,然后溶解红细胞;②将红细胞溶解后再进行荧光染色;③通过梯度离心分离出所需的细胞,再进行荧光染色。后两种方法由于操作繁琐,在直接免疫荧光染色中应用较少;而第1种方法是目前使用最多的方法,且可自动制样。该法一般需要染色、溶解红细胞、稳定荧光复合物和固定细胞等步骤。其中红细胞溶解程度是操作中的关键步骤,溶解过度或不足都会影响测定结果的准确性。
免疫学样品制备仪可将荧光染色后的全血样品自动完成红细胞溶解、荧光复合物稳定和细胞固定,从而大大降低了制样误差。但由于用于该仪器的专用试剂费用较高,可使制样的成本提高,不利于FCM的广泛应用。我们研制的自制试剂Ⅱ由溶解剂、稳定剂和固定剂3部分组成,经与进口试剂进行对比试验表明,对白细胞的分群、CD3+淋巴细胞的百分率和CD3分子的表达量、染色结果的稳定性,以及试剂在室温下保存的稳定性等,均达到了进口试剂的效果,而自制试剂的成本只有进口试剂的2%。
, 百拇医药
作者简介:曹云新,女,39岁,实验师。西安市长乐西路17号,Tel.(029)3374573
参考文献
[1]宋根平,李素文.流式细胞术的原理和应用.北京师范大学出版社,北京:1992:140~252
[2]Davies EG, Levinsky RJ, Butter M, et al.Lymphocyte subpopulations in primary immunodeficience disorders. Arch Dis Child, 1983; 58:346~351
[3]Shackney SE.The use of flow cytometry in the diagnosis and biological characterization of the non-Hodgkin′s lymphomas. Ann NY Acad Sci,1986;468:171~177
, http://www.100md.com
[4]Eichner RD. LAV/HTLV-Ⅲ plays a dominant role in the etiology of AIDS. AIDS Res, 1984; 1(4):237~241
[5]Caldwell CW,Taylor HM. A rapid no-wash technique for Immunophenotypic analysis by flow cytometry. Am J Clin Path, 1986; 86(5):600~607
[6]Barker JW. An innovative lymphocyte preparation system for flow cytometry.Am Clin Lab, 1988; 7(7):32~39
[7]Kotylo PK.Rapid analysis of lymphocyte subsets in cord blood. Am J Clin Path, 1990; 93(2):263~ 266
[8]蔡文琴,王伯 .实用免疫细胞化学与核酸分子杂交技术.四川科学技术出版社,成都:1994:214~221
.实用免疫细胞化学与核酸分子杂交技术.四川科学技术出版社,成都:1994:214~221
收稿:1998-08-03
修回:1998-10-08, 百拇医药
单位:第四军医大学中心实验室,西安,710032
关键词:
细胞与分子免疫学杂志990230流式细胞仪(flow cytometer,FCM)以快速、准确、灵敏度高等优点,已广泛用于医学基础和临床研究〔1〕。特别是近年来,由于已获得多种抗白细胞膜表面抗原的单克隆抗体(mAb),以及这些mAb荧光直接标记物的出现,使FCM对外周血白细胞表面标志物的分析,已成为临床、基础研究和诊断的一项重要指标[2~4],如淋巴细胞亚群分析、白血病分型和免疫功能测定等。但由于供FCM分析的样品,一般是经荧光染色的单细胞悬液,且全血样品中除有测定的细胞外,还含有其它细胞,因此,对全血样品的制备乃是FCM分析的关键。1987年,Coulter公司已推出流式细胞仪配套的免疫学样品制备仪及其相应的全血白细胞样品制备试剂,并提供了全血样品快速、自动化的制样方法,但该制备试剂(称进口试剂)为独家生产,价格较高(不包括荧光mAb,每份样品需1.4美元)。为此,我们参照文献[5~7]的制样方法,经过反复试验,研制出了供免疫学样品制备仪用的白细胞样品制备试剂(称自制试剂),经过半年多的试用证明,自制试剂达到了进口试剂的效果,而成本却大大降低。
, http://www.100md.com
1 材料和方法
1.1 仪器和试剂 EliteESP型流式细胞仪,Q-prep型免疫学样品制备仪,全血白细胞样品制备试剂(进口试剂),抗CD3 mAb-FITC及MSIgG1-FI-TC,均为美国Coulter公司产品。
1.2 自制试剂的配制 全血白细胞样品制备试剂参照文献[5-7]略有改进。制备中全部采用国产分析纯试剂,共配制了3套不同的试剂,即自制试剂Ⅰ、自制试剂Ⅱ和自制试剂Ⅲ。其中每套试剂均由溶血剂(甲酸水溶液)、稳定剂(碳酸钠-氯化钠水溶液)、固定剂(多聚甲醛-磷酸钠缓冲液)组成,3套试剂的组成相同,但配制方法和浓度不同。
1.3 制备方法
1.3.1 荧光染色 取肝素抗凝或EDTA抗凝全血100μl,置12mm×75mm专用试管中(若全血中白细胞总数>1010/L,则用PBS调整白细胞浓度到3×109/L~1×1010/L),并小心地将样品加入试管底部(若样品碰到管壁,则必需用棉签擦干净,否则会影响测定结果),加入10μl荧光标记的mAb,小心混合,避光、室温下反应10min~15min后,上Q-prep型免疫学样品制备仪。
, 百拇医药
1.3.2 样品制备 荧光染色后的全血样品(用进口试剂和自制试剂),按照免疫学样品制备仪操作自动完成制样,进行FCM分析(若不立即分析,则将制备好的样品放于4℃~8℃保存)。
1.4 自制试剂的筛选 取同一份全血样品分为4组,每组2份。按照1.3.1的方法,1份用于MSIgG1-FITC染色(阴性对照),1份用于抗CD3 mAb-FITC染色。按照1.3.2的方法,4组样品分别用进口试剂和自制试剂(Ⅰ,Ⅱ,Ⅲ)制样,分别进行FCM分析,观察细胞在直方图中的分布,CD3+和CD3-淋巴细胞的荧光强度,以及CD3+淋巴细胞的百分率,通过比较筛选出与进口试剂结果相同的自制试剂。
1.5 白细胞分群的对比试验 取同一份全血样品分成2份,按照1.3.1的方法,进行MSIgG1-FITC染色。按照1.3.2的方法,分别用进口试剂和筛选出的自制试剂制样,进行FCM分析,于同一条件下,观察白细胞在直方图中的分群情况。
, http://www.100md.com
1.6 自制试剂的稳定性 以筛选出的自制试剂制备CD3样品,分别于4°C~8°C保存1h,4h,8h和24h,用FCM进行测定,观察用自制试剂制备的样品放置不同时间后,对CD3+淋巴细胞百分率和CD3分子表达量的影响。
1.7 自制试剂的使用期 将自制试剂在室温中放置0d,15d,30d和45d后,按照1.3的方法制备全血样品,观察自制试剂对白细胞分群的影响。
2 结果
2.1 自制试剂的筛选 用进口试剂和自制试剂制备的全血样品,经FCM分析表明:①自2制试剂Ⅱ与进口试剂制备的全血样品,细胞的分布基本相同(P>0.05),而自制试剂Ⅰ,Ⅲ制备的样品对细胞的分布略差(图1);②自制试剂Ⅱ与进口试剂的非特异性荧光也相同(P>0.05),而自制试剂Ⅰ,Ⅲ的非特异性荧光明显低于进口试剂(P<0.01);③自制试剂Ⅱ与进口试剂制备的样品CD3+淋巴细胞的百分率和CD3分子的表达量(荧光强度)高度一致(P>0.05),而自制试剂Ⅰ、Ⅲ制备的样品CD3+淋巴细胞的百分率虽然与进口试剂相同(P>0.05),但CD3+淋巴细胞上CD3分子的表达量明显降低(P<0.01)(表1)。因此,我们选用自制试剂Ⅱ作为免疫学样品制备仪全血白细胞制样试剂。

, 百拇医药
图1 进口试剂和自制试剂对MSIgG1-FITC的FCM分析
表1 自制试剂制备样品CD3+淋巴细胞的FCM测定
试剂
CD3+细胞
(%)
CD3+分子的荧光强度
(
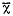 ±SD)
±SD)进口试剂
69.4
7.04±3.72
, http://www.100md.com
自制试剂Ⅰ
68.9
3.58±2.02**
自制试剂Ⅱ
70.2
8.03±3.98
自制试剂Ⅲ
69.1
3.63±1.71**
与进口试剂相比较,**P<0.01
2.2 白细胞分群试验 用进口试剂和自制试剂Ⅱ制备的样品,经FCM分析表明:自制试剂Ⅱ与进口试剂制备的样品中淋巴细胞、单核细胞和粒细胞的分布一致(P>0.05),前向散射光和侧向散射光直方图基本相同(图2)。

, http://www.100md.com
图2 进口试剂和自制试剂Ⅱ制样的白细胞分群
2.3 自制试剂的稳定性 用自制试剂Ⅱ制备的CD3样品,于4℃~8℃放置不同时间后,测定CD3+淋巴细胞的百分率和CD3分子的表达量,结果均相同(P>0.05),表明用自制试剂制备的样品在24h内测定,不影响测定的结果(表2)。
表2 自制试剂Ⅱ制备样品CD3+淋巴细胞的稳定性
时间(h)
CD3+细胞
(%)
CD3+分子的荧光强度
(
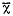 ±SD)
±SD), 百拇医药
1
70.2
8.03±3.98
4
69.5
8.10±3.69
8
70.4
7.97±3.82
24
69.9
8.06±4.01
2.4 自制试剂的使用期 自制试剂Ⅱ在室温下放置不同时间后制备的样品,经FCM分析表明,该试剂在室温下放置45d后,对白细胞的分群无影响(图3)。

, http://www.100md.com
图3 自制试剂Ⅱ的使用期
2 讨论
在全血样品的FCM分析中,样品制备的好坏直接影响测定的结果,目前用于FCM全血样品制备的方法有3种[8]:①用荧光抗体染色全血,然后溶解红细胞;②将红细胞溶解后再进行荧光染色;③通过梯度离心分离出所需的细胞,再进行荧光染色。后两种方法由于操作繁琐,在直接免疫荧光染色中应用较少;而第1种方法是目前使用最多的方法,且可自动制样。该法一般需要染色、溶解红细胞、稳定荧光复合物和固定细胞等步骤。其中红细胞溶解程度是操作中的关键步骤,溶解过度或不足都会影响测定结果的准确性。
免疫学样品制备仪可将荧光染色后的全血样品自动完成红细胞溶解、荧光复合物稳定和细胞固定,从而大大降低了制样误差。但由于用于该仪器的专用试剂费用较高,可使制样的成本提高,不利于FCM的广泛应用。我们研制的自制试剂Ⅱ由溶解剂、稳定剂和固定剂3部分组成,经与进口试剂进行对比试验表明,对白细胞的分群、CD3+淋巴细胞的百分率和CD3分子的表达量、染色结果的稳定性,以及试剂在室温下保存的稳定性等,均达到了进口试剂的效果,而自制试剂的成本只有进口试剂的2%。
, 百拇医药
作者简介:曹云新,女,39岁,实验师。西安市长乐西路17号,Tel.(029)3374573
参考文献
[1]宋根平,李素文.流式细胞术的原理和应用.北京师范大学出版社,北京:1992:140~252
[2]Davies EG, Levinsky RJ, Butter M, et al.Lymphocyte subpopulations in primary immunodeficience disorders. Arch Dis Child, 1983; 58:346~351
[3]Shackney SE.The use of flow cytometry in the diagnosis and biological characterization of the non-Hodgkin′s lymphomas. Ann NY Acad Sci,1986;468:171~177
, http://www.100md.com
[4]Eichner RD. LAV/HTLV-Ⅲ plays a dominant role in the etiology of AIDS. AIDS Res, 1984; 1(4):237~241
[5]Caldwell CW,Taylor HM. A rapid no-wash technique for Immunophenotypic analysis by flow cytometry. Am J Clin Path, 1986; 86(5):600~607
[6]Barker JW. An innovative lymphocyte preparation system for flow cytometry.Am Clin Lab, 1988; 7(7):32~39
[7]Kotylo PK.Rapid analysis of lymphocyte subsets in cord blood. Am J Clin Path, 1990; 93(2):263~ 266
[8]蔡文琴,王伯
 .实用免疫细胞化学与核酸分子杂交技术.四川科学技术出版社,成都:1994:214~221
.实用免疫细胞化学与核酸分子杂交技术.四川科学技术出版社,成都:1994:214~221收稿:1998-08-03
修回:1998-10-08, 百拇医药