IFN-α/HBVPreS2融合基因表达载体的构建和表达
作者:徐东平 王福生 施红 韩风连 程云 金磊
单位:徐东平(解放军302医院生物工程室);王福生(解放军302医院生物工程室);施红(解放军302医院生物工程室);韩风连(解放军302医院生物工程室);程云(免疫研究室,北京100039);金磊(解放军302医院生物工程室)
关键词:HBVPreS2;α-干扰素;融合蛋白
细胞与分子免疫学杂志000204
摘要:目的 构建IFN-α/HBVPreS2融合基因表达载体并进行表达。方法 采用PCR技术分别扩增IFN-α2b和HBVPreS2编码基因片段,并经分步克隆获得IFN-α/HBVPreS2融合基因。然后将其插入质粒pBV220,构建重组表达载体pBV-IFN-PreS2。结果 经转化E.coli后,诱导表达出相对分子质量(Mr)为27000的融合蛋白。SDS-PAGE分析显示,表达量占菌体总蛋白质的15%。Westemblot分析表明,表达蛋白能与抗IFN-α2b抗体结合。结论 IFN-α/HBVPreS2融合基因表达载体的构建,为进一步探讨HBV感染的特异性免疫治疗提供了实验依据。
, 百拇医药
中图号:R392.11
文献标识码:A
文章编号:1007-8738(2000)02-0103-03
Construction and expression of a recombinant expresson vector for IFN- α 2b/HBV Pre S2 fusion gene
XU Dong- ping
(1Department ofBiological Engineering)
WANG Fu- sheng
(1Department ofBiological Engineering)
, 百拇医药
(1Department ofBiological Engineering)
SHI Hong
(1Department ofBiological Engineering)
HAN Feng- lian
(1Department ofBiological Engineering)
CHENG Yun
(Department of Immunology, 302 Hospital of PLA, Beijing 100039, China)
JIN Lei
, 百拇医药
(1Department ofBiological Engineering)
Abstract: Aim To construct and express a recombinant expression vector bearing IFN- α 2b/HBV pre S2 fusiongene. Methods Through PCR and recombinant DNA techniques, the full length of cDNA encoding human IFN- α 2band HBV Pre S2 were respectively amplified and then together cloned into vector pBV220 in fusion form. Thus, arecombinant vector pBV- IFN- Pre S2 expressing human IFN- α 2b and HBV Pre S2 was successfullconstructed. Results After temperature induction, a fusion protein with relative molecule mass(Mr) of 27 000 wasexpressed, representing 15% of total bacterial protein in E.coli. Western blot analysis showed the protein could bebinded with anti- IFN- α 2b antibody. Conclusion The successful construction of the vector might provide anexperimental basis for specific immunotherapy for HBV infection.
, http://www.100md.com
Keywords: HBV Pre S2; interfcron- α ; fusion protein
目前,针对乙型肝炎的抗病毒治疗药物中IFN-α仍为临床上首选药物,但其疗效不够理想。提高IFN-α疗效的一个思路是在IFN-α分子中连接上抗体或配体分子,以使药物的作用具有靶向性,从而提高其在局部的浓度。HBVPreS2基因编码蛋白含55个氨基酸残基,具有多聚人血清白蛋白受体(PHSA-R)活性。在PHSA介导下,HBV可与人肝细胞表面的PHSA-R结合,为HBV感染具有嗜肝性的重要机制之一〔1,2〕。将HBVPreS2基因与IFN-α基因融合后表达的融合蛋白,若能保持二者的生物学活性,就有可能通过PHSA-R的结合作用将融合分子导向肝细胞,达到靶向给药的目的。此外,IFN-α为一种多功能的免疫调节因子,与HBVPreS2的融合表达产物有可能增强PreS2抗原递呈的效能,增强机体对HBV的免疫应答。我们采用基因重组技术,构建了IFN-α/HBVPreS2融合基因表达载体pBV-IFN-PreS2,并在E.coli中表达了IFN-PreS2融合蛋白。
, 百拇医药
1 材料和方法
1.1 材料 含有头尾相连HBV ayw全长DNA双体的pCP10质粒,E.coli表达载体pBV220和DH-5α菌株,均由军事医学科学院逯好英教授提供。含有人IFN-α2b编码基因的pB-IFN质粒由本室构建。pGEM3Zf(-)质粒购自华美公司。工具酶购自美国Promega公司和华美公司。PCR产物纯化试剂盒为美国Clontech公司产品。抗人IFN-α 2bHRP标记物为邦定医学生物公司产品。转膜用硝酸纤维素滤膜为美国Schlcher & Schuell公司产品。PCR引物由 上海生物工程公司合成。
1.2 方法
1.2.1 重组质粒的构建 利用设计的两对引物,分别从质粒 模板中扩增498bp的IFN-α 2b编码基因片段(引物P1+P2扩增pB-IFN)和165 bp的HBVPreS2基因片段(引物P3+P4扩增pCP10),引物的序列如下:
, 百拇医药
P1:5′-GGAATTCATGTGTGACCTGCCGCA-3′;
P2:5′-GGGGATCCTGGGCTTTCTTTAGAACGCAGA-3′;
P3:5′-CGGGATCCATGCAGTGGAATTCCA-3′;
P4:5′-GCGTCGACTTAGTTCAGCGCAGGGTC-3′.
采用分步克隆法,即先将IFN-α 2b编码基因克隆入载体pGEM3Zf(-),再利用基因间连接序列上设计的BamHI位点,将HBV Pre S2基因连接到IFN-α 2b基因的3′末端,转化JM109菌,获得含有融合基因的pGEM-IFN-PreS2克隆。连接序列为AGCCCAGGATCC,编码丝氨酸-脯氨酸-甘氨酸-丝氨酸。提取重组质粒,用EcoR I+Sal I双酶切获取690bp的融合基因片段,与用相同酶切处理的载体pBV220连接,转化DH-5α宿主菌,获得pBV-IFN-PreS2表达克隆。然后,对重组质粒进行酶切和DNA序列的 分析鉴定(图1)。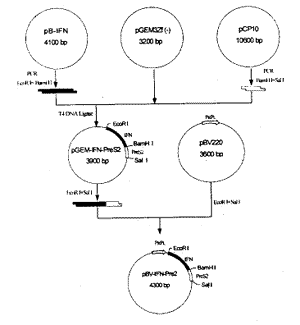
, 百拇医药
图1 融合干扰素基因重组质粒的构建
Fig1 Construction of expression plasmid pBV-IFN-PreS2
1.2.2 融合蛋白的表达 挑取pBV-IFN-PreS2表达克隆单菌落,接种于LB培养基进行一级扩增。扩增产物以1∶5接种于M9CA培养基,在30℃振荡培养6~7h后,升温至42℃诱导表达4h,离心收集菌体。菌体经溶菌酶和DNaseI酶处理后,置冰浴进行超声粉碎。粉碎液经4℃离心(12000r/min)15min,收集沉淀即为粗制包 涵体。
1.2.3 Westernblot 参照文献〔3〕的方法进行电泳和转膜,所用滤膜为0.45μm孔径的硝酸纤维素滤膜,用抗IFN-α mAb-HRP 进行检测。
2 结果
, 百拇医药
2.1 融合基因的构建 经酶切和DNA序列分析证实,构建的融合基因同预期的结果完全相符。融合基因的DNA序列测定结果 见图2。
图2 人IFN-α2b/HBV Pre S2融合基因的序列
Fig2 Sequence of human IFN-α2b/HBV PreS2 fusion gene
====Linking sequence between two genes;
GAA TTC EcoR I site;GTC GAC sal I site.
2.2 融合蛋白的表达 重组人IFN-α 2b分子由166个氨基酸残基组成,相对分子质量(Mr)为19000;HBV Pre S2分子由55个氨基酸残基组成,加上连接序列编码的4个氨基酸残基,融合基因编码的IFN-PreS2融合蛋白共含225个氨基酸残基,推测其Mr为25000~27000。SDS-PAGE分析表明,pBV-IFN-PreS2转化菌经温度诱导后,在Mr27000处有1条明显的表达带,其Mr的大小与推测的融合蛋白的Mr相一致。表达量占菌体总蛋白的15%。离心后收集的粗制包涵体中,目的蛋白的含量达到总蛋白的70%以上。SDS-PAGE的结果见图3,所用聚 丙烯酰胺凝胶的质量浓度为120g/L。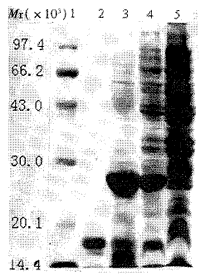
, http://www.100md.com
图3 融合蛋白的SDS-PAGE鉴定
Fig3 SDS-PAGE analysis for IFN-Pre S2 fusion protein
1:Marker(Mr);2:rhIFN-α;3:Inclusion body;
4:Lysate of induced bac teria;5:Lysate of uninduced bacteria.
2.3 Westernblot 表达蛋白按照常规的方法经SDS-PAGE后,再电泳转膜,用抗IFN-α mAb-HRP检测,在Mr27000处可清晰 地发现1条抗原、抗体特异性结合带(图4)。
图4 融合蛋白的Western blot分析
, http://www.100md.com
Fig4 Western blot analysis for fusion protein
M:Marker(Mr)(staining with amino black 10B);
1,2:Fusion protein probing with anti-IFNα mAb-HRP;
3:DH5α control(probing with anti-IFNα mAb-HRP).
3 讨论
HBV Pre S2蛋白的重要特性之一,是具有PHSAR活性,在PHSA介导下可与肝细胞膜上的同类受体结合,成为HBV嗜肝性感染的重要机制之一。HBV Pre S2基因的编码产物含有人T细胞和B细胞
, 百拇医药
识别表位,可诱导机体产生保护性免疫应答〔4〕。将具有免疫学活性的细胞因子,如IL-2基因与Pre S2基因进行融合表达,可显著增强Pre S2的抗原递呈效能〔5〕。近来研究还表明,Pre S2基因的编码产物对于维持HBV颗粒的完整性及其感染性至关重要〔6〕。将人IFN-α和HBV Pre S2基因融合表达产生的融合蛋白,有可能通过PHSA-R的活性介导IFN-α分子结合至肝细胞上,并增强Pre S2分子诱导机体产生有效的保护性免疫应答。为此,IFN-α /HBV Pre S2融合基因表达载体的构建,为进一步开展与防治HBV感染有关的研究奠定了必要的实验基础。
作者简介:徐东平,男,38岁,硕士,副研究员北京市丰台路26号,Tel.(010)66933333
2000byJCellMolImmunolPress www.immunology.net/jcmi;Email.immuedit@fmmu.edu.cn
, http://www.100md.com
参考文献:
〔1〕 Ohnuma H, Takahashi K, Kishimoto S, et al. Large hepatitis B surface antigen polypeptides of Dane particles
with the receptor for polymerized human serum albumin〔 J〕 . Gastroenterology, 1986;90:695- 701.
〔2〕 成军, 杨守 ,主编 . 现代肝炎病毒分子生物学〔 M〕 .北京 :人民军医出版社 ,1997: 25- 43.
〔3〕 Sambrook J, Fritsch EF, Maniatis T. Molecular Cloning〔 M〕 . 2nd ed. Cold Spring Harbor Laboratory
, http://www.100md.com
Press, 1989:1860- 1874.
〔4〕 Chenghua S, Cheng C, Jingsheng Z, et al. Gene fusion of cholera toxin B subunit and HBV pre S2 epitope and
the antigenicity of fusion protein〔 J〕 . Vaccine, 1995;13(10):933- 937.
〔5〕 陈章国 ,马大龙,张颖妹,等 .白细胞介素2-乙型肝炎病毒前S抗原融合蛋白的免疫原性 研究〔 J〕. 中华医学杂志,1996;76(1):34- 37.
〔6〕 Seyec JL, Chouteau P, Cannie I, et al. Role of the pre- S2 domain of the large envelope protein in hepatitis B
virus assembly and infectivity〔 J〕 . J Virol, 1998;72(7):5573- 5578.
收稿日期:1999-07-02
修回日期:1999-09-08, http://www.100md.com
单位:徐东平(解放军302医院生物工程室);王福生(解放军302医院生物工程室);施红(解放军302医院生物工程室);韩风连(解放军302医院生物工程室);程云(免疫研究室,北京100039);金磊(解放军302医院生物工程室)
关键词:HBVPreS2;α-干扰素;融合蛋白
细胞与分子免疫学杂志000204
摘要:目的 构建IFN-α/HBVPreS2融合基因表达载体并进行表达。方法 采用PCR技术分别扩增IFN-α2b和HBVPreS2编码基因片段,并经分步克隆获得IFN-α/HBVPreS2融合基因。然后将其插入质粒pBV220,构建重组表达载体pBV-IFN-PreS2。结果 经转化E.coli后,诱导表达出相对分子质量(Mr)为27000的融合蛋白。SDS-PAGE分析显示,表达量占菌体总蛋白质的15%。Westemblot分析表明,表达蛋白能与抗IFN-α2b抗体结合。结论 IFN-α/HBVPreS2融合基因表达载体的构建,为进一步探讨HBV感染的特异性免疫治疗提供了实验依据。
, 百拇医药
中图号:R392.11
文献标识码:A
文章编号:1007-8738(2000)02-0103-03
Construction and expression of a recombinant expresson vector for IFN- α 2b/HBV Pre S2 fusion gene
XU Dong- ping
(1Department ofBiological Engineering)
WANG Fu- sheng
(1Department ofBiological Engineering)
, 百拇医药
(1Department ofBiological Engineering)
SHI Hong
(1Department ofBiological Engineering)
HAN Feng- lian
(1Department ofBiological Engineering)
CHENG Yun
(Department of Immunology, 302 Hospital of PLA, Beijing 100039, China)
JIN Lei
, 百拇医药
(1Department ofBiological Engineering)
Abstract: Aim To construct and express a recombinant expression vector bearing IFN- α 2b/HBV pre S2 fusiongene. Methods Through PCR and recombinant DNA techniques, the full length of cDNA encoding human IFN- α 2band HBV Pre S2 were respectively amplified and then together cloned into vector pBV220 in fusion form. Thus, arecombinant vector pBV- IFN- Pre S2 expressing human IFN- α 2b and HBV Pre S2 was successfullconstructed. Results After temperature induction, a fusion protein with relative molecule mass(Mr) of 27 000 wasexpressed, representing 15% of total bacterial protein in E.coli. Western blot analysis showed the protein could bebinded with anti- IFN- α 2b antibody. Conclusion The successful construction of the vector might provide anexperimental basis for specific immunotherapy for HBV infection.
, http://www.100md.com
Keywords: HBV Pre S2; interfcron- α ; fusion protein
目前,针对乙型肝炎的抗病毒治疗药物中IFN-α仍为临床上首选药物,但其疗效不够理想。提高IFN-α疗效的一个思路是在IFN-α分子中连接上抗体或配体分子,以使药物的作用具有靶向性,从而提高其在局部的浓度。HBVPreS2基因编码蛋白含55个氨基酸残基,具有多聚人血清白蛋白受体(PHSA-R)活性。在PHSA介导下,HBV可与人肝细胞表面的PHSA-R结合,为HBV感染具有嗜肝性的重要机制之一〔1,2〕。将HBVPreS2基因与IFN-α基因融合后表达的融合蛋白,若能保持二者的生物学活性,就有可能通过PHSA-R的结合作用将融合分子导向肝细胞,达到靶向给药的目的。此外,IFN-α为一种多功能的免疫调节因子,与HBVPreS2的融合表达产物有可能增强PreS2抗原递呈的效能,增强机体对HBV的免疫应答。我们采用基因重组技术,构建了IFN-α/HBVPreS2融合基因表达载体pBV-IFN-PreS2,并在E.coli中表达了IFN-PreS2融合蛋白。
, 百拇医药
1 材料和方法
1.1 材料 含有头尾相连HBV ayw全长DNA双体的pCP10质粒,E.coli表达载体pBV220和DH-5α菌株,均由军事医学科学院逯好英教授提供。含有人IFN-α2b编码基因的pB-IFN质粒由本室构建。pGEM3Zf(-)质粒购自华美公司。工具酶购自美国Promega公司和华美公司。PCR产物纯化试剂盒为美国Clontech公司产品。抗人IFN-α 2bHRP标记物为邦定医学生物公司产品。转膜用硝酸纤维素滤膜为美国Schlcher & Schuell公司产品。PCR引物由 上海生物工程公司合成。
1.2 方法
1.2.1 重组质粒的构建 利用设计的两对引物,分别从质粒 模板中扩增498bp的IFN-α 2b编码基因片段(引物P1+P2扩增pB-IFN)和165 bp的HBVPreS2基因片段(引物P3+P4扩增pCP10),引物的序列如下:
, 百拇医药
P1:5′-GGAATTCATGTGTGACCTGCCGCA-3′;
P2:5′-GGGGATCCTGGGCTTTCTTTAGAACGCAGA-3′;
P3:5′-CGGGATCCATGCAGTGGAATTCCA-3′;
P4:5′-GCGTCGACTTAGTTCAGCGCAGGGTC-3′.
采用分步克隆法,即先将IFN-α 2b编码基因克隆入载体pGEM3Zf(-),再利用基因间连接序列上设计的BamHI位点,将HBV Pre S2基因连接到IFN-α 2b基因的3′末端,转化JM109菌,获得含有融合基因的pGEM-IFN-PreS2克隆。连接序列为AGCCCAGGATCC,编码丝氨酸-脯氨酸-甘氨酸-丝氨酸。提取重组质粒,用EcoR I+Sal I双酶切获取690bp的融合基因片段,与用相同酶切处理的载体pBV220连接,转化DH-5α宿主菌,获得pBV-IFN-PreS2表达克隆。然后,对重组质粒进行酶切和DNA序列的 分析鉴定(图1)。

, 百拇医药
图1 融合干扰素基因重组质粒的构建
Fig1 Construction of expression plasmid pBV-IFN-PreS2
1.2.2 融合蛋白的表达 挑取pBV-IFN-PreS2表达克隆单菌落,接种于LB培养基进行一级扩增。扩增产物以1∶5接种于M9CA培养基,在30℃振荡培养6~7h后,升温至42℃诱导表达4h,离心收集菌体。菌体经溶菌酶和DNaseI酶处理后,置冰浴进行超声粉碎。粉碎液经4℃离心(12000r/min)15min,收集沉淀即为粗制包 涵体。
1.2.3 Westernblot 参照文献〔3〕的方法进行电泳和转膜,所用滤膜为0.45μm孔径的硝酸纤维素滤膜,用抗IFN-α mAb-HRP 进行检测。
2 结果
, 百拇医药
2.1 融合基因的构建 经酶切和DNA序列分析证实,构建的融合基因同预期的结果完全相符。融合基因的DNA序列测定结果 见图2。

图2 人IFN-α2b/HBV Pre S2融合基因的序列
Fig2 Sequence of human IFN-α2b/HBV PreS2 fusion gene
====Linking sequence between two genes;
GAA TTC EcoR I site;GTC GAC sal I site.
2.2 融合蛋白的表达 重组人IFN-α 2b分子由166个氨基酸残基组成,相对分子质量(Mr)为19000;HBV Pre S2分子由55个氨基酸残基组成,加上连接序列编码的4个氨基酸残基,融合基因编码的IFN-PreS2融合蛋白共含225个氨基酸残基,推测其Mr为25000~27000。SDS-PAGE分析表明,pBV-IFN-PreS2转化菌经温度诱导后,在Mr27000处有1条明显的表达带,其Mr的大小与推测的融合蛋白的Mr相一致。表达量占菌体总蛋白的15%。离心后收集的粗制包涵体中,目的蛋白的含量达到总蛋白的70%以上。SDS-PAGE的结果见图3,所用聚 丙烯酰胺凝胶的质量浓度为120g/L。

, http://www.100md.com
图3 融合蛋白的SDS-PAGE鉴定
Fig3 SDS-PAGE analysis for IFN-Pre S2 fusion protein
1:Marker(Mr);2:rhIFN-α;3:Inclusion body;
4:Lysate of induced bac teria;5:Lysate of uninduced bacteria.
2.3 Westernblot 表达蛋白按照常规的方法经SDS-PAGE后,再电泳转膜,用抗IFN-α mAb-HRP检测,在Mr27000处可清晰 地发现1条抗原、抗体特异性结合带(图4)。

图4 融合蛋白的Western blot分析
, http://www.100md.com
Fig4 Western blot analysis for fusion protein
M:Marker(Mr)(staining with amino black 10B);
1,2:Fusion protein probing with anti-IFNα mAb-HRP;
3:DH5α control(probing with anti-IFNα mAb-HRP).
3 讨论
HBV Pre S2蛋白的重要特性之一,是具有PHSAR活性,在PHSA介导下可与肝细胞膜上的同类受体结合,成为HBV嗜肝性感染的重要机制之一。HBV Pre S2基因的编码产物含有人T细胞和B细胞
, 百拇医药
识别表位,可诱导机体产生保护性免疫应答〔4〕。将具有免疫学活性的细胞因子,如IL-2基因与Pre S2基因进行融合表达,可显著增强Pre S2的抗原递呈效能〔5〕。近来研究还表明,Pre S2基因的编码产物对于维持HBV颗粒的完整性及其感染性至关重要〔6〕。将人IFN-α和HBV Pre S2基因融合表达产生的融合蛋白,有可能通过PHSA-R的活性介导IFN-α分子结合至肝细胞上,并增强Pre S2分子诱导机体产生有效的保护性免疫应答。为此,IFN-α /HBV Pre S2融合基因表达载体的构建,为进一步开展与防治HBV感染有关的研究奠定了必要的实验基础。
作者简介:徐东平,男,38岁,硕士,副研究员北京市丰台路26号,Tel.(010)66933333
2000byJCellMolImmunolPress www.immunology.net/jcmi;Email.immuedit@fmmu.edu.cn
, http://www.100md.com
参考文献:
〔1〕 Ohnuma H, Takahashi K, Kishimoto S, et al. Large hepatitis B surface antigen polypeptides of Dane particles
with the receptor for polymerized human serum albumin〔 J〕 . Gastroenterology, 1986;90:695- 701.
〔2〕 成军, 杨守 ,主编 . 现代肝炎病毒分子生物学〔 M〕 .北京 :人民军医出版社 ,1997: 25- 43.
〔3〕 Sambrook J, Fritsch EF, Maniatis T. Molecular Cloning〔 M〕 . 2nd ed. Cold Spring Harbor Laboratory
, http://www.100md.com
Press, 1989:1860- 1874.
〔4〕 Chenghua S, Cheng C, Jingsheng Z, et al. Gene fusion of cholera toxin B subunit and HBV pre S2 epitope and
the antigenicity of fusion protein〔 J〕 . Vaccine, 1995;13(10):933- 937.
〔5〕 陈章国 ,马大龙,张颖妹,等 .白细胞介素2-乙型肝炎病毒前S抗原融合蛋白的免疫原性 研究〔 J〕. 中华医学杂志,1996;76(1):34- 37.
〔6〕 Seyec JL, Chouteau P, Cannie I, et al. Role of the pre- S2 domain of the large envelope protein in hepatitis B
virus assembly and infectivity〔 J〕 . J Virol, 1998;72(7):5573- 5578.
收稿日期:1999-07-02
修回日期:1999-09-08, http://www.100md.com