�ۺ�ø����Ӧ��Ͼ��ž���Ⱦ��ʵ���о�
���ߣ�����ƽ ʯҢ�� ��һƽ ������ ������ ���Ļ� �����
��λ��200040 �Ϻ�ҽ�ƴ�ѧ��ɽҽԺ(����ƽ��ʯҢ�ҡ���һƽ�����Ļ��������)���Ϻ�ҽ�ƴ�ѧ��ɽҽԺ(������)��������ѧ�����Ŵ��о���(������)
�ؼ��ʣ��ۺ�ø����Ӧ�����Ų��˾���������mip
�л���Ⱦ����־980312 ��ժҪ�� Ŀ�� ������Ͼ��ž���Ⱦ������ ���þۺ�ø����Ӧ(PCR)����ȷξ��ž�(Lp)mip�����������Ƭ�Σ���Ӧ���������˴��¾��ž�(Lm)��Ⱦ�����֯�걾��⡣��� ����������LpI�ͺ�Lm630bp��������Ƭ�Σ������ٴ������겻����ã����������Ϊ150fg���ž�������DNA(�൱��15��30�����ž�)����22��Lm��Ⱦ��ͬʱ���ȡ��������֯�걾��Ӧ�ø÷���������������Ƚ���ʾ���ڸ�Ⱦ��3.5��������������Ϊ88.9%��PCR��100%���ڸ�Ⱦ��7.5��������������Ϊ0����PCR������22.2%�������ʡ����� ���������С����죬���ܼ���ȷξ��ž������ܲ��Lm���������˾��Ų�������ʡ�
, http://www.100md.com
Study on the diagnosis of Legionella infection by polymerase chain reaction Zhu Liping, Shi Yaozhong, Cheng Yiping, et al. Department of Infectious Diseases, Hua Shan Hospital, Shanghai Medical University, Shanghai 200040
��Abstract�� Objective To diagnose the infection of legionella early. Methods Polymerase chain reaction(PCR) was used to amplify the specific fragment of Legionella pneumophila(Lp) mip gene, and the tissues of guinea pigs infected by Legionella micdadei were detected by the technique. Results The 630bp sequence of Lp and Lm were specifically amplified, whereas other clinical isolates could not be detected. The lower limit of detection was 150fg DNA of legionella (corresponding to 15��30 organisms). Twenty-two specimens were obtained from tissues of guinea pigs infected by Lm in different time courses, and then detected by PCR and culture, respectively. The positive rate of culture in 3.5 days after infection was 88.9%; however, the positive rate of PCR was 100%. In 7.5 days, all samples were negative by culture, nevertheless the positive rate of PCR was 22.2%. Conclusion These results indicated that the PCR assay was a specific and sensitive technique for the diagnosis of legionella infection.
, ��Ĵҽҩ
��Key words�� Polymerase chain reaction Legionella Gene mip
���Ų�(Legionnaires' disease)���ɾ��ž���Ⱦ�����һ�ּ��Դ�Ⱦ�Լ����������ٴ����ֲ�������ͨϸ���Է��������𣬹��ٴ��ϳ������δ����ʱ��Ϻ���Ч���������ƵĻ��ߣ������ʽϸߡ����У��˴��¾��ž�(Lm)��Ⱦ�÷�������ȱ�ݻ��ߡ���ˣ�����������൱��Ҫ���ٴ���ֵ��Ŀǰ���ϵ�ʵ������Ϸ�����Ҫ��Ѫ�忹��ⶨ��ֱ������ӫ�⿹�巨�����ž�����������������Կ�ԭ������̽���ӽ���[1]������ȱ��һ���ڼ�������ʹ�õ����С��������Ϸ�������ʵ��ּ�ڲ��þۺ�ø����Ӧ(PCR)�����ž�����Ӧ������������Lm��Ⱦ��
�����뷽��
һ�����꼰��DNA����ȡ
�ȷξ��ž�Ѫ����I��(Lp1)��Lm��������������CDC�����Ϻ�����������վ�ṩ��ͭ�̼ٵ��������˾���������θ˾������ɫ���������������Ѫ�˾���������������˾�����˸˾��������ٴ�������꣬���Ϻ�ҽ�ƴ�ѧ��ɽҽԺϸ���ҺͿ��������ṩ������֧ԭ�塢������ԭ��DNAΪPCR�����Լ����е�����DNAģ�壬������������˹�����Ƽ���������˾�ṩ�������DNA������õ���øK���������ȷ³���ľ��䷽������[2]������ֹ��ȷ��ⶨ����Lp1 DNA������
, http://www.100md.com
����PCR���PPCR����
(һ) ���� ѡ��Lp mip�������ڣ���������[3]�������Lmip-1��������Ϊ5��-GGTGACTGCGGCTGTTATGG-3�䣬����Lmip-2��������Ϊ5��-GGCCAATAGGTCCGCCAACG-3�䣬�������ﳤ��Ϊ630bp������ϳ�ί���й���ѧԺ�Ϻ����ﻯѧ�о�����ɡ�
(��) PCR���� ��25��l PCR��Ӧ��ϵ�У���10������Һ2.5��l������dNTP��0.2mmol/L������0.2��mol/L��ģ��DNA 5��l��1 U Taq DNA�ۺ�ø(�����Ϻ�Sangon���﹤�̹�˾)�������˫��ˮ�������25��l������ʯ������Һ�档���Һ��93��C����5���ӣ���PCR�Զ�ѭ����(�Ϻ�������˾����)������ѭ��40�Σ�ÿ��ѭ������Ϊ93��C 30�룬64��C 60�룬72��C 60�룬���һѭ����72��C����7���ӡ�
��������������֬��������Ӿ
, ��Ĵҽҩ
ȡ5��l���������1.5%��֬��������Ӿ���廯�Ҷ�Ⱦɫ��������¹۲죬�Գ���630bp����������Ϊ���Խ�������ա�174/Hae����Ϊ����������
�ġ�����ʵ��
����(250��400g)���Ϻ�ҽ�ƴ�ѧ���ﲿ�ṩ��ʵ��������7ֻ���ֱ�ǻע��108CFU/ml Lm��Һ1ml�����ڸ�Ⱦ��3.5�졢7.5�����������3ֻ�������������Խ��ʣ�����������2ֻ����ǻע��1ml���������ˮ��4�����ʡ���������ȡ�Ρ��Ρ�Ƣ��֯��������ѹӡ��BCYE��ƽ���Ѫƽ���ϣ����ֻ����֣���37��C��5%CO2����������4��7�죬�ò�Ƭ����������Ⱦɫ�����ٷ��������ȡ����֯�걾0.25g��������в���ĥ���Ƚ���DNA���ᡢPCR��������ͬǰ��������ȡС�����ʷ���֯��10%�������̶ֹ���ʯ��������Ƭ��HEȾɫ��
���
, http://www.100md.com
һ�������Ժ������Լ��
������Ա�����Lp1��Lm DNA��������������630bp������һ��DNA�������÷���������˾���ͭ�̼ٵ�����������֧ԭ�塢���˾���DNA��ģ��������δ��������������(ͼ1)�������Լ����Lp1 DNA��ģ��1��10�ݶ�ϡ�ͣ���С�����Ϊ150fg DNAƬ��(ͼ2)��
1.Lp1 2.Lm 3��8.�ٴ��������� 9.�հ���
ͼ1 PCR����Lp mip�����Ӿ���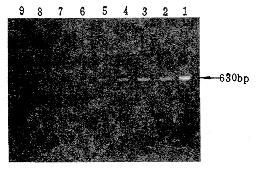
1��8.����Ϊ1.5��g��150ng��15ng��1.5ng��150pg��15pg��1.5pg��150fg��15fg Lp1 DNA��9.����
, http://www.100md.com
ͼ2 PCR����Lp mip���������Խ��
������֯�걾���
�ڸ�Ⱦ���3��1ֻ��������(�и�ˮ����)�����������ڸ�Ⱦ��3.5�졢7.5����ʣ�����22����֯�걾������������PCR�����������������������֯�걾��6�ݣ��������������ԡ�
���� ��Ⱦ��ͬʱ����������PCR��������ʱȽ� ��Ŀ
��Ⱦ������
3
3.5
7.5
������
100(4/4)
, http://www.100md.com
88.9(8/9)
0(9/9)
PCR
100(4/4)
100(9/9)
22.2(2/9)
ע�������ڷ���Ϊ���Ա걾������ĸΪ�걾����
������������Ⱦʱ����ӳ���������PCR���������ʾ����½���������Ⱦ���7.5�죬9�ݱ걾���������ԣ���PCR��������2�ݱ걾���ԡ�
�����Ⱦ��ķ���֯����������ڸ�Ⱦ������ڲ�ͬ�̶ȵ���֢�ı䣬�ɼ����ݱ�ëϸѪ�����š���Ѫ�����ݱ������ݼ������֢ϸ�������ݽṹ�����ƻ������ڸ�Ⱦ���没���ӳ�����֯�IJ����ı��Ϊ���أ������ױ������ȷξ��ž���Ⱦ����ģ�ͽ����һ��[4]������
, ��Ĵҽҩ
���²��Ծ��ž���Lpռ85%���ϣ�Lmռ8%���ϣ���Lm�����ҽԺ�ڸ�Ⱦ�����ȷξ��ž�����Ⱦ�������ƻ��ߣ��糤��ʹ����������Ƥ�ʼ��ء�������ֲ������������[5]����ˣ������ߵļ�������Ҫ���ٴ���ֵ�����ž���������������Ϊ��Ͼ��ž���Ⱦ�ġ�������������ٴ��걾�����Ӿ���Ⱦ�����ٴ��ϳ���BMPA����Ϊ��ѡ���������������Ʊ걾�е��Ӿ����ֿɴٽ����ž�������������Lm������ȴ����������[6��7]�������Lm��Ⱦ��ϴ��������ѡ�
Ŀǰ���ž�PCR��⣬���������������ɲ�����о��ž��������������²�����²��ԣ����������������ɲ���ȷξ��ž��������ܲ�����ȷε��²��Ծ��ž�[8��9]��������Jaulhac��[10��11]��������Lp mip����������Ƭ�ν�����������������Lm����������ͬԴ�Խϸߣ����Ƚ�����Lmip-1��LmͬԴ�Դ�76%��Lmip-2����ȫ��Lm��ԣ�����ʵ����һ�£�����Ч�ؼ��Lp��Lm�����ٴ������ĸ�Ⱦ���������������˾���ͭ�̼ٵ�����������֧ԭ�塢������ԭ��Ⱦ�������á�Jaulhac��[3]ʵ������ͬ����ʾ�ɲ���²��Ծ��ž�Lp��Lm��Lb���������ž���ϸ��������á�Lb���ԭ���в������
, http://www.100md.com
Ϊ�˽Ȿ�����������ԣ����ǽ�Lp1�����꾭���䷽�����ᴿ��DNA��1��10����ϡ�Ͳ�PCR������⣬����ɲ��150fg Lp������DNA���൱��15��30�����ž�������ⱨ���ļ��ˮƽ��һ��[8]��
22������Lm��Ⱦ�����֯�걾��Lm DNA�����������PCR�����������ɲ����֯�걾�е�Lm�����������ϱ����������Ⱦ��6����֯�о��ž��������½�[12��13]���ұ���ʵ��Ҳ��ʾ��Ⱦ���7.5������������Ϊ0�����ǣ�PCR����22.2%�������ʣ���ʾ�нϺõļ��Ч�����Ӹ÷����ij�������������˷������С����죬���Դ����߾��Ų�������ʡ�
�����
1 ����ƽ��ʯҢ��.���ž�������Ľ�չ.�л���Ⱦ����־��1995��13��40-42.
2 [��]��ά˹��.��������ѧ����ʵ�鷽��.���ڵ���.�Ϻ���������ѧ�����磬1989.305-307.
, ��Ĵҽҩ
3 Jaulhac B, Nowicki M, Bornstein N, et al. Detection of legionella spp. in bronchoalveolar lavage fluids by DNA amplification. J Clin Microbiol,1992,30:920-924.
4 Chander FW, McDade JE, Hicklin MD, et al. Pathologic findings in guinea pigs inoculated intraperitoneally with the Legionnaires' disease bacterium. Ann Inter Med,1979,90:671-675.
5 Muder RR, Yu VL. Other Legionella species. In: Mandell GL, Bennett JE, Dolin R, eds. Principles and practice of infectious diseases. 4th ed. New York: Churchill Livingstone,1995.2097-2103.
, ��Ĵҽҩ
6 Edelstein PH. Improved semiselective medium for isolation of Legionella pneumophila from contaminated clinical and enviromental specimens. J Clin Microbiol,1981,14:298-303.
7 Lee TC, Vickers RM, Yu VL, et al. Growth of 28 legionella species on selective culture media: A comparative study. J Clin Microbiol,1993,31:2764-2768.
8 Mahbubani MH, Bej AK, Miller R, et al. Detection of Legionella with polymerase chain reaction and gene probe methods. Mol Cell Probes,1990,4:175-187.
, ��Ĵҽҩ
9 Lindsay DSJ, Abraham WH, Fallon RJ. Detection of mip gene by PCR for diagnosis of Legionnaires' disease. J Clin Microbiol,1994,32:3068-3069.
10 Engleberg NC, Carter C, Weber DR, et al. DNA sequence of mip, a Legionella pneumophila gene associated with macrophage infectivity. Infect Immun,1989,57:1263-1270.
11 Bangsborg JM�� Cianciotto NP�� Hindersson P. Nucleotide sequence analysis of the Legionella micdadei mip gene, encoding a 30-kilodalton analog of the Legionella pneumophila mip protein. Infect Immun,1991,59:3836-3840.
, ��Ĵҽҩ
12 Brieland J, Freeman P, Kunkel R, et al. Replicative Legionella pneumophila lung infection in intratracheally inoculated A/J mice. A murine model of human Legionnaires' disease. Am J Pathol,1994,145:1537-1546.
13 Davis GS, Winn WC, Gump DW, et al. The kinetics of early inflammatory events during experimental pneumonia due to Legionella pneumophila in guinea pigs. J Infect Dis,1983,148:823-835., http://www.100md.com
��λ��200040 �Ϻ�ҽ�ƴ�ѧ��ɽҽԺ(����ƽ��ʯҢ�ҡ���һƽ�����Ļ��������)���Ϻ�ҽ�ƴ�ѧ��ɽҽԺ(������)��������ѧ�����Ŵ��о���(������)
�ؼ��ʣ��ۺ�ø����Ӧ�����Ų��˾���������mip
�л���Ⱦ����־980312 ��ժҪ�� Ŀ�� ������Ͼ��ž���Ⱦ������ ���þۺ�ø����Ӧ(PCR)����ȷξ��ž�(Lp)mip�����������Ƭ�Σ���Ӧ���������˴��¾��ž�(Lm)��Ⱦ�����֯�걾��⡣��� ����������LpI�ͺ�Lm630bp��������Ƭ�Σ������ٴ������겻����ã����������Ϊ150fg���ž�������DNA(�൱��15��30�����ž�)����22��Lm��Ⱦ��ͬʱ���ȡ��������֯�걾��Ӧ�ø÷���������������Ƚ���ʾ���ڸ�Ⱦ��3.5��������������Ϊ88.9%��PCR��100%���ڸ�Ⱦ��7.5��������������Ϊ0����PCR������22.2%�������ʡ����� ���������С����죬���ܼ���ȷξ��ž������ܲ��Lm���������˾��Ų�������ʡ�
, http://www.100md.com
Study on the diagnosis of Legionella infection by polymerase chain reaction Zhu Liping, Shi Yaozhong, Cheng Yiping, et al. Department of Infectious Diseases, Hua Shan Hospital, Shanghai Medical University, Shanghai 200040
��Abstract�� Objective To diagnose the infection of legionella early. Methods Polymerase chain reaction(PCR) was used to amplify the specific fragment of Legionella pneumophila(Lp) mip gene, and the tissues of guinea pigs infected by Legionella micdadei were detected by the technique. Results The 630bp sequence of Lp and Lm were specifically amplified, whereas other clinical isolates could not be detected. The lower limit of detection was 150fg DNA of legionella (corresponding to 15��30 organisms). Twenty-two specimens were obtained from tissues of guinea pigs infected by Lm in different time courses, and then detected by PCR and culture, respectively. The positive rate of culture in 3.5 days after infection was 88.9%; however, the positive rate of PCR was 100%. In 7.5 days, all samples were negative by culture, nevertheless the positive rate of PCR was 22.2%. Conclusion These results indicated that the PCR assay was a specific and sensitive technique for the diagnosis of legionella infection.
, ��Ĵҽҩ
��Key words�� Polymerase chain reaction Legionella Gene mip
���Ų�(Legionnaires' disease)���ɾ��ž���Ⱦ�����һ�ּ��Դ�Ⱦ�Լ����������ٴ����ֲ�������ͨϸ���Է��������𣬹��ٴ��ϳ������δ����ʱ��Ϻ���Ч���������ƵĻ��ߣ������ʽϸߡ����У��˴��¾��ž�(Lm)��Ⱦ�÷�������ȱ�ݻ��ߡ���ˣ�����������൱��Ҫ���ٴ���ֵ��Ŀǰ���ϵ�ʵ������Ϸ�����Ҫ��Ѫ�忹��ⶨ��ֱ������ӫ�⿹�巨�����ž�����������������Կ�ԭ������̽���ӽ���[1]������ȱ��һ���ڼ�������ʹ�õ����С��������Ϸ�������ʵ��ּ�ڲ��þۺ�ø����Ӧ(PCR)�����ž�����Ӧ������������Lm��Ⱦ��
�����뷽��
һ�����꼰��DNA����ȡ
�ȷξ��ž�Ѫ����I��(Lp1)��Lm��������������CDC�����Ϻ�����������վ�ṩ��ͭ�̼ٵ��������˾���������θ˾������ɫ���������������Ѫ�˾���������������˾�����˸˾��������ٴ�������꣬���Ϻ�ҽ�ƴ�ѧ��ɽҽԺϸ���ҺͿ��������ṩ������֧ԭ�塢������ԭ��DNAΪPCR�����Լ����е�����DNAģ�壬������������˹�����Ƽ���������˾�ṩ�������DNA������õ���øK���������ȷ³���ľ��䷽������[2]������ֹ��ȷ��ⶨ����Lp1 DNA������
, http://www.100md.com
����PCR���PPCR����
(һ) ���� ѡ��Lp mip�������ڣ���������[3]�������Lmip-1��������Ϊ5��-GGTGACTGCGGCTGTTATGG-3�䣬����Lmip-2��������Ϊ5��-GGCCAATAGGTCCGCCAACG-3�䣬�������ﳤ��Ϊ630bp������ϳ�ί���й���ѧԺ�Ϻ����ﻯѧ�о�����ɡ�
(��) PCR���� ��25��l PCR��Ӧ��ϵ�У���10������Һ2.5��l������dNTP��0.2mmol/L������0.2��mol/L��ģ��DNA 5��l��1 U Taq DNA�ۺ�ø(�����Ϻ�Sangon���﹤�̹�˾)�������˫��ˮ�������25��l������ʯ������Һ�档���Һ��93��C����5���ӣ���PCR�Զ�ѭ����(�Ϻ�������˾����)������ѭ��40�Σ�ÿ��ѭ������Ϊ93��C 30�룬64��C 60�룬72��C 60�룬���һѭ����72��C����7���ӡ�
��������������֬��������Ӿ
, ��Ĵҽҩ
ȡ5��l���������1.5%��֬��������Ӿ���廯�Ҷ�Ⱦɫ��������¹۲죬�Գ���630bp����������Ϊ���Խ�������ա�174/Hae����Ϊ����������
�ġ�����ʵ��
����(250��400g)���Ϻ�ҽ�ƴ�ѧ���ﲿ�ṩ��ʵ��������7ֻ���ֱ�ǻע��108CFU/ml Lm��Һ1ml�����ڸ�Ⱦ��3.5�졢7.5�����������3ֻ�������������Խ��ʣ�����������2ֻ����ǻע��1ml���������ˮ��4�����ʡ���������ȡ�Ρ��Ρ�Ƣ��֯��������ѹӡ��BCYE��ƽ���Ѫƽ���ϣ����ֻ����֣���37��C��5%CO2����������4��7�죬�ò�Ƭ����������Ⱦɫ�����ٷ��������ȡ����֯�걾0.25g��������в���ĥ���Ƚ���DNA���ᡢPCR��������ͬǰ��������ȡС�����ʷ���֯��10%�������̶ֹ���ʯ��������Ƭ��HEȾɫ��
���
, http://www.100md.com
һ�������Ժ������Լ��
������Ա�����Lp1��Lm DNA��������������630bp������һ��DNA�������÷���������˾���ͭ�̼ٵ�����������֧ԭ�塢���˾���DNA��ģ��������δ��������������(ͼ1)�������Լ����Lp1 DNA��ģ��1��10�ݶ�ϡ�ͣ���С�����Ϊ150fg DNAƬ��(ͼ2)��

1.Lp1 2.Lm 3��8.�ٴ��������� 9.�հ���
ͼ1 PCR����Lp mip�����Ӿ���

1��8.����Ϊ1.5��g��150ng��15ng��1.5ng��150pg��15pg��1.5pg��150fg��15fg Lp1 DNA��9.����
, http://www.100md.com
ͼ2 PCR����Lp mip���������Խ��
������֯�걾���
�ڸ�Ⱦ���3��1ֻ��������(�и�ˮ����)�����������ڸ�Ⱦ��3.5�졢7.5����ʣ�����22����֯�걾������������PCR�����������������������֯�걾��6�ݣ��������������ԡ�
���� ��Ⱦ��ͬʱ����������PCR��������ʱȽ� ��Ŀ
��Ⱦ������
3
3.5
7.5
������
100(4/4)
, http://www.100md.com
88.9(8/9)
0(9/9)
PCR
100(4/4)
100(9/9)
22.2(2/9)
ע�������ڷ���Ϊ���Ա걾������ĸΪ�걾����
������������Ⱦʱ����ӳ���������PCR���������ʾ����½���������Ⱦ���7.5�죬9�ݱ걾���������ԣ���PCR��������2�ݱ걾���ԡ�
�����Ⱦ��ķ���֯����������ڸ�Ⱦ������ڲ�ͬ�̶ȵ���֢�ı䣬�ɼ����ݱ�ëϸѪ�����š���Ѫ�����ݱ������ݼ������֢ϸ�������ݽṹ�����ƻ������ڸ�Ⱦ���没���ӳ�����֯�IJ����ı��Ϊ���أ������ױ������ȷξ��ž���Ⱦ����ģ�ͽ����һ��[4]������
, ��Ĵҽҩ
���²��Ծ��ž���Lpռ85%���ϣ�Lmռ8%���ϣ���Lm�����ҽԺ�ڸ�Ⱦ�����ȷξ��ž�����Ⱦ�������ƻ��ߣ��糤��ʹ����������Ƥ�ʼ��ء�������ֲ������������[5]����ˣ������ߵļ�������Ҫ���ٴ���ֵ�����ž���������������Ϊ��Ͼ��ž���Ⱦ�ġ�������������ٴ��걾�����Ӿ���Ⱦ�����ٴ��ϳ���BMPA����Ϊ��ѡ���������������Ʊ걾�е��Ӿ����ֿɴٽ����ž�������������Lm������ȴ����������[6��7]�������Lm��Ⱦ��ϴ��������ѡ�
Ŀǰ���ž�PCR��⣬���������������ɲ�����о��ž��������������²�����²��ԣ����������������ɲ���ȷξ��ž��������ܲ�����ȷε��²��Ծ��ž�[8��9]��������Jaulhac��[10��11]��������Lp mip����������Ƭ�ν�����������������Lm����������ͬԴ�Խϸߣ����Ƚ�����Lmip-1��LmͬԴ�Դ�76%��Lmip-2����ȫ��Lm��ԣ�����ʵ����һ�£�����Ч�ؼ��Lp��Lm�����ٴ������ĸ�Ⱦ���������������˾���ͭ�̼ٵ�����������֧ԭ�塢������ԭ��Ⱦ�������á�Jaulhac��[3]ʵ������ͬ����ʾ�ɲ���²��Ծ��ž�Lp��Lm��Lb���������ž���ϸ��������á�Lb���ԭ���в������
, http://www.100md.com
Ϊ�˽Ȿ�����������ԣ����ǽ�Lp1�����꾭���䷽�����ᴿ��DNA��1��10����ϡ�Ͳ�PCR������⣬����ɲ��150fg Lp������DNA���൱��15��30�����ž�������ⱨ���ļ��ˮƽ��һ��[8]��
22������Lm��Ⱦ�����֯�걾��Lm DNA�����������PCR�����������ɲ����֯�걾�е�Lm�����������ϱ����������Ⱦ��6����֯�о��ž��������½�[12��13]���ұ���ʵ��Ҳ��ʾ��Ⱦ���7.5������������Ϊ0�����ǣ�PCR����22.2%�������ʣ���ʾ�нϺõļ��Ч�����Ӹ÷����ij�������������˷������С����죬���Դ����߾��Ų�������ʡ�
�����
1 ����ƽ��ʯҢ��.���ž�������Ľ�չ.�л���Ⱦ����־��1995��13��40-42.
2 [��]��ά˹��.��������ѧ����ʵ�鷽��.���ڵ���.�Ϻ���������ѧ�����磬1989.305-307.
, ��Ĵҽҩ
3 Jaulhac B, Nowicki M, Bornstein N, et al. Detection of legionella spp. in bronchoalveolar lavage fluids by DNA amplification. J Clin Microbiol,1992,30:920-924.
4 Chander FW, McDade JE, Hicklin MD, et al. Pathologic findings in guinea pigs inoculated intraperitoneally with the Legionnaires' disease bacterium. Ann Inter Med,1979,90:671-675.
5 Muder RR, Yu VL. Other Legionella species. In: Mandell GL, Bennett JE, Dolin R, eds. Principles and practice of infectious diseases. 4th ed. New York: Churchill Livingstone,1995.2097-2103.
, ��Ĵҽҩ
6 Edelstein PH. Improved semiselective medium for isolation of Legionella pneumophila from contaminated clinical and enviromental specimens. J Clin Microbiol,1981,14:298-303.
7 Lee TC, Vickers RM, Yu VL, et al. Growth of 28 legionella species on selective culture media: A comparative study. J Clin Microbiol,1993,31:2764-2768.
8 Mahbubani MH, Bej AK, Miller R, et al. Detection of Legionella with polymerase chain reaction and gene probe methods. Mol Cell Probes,1990,4:175-187.
, ��Ĵҽҩ
9 Lindsay DSJ, Abraham WH, Fallon RJ. Detection of mip gene by PCR for diagnosis of Legionnaires' disease. J Clin Microbiol,1994,32:3068-3069.
10 Engleberg NC, Carter C, Weber DR, et al. DNA sequence of mip, a Legionella pneumophila gene associated with macrophage infectivity. Infect Immun,1989,57:1263-1270.
11 Bangsborg JM�� Cianciotto NP�� Hindersson P. Nucleotide sequence analysis of the Legionella micdadei mip gene, encoding a 30-kilodalton analog of the Legionella pneumophila mip protein. Infect Immun,1991,59:3836-3840.
, ��Ĵҽҩ
12 Brieland J, Freeman P, Kunkel R, et al. Replicative Legionella pneumophila lung infection in intratracheally inoculated A/J mice. A murine model of human Legionnaires' disease. Am J Pathol,1994,145:1537-1546.
13 Davis GS, Winn WC, Gump DW, et al. The kinetics of early inflammatory events during experimental pneumonia due to Legionella pneumophila in guinea pigs. J Infect Dis,1983,148:823-835., http://www.100md.com