卡托普利对家兔动脉粥样硬化纤溶酶原激活物抑制物-1基因表达的影响
作者:陈良华 陆国平 吴春芳 龚兰生
单位:陈良华(250021 济南市 山东省立医院心内科);陆国平 吴春芳 龚兰生(200025 上海市 上海第二医科大学附属瑞金医院心内科)
关键词:动脉粥样硬化;纤溶酶原激活物抑制物-1;卡托普利
岭南心血管病杂志000218 【摘要】 目的 研究卡托普利对家兔动脉粥样硬化纤溶酶原激活物抑制物-1(PAI-1)基因表达的影响。方法 37只家兔随机分为正常对照组、胆固醇喂养组、卡托普利组,饲养12周。取一段靠近升主动脉起始部的动脉做常规病理切片,一近端胸主动脉抽提总RNA,应用逆转录多聚酶链式反应测定PAI-1 mRNA的表达。结果 卡托普利尽管不影响血浆总胆固醇水平,但能抑制动脉粥样硬化的形成。而3组动脉壁PAI-1 mRNA的相对值分别为0.510±0.075、1.321±0.056、0.687±0.119,相互间有统计学差异(P<0.01)。结论 卡托普利能抑制动脉粥样硬化时PAI-1基因的过度表达,这种作用可能是血管紧张素转化酶抑制剂治疗效益的重要机制之一。
, http://www.100md.com
Effect of captopril on arterial gene expression of plasminogen activator inhibitor type 1 in atherosclerotic rabbits
Chen Lianghua
(Department of Cardiology, Shandong Provincial Hospital, Jinan 250021)
Lu Guoping,Wu Chunfang
(Department of Cardiology, Affiliated Hospital to Shanghai Second Medical University, Shanghai 200025)
, http://www.100md.com 【Abstract】 Objective To examine the effect of captopril on arterial gene expression of plasminogen activator inhibitor type 1 (PAI-1) in atherosclerotic rabbits. Methods Thir seven rabbits were randomly divided into 3 groups, i.e, control, cholesterol diet, captopril group, which were fed for 12 weeks. A segment of ascending aorta (0.5 cm) was obtained for pathologic slices, and another one from thoracic aorta (1 cm) for the measurement of PAI-1 mRNA using reverse transcription-polymerase reaction (RT-PCR).Results Captopril could not lower plasma total cholesterol, however it did inhibit the formation of atherosclerosis. The relative values of arterial PAI-1mRNA in 3 groups were 0.510±0.075,1.321±0.056,0.687±0.119, respectively with significant difference among them (P<0.01).Conclusion Captopril can inhibit excessive expression of arterial PAI-1 gene in atherosclerosis and this action may be one of the important mechanisms involved in clinical effect of angiotensin converting enzyme inhibitors.
, http://www.100md.com
【Key words】 Atherosclerosis Plasminogen activator inhibitor type 1 Captopril
纤溶酶原激活物抑制物-1(PAI-1)是纤溶系统中主要的抑制因素,其水平的增高必然导致纤维蛋白在体内沉积,尤其在血管壁内。后者可刺激血管平滑肌细胞增生并与低密度脂蛋白(LDL)特别是脂蛋白(a)[Lp(a)]结合而促进动脉粥样硬化(AS)斑块形成和发展,因而血浆PAI-1水平的升高认为是AS的危险因素[1]。而血管局部肾素-血管紧张素系统(renin angiotensin system, RAS)在AS的形成与发展中也起一定作用[2]。血管紧张素Ⅱ(angiotensin Ⅱ, Ang Ⅱ)直接注射于人体可引起循环PAI-1水平升高,提示RAS与纤溶系统存在某种内在联系[3]。最近,van Leeuwen等[4]通过体外研究表明卡托普利(captopril)可完全抑制大鼠主动脉平滑肌细胞Ang Ⅰ引起的PAI-1分泌,但尚无类似的体内研究。本研究即通过家兔AS模型观察卡托普利是否具有降低AS斑块中PAI-1基因过度表达的作用。
, http://www.100md.com
材料与方法
1.材料
新西兰纯种雄性大白兔由上海陈行实验用兔繁殖饲养场提供,胆固醇由上海生物化学试剂总公司提供,卡托普利购自江苏常州制药厂,TRIZOLRNA抽提试剂由GIBCOBRL提供,PAI-1活性测定试剂购自上海实业一医大生物技术有限公司,各种RT-PCR试剂购自华美生物技术公司。PAI-1引物根据文献报道[5]的cDNA序列合成,上游:5′ATGGAATTCCCGTGGAACAAGAATGAGATCAG3′,下游:5′TGAGCCATCATGGGCACAGAG3′,扩增片段大约360 bp,β-actin引物由中科院上海细胞生物研究所提供,上游:5′ATCTGGCACCACACCTTCTACAATGAGCTG3′,下游:5′CGTCATACTCCTGCTTGCTGATCCACATCTGC3′,扩增片段828bp。
, 百拇医药
2.方法
(1)实验分组: 27只白兔随机分为3组,即:正常对照组,7只,普通饲料喂养;胆固醇喂养组,10只,高脂高胆固醇饲养(胆固醇用量每天1 g/只,猪油为每天10 g/只,拌于普通饲料中);卡托普利(每天25 mg/kg)组,10只,高脂高胆固醇饲养加卡托普利。
(2)血浆总胆固醇及PAI-1活性测定:于高脂饲养前、饲养6周、12周时抽取血标本,分离得到血浆,用胆固醇氧化酶法测定血浆总胆固醇浓度,用发色底物法测定血浆PAI-1活性。
(3)病理形态学检查: 12周时处死动物,选取靠近升主动脉根部约0.5 cm左右的动脉段,置于10%中性福尔马林溶液中浸泡固定,常规酒精脱水,石蜡包埋,制成6 μm厚连续切片,光镜下观察形态学变化,计算平均最大脂纹厚度。
(4)胸主动脉总RNA抽提及RT-PCR反应:动物处死后选取靠近升主动脉起始处的胸主动脉约1 cm,迅速液氮冷冻并置于液氮罐中保存备用。将其迅速剪碎后加1 mL TRIzol试剂,置于组织匀浆器中匀浆,抽提总RNA,采用紫外分光光度计测定其浓度。取2 μg总RNA进行RT反应,RT体系20 μL含2 μg总RNA、随机引物100 ng、RNAsin 40U、M-MLV逆转录酶200U、NTP 1 mmol,每一标本取RT产物各5 μL进行PAI-1与β-actin的PCR反应。PCR反应体系含相应上、下游引物30 pmol、Taq酶2U。PAI-1 PCR反应条件:94℃15s,54℃ 30s,72℃ 30s,29个循环。β-actin PCR反应条件:94℃ 30s, 54℃ 1min, 72℃ 1min。首次循环均94℃ 3min,结束前72℃ 10min。各取PCR产物10 μL,经2%琼脂糖凝胶电泳,溴化乙锭染色、照相并经光密度仪扫描分析,以β-actin光密度值进行标准校正,计算PAI-1产物的相对量。计算公式:PAI-1相对量=PAI-1产物电泳条带密度/β-actin产物电泳条带密度。
, 百拇医药
3.统计学处理方法
所有指标用均数±标准差表示,采用t检验,以P<0.05差异有显著性。
结 果
1.血浆总胆固醇浓度及体重变化
从表1中可见,新西兰家兔喂饲胆固醇6周后,血浆总胆固醇水平显著升高,12周时增高更为明显,而卡托普利对血浆总胆固醇水平无影响,即无降低胆固醇作用。3组家兔处死前,体重均显著增加,但组间无统计学差异。
表1 血浆总胆固醇浓度及体重变化 组别
血浆总胆固醇浓度(mg/dL)
体重(kg)
0周
, 百拇医药
6周
12周
开始
结束
正常对照组
48.6±14.0
39.3±7.4
40.3±5.7
2.4±0.3
3.2±0.4
胆固醇喂养组
45.7±12.4
, http://www.100md.com 455.4±35.9*
1 015.3±46.2*
2.7±0.6
3.4±0.1*
卡托普利组
40.9±13.4
465.2±33.0*
1 023.0±68.5*
2.6±0.2
3.2±0.2*
, 百拇医药
注:*与0周时比较,P<0.01。
2.血浆PAI-1活性的改变
表2显示3组在0周、6周及12周时血浆PAI-1活性的变化。胆固醇喂养组在6周时即可见PAI-1活性升高(P<0.05),12周时尤为明显(P<0.01),而卡托普利对血浆PAI-1活性亦无影响。
3.病理形态学改变表2 血浆PAI-1活性变化 组别
PAI-1活性(Au/mL)
0周
6周
12周
正常对照组
, http://www.100md.com
5.6±2.6
6.8±1.4
4.8±2.2
胆固醇喂养组
4.9±3.1
7.7±1.1*
14.0±2.5**
卡托普利组
6.1±3.2
8.9±1.8*
14.0±4.7**
, 百拇医药
注:*与0周时比较,P<0.05;**与0周时比较,P<0.01。
肉眼观察可见胆固醇喂养组主动脉管壁有大量黄色脂样物向管腔凸出,从升主动脉起始部到胸主动脉远端脂纹逐渐减轻,卡托普利组脂纹数量明显减少。光镜下胆固醇喂养组动脉管腔不规则,内膜明显增厚,管壁弥漫性隆起,内含大量泡沫细胞,几乎覆盖整个管腔,中膜平滑肌细胞增生明显。卡托普利组动脉病变较胆固醇喂养组明显减轻,虽与正常对照组相比管腔扩大,中层平滑肌细胞有所增生,但内膜增厚不明显,呈局限性隆起,泡沫细胞数量减少。平均最大脂纹厚度(以占整个血管壁厚度的百分数表示)3组分别为0、(50±10)%、(20±9)%,相互间比较有显著性差异(P均<0.01),表明卡托普利组能抑制AS斑块的形成。
4.动脉壁PAI-1 mRNA表达的改变
所有PAI-1及β-actin的扩增产物经2%琼脂糖凝胶电泳,所示条带分别为大约360 bp和828 bp,符合设计的片段大小(图1)。3组动脉壁PAI-1 mRNA/β-actin mRNA比值分别为:0.510±0.075、1.321±0.056、0.687±0.119,相互间有显著性差异(P<0.01),表明AS血管局部PAI-1过度表达,而卡托普利能抑制这种过度表达。具体情形见图2。
, 百拇医药
讨 论
近年来的许多研究表明AS斑块中PAI-1 mRNA表达增强,且与AS的严重程度正相关,而TPA mRNA表达降低,玻璃体连接蛋白(vitronectin) mRNA表达亦增加,后者与PAI-1相结合,增强PAI-1的稳定性,即加强PAI-1的生物作用。因而粥样硬化性血管局部纤溶活性减弱,抗纤溶活性增强,使纤维蛋白易于沉积,促进了AS的发展[6,7]。本研究表明新西兰白兔喂食胆固醇3月后可见血浆PAI-1活性明显升高,主动脉PAI-1 mRNA表达增强。Sava等[6]通过Northern blot的方法发现新西兰白兔喂养胆固醇(2%)8周后血浆PAI-1活性增高2倍,主动脉PAI-1 mRNA表达增加,与我们的研究结果基本相符。
图1 PAI-1与β-actin RT-PCR扩增结果(M=PCR
, http://www.100md.com
marker; 1~4=β-actin扩增片段,828 bp;
5~7=PAI-扩增片段,大约360 bp)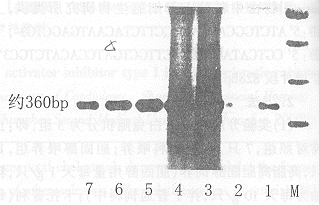
图2 卡托普利对家兔动脉粥样硬化PAI-1表达的影响
(M=PCR marker, 1、2分别为对照组,3~5
为胆固醇喂养组,6、7为卡托普利组)
AS时局部血管壁PAI-1 mRNA表达增加的机制,目前还很不清楚。体外研究发现很多因素都能刺激血管壁细胞(主要是内皮细胞及平滑肌细胞)PAI-1的分泌。其中主要有LDL、VLDL、Lp(a)、转化生长因子β(TGP-β)、肿瘤坏死因子(TNF)、血小板源性生长因子(PDGF)、白细胞介素-1(IL-1)等[1],1992年Vaugham等[8]发现Ang Ⅱ体外亦可诱导内皮细胞分泌PAI-1,但在体内哪一个占主导地位尚未明了。
, http://www.100md.com
血管紧张素转化酶抑制剂(ACEI)抗动脉粥样硬化的机制多种多样,但主要一点仍是抑制AngⅡ的生成。临床试验资料表明ACEI应用于心肌梗死后心功能不全的病人能减少再发冠脉血栓形成(recurrent coronary thrombosis)[9],因而可能Ang Ⅱ直接涉及到血栓过程。而PAI-1水平升高是再发冠脉血栓形成的一个危险标志[10]。1993年,Ridker等[3]观察到Ang Ⅱ直接注射于人体内可引起血PAI-1水平升高,强烈提示Ang Ⅱ与纤溶系统存在某种关联,而应用ACEI抑制AngⅡ的生成则有可能通过降低PAI-1的水平而发挥其抗血栓效应。van Leeuwen等[4]首次体外研究表明卡托普利(5 μg/mL)可完全抑制大鼠主动脉平滑肌细胞Ang Ⅰ引起的PAI-1刺激作用。本研究结果则表明卡托普利尽管对血浆总胆固醇水平及PAI-1活性无影响,但能抑制AS的形成和动脉壁局部PAI-1基因的过度表达,而这种局部抗血栓效应可能是ACEI临床效益的重要机制之一。
, 百拇医药
血浆PAI-1的来源主要有三个方面:血管内皮细胞,肝细胞及血小板,但何者占优,目前尚不明确[11]。本研究显示卡托普利尽管能降低血管壁PAI-1基因的表达,但对升高的血浆PAI-1活性无影响,同时我们还发现卡托普利不能降低高脂血症家兔肝脏PAI-1 mRNA的过度表达(结果未显示)。因而肝脏可能是血浆PAI-1的主要来源。
参考文献
1,陈良华,陆国平. 纤溶酶原激活物抑制物-1与动脉粥样硬化. 心血管病学进展,1999, 20:23~26
2,Dzau VJ. Circulating versus local renin-angiotensin system in cardiovascular homeostasis. Circulation, 1988, 77(suppl Ⅰ): Ⅰ4~Ⅰ13
, 百拇医药
3,Ridker PM, Gaboury CL, Conlin PR, et al. Stimulation of plasminogen activator inhibitor in vivo by infusion of angiotensin Ⅱ. Circulation, 1993, 87: 1969~1973
4,van Leeuwen RTJ, Kol A, Andreotti F, et al. Angiotensin Ⅱ increases plasminogen activator inhibitor type 1 and tissue-type plasminogen activator messenger RNA in cultured rat aortic smooth muscle cells. Circulation, 1994, 90: 362~368
5,Rea TJ, DeMattos RB, Pape ME. Hepatic expression of genes regulating lipid metabolism ion rabbits. J Lipid Res, 1993, 34: 1901~1910
, http://www.100md.com
6,Sava H, Sobel BE, Fujii S. Potentiation by hypercholesterolemia of the induction of aortic intramural synthesis of plasminogen activator inhibitor type 1 by endothelial injury. Circ Res, 1993, 73: 671~680
7,Robbie LA, Booth NA, Brown PAJ, et al. Inhibitors of fibrinolysis are elevated in atherosclerotic plaque. Arterioscler Thromb Vasc Biol, 1996, 16: 539~545
8,Vaughan DE, Shen C, Lazos SA. Angiotensin Ⅱ induces plasminogen activator inhibitor (PAI-1) in vitro. Circulation, 1992, 86(suppl Ⅰ): Ⅰ~557
, 百拇医药
9,Pfeffer MA, Braunwald E. Moye LA, et al. For the SAVE Investigators: Effects of captopril on mortality and morbidity in patients with left ventricular dysfunction after myocardial infarction. N Engl J Med, 1992, 327: 676~677
10,Hamsten A, Defaire U, Walldius G, et al. Plasminogen activator inhibitor in plasma: risk factor for recurrent myocardial infarction. Lancet, 1987, 2:3~9
11,Dawson S, Henney A. The status of PAI-1 as a risk factor for arterial and thrombotic disease: a review. Atherosclerosis, 1992, 95: 105~117, 百拇医药
单位:陈良华(250021 济南市 山东省立医院心内科);陆国平 吴春芳 龚兰生(200025 上海市 上海第二医科大学附属瑞金医院心内科)
关键词:动脉粥样硬化;纤溶酶原激活物抑制物-1;卡托普利
岭南心血管病杂志000218 【摘要】 目的 研究卡托普利对家兔动脉粥样硬化纤溶酶原激活物抑制物-1(PAI-1)基因表达的影响。方法 37只家兔随机分为正常对照组、胆固醇喂养组、卡托普利组,饲养12周。取一段靠近升主动脉起始部的动脉做常规病理切片,一近端胸主动脉抽提总RNA,应用逆转录多聚酶链式反应测定PAI-1 mRNA的表达。结果 卡托普利尽管不影响血浆总胆固醇水平,但能抑制动脉粥样硬化的形成。而3组动脉壁PAI-1 mRNA的相对值分别为0.510±0.075、1.321±0.056、0.687±0.119,相互间有统计学差异(P<0.01)。结论 卡托普利能抑制动脉粥样硬化时PAI-1基因的过度表达,这种作用可能是血管紧张素转化酶抑制剂治疗效益的重要机制之一。
, http://www.100md.com
Effect of captopril on arterial gene expression of plasminogen activator inhibitor type 1 in atherosclerotic rabbits
Chen Lianghua
(Department of Cardiology, Shandong Provincial Hospital, Jinan 250021)
Lu Guoping,Wu Chunfang
(Department of Cardiology, Affiliated Hospital to Shanghai Second Medical University, Shanghai 200025)
, http://www.100md.com 【Abstract】 Objective To examine the effect of captopril on arterial gene expression of plasminogen activator inhibitor type 1 (PAI-1) in atherosclerotic rabbits. Methods Thir seven rabbits were randomly divided into 3 groups, i.e, control, cholesterol diet, captopril group, which were fed for 12 weeks. A segment of ascending aorta (0.5 cm) was obtained for pathologic slices, and another one from thoracic aorta (1 cm) for the measurement of PAI-1 mRNA using reverse transcription-polymerase reaction (RT-PCR).Results Captopril could not lower plasma total cholesterol, however it did inhibit the formation of atherosclerosis. The relative values of arterial PAI-1mRNA in 3 groups were 0.510±0.075,1.321±0.056,0.687±0.119, respectively with significant difference among them (P<0.01).Conclusion Captopril can inhibit excessive expression of arterial PAI-1 gene in atherosclerosis and this action may be one of the important mechanisms involved in clinical effect of angiotensin converting enzyme inhibitors.
, http://www.100md.com
【Key words】 Atherosclerosis Plasminogen activator inhibitor type 1 Captopril
纤溶酶原激活物抑制物-1(PAI-1)是纤溶系统中主要的抑制因素,其水平的增高必然导致纤维蛋白在体内沉积,尤其在血管壁内。后者可刺激血管平滑肌细胞增生并与低密度脂蛋白(LDL)特别是脂蛋白(a)[Lp(a)]结合而促进动脉粥样硬化(AS)斑块形成和发展,因而血浆PAI-1水平的升高认为是AS的危险因素[1]。而血管局部肾素-血管紧张素系统(renin angiotensin system, RAS)在AS的形成与发展中也起一定作用[2]。血管紧张素Ⅱ(angiotensin Ⅱ, Ang Ⅱ)直接注射于人体可引起循环PAI-1水平升高,提示RAS与纤溶系统存在某种内在联系[3]。最近,van Leeuwen等[4]通过体外研究表明卡托普利(captopril)可完全抑制大鼠主动脉平滑肌细胞Ang Ⅰ引起的PAI-1分泌,但尚无类似的体内研究。本研究即通过家兔AS模型观察卡托普利是否具有降低AS斑块中PAI-1基因过度表达的作用。
, http://www.100md.com
材料与方法
1.材料
新西兰纯种雄性大白兔由上海陈行实验用兔繁殖饲养场提供,胆固醇由上海生物化学试剂总公司提供,卡托普利购自江苏常州制药厂,TRIZOLRNA抽提试剂由GIBCOBRL提供,PAI-1活性测定试剂购自上海实业一医大生物技术有限公司,各种RT-PCR试剂购自华美生物技术公司。PAI-1引物根据文献报道[5]的cDNA序列合成,上游:5′ATGGAATTCCCGTGGAACAAGAATGAGATCAG3′,下游:5′TGAGCCATCATGGGCACAGAG3′,扩增片段大约360 bp,β-actin引物由中科院上海细胞生物研究所提供,上游:5′ATCTGGCACCACACCTTCTACAATGAGCTG3′,下游:5′CGTCATACTCCTGCTTGCTGATCCACATCTGC3′,扩增片段828bp。
, 百拇医药
2.方法
(1)实验分组: 27只白兔随机分为3组,即:正常对照组,7只,普通饲料喂养;胆固醇喂养组,10只,高脂高胆固醇饲养(胆固醇用量每天1 g/只,猪油为每天10 g/只,拌于普通饲料中);卡托普利(每天25 mg/kg)组,10只,高脂高胆固醇饲养加卡托普利。
(2)血浆总胆固醇及PAI-1活性测定:于高脂饲养前、饲养6周、12周时抽取血标本,分离得到血浆,用胆固醇氧化酶法测定血浆总胆固醇浓度,用发色底物法测定血浆PAI-1活性。
(3)病理形态学检查: 12周时处死动物,选取靠近升主动脉根部约0.5 cm左右的动脉段,置于10%中性福尔马林溶液中浸泡固定,常规酒精脱水,石蜡包埋,制成6 μm厚连续切片,光镜下观察形态学变化,计算平均最大脂纹厚度。
(4)胸主动脉总RNA抽提及RT-PCR反应:动物处死后选取靠近升主动脉起始处的胸主动脉约1 cm,迅速液氮冷冻并置于液氮罐中保存备用。将其迅速剪碎后加1 mL TRIzol试剂,置于组织匀浆器中匀浆,抽提总RNA,采用紫外分光光度计测定其浓度。取2 μg总RNA进行RT反应,RT体系20 μL含2 μg总RNA、随机引物100 ng、RNAsin 40U、M-MLV逆转录酶200U、NTP 1 mmol,每一标本取RT产物各5 μL进行PAI-1与β-actin的PCR反应。PCR反应体系含相应上、下游引物30 pmol、Taq酶2U。PAI-1 PCR反应条件:94℃15s,54℃ 30s,72℃ 30s,29个循环。β-actin PCR反应条件:94℃ 30s, 54℃ 1min, 72℃ 1min。首次循环均94℃ 3min,结束前72℃ 10min。各取PCR产物10 μL,经2%琼脂糖凝胶电泳,溴化乙锭染色、照相并经光密度仪扫描分析,以β-actin光密度值进行标准校正,计算PAI-1产物的相对量。计算公式:PAI-1相对量=PAI-1产物电泳条带密度/β-actin产物电泳条带密度。
, 百拇医药
3.统计学处理方法
所有指标用均数±标准差表示,采用t检验,以P<0.05差异有显著性。
结 果
1.血浆总胆固醇浓度及体重变化
从表1中可见,新西兰家兔喂饲胆固醇6周后,血浆总胆固醇水平显著升高,12周时增高更为明显,而卡托普利对血浆总胆固醇水平无影响,即无降低胆固醇作用。3组家兔处死前,体重均显著增加,但组间无统计学差异。
表1 血浆总胆固醇浓度及体重变化 组别
血浆总胆固醇浓度(mg/dL)
体重(kg)
0周
, 百拇医药
6周
12周
开始
结束
正常对照组
48.6±14.0
39.3±7.4
40.3±5.7
2.4±0.3
3.2±0.4
胆固醇喂养组
45.7±12.4
, http://www.100md.com 455.4±35.9*
1 015.3±46.2*
2.7±0.6
3.4±0.1*
卡托普利组
40.9±13.4
465.2±33.0*
1 023.0±68.5*
2.6±0.2
3.2±0.2*
, 百拇医药
注:*与0周时比较,P<0.01。
2.血浆PAI-1活性的改变
表2显示3组在0周、6周及12周时血浆PAI-1活性的变化。胆固醇喂养组在6周时即可见PAI-1活性升高(P<0.05),12周时尤为明显(P<0.01),而卡托普利对血浆PAI-1活性亦无影响。
3.病理形态学改变表2 血浆PAI-1活性变化 组别
PAI-1活性(Au/mL)
0周
6周
12周
正常对照组
, http://www.100md.com
5.6±2.6
6.8±1.4
4.8±2.2
胆固醇喂养组
4.9±3.1
7.7±1.1*
14.0±2.5**
卡托普利组
6.1±3.2
8.9±1.8*
14.0±4.7**
, 百拇医药
注:*与0周时比较,P<0.05;**与0周时比较,P<0.01。
肉眼观察可见胆固醇喂养组主动脉管壁有大量黄色脂样物向管腔凸出,从升主动脉起始部到胸主动脉远端脂纹逐渐减轻,卡托普利组脂纹数量明显减少。光镜下胆固醇喂养组动脉管腔不规则,内膜明显增厚,管壁弥漫性隆起,内含大量泡沫细胞,几乎覆盖整个管腔,中膜平滑肌细胞增生明显。卡托普利组动脉病变较胆固醇喂养组明显减轻,虽与正常对照组相比管腔扩大,中层平滑肌细胞有所增生,但内膜增厚不明显,呈局限性隆起,泡沫细胞数量减少。平均最大脂纹厚度(以占整个血管壁厚度的百分数表示)3组分别为0、(50±10)%、(20±9)%,相互间比较有显著性差异(P均<0.01),表明卡托普利组能抑制AS斑块的形成。
4.动脉壁PAI-1 mRNA表达的改变
所有PAI-1及β-actin的扩增产物经2%琼脂糖凝胶电泳,所示条带分别为大约360 bp和828 bp,符合设计的片段大小(图1)。3组动脉壁PAI-1 mRNA/β-actin mRNA比值分别为:0.510±0.075、1.321±0.056、0.687±0.119,相互间有显著性差异(P<0.01),表明AS血管局部PAI-1过度表达,而卡托普利能抑制这种过度表达。具体情形见图2。
, 百拇医药
讨 论
近年来的许多研究表明AS斑块中PAI-1 mRNA表达增强,且与AS的严重程度正相关,而TPA mRNA表达降低,玻璃体连接蛋白(vitronectin) mRNA表达亦增加,后者与PAI-1相结合,增强PAI-1的稳定性,即加强PAI-1的生物作用。因而粥样硬化性血管局部纤溶活性减弱,抗纤溶活性增强,使纤维蛋白易于沉积,促进了AS的发展[6,7]。本研究表明新西兰白兔喂食胆固醇3月后可见血浆PAI-1活性明显升高,主动脉PAI-1 mRNA表达增强。Sava等[6]通过Northern blot的方法发现新西兰白兔喂养胆固醇(2%)8周后血浆PAI-1活性增高2倍,主动脉PAI-1 mRNA表达增加,与我们的研究结果基本相符。

图1 PAI-1与β-actin RT-PCR扩增结果(M=PCR
, http://www.100md.com
marker; 1~4=β-actin扩增片段,828 bp;
5~7=PAI-扩增片段,大约360 bp)

图2 卡托普利对家兔动脉粥样硬化PAI-1表达的影响
(M=PCR marker, 1、2分别为对照组,3~5
为胆固醇喂养组,6、7为卡托普利组)
AS时局部血管壁PAI-1 mRNA表达增加的机制,目前还很不清楚。体外研究发现很多因素都能刺激血管壁细胞(主要是内皮细胞及平滑肌细胞)PAI-1的分泌。其中主要有LDL、VLDL、Lp(a)、转化生长因子β(TGP-β)、肿瘤坏死因子(TNF)、血小板源性生长因子(PDGF)、白细胞介素-1(IL-1)等[1],1992年Vaugham等[8]发现Ang Ⅱ体外亦可诱导内皮细胞分泌PAI-1,但在体内哪一个占主导地位尚未明了。
, http://www.100md.com
血管紧张素转化酶抑制剂(ACEI)抗动脉粥样硬化的机制多种多样,但主要一点仍是抑制AngⅡ的生成。临床试验资料表明ACEI应用于心肌梗死后心功能不全的病人能减少再发冠脉血栓形成(recurrent coronary thrombosis)[9],因而可能Ang Ⅱ直接涉及到血栓过程。而PAI-1水平升高是再发冠脉血栓形成的一个危险标志[10]。1993年,Ridker等[3]观察到Ang Ⅱ直接注射于人体内可引起血PAI-1水平升高,强烈提示Ang Ⅱ与纤溶系统存在某种关联,而应用ACEI抑制AngⅡ的生成则有可能通过降低PAI-1的水平而发挥其抗血栓效应。van Leeuwen等[4]首次体外研究表明卡托普利(5 μg/mL)可完全抑制大鼠主动脉平滑肌细胞Ang Ⅰ引起的PAI-1刺激作用。本研究结果则表明卡托普利尽管对血浆总胆固醇水平及PAI-1活性无影响,但能抑制AS的形成和动脉壁局部PAI-1基因的过度表达,而这种局部抗血栓效应可能是ACEI临床效益的重要机制之一。
, 百拇医药
血浆PAI-1的来源主要有三个方面:血管内皮细胞,肝细胞及血小板,但何者占优,目前尚不明确[11]。本研究显示卡托普利尽管能降低血管壁PAI-1基因的表达,但对升高的血浆PAI-1活性无影响,同时我们还发现卡托普利不能降低高脂血症家兔肝脏PAI-1 mRNA的过度表达(结果未显示)。因而肝脏可能是血浆PAI-1的主要来源。
参考文献
1,陈良华,陆国平. 纤溶酶原激活物抑制物-1与动脉粥样硬化. 心血管病学进展,1999, 20:23~26
2,Dzau VJ. Circulating versus local renin-angiotensin system in cardiovascular homeostasis. Circulation, 1988, 77(suppl Ⅰ): Ⅰ4~Ⅰ13
, 百拇医药
3,Ridker PM, Gaboury CL, Conlin PR, et al. Stimulation of plasminogen activator inhibitor in vivo by infusion of angiotensin Ⅱ. Circulation, 1993, 87: 1969~1973
4,van Leeuwen RTJ, Kol A, Andreotti F, et al. Angiotensin Ⅱ increases plasminogen activator inhibitor type 1 and tissue-type plasminogen activator messenger RNA in cultured rat aortic smooth muscle cells. Circulation, 1994, 90: 362~368
5,Rea TJ, DeMattos RB, Pape ME. Hepatic expression of genes regulating lipid metabolism ion rabbits. J Lipid Res, 1993, 34: 1901~1910
, http://www.100md.com
6,Sava H, Sobel BE, Fujii S. Potentiation by hypercholesterolemia of the induction of aortic intramural synthesis of plasminogen activator inhibitor type 1 by endothelial injury. Circ Res, 1993, 73: 671~680
7,Robbie LA, Booth NA, Brown PAJ, et al. Inhibitors of fibrinolysis are elevated in atherosclerotic plaque. Arterioscler Thromb Vasc Biol, 1996, 16: 539~545
8,Vaughan DE, Shen C, Lazos SA. Angiotensin Ⅱ induces plasminogen activator inhibitor (PAI-1) in vitro. Circulation, 1992, 86(suppl Ⅰ): Ⅰ~557
, 百拇医药
9,Pfeffer MA, Braunwald E. Moye LA, et al. For the SAVE Investigators: Effects of captopril on mortality and morbidity in patients with left ventricular dysfunction after myocardial infarction. N Engl J Med, 1992, 327: 676~677
10,Hamsten A, Defaire U, Walldius G, et al. Plasminogen activator inhibitor in plasma: risk factor for recurrent myocardial infarction. Lancet, 1987, 2:3~9
11,Dawson S, Henney A. The status of PAI-1 as a risk factor for arterial and thrombotic disease: a review. Atherosclerosis, 1992, 95: 105~117, 百拇医药