转基因细胞SPC-A-1/IL-2的致突变性研究
作者:李贺书 李殿俊 解丽华 刘旭 曹雪涛 叶胜龙
单位:李贺书 李殿俊 解丽华 刘旭 曹雪涛 叶胜龙(哈尔滨医科大学肿瘤研究所 哈尔滨 150040)
关键词:逆转录病毒;肿瘤基因治疗;白细胞介素-2;Ames;微核
中国肿瘤生物治疗杂志000212
摘 要 目的: 观察转基因细胞SPC-A-1/IL-2的致突变作用,为转基因肿瘤细胞作为瘤苗进行临床应用的安全性检测提供依据。方法: 在人IL-2的cDNA与逆转录病毒载体pLXSN重组并完成PA317/pLIL-2SN包装体系的基础上,将IL-2基因导入人肺腺癌胸膜转移细胞系SPC-A-1中并得到IL-2基因的稳定表达,然后通过遗传毒理学实验技术对转基因细胞SPC-A-1/IL-2的DNA及培养上清液进行体内和体外的致突变性实验研究。结果: 转基因细胞SPC-A-1/IL-2的DNA及培养上清液均未显出致突变作用。结论: 转基因细胞SPC-A-1/IL-2作为瘤苗应用可初步视为是安全可靠的。
, http://www.100md.com
《中国图书资料分类法》分类号 R730.54
Mutagenesis of Transgenic Human Lung Adenocarcinoma Cell Line SPC-A-1/IL-2
Li Heshu Li Dianjun Xie Lihua Liu Xu Cao Xuetao Ye Shenglong
(Tumor Institute of Harbin Medical University, Harbin 150040)
Abstract Objective: To investigate the safety of transgenic human lung adenocarcinoma cell line SPC-A-1/IL-2 as tumor vaccine. Methods: IL-2 gene was introduced into human lung adenocarcinoma cell line SPC-A-1 and was expressed stably on the basis of the construction of retroviral packing cell line PA317/pLIL-2SN. The mutagenesis of both the DNA and supernatant of SPC-A-1/IL-2 in vivo and in vitro was tested by means of genetic toxicological techniques. Results: The result indicated that mutagenesis of both the DNA and the supernatant of transgenic cell SPC-A-1/IL-2 was not observed. Conclusion: The initial experiment suggested that the application of transgenic cell SPC-A-1/IL-2 as tumor vaccine was bisically safe and reliable.
, 百拇医药
Key words retrovirus; cancer gene therapy; interleukin-2; Ames; micronucleus;
随着肿瘤基因治疗研究的进展,肿瘤基因治疗的安全性问题日益引起人们的重视。本文在对培养的转基因细胞SPC-A-1/IL-2进行了细菌、真菌和支原体检测以及野生型病毒复制检测并证明无污染的情况下[1],对SPC-A-1/IL-2的DNA及培养上清液进行了体内和体外的致突变性研究,目的是为转基因肿瘤细胞作为瘤苗进行临床应用的安全性检测提供依据。目前,国内外未见有关于这方面的报导。
1 材料与方法
1.1 细胞与细胞培养
人IL-2的cDNA与逆转录病毒载体pLXSN的重组和包装由上海市肿瘤研究所完成,并且提供包装细胞PA317/pLIL-2SN,NIH3T3,PA317,人肺腺癌胸膜转移细胞系SPC-A-1由上海市细胞生物所提供。
, 百拇医药
DMEM培养液用于包装细胞PA317/pLIL-2SN,NIH3T3和PA317的培养,其中含15%FBS,pH=7.4~7.6。RPMI 1640培养液用于SPC-A-1/IL-2和SPC-A-1细胞的培养,其中含15%FBS,pH=7.4~7.6。细胞的培养在37℃,5%CO2的饱和湿化空气中进行。
1.2 转基因细胞的构建
1.2.1 PA317/pLIL-2SN包装细胞在含有200~400 μg/ml G418(Geneticin,GIBCO公司产品)的DMEM培养液中培养16~18 h以后,收其上清液。
1.2.2 用上述上清液(含8 μg/ml Polybrene,SIGMA公司产品)培养SPC-A-1细胞(2×105/瓶)3~4 h后弃上清液,加入新鲜的DMEM培养液(其中含G418 200~400 μg/ml)培养、筛选10~14 d,即得到抗G418的转基因细胞的阳性克隆。
, 百拇医药
1.3 外源基因表达及其检测
1.3.1 转基因细胞基因组DNA的提取、定量方法见文献[2]。
DNA纯度=OD260/OD280=1.126/0.614=1.833
DNA浓度=1.126×50×10=563 μg/ml。
1.3.2 外源基因及标记基因检测
应用华美生物工程公司生产的DNA扩增系统B试剂盒在eppendorf自动基因扩增仪中进行人IL-2基因和NeoR基因的扩增。反应温度和时间依次为94℃ 30 min,55℃ 60 min,72℃ 120 min,共30个循环。常规方法进行琼脂糖凝胶电泳记录结果。
, http://www.100md.com
1.4 Ames实验
本实验以中华人民共和国国家标准(卫生部GB15193,4-94)为准则,利用鼠伤寒沙门氏菌(salmonella typhimurium)组氨酸营养缺陷型回变原理,采用平皿掺入法对转基因细胞SPC-A-1/IL-2的DNA及培养上清液进行致突变性检测。共使用4种鉴定合格的菌株:TA97,TA98,TA100,TA102,分别进行代谢活化(S-9m+)和非代谢活化(S-9m-)两种处理,阴性对照为TE缓冲液(细胞DNA)和DMSO(培养上清液),阳性对照分别为敌克松(Dexon)和二氨基芴(2-AF,2-Amino-Fluorene),SPC-A-1/IL-2和DNA及培养上清液各设5个剂量,3次重复,具体实验方法参见文献[3]。
1.5 小鼠微核实验
, http://www.100md.com
小鼠微核实验是一种检测致变性的体内实验,它是以昆明小鼠为实验对象,按照中华人民共和国国家标准(卫生部GB15193,4-94)规定的方法进行。SPC-A-1/IL-2的DNA及培养上清液的设计剂量均为250,500和1 000 mg/kg,6组动物,3次重复,阴性对照为蒸馏水,阳性对照为环磷酰胺(cyclophosphamide,CP),具体实验方法参见文献[3]。
2 结 果
2.1 目的基因和标记基因的检测
SPC-A-1细胞转基因后,通过G418的筛选得到阳性克隆。抽提转基因细胞基因组和PA317/pLIL-2SN细胞基因组的DNA进行IL-2基因和NeoR基因的扩增,结果表明,SPC-A-IL-2细胞和PA317/pLIL-2SN细胞的IL-2基因和NeoR基因均为阳性,表明逆转录病毒载体pLXSN能稳定地将人细胞因子基因IL-2导入人肺腺癌胸膜转移细胞系SPC-A-1中[4]。
, 百拇医药
2.2 Ames实验
SPC-A-1/IL-2细胞DNA及培养上清液的Ames实验结果表明,其未见致突变性,推测SPC-A-1/IL-2细胞系可能没有致癌的潜在危险(见表1)。
表1 SPC-A-1/IL-2细胞DNA及培养上清液的Ames实验结果
Tab.1 Results of Ames for the DNA and supernatant of SPC-A-1/IL-2 cells
Per plate
TA97
TA98
TA100
, http://www.100md.com
TA102
S-9m-
S-9m+
S-9m-
S-9m+
S-9m-
S-9m+
S-9m-
S-9m+
, 百拇医药
DNA
2 500 μg
101
107
28
33
136
133
236
212
DNA
500 μg
94
, http://www.100md.com
110
30
33
143
136
236
218
DNA
100 μg
100
109
31
29
, 百拇医药
131
146
227
224
DNA
20 μg
97
101
28
29
135
142
216
, 百拇医药
219
DNA
4 μg
109
109
29
28
141
134
235
223
TE
0.1 ml
, 百拇医药
113
125
30
31
116
142
241
243
Dexon
50 μg
1 786
1 836
1 050
, 百拇医药
1 003
2-AF
50 μg
1 271
1 936
972
251
Supernatant
2 500 μg
83
107
23
26
, 百拇医药
97
160
214
210
Supernatant
500 μg
91
110
23
25
99
153
215
, 百拇医药
224
Supernatant
100 μg
85
102
26
27
100
142
210
241
Supernatant
20 μg
, http://www.100md.com
86
105
24
26
104
155
232
219
Supernatant
4 μg
97
95
24
, 百拇医药
24
98
142
223
235
DMSO
0.1 ml
112
126
26
28
108
149
, 百拇医药
240
240
Dexon
50 μg
1 790
1 783
1 003
1 003
2-AF
20 μg
1 307
1 955
1 004
, http://www.100md.com
251
2.3 微核实验
小鼠骨髓嗜多染红细胞微核实验证明,SPC-A-1/IL-2细胞系DNA及培养上清液对小鼠无微核诱发作用,各剂量组的微核率与阴性对照组比较均无显著性差异(P>0.05),见表2。表2 SPC-A-1/IL-2细胞DNA及培养上清液对
小鼠微核诱发率实验结果
Tab.2 Micronucleated inductivity of DNA and
supernatant of SPC-A-1/IL-2 cell
Groups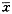
, http://www.100md.com
SD
P
A
B
C
D
E
F
H2O
1
3
2
0
2
, 百拇医药
2
1.67
1.03
DNA250
2
1
4
1
2
2
2
1.09
>0.05
, 百拇医药
DNA500
1
0
2
0
1
3
1.17
1.17
>0.05
DNA1000
1
2
, 百拇医药
2
3
2
0
1.67
1.03
>0.05
CP
23
17
20
24
18
28
, 百拇医药
21.67
4.13
<0.01
3 讨 论
3.1 细胞DNA及培养上清液的致突变作用
Ames认为,致癌剂与致突剂有83%的相关关系。因而,阳性诱变剂可被视为有致癌危险的物质,对人类有潜在危害。SPC-A-1/IL-2细胞DNA及培养上清液在体外条件下,经Ames实验显示出对鼠伤寒沙门氏菌TA97,TA98,TA100,TA102均未表现阳性回复突变。说明SPC-A-1/IL-2细胞DNA及培养上清液不具有细菌诱变作用,进而推测它们可能没有潜在的致癌作用。
动物体内的诱变实验显示,SPC-A-1/IL-2细胞DNA及培养上清液不能诱导小鼠骨髓细胞染色体畸变及微核形成的阳性反应。上述结果表明,无论是体外致突变实验还是体内致突变实验,SPC-A-1/IL-2细胞DNA及培养上清液既无诱变性也无遗传毒性。因此,可以初步肯定转基因细胞SPC-A-1/IL-2的安全性。
, 百拇医药
3.2 关于程序外DNA合成
值得提及的是,具有遗传毒性的致癌物,其作用特点是对遗传物质DNA的直接损伤,可诱发细胞的程序外DNA合成。有一些在细菌诱变实验中呈低活性或无活性的物质,可能是细胞发生程序外DNA合成的阳性物质。Ames实验是以酶活性的回复来表明的,如果一个突变不发生在编码组氨酸的DNA序列,就不能观察到这个突变。因此,本文报导结果只能初步肯定Ames实验和小鼠微核实验的阴性结果。要想最终说明SPC-A-1/IL-2细胞DNA及培养上清液有没有致突变作用,必须进行细胞程序外DNA合成的检测。
3.3 诱变性与致癌性的探讨
尽管诱变性与致癌性密切相关,但二者并不完全相同,由于这种相关性受致癌物和诱变剂本身的结构与代谢特性的影响,因此,常有假阳性或假阴性的结果出现。细胞转化是细胞发生遗传性改变的一种变化,即涉及DNA或基因的改变。细胞发生转化后的性状可以代代相传能够长期维持和存在,但转化不一定就是癌变,只有细胞发生恶性转化才是癌变。对细胞转化活性的影响,染毒时间和染毒次数比染毒剂量更重要。有学者曾经用酪胺的亚硝化产物进行染毒实验,发现2次染毒间隔72 h处理的细胞发生克隆生长形成转移灶的数目明显高于1次染毒间隔48 h处理的细胞。尽管本文所进行的体内和体外的致突变实验是按国家标准(卫生部GB15193,4-94)进行的,本文作者还是认为在应用SPC-A-1/IL-2细胞时,应该跟踪监测其诱变性,避免可能的慢性毒性作用而导致的DNA或基因改变,使它更好地为人类发挥作用。
, 百拇医药
国家九五攻关课题基金(96-906A-01-20)资助
李贺书,男,36岁,硕士,主要从事肿瘤基因治疗的研究
参 考 文 献
1,解丽华, 李殿俊, 刘 旭, 等. 逆转录病毒介导癌基因疗法体外安全实验. 哈尔滨医科大学学报, 1998, 32(6): 413
2,司徒镇强, 吴军正. 细胞培养. 北京: 世界图书出版公司, 1996
3,李百祥, 万丽葵, 朱宽胜, 等. 卫生毒理学实验教程. 黑龙江: 黑龙江科学技术出版社, 1997
4,解丽华, 李殿俊, 马玉彦, 等. 转基因人肺腺癌细胞株的建立及其生物学特性的研究. 中国肿瘤生物治疗杂志, 1997, 4(4): 323
(1999-11-02收稿; 1999-12-13修回), 百拇医药
单位:李贺书 李殿俊 解丽华 刘旭 曹雪涛 叶胜龙(哈尔滨医科大学肿瘤研究所 哈尔滨 150040)
关键词:逆转录病毒;肿瘤基因治疗;白细胞介素-2;Ames;微核
中国肿瘤生物治疗杂志000212
摘 要 目的: 观察转基因细胞SPC-A-1/IL-2的致突变作用,为转基因肿瘤细胞作为瘤苗进行临床应用的安全性检测提供依据。方法: 在人IL-2的cDNA与逆转录病毒载体pLXSN重组并完成PA317/pLIL-2SN包装体系的基础上,将IL-2基因导入人肺腺癌胸膜转移细胞系SPC-A-1中并得到IL-2基因的稳定表达,然后通过遗传毒理学实验技术对转基因细胞SPC-A-1/IL-2的DNA及培养上清液进行体内和体外的致突变性实验研究。结果: 转基因细胞SPC-A-1/IL-2的DNA及培养上清液均未显出致突变作用。结论: 转基因细胞SPC-A-1/IL-2作为瘤苗应用可初步视为是安全可靠的。
, http://www.100md.com
《中国图书资料分类法》分类号 R730.54
Mutagenesis of Transgenic Human Lung Adenocarcinoma Cell Line SPC-A-1/IL-2
Li Heshu Li Dianjun Xie Lihua Liu Xu Cao Xuetao Ye Shenglong
(Tumor Institute of Harbin Medical University, Harbin 150040)
Abstract Objective: To investigate the safety of transgenic human lung adenocarcinoma cell line SPC-A-1/IL-2 as tumor vaccine. Methods: IL-2 gene was introduced into human lung adenocarcinoma cell line SPC-A-1 and was expressed stably on the basis of the construction of retroviral packing cell line PA317/pLIL-2SN. The mutagenesis of both the DNA and supernatant of SPC-A-1/IL-2 in vivo and in vitro was tested by means of genetic toxicological techniques. Results: The result indicated that mutagenesis of both the DNA and the supernatant of transgenic cell SPC-A-1/IL-2 was not observed. Conclusion: The initial experiment suggested that the application of transgenic cell SPC-A-1/IL-2 as tumor vaccine was bisically safe and reliable.
, 百拇医药
Key words retrovirus; cancer gene therapy; interleukin-2; Ames; micronucleus;
随着肿瘤基因治疗研究的进展,肿瘤基因治疗的安全性问题日益引起人们的重视。本文在对培养的转基因细胞SPC-A-1/IL-2进行了细菌、真菌和支原体检测以及野生型病毒复制检测并证明无污染的情况下[1],对SPC-A-1/IL-2的DNA及培养上清液进行了体内和体外的致突变性研究,目的是为转基因肿瘤细胞作为瘤苗进行临床应用的安全性检测提供依据。目前,国内外未见有关于这方面的报导。
1 材料与方法
1.1 细胞与细胞培养
人IL-2的cDNA与逆转录病毒载体pLXSN的重组和包装由上海市肿瘤研究所完成,并且提供包装细胞PA317/pLIL-2SN,NIH3T3,PA317,人肺腺癌胸膜转移细胞系SPC-A-1由上海市细胞生物所提供。
, 百拇医药
DMEM培养液用于包装细胞PA317/pLIL-2SN,NIH3T3和PA317的培养,其中含15%FBS,pH=7.4~7.6。RPMI 1640培养液用于SPC-A-1/IL-2和SPC-A-1细胞的培养,其中含15%FBS,pH=7.4~7.6。细胞的培养在37℃,5%CO2的饱和湿化空气中进行。
1.2 转基因细胞的构建
1.2.1 PA317/pLIL-2SN包装细胞在含有200~400 μg/ml G418(Geneticin,GIBCO公司产品)的DMEM培养液中培养16~18 h以后,收其上清液。
1.2.2 用上述上清液(含8 μg/ml Polybrene,SIGMA公司产品)培养SPC-A-1细胞(2×105/瓶)3~4 h后弃上清液,加入新鲜的DMEM培养液(其中含G418 200~400 μg/ml)培养、筛选10~14 d,即得到抗G418的转基因细胞的阳性克隆。
, 百拇医药
1.3 外源基因表达及其检测
1.3.1 转基因细胞基因组DNA的提取、定量方法见文献[2]。
DNA纯度=OD260/OD280=1.126/0.614=1.833
DNA浓度=1.126×50×10=563 μg/ml。
1.3.2 外源基因及标记基因检测
应用华美生物工程公司生产的DNA扩增系统B试剂盒在eppendorf自动基因扩增仪中进行人IL-2基因和NeoR基因的扩增。反应温度和时间依次为94℃ 30 min,55℃ 60 min,72℃ 120 min,共30个循环。常规方法进行琼脂糖凝胶电泳记录结果。
, http://www.100md.com
1.4 Ames实验
本实验以中华人民共和国国家标准(卫生部GB15193,4-94)为准则,利用鼠伤寒沙门氏菌(salmonella typhimurium)组氨酸营养缺陷型回变原理,采用平皿掺入法对转基因细胞SPC-A-1/IL-2的DNA及培养上清液进行致突变性检测。共使用4种鉴定合格的菌株:TA97,TA98,TA100,TA102,分别进行代谢活化(S-9m+)和非代谢活化(S-9m-)两种处理,阴性对照为TE缓冲液(细胞DNA)和DMSO(培养上清液),阳性对照分别为敌克松(Dexon)和二氨基芴(2-AF,2-Amino-Fluorene),SPC-A-1/IL-2和DNA及培养上清液各设5个剂量,3次重复,具体实验方法参见文献[3]。
1.5 小鼠微核实验
, http://www.100md.com
小鼠微核实验是一种检测致变性的体内实验,它是以昆明小鼠为实验对象,按照中华人民共和国国家标准(卫生部GB15193,4-94)规定的方法进行。SPC-A-1/IL-2的DNA及培养上清液的设计剂量均为250,500和1 000 mg/kg,6组动物,3次重复,阴性对照为蒸馏水,阳性对照为环磷酰胺(cyclophosphamide,CP),具体实验方法参见文献[3]。
2 结 果
2.1 目的基因和标记基因的检测
SPC-A-1细胞转基因后,通过G418的筛选得到阳性克隆。抽提转基因细胞基因组和PA317/pLIL-2SN细胞基因组的DNA进行IL-2基因和NeoR基因的扩增,结果表明,SPC-A-IL-2细胞和PA317/pLIL-2SN细胞的IL-2基因和NeoR基因均为阳性,表明逆转录病毒载体pLXSN能稳定地将人细胞因子基因IL-2导入人肺腺癌胸膜转移细胞系SPC-A-1中[4]。
, 百拇医药
2.2 Ames实验
SPC-A-1/IL-2细胞DNA及培养上清液的Ames实验结果表明,其未见致突变性,推测SPC-A-1/IL-2细胞系可能没有致癌的潜在危险(见表1)。
表1 SPC-A-1/IL-2细胞DNA及培养上清液的Ames实验结果
Tab.1 Results of Ames for the DNA and supernatant of SPC-A-1/IL-2 cells
Per plate
TA97
TA98
TA100
, http://www.100md.com
TA102
S-9m-
S-9m+
S-9m-
S-9m+
S-9m-
S-9m+
S-9m-
S-9m+
, 百拇医药
DNA
2 500 μg
101
107
28
33
136
133
236
212
DNA
500 μg
94
, http://www.100md.com
110
30
33
143
136
236
218
DNA
100 μg
100
109
31
29
, 百拇医药
131
146
227
224
DNA
20 μg
97
101
28
29
135
142
216
, 百拇医药
219
DNA
4 μg
109
109
29
28
141
134
235
223
TE
0.1 ml
, 百拇医药
113
125
30
31
116
142
241
243
Dexon
50 μg
1 786
1 836
1 050
, 百拇医药
1 003
2-AF
50 μg
1 271
1 936
972
251
Supernatant
2 500 μg
83
107
23
26
, 百拇医药
97
160
214
210
Supernatant
500 μg
91
110
23
25
99
153
215
, 百拇医药
224
Supernatant
100 μg
85
102
26
27
100
142
210
241
Supernatant
20 μg
, http://www.100md.com
86
105
24
26
104
155
232
219
Supernatant
4 μg
97
95
24
, 百拇医药
24
98
142
223
235
DMSO
0.1 ml
112
126
26
28
108
149
, 百拇医药
240
240
Dexon
50 μg
1 790
1 783
1 003
1 003
2-AF
20 μg
1 307
1 955
1 004
, http://www.100md.com
251
2.3 微核实验
小鼠骨髓嗜多染红细胞微核实验证明,SPC-A-1/IL-2细胞系DNA及培养上清液对小鼠无微核诱发作用,各剂量组的微核率与阴性对照组比较均无显著性差异(P>0.05),见表2。表2 SPC-A-1/IL-2细胞DNA及培养上清液对
小鼠微核诱发率实验结果
Tab.2 Micronucleated inductivity of DNA and
supernatant of SPC-A-1/IL-2 cell
Groups
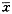
, http://www.100md.com
SD
P
A
B
C
D
E
F
H2O
1
3
2
0
2
, 百拇医药
2
1.67
1.03
DNA250
2
1
4
1
2
2
2
1.09
>0.05
, 百拇医药
DNA500
1
0
2
0
1
3
1.17
1.17
>0.05
DNA1000
1
2
, 百拇医药
2
3
2
0
1.67
1.03
>0.05
CP
23
17
20
24
18
28
, 百拇医药
21.67
4.13
<0.01
3 讨 论
3.1 细胞DNA及培养上清液的致突变作用
Ames认为,致癌剂与致突剂有83%的相关关系。因而,阳性诱变剂可被视为有致癌危险的物质,对人类有潜在危害。SPC-A-1/IL-2细胞DNA及培养上清液在体外条件下,经Ames实验显示出对鼠伤寒沙门氏菌TA97,TA98,TA100,TA102均未表现阳性回复突变。说明SPC-A-1/IL-2细胞DNA及培养上清液不具有细菌诱变作用,进而推测它们可能没有潜在的致癌作用。
动物体内的诱变实验显示,SPC-A-1/IL-2细胞DNA及培养上清液不能诱导小鼠骨髓细胞染色体畸变及微核形成的阳性反应。上述结果表明,无论是体外致突变实验还是体内致突变实验,SPC-A-1/IL-2细胞DNA及培养上清液既无诱变性也无遗传毒性。因此,可以初步肯定转基因细胞SPC-A-1/IL-2的安全性。
, 百拇医药
3.2 关于程序外DNA合成
值得提及的是,具有遗传毒性的致癌物,其作用特点是对遗传物质DNA的直接损伤,可诱发细胞的程序外DNA合成。有一些在细菌诱变实验中呈低活性或无活性的物质,可能是细胞发生程序外DNA合成的阳性物质。Ames实验是以酶活性的回复来表明的,如果一个突变不发生在编码组氨酸的DNA序列,就不能观察到这个突变。因此,本文报导结果只能初步肯定Ames实验和小鼠微核实验的阴性结果。要想最终说明SPC-A-1/IL-2细胞DNA及培养上清液有没有致突变作用,必须进行细胞程序外DNA合成的检测。
3.3 诱变性与致癌性的探讨
尽管诱变性与致癌性密切相关,但二者并不完全相同,由于这种相关性受致癌物和诱变剂本身的结构与代谢特性的影响,因此,常有假阳性或假阴性的结果出现。细胞转化是细胞发生遗传性改变的一种变化,即涉及DNA或基因的改变。细胞发生转化后的性状可以代代相传能够长期维持和存在,但转化不一定就是癌变,只有细胞发生恶性转化才是癌变。对细胞转化活性的影响,染毒时间和染毒次数比染毒剂量更重要。有学者曾经用酪胺的亚硝化产物进行染毒实验,发现2次染毒间隔72 h处理的细胞发生克隆生长形成转移灶的数目明显高于1次染毒间隔48 h处理的细胞。尽管本文所进行的体内和体外的致突变实验是按国家标准(卫生部GB15193,4-94)进行的,本文作者还是认为在应用SPC-A-1/IL-2细胞时,应该跟踪监测其诱变性,避免可能的慢性毒性作用而导致的DNA或基因改变,使它更好地为人类发挥作用。
, 百拇医药
国家九五攻关课题基金(96-906A-01-20)资助
李贺书,男,36岁,硕士,主要从事肿瘤基因治疗的研究
参 考 文 献
1,解丽华, 李殿俊, 刘 旭, 等. 逆转录病毒介导癌基因疗法体外安全实验. 哈尔滨医科大学学报, 1998, 32(6): 413
2,司徒镇强, 吴军正. 细胞培养. 北京: 世界图书出版公司, 1996
3,李百祥, 万丽葵, 朱宽胜, 等. 卫生毒理学实验教程. 黑龙江: 黑龙江科学技术出版社, 1997
4,解丽华, 李殿俊, 马玉彦, 等. 转基因人肺腺癌细胞株的建立及其生物学特性的研究. 中国肿瘤生物治疗杂志, 1997, 4(4): 323
(1999-11-02收稿; 1999-12-13修回), 百拇医药