心脏直视手术后多脏器衰竭患者的细胞因子变化
作者:李彤 刘维永 祝恒山
单位:李彤(第四军医大学西京医院心血管外科中心,陕西 西安 710033);刘维永(第四军医大学西京医院心血管外科中心,陕西 西安 710033);祝恒山(第四军医大学西京医院心血管外科中心,陕西 西安 710033)
关键词:多器官衰竭;心脏直视手术;细胞因子
第四军医大学学报000517 摘 要: 目的 检测心脏直视手术后多器官功能衰竭(MOF)患者血清肿瘤坏死因子(TNF-α)、白细胞介素1β(IL-1β)、白细胞介素6(IL-6)、白细胞介素8(IL-8)的含量变化并探讨其意义. 方法 选择心脏直视手术后发生多器官衰竭患者13例,采用放射免疫方法检测患者血清TNF-α,IL-1β,IL-6,IL-8的含量. 结果 多器官衰竭发生存活组和死亡组3 d后TNF-α (0.61±0.08), (0.81±0.09) vs (0.20±0.05) μg.L-1(P<0.05, 0.01); IL-1β (0.52±0.09), (0.69±0.04) vs (0.16±0.03) μg.L-1(P<0.01, 0.01); IL-6 (0.41±0.08), (0.56±0.07) vs (0.17±0.03) μg.L-1 (P<0.05, 0.05); IL-8 (3.70±0.80), (4.92±0.78) vs (1.6±0.40) μg.L-1(P<0.05,0.05)的含量比对照组明显升高,且IL-6,IL-8升高时限滞后于TNF-α,IL-1β. 结论 细胞因子过多释放是心脏直视手术后多器官衰竭的重要因素. TNF-α,IL-1β是引发多器官衰竭的始动因子.
, 百拇医药
中图号:R654.1 文献标识码:A
文章编号:1000-2790(2000)05-0574-02
Serum cytokines in patients with multiple organ failure following open-heart-surgery
LI Tong, LIU Wei-Yong, ZHU Heng-Shan
(Center of Cardiovascular Surgery, Xijing Hospital, Fourth Military Medical University, Xi'an 710033, China)
Abstract: AIM To evaluate the clinical significance of the changes in serum tumor necrosis factor-α (TNF-α), interleukin-β (IL-1β), interleukin-6 (IL-6), interleukin-8 (IL-8). METHODS Thirteen patients with multiple organ failure following open-heart-surgery were selected. Serum TNF-α, IL-1β, IL-6, IL-8 levels were measured by enzyme-linked immunosorbent assay (ELISA). RESULTS The levels of plasma TNF-α (0.61±0.08), (0.81±0.09) vs (0.20±0.05) μg.L-1 (P<0.05, 0.01); IL-1β (0.52±0.09), (0.69±0.04) vs (0.16±0.03) μg.L-1 (P<0.01, 0.01); IL-6 (0.41±0.08), (0.56±0.07) vs (0.17±0.03) μg.L-1 (P<0.05,0.05); IL-8 (3.70±0.80), (4.92±0.78) vs (1.6±0.40) μg.L-1(P<0.05, 0.05) rose markedly after MOF. The time of reaching the peak value in IL-6, IL-8 was slower than that in TNF-α, IL-1β. CONCLUSION The abnormal release of the cellular factors is an important cause of MOF after open-heart-surgery. TNF-α,IL-1β are triggling factors.
, http://www.100md.com
Keywords: multiple organ failure; open-heart-surgery; cellular factor
0 引言
心脏直视手术后多器官衰竭(MOF)发病急,进展快,死亡率高,但其发病机制较复杂. 我们通过13例心脏直视手术后多器官衰竭患者细胞因子变化观察,了解细胞因子介导的全身自我破坏炎症反应过程,探讨其临床意义.
1 对象和方法
1.1 对象 选择我科心脏直视手术后发生MOF 13(男6,女7)例,年龄4~56(平均46)岁,体质量17~74(平均54) kg. 术前心功能,按NYHA心功分级,心功Ⅲ级7例,心功Ⅳ级6例. MOF诊断按95全国危重病急救医学学术会议通过的标准[1]. 13例患者均有心功能衰竭,合并肾功能衰竭4例,呼吸功能衰竭6例,肝功能衰竭4例,胃肠功能衰竭6例,脑功能衰竭5例. 13例中2个器官功能衰竭4例;3个器官功能衰竭6例;4个器官功能衰竭3例.
, http://www.100md.com
1.2 方法 采用胸骨正中切口,全身肝素化,升主动脉,上、下腔静脉插管,建立体外循环,右上肺静脉置左房引流管. 应用冷心停搏液和局部深低温保护心肌. 13例患者中行二尖瓣置换术2例,主动脉瓣置换术3例;二尖瓣、主动脉瓣双瓣膜置换术5例;瓦氏窦瘤破裂修补术1例;复杂先心病畸形矫治2例. 总转流时间为(118±22) min;冠脉循环阻断时间为(78±14) min. 于MOF发生后1,2,3,4,5 d,采血分离血浆,采用ELISA法测定肿瘤坏死因子-α (TNF-α);白细胞介素1β (IL-1β);白细胞介素6 (IL-6);白细胞介素8 (IL-8)含量,单位以μg.L-1表示. TNF-α,IL-6,IL-8药盒由本校免疫学教研室提供,IL-1β药盒由解放军军事科学院提供. 操作由专人按说明书进行.
另选择术后未曾发生MOF的先心病及风心患者10例,于术后第3日采血测定血浆TNF-α,IL-1β,IL-6,IL-8含量作为对照. 男5例,女5例,年龄6~62(平均50)岁,体质量20~70(平均48) kg. 术前心功Ⅲ级6例,Ⅳ级4例. 10例中行复杂心矫治术3例,二尖瓣置换术2例,主动脉瓣置换术1例,二尖瓣、主动脉瓣双瓣膜置换术4例.
, 百拇医药
统计学处理:组间差异采用t检验.
2 结果
心脏直视手术后多器官衰竭患者13例,死亡6例,占46%. 全部患者发生多器官功能衰竭后1 d开始TNF-α,IL-1β水平较对照组明显升高,2~3 d时达到峰值;IL-6,IL-8水平在发生多器官功能衰竭后2~3 d开始明显升高,4~5 d达到峰值. IL-6,IL-8升高时限滞后于TNF-α,IL-1β. 细胞因子TNF-α,IL-1β,IL-6,IL-8水平两组间有显著差异,死亡病例组明显高于存活病例组(Tab 1).
表1 心脏直视手术后多器官衰竭细胞因子变化
Tab 1 Serum cytokines in multiple organ failure
following open heart surgery (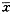 ±s, μg.L-1) Cytokines
±s, μg.L-1) Cytokines
, 百拇医药
Control
MOF
1 d
2 d
3 d
4 d
5 d
TNF-α
0.20±0.05
1
0.40±0.06
0.57±0.08a
, http://www.100md.com 0.61±0.08a
0.51±0.03a
0.52±0.06a
2
0.56±0.08a
0.78±0.06b
0.81±0.09b
0.72±0.04b
0.70±0.66b
IL-1β
, 百拇医药
0.16±0.03
1
0.33±0.10
0.50±0.04a
0.52±0.09b
0.40±0.08a
0.47±0.05a
2
0.50±0.06a
0.67±0.05b
, 百拇医药
0.69±0.04b
0.59±0.10b
0.56±0.05a
IL-6
0.17±0.13
1
0.21±0.03
0.33±0.03
0.41±0.08a
0.52±0.06a
0.53±0.06a
, 百拇医药
2
0.19±0.05
0.46±0.08a
0.56±0.07a
0.83±0.09b
0.79±0.06b
IL-8
1.61±0.40
1
1.70±0.42
2.61±0.56
, 百拇医药
3.70±0.80a
4.95±1.23a
5.01±0.86a
2
2.01±0.38
3.92±0.81
4.92±0.78a
7.30±1.40b
7.14±0.72b
aP<0.05, bP<0.01 vs control. 1: live group, 2: death group.3 讨论
, 百拇医药
多器官功能衰竭是心脏直视手术后严重的并发症之一,死亡率极高. 同其他严重创伤、休克和感染等导致多器官衰竭一样,发病机制十分复杂. 广泛涉及神经体液、内分泌、营养代谢、免疫等许多系统,学说较多. 然而目前较趋一致的看法是由创伤所致“免疫―炎症反应”是MOF发生的最根本原因[2]. 为了验证这一学说,探讨多器官发生本质,我们对心脏直视手术多器官衰竭患者细胞因子进行动态观察. 结果显示多器官衰竭发生后TNF-α,IL-1β,IL-6,IL-8水平较对照组明显升高. 表明本组患者细胞因子持续过多地释放是介导、放大炎症介质级联效应,引起多器官衰竭的病理基础. 而IL-6,IL-8增高及达到峰值时限滞后于TNF-α,IL-1β,提示TNF-α,IL-8是细胞因子级联反应的始动因子[3].
在致病因素作用下,单核巨噬细胞被激活,释放TNF-α和IL-1β,此二因子进一步诱导中性粒细胞在肺、肝等器官组织聚集、粘附,大量中性粒细胞与内皮细胞粘附的同时,释放大量IL-6,IL-8引发了全身炎症反应失调. 分析临床资料,探索其致病因素. 本组患者术前心功能差、危重;术中体外循环时间长,使细胞破坏,纤维蛋白原和血小板激活造成凝血机制紊乱及术后低心排,胃肠壁微循环障碍,造成组织水肿,毛细血管通透性增加,菌群失调,细菌、毒素移位等是介导发生MOF的重要原因. 文献报道胃肠道是MOF“启动器官”,本组有近一半患者存在胃肠道功能紊乱,在引发MOF发生中是不可忽视的因素[4]. 因此如何监测、保护胃肠粘膜屏障是防止MOF发生极其重要环节.
, 百拇医药
增高的细胞因子具有多种生物学活性,它们可通过激活中性粒细胞,产生呼吸爆发释放大量氧自由基、蛋白溶解酶以及产生的白三烯等造成机体严重的损伤和紊乱. 本结果显示死亡病例组细胞因子水平明显高于存活病例组,这不仅进一步证实细胞因子在介导损伤中的作用,而且也提示抑制细胞因子的释放是提高治愈MOF的一个重要途径[5].
作者简介:李 彤(1963-),男(汉族),辽宁省辽阳市人.博士,副教授,副主任医师.
Tel.(029)3375311 Email. Litong@fmmu.edu.cn
参考文献:
[1] 王今达,王宣恩. MODS病理分期及严重程度评分标准[J]. 中国危重病急救医学, 1995;7(6):346-346.
[2] Cannon JG. Circulating interleukin-1 and tumor necrasis factor in septic shlck and experimental endotoxin fever [J]. J Infect Dis, 1990;161(1):79-86.
, http://www.100md.com
[3] Spooner CE, Markowitz NP. The role of tumor necrosis factor in sepsis [J]. Clin Immunol Immunopathol, 1992;62(4):511-516.
[4] 王今达. 多脏器功能失常综合征与肠道内细菌及内毒素易位[J]. 中国危重病免救医学, 1995;7(6):321-323.
[5] Deitch EA. Multiple organ failure: Pathophysiology and petential future therapy [J]. Am Surg, 1992;216(20):117-223.
收稿日期:2000-01-18; 修回日期:2000-02-16, http://www.100md.com
单位:李彤(第四军医大学西京医院心血管外科中心,陕西 西安 710033);刘维永(第四军医大学西京医院心血管外科中心,陕西 西安 710033);祝恒山(第四军医大学西京医院心血管外科中心,陕西 西安 710033)
关键词:多器官衰竭;心脏直视手术;细胞因子
第四军医大学学报000517 摘 要: 目的 检测心脏直视手术后多器官功能衰竭(MOF)患者血清肿瘤坏死因子(TNF-α)、白细胞介素1β(IL-1β)、白细胞介素6(IL-6)、白细胞介素8(IL-8)的含量变化并探讨其意义. 方法 选择心脏直视手术后发生多器官衰竭患者13例,采用放射免疫方法检测患者血清TNF-α,IL-1β,IL-6,IL-8的含量. 结果 多器官衰竭发生存活组和死亡组3 d后TNF-α (0.61±0.08), (0.81±0.09) vs (0.20±0.05) μg.L-1(P<0.05, 0.01); IL-1β (0.52±0.09), (0.69±0.04) vs (0.16±0.03) μg.L-1(P<0.01, 0.01); IL-6 (0.41±0.08), (0.56±0.07) vs (0.17±0.03) μg.L-1 (P<0.05, 0.05); IL-8 (3.70±0.80), (4.92±0.78) vs (1.6±0.40) μg.L-1(P<0.05,0.05)的含量比对照组明显升高,且IL-6,IL-8升高时限滞后于TNF-α,IL-1β. 结论 细胞因子过多释放是心脏直视手术后多器官衰竭的重要因素. TNF-α,IL-1β是引发多器官衰竭的始动因子.
, 百拇医药
中图号:R654.1 文献标识码:A
文章编号:1000-2790(2000)05-0574-02
Serum cytokines in patients with multiple organ failure following open-heart-surgery
LI Tong, LIU Wei-Yong, ZHU Heng-Shan
(Center of Cardiovascular Surgery, Xijing Hospital, Fourth Military Medical University, Xi'an 710033, China)
Abstract: AIM To evaluate the clinical significance of the changes in serum tumor necrosis factor-α (TNF-α), interleukin-β (IL-1β), interleukin-6 (IL-6), interleukin-8 (IL-8). METHODS Thirteen patients with multiple organ failure following open-heart-surgery were selected. Serum TNF-α, IL-1β, IL-6, IL-8 levels were measured by enzyme-linked immunosorbent assay (ELISA). RESULTS The levels of plasma TNF-α (0.61±0.08), (0.81±0.09) vs (0.20±0.05) μg.L-1 (P<0.05, 0.01); IL-1β (0.52±0.09), (0.69±0.04) vs (0.16±0.03) μg.L-1 (P<0.01, 0.01); IL-6 (0.41±0.08), (0.56±0.07) vs (0.17±0.03) μg.L-1 (P<0.05,0.05); IL-8 (3.70±0.80), (4.92±0.78) vs (1.6±0.40) μg.L-1(P<0.05, 0.05) rose markedly after MOF. The time of reaching the peak value in IL-6, IL-8 was slower than that in TNF-α, IL-1β. CONCLUSION The abnormal release of the cellular factors is an important cause of MOF after open-heart-surgery. TNF-α,IL-1β are triggling factors.
, http://www.100md.com
Keywords: multiple organ failure; open-heart-surgery; cellular factor
0 引言
心脏直视手术后多器官衰竭(MOF)发病急,进展快,死亡率高,但其发病机制较复杂. 我们通过13例心脏直视手术后多器官衰竭患者细胞因子变化观察,了解细胞因子介导的全身自我破坏炎症反应过程,探讨其临床意义.
1 对象和方法
1.1 对象 选择我科心脏直视手术后发生MOF 13(男6,女7)例,年龄4~56(平均46)岁,体质量17~74(平均54) kg. 术前心功能,按NYHA心功分级,心功Ⅲ级7例,心功Ⅳ级6例. MOF诊断按95全国危重病急救医学学术会议通过的标准[1]. 13例患者均有心功能衰竭,合并肾功能衰竭4例,呼吸功能衰竭6例,肝功能衰竭4例,胃肠功能衰竭6例,脑功能衰竭5例. 13例中2个器官功能衰竭4例;3个器官功能衰竭6例;4个器官功能衰竭3例.
, http://www.100md.com
1.2 方法 采用胸骨正中切口,全身肝素化,升主动脉,上、下腔静脉插管,建立体外循环,右上肺静脉置左房引流管. 应用冷心停搏液和局部深低温保护心肌. 13例患者中行二尖瓣置换术2例,主动脉瓣置换术3例;二尖瓣、主动脉瓣双瓣膜置换术5例;瓦氏窦瘤破裂修补术1例;复杂先心病畸形矫治2例. 总转流时间为(118±22) min;冠脉循环阻断时间为(78±14) min. 于MOF发生后1,2,3,4,5 d,采血分离血浆,采用ELISA法测定肿瘤坏死因子-α (TNF-α);白细胞介素1β (IL-1β);白细胞介素6 (IL-6);白细胞介素8 (IL-8)含量,单位以μg.L-1表示. TNF-α,IL-6,IL-8药盒由本校免疫学教研室提供,IL-1β药盒由解放军军事科学院提供. 操作由专人按说明书进行.
另选择术后未曾发生MOF的先心病及风心患者10例,于术后第3日采血测定血浆TNF-α,IL-1β,IL-6,IL-8含量作为对照. 男5例,女5例,年龄6~62(平均50)岁,体质量20~70(平均48) kg. 术前心功Ⅲ级6例,Ⅳ级4例. 10例中行复杂心矫治术3例,二尖瓣置换术2例,主动脉瓣置换术1例,二尖瓣、主动脉瓣双瓣膜置换术4例.
, 百拇医药
统计学处理:组间差异采用t检验.
2 结果
心脏直视手术后多器官衰竭患者13例,死亡6例,占46%. 全部患者发生多器官功能衰竭后1 d开始TNF-α,IL-1β水平较对照组明显升高,2~3 d时达到峰值;IL-6,IL-8水平在发生多器官功能衰竭后2~3 d开始明显升高,4~5 d达到峰值. IL-6,IL-8升高时限滞后于TNF-α,IL-1β. 细胞因子TNF-α,IL-1β,IL-6,IL-8水平两组间有显著差异,死亡病例组明显高于存活病例组(Tab 1).
表1 心脏直视手术后多器官衰竭细胞因子变化
Tab 1 Serum cytokines in multiple organ failure
following open heart surgery (
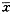 ±s, μg.L-1) Cytokines
±s, μg.L-1) Cytokines, 百拇医药
Control
MOF
1 d
2 d
3 d
4 d
5 d
TNF-α
0.20±0.05
1
0.40±0.06
0.57±0.08a
, http://www.100md.com 0.61±0.08a
0.51±0.03a
0.52±0.06a
2
0.56±0.08a
0.78±0.06b
0.81±0.09b
0.72±0.04b
0.70±0.66b
IL-1β
, 百拇医药
0.16±0.03
1
0.33±0.10
0.50±0.04a
0.52±0.09b
0.40±0.08a
0.47±0.05a
2
0.50±0.06a
0.67±0.05b
, 百拇医药
0.69±0.04b
0.59±0.10b
0.56±0.05a
IL-6
0.17±0.13
1
0.21±0.03
0.33±0.03
0.41±0.08a
0.52±0.06a
0.53±0.06a
, 百拇医药
2
0.19±0.05
0.46±0.08a
0.56±0.07a
0.83±0.09b
0.79±0.06b
IL-8
1.61±0.40
1
1.70±0.42
2.61±0.56
, 百拇医药
3.70±0.80a
4.95±1.23a
5.01±0.86a
2
2.01±0.38
3.92±0.81
4.92±0.78a
7.30±1.40b
7.14±0.72b
aP<0.05, bP<0.01 vs control. 1: live group, 2: death group.3 讨论
, 百拇医药
多器官功能衰竭是心脏直视手术后严重的并发症之一,死亡率极高. 同其他严重创伤、休克和感染等导致多器官衰竭一样,发病机制十分复杂. 广泛涉及神经体液、内分泌、营养代谢、免疫等许多系统,学说较多. 然而目前较趋一致的看法是由创伤所致“免疫―炎症反应”是MOF发生的最根本原因[2]. 为了验证这一学说,探讨多器官发生本质,我们对心脏直视手术多器官衰竭患者细胞因子进行动态观察. 结果显示多器官衰竭发生后TNF-α,IL-1β,IL-6,IL-8水平较对照组明显升高. 表明本组患者细胞因子持续过多地释放是介导、放大炎症介质级联效应,引起多器官衰竭的病理基础. 而IL-6,IL-8增高及达到峰值时限滞后于TNF-α,IL-1β,提示TNF-α,IL-8是细胞因子级联反应的始动因子[3].
在致病因素作用下,单核巨噬细胞被激活,释放TNF-α和IL-1β,此二因子进一步诱导中性粒细胞在肺、肝等器官组织聚集、粘附,大量中性粒细胞与内皮细胞粘附的同时,释放大量IL-6,IL-8引发了全身炎症反应失调. 分析临床资料,探索其致病因素. 本组患者术前心功能差、危重;术中体外循环时间长,使细胞破坏,纤维蛋白原和血小板激活造成凝血机制紊乱及术后低心排,胃肠壁微循环障碍,造成组织水肿,毛细血管通透性增加,菌群失调,细菌、毒素移位等是介导发生MOF的重要原因. 文献报道胃肠道是MOF“启动器官”,本组有近一半患者存在胃肠道功能紊乱,在引发MOF发生中是不可忽视的因素[4]. 因此如何监测、保护胃肠粘膜屏障是防止MOF发生极其重要环节.
, 百拇医药
增高的细胞因子具有多种生物学活性,它们可通过激活中性粒细胞,产生呼吸爆发释放大量氧自由基、蛋白溶解酶以及产生的白三烯等造成机体严重的损伤和紊乱. 本结果显示死亡病例组细胞因子水平明显高于存活病例组,这不仅进一步证实细胞因子在介导损伤中的作用,而且也提示抑制细胞因子的释放是提高治愈MOF的一个重要途径[5].
作者简介:李 彤(1963-),男(汉族),辽宁省辽阳市人.博士,副教授,副主任医师.
Tel.(029)3375311 Email. Litong@fmmu.edu.cn
参考文献:
[1] 王今达,王宣恩. MODS病理分期及严重程度评分标准[J]. 中国危重病急救医学, 1995;7(6):346-346.
[2] Cannon JG. Circulating interleukin-1 and tumor necrasis factor in septic shlck and experimental endotoxin fever [J]. J Infect Dis, 1990;161(1):79-86.
, http://www.100md.com
[3] Spooner CE, Markowitz NP. The role of tumor necrosis factor in sepsis [J]. Clin Immunol Immunopathol, 1992;62(4):511-516.
[4] 王今达. 多脏器功能失常综合征与肠道内细菌及内毒素易位[J]. 中国危重病免救医学, 1995;7(6):321-323.
[5] Deitch EA. Multiple organ failure: Pathophysiology and petential future therapy [J]. Am Surg, 1992;216(20):117-223.
收稿日期:2000-01-18; 修回日期:2000-02-16, http://www.100md.com