甲壳素和甲壳胺对聚乳酸体外降解的影响*
作者:廖凯荣 唐舫成 罗力力 卢泽俭 黄会刚
单位:廖凯荣 唐舫成 罗力力 卢泽俭(中山大学 高分子研究所,广州 510275);黄会刚(广东省化工研究院,广州 510000)
关键词:DL-聚乳酸;甲壳素;甲壳胺;体外降解;抑制作用
生物医学工程学杂志990302 摘要 考察了DL-聚乳酸(DL-PLA)/甲壳素(CHI),DL-PLA/甲壳胺(CHS)两种复合物在生理盐水降解过程中生理盐水的pH值、试样的失重率和外观形态以及DL-PLA分子量的变化,结果表明:CHI和CHS对DL-PLA的降解速度有明显的抑制作用,并对抑制机理进行了探讨。
Effects of Chitin and Chitosan on Degradation
of DL-Polylactide in vitro
, http://www.100md.com
Liao Kairong1 Tang Fangcheng1 Luo Lili1 Lu Zejian1 Huang Huigang2
1 (Institute of Polymer Science, Zhongshan University, Guangzhou 510275)
2 (Institute of Chemical Engineering of Guangdong Province, Guangzhou 510000)
Abstract The authors assessed the variations of pH-values of the physiological saline used for in vitro degradation tests of DL-Polylactide(DL-PLA)/chitin and DL-PLA/chitosan composites and DL-PLA. The weight-loss rations, the appearance and morphology of the tested specimens, and the molecular weights of DL-PLA in composites and pure DL-PLA were alse investigated. The results showed that both chitin and chitosan had significant inhibitory effects on the degradation of DL-PLA, and the effect of chitosan was stronger than that of chitin. A discussion on the mechanism of such inhibition is presented.
, 百拇医药
Key words DL-Polylactide Chitin Chitosan Degradation in vitro Retardation
1 前 言
聚乳酸(PLA)是一种具有很好生物相容性和可降解吸收的高分子材料,医学上可用于药物缓释、手术缝线、防粘连膜、神经保护和接合导管以及骨折内固定材料[1~9]。由于PLA降解过程中产生的酸性降解产物一方面起自催化作用,加速母体的降解,使材料的初始力学性能下降过快,另一方面又可能产生非感染性炎症。因此有报道[10]通过共聚或共混方法加入如水杨酸类的消炎药物,以克服非感染性炎症。但这种方法不能解决根本问题。考虑到甲壳素(CHI)和它的衍生物甲壳胺(CHS)具有良好的生物相容性,也是可降解吸收的医用天然高分子材料,其水解产物氨基葡萄糖的氨基具有碱性,可有效地与PLA的降解产物的酸性中和,抑制PLA的自催化水解和非感染性炎症。我们分别用CHI和CHS与DL-PLA共混,制备DL-PLA/CHI和DL-PLA/CHS复合材料,在生理盐水中进行体外降解试验,从生理盐水的pH值、试样的失重率和外观形态以及复合材料中DL-PLA分子量的变化,考察了CHI和CHS对DL-PLA降解的影响。
, 百拇医药
2 实验部分
2.1 材料
DL-PLA:自合成,Mv(分子量)=3.0×104。
CHI:工业品,Mv=6.12×105;CHS:工业品,Mv=4.65×105,脱乙酰度83.5%。它们使用前均经纯化处理[11],再研磨过筛,取过300目部分,70 ℃真空干燥48 h备用。
2.2 DL-PLA/CHI和DL-PLA/CHS复合物及试样的制备
在不锈钢的加热台上将DL-PLA加热至粘流态(约85℃),分别加入计量的CHI和CHS粉末,以获取不同比例的DL-PLA/CHI与DL-PLA/CHS复合物。用口宽约8 mm的不锈钢铲混炼5 min后取出,再模压成厚为2.0 mm的片材,最后裁成40 mm×10 mm×2.0 mm的样条供降解试验。
, 百拇医药
2.3 降解试验
降解试验在试管中进行。降解液为生理盐水,pH=6.22(实测),降解温度37 ℃。试验期间,样条(预先称重)完全浸泡在降解液中,每个试管浸泡1条样条。
2.4 表征
定期随机取出降解试验样条,并对降解液和样条进行如下表征:
降解液的pH值:用pHS-25型酸度计(上海雷磁仪器厂)测定。
试样的外观形态:通过肉眼观察确定。
失重率的测定:样条先用蒸馏水充分洗涤,40 ℃真空干燥48 h后,称重,计算其失重率。
DL-PLA分子量的测定:粘度法,温度25 ℃。测定时将洗涤干燥好的样条用氯仿溶解,滤去不溶物。DL-PLA的分子量按下式[12]计算:
, http://www.100md.com
[η]=5.45×10-4×Mv0.73
3 结果与讨论
3.1 DL-PLA和DL-PLA/CHI、DL-PLA/CHS复合物降解过程中降解液pH值的变化
DL-PLA和DL-PLA/CHI、DL-PLA/CHS复合物降解过程中降解液pH值的变化如图1、2所示。从图中可以看到,纯DL-PLA在降解的前12周,降解液的pH值基本不变,12周后pH值迅速降低,至16周时降至2.2。而对于DL-PLA/CHI复合物,在前12周,与纯DL-PLA相比,其降液的pH值却略有升高,并且随CHI含量增加而增高。降解至12周后,降解液的pH值也迅速下降,至16周时降至2.0~3.0。DL-PLA/CHS复合物降解液pH值的变化规律与DL-PLA/CHI系列相似,但相应的各个时期的pH值较高,且随复合物中CHS含量的增加而增大。当CHS含量为30%,降解至16周时降解液的pH值为5.5。
, http://www.100md.com
图1 DL-PLA/CHI的降解时间对生理盐水pH值的影响
Fig 1 Dependence of pH-values of physiological saline
on degradation time for DL-PLA/CHI
a.DL-PLA;b.DL-PLA/CHI=90/10;c.DL-PLA/CHI=
80/20;d.DL-PLA/CHI=70/30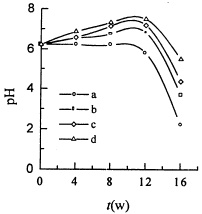
图2 DL-PLA/CHS的降解时间对生理盐水pH值的影响
Fig 2 Depaendence of pH-values of physiological saline
, 百拇医药
on degradation time for DL-PLA/CHS
a.DL-PLA;b.DL-PLA/CHS=90/10;c.DL-PLA/CHS=
80/20;d.DL-PLA/CHS=70/30
3.2 CHI和CHS对DL-PLA降解过程中分子量的影响
表1是DL-PLA和DL-PLA/CHI、DL-PLA/CHS复合物在降解过程中DL-PLA分子量(Mv)随时间变化的结果。可以看到,复合物的DL-PLA在降解的各个时期的Mv都比同时期的纯DL-PLA的高,而且CHI或CHS的含量越高,其DL-PLA的Mv越高,说明复合物中DL-PLA的降解速度比纯DL-PLA的慢。CHI和CHS在不同程度上对DL-PLA的降解有抑制作用。表1的结果表明,纯DL-PLA分子量降解半衰期约4周,而两个复合系列中的DL-PLA分子量降解半衰期约为4~8周。
, http://www.100md.com
表1 DL-PLA和DL-PLA/CHI、DL-PLA/CHS中DL-PLA分子量(Mv)随降解时间的变化
Table 1 Variations of molecular weight(Mv) of DL-PLA with degradation time for DL-PLA, DL-PLA/CHI and DL-PLA/CHS Time
(wk)
DL-PLA
DL-PLA/CHI
DL-PLA/CHS
90/10
70/30
90/10
, http://www.100md.com
70/30
0
3.0×104
3.0×104
3.0×104
3.0×104
3.0×104
4
1.4×104
1.5×104
1.6×104
, 百拇医药
1.6×104
1.9×104
8
0.61×104
0.72×104
0.91×104
0.85×104
1.1×104
12
0.27×104
, 百拇医药
0.35×104
0.50×104
0.44×104
0.65×104
16
0.12×104
0.15×104
0.24×104
0.23×104
0.39×104
, 百拇医药
3.3 DL-PLA降解机理和CHI、CHS对DL-PLA降解的影响
3.3.1 DL-PLA降解机理 降解时间对DL-PLA、DL-PLA/CHI和DL-PLA/CHS的失重率的影响见表2。纯DL-PLA在降解的前12周,失重率很小且变化缓慢,降解液的pH值(图1、2曲线a)下降也很小,说明此时DL-PLA降解成可溶于水的小分子的数目仍很少。而在降解12周后的4周时间,失重率成倍增加,降解液的pH值也从12周起发生突变,至16周时下降至2.2,说明此时DL-PLA降解成可溶于水的小分子的数目增多。由此可见,DL-PLA在降解液中的降解是大分子链的随机断裂过程,分子量由大变小(见表1),而不是直接解聚成小分子乳酸。这与文献[13]报道聚乳酸的水解机理相符。表2 降解时间对DL-PLA、DL-PLA/CHI和DL-PLA/CHS的失重率的影响
Table 2 Dependence of weight-loss ratios(%) on degradation time for DL-PLA, DL-PLA/CHI and DL-PLA/CHS Time
, 百拇医药
(wk)
DL-PLA
DL-PLA/CHI
DL-PLA/CHS
90/10
80/20
70/30
90/10
80/20
70/30
4
0.00
0.16
, http://www.100md.com
0.28
0.32
0.40
0.90
1.14
8
0.16
0.25
0.36
0.48
0.73
1.40
1.87
, http://www.100md.com
12
0.18
0.31
0.42
0.63
1.38
2.22
2.15
16
0.37
a
a
a
, 百拇医药
3.64
3.60
a.Specimens broken and could not be determined/试样碎裂,未能测定
3.3.2 CHI和CHS对DL-PLA降解的影响 CHI和CHS对DL-PLA降解的影响可归结为两个方面:(1)CHI和CHS都具有较强的亲水性,它们与DL-PLA共混后,使水渗透到试样内部的速率增大(可从试样在降解液中浸泡4周后即变形,而DL-PLA对照样仍透明和外观无变化得到反映,见表3)而使DL-PLA分子链中的不稳定键即酯键的水解速率加快;(2)CHI和CHS的降解产物或其自身含有的氨基,能与DL-PLA降解的酸性产物起中和反应,可抑制DL-PLA的酸自催化加速水解作用。从实验结果(见图1、2和表1)看,后者作用更强于前者。这可能是CHI和CHS在降解一开始就可以水解成可溶于水的小分子甚至是氨基葡萄糖,而DL-PLA则没有一开始降解就有这种作用。由于可溶于水的小分子单糖及多糖的碱性使降解液的pH值升高。但降解时间超过12周后,CHI和CHS继续水解的同时,DL-PLA水解成可溶于水的酸性小分子物质开始产生并迅速增加,其引起的酸性超过了CHI和CHS水解产生的碱性的速度,因而降解液的pH值下降。
, 百拇医药
表3 降解时间对试样外观形态的影响
Table 3 Effects of degradation time on appearance and morpholgoy of specimens Time(wk)
DL-PLA
DL-PLA/CHI
DL-PLA/CHS
4
transparent and no change in
appearance
softening and deformed
, http://www.100md.com
softening and deformed
8
whitening and opaque
being pale in color, others
basically the smae as above
the same as the DL-PLA/CHI
specimens
12
softening but not sticking
basically the same as above
, 百拇医药
the same as the DL-PLA/CHI
specimens
16
softening and sticking
specimens broken and small
amount of CHI powder free
of the matrixes
the same as the DL-PLA/CHI
specimens
比较CHI和CHS对DL-PLA降解的影响,CHS更能抑制DL-PLA的降解。这主要是因为CHS较CHI具有更多的氨基所致。
, 百拇医药
4 结 论
DL-PLA降解过程是大分子链的随机断裂过程,其实质是聚酯分子链中酯键的水解,可由于降解产物的酸性催化作用而加速。CHI和CHS与DL-PLA复合后,虽然由于它们的较强的亲水性而使水渗透到材料内部的速率增大而可能使DL-PLA的降解加快,但CHI和CHS的水解产物或其自身所含有的氨基的碱性作用,中和了DL-PLA降解产物乳酸的酸性,在一定程度上抑制了DL-PLA的酸自催化加速水解作用,使DL-PLA的降解作用抑制。由于CHS有更多的氨基,CHS的这种抑制作用要强于CHI。
* 广东省自然科学基金资助项目(960020,970160)
参考文献
1 陈世龙,熊德举,赵应慧.可吸收骨折内固定材料.生物医学工程学杂志,1993;10(2)∶169
, 百拇医药
2 胡培成,吴兰亭,杨士林.医用生物降解材料―聚乳酸及其共聚物.生物医学工程学杂志,1993;10(2)∶183
3 王远亮,赵建华.生物可降解聚乳酸骨科材料研究进展.功能材料,1995;26(6)∶567
4 Suuronen R, Pohjonen T, Taurio R et al. Strength retention of self-reinforced poly-L-lactide screws and plates:an in vivo and in vitro study. J Mat Sci:Mat in Med, 1992; 3∶426
5 刘建国,徐莘香.骨科生物降解可吸收材料30年进展.中华创伤杂志,1996;12(1)∶64
6 Satish Pulapura, Joachim KoHn.医用生物可吸收性聚合物的发展趋势.国外医学生物医学分册,1992;15(5)∶281
, 百拇医药
7 B stman OM.Current concepts review:Absorbable implants for the fixation of fractures. J Bone and Joint Surg, 1991; 75-A(1)∶148
stman OM.Current concepts review:Absorbable implants for the fixation of fractures. J Bone and Joint Surg, 1991; 75-A(1)∶148
8 Suuronen R. Biodegradable fracture-fixation devices in maxillofacial surgery. Int J Oral Maxillofac Surg, 1993; 22∶50
9 陈希哲,王永海.可吸收骨折内固定物及其在颌面外科的应用.国外医学口腔分册,1995;22(2)∶65
10 Super H, Grilpman DW, Pennings A. Incorporation of salicylates into poly(L-lactide).J Polym Bull, 1994; 32∶509
, 百拇医药
11 唐舫成.生物降解材料聚乳酸/甲壳素复合物的基础研究.中山大学硕士论文,1997
12 Schindler A, Harper D. Polylactide:Ⅱ.Viscosity-molecular weight relationships and unperturbed chain dimensions. J Polym Sci: Polym Chem Ed, 1979; 17∶2593
13 沈正荣,朱家蕙,吴兰亭等.DL-聚乳酸微球大鼠体内的降解.生物医学工程学杂志,1994;11(2)∶98
(收稿:1998-03-20 修回:1998-07-28), 百拇医药
单位:廖凯荣 唐舫成 罗力力 卢泽俭(中山大学 高分子研究所,广州 510275);黄会刚(广东省化工研究院,广州 510000)
关键词:DL-聚乳酸;甲壳素;甲壳胺;体外降解;抑制作用
生物医学工程学杂志990302 摘要 考察了DL-聚乳酸(DL-PLA)/甲壳素(CHI),DL-PLA/甲壳胺(CHS)两种复合物在生理盐水降解过程中生理盐水的pH值、试样的失重率和外观形态以及DL-PLA分子量的变化,结果表明:CHI和CHS对DL-PLA的降解速度有明显的抑制作用,并对抑制机理进行了探讨。
Effects of Chitin and Chitosan on Degradation
of DL-Polylactide in vitro
, http://www.100md.com
Liao Kairong1 Tang Fangcheng1 Luo Lili1 Lu Zejian1 Huang Huigang2
1 (Institute of Polymer Science, Zhongshan University, Guangzhou 510275)
2 (Institute of Chemical Engineering of Guangdong Province, Guangzhou 510000)
Abstract The authors assessed the variations of pH-values of the physiological saline used for in vitro degradation tests of DL-Polylactide(DL-PLA)/chitin and DL-PLA/chitosan composites and DL-PLA. The weight-loss rations, the appearance and morphology of the tested specimens, and the molecular weights of DL-PLA in composites and pure DL-PLA were alse investigated. The results showed that both chitin and chitosan had significant inhibitory effects on the degradation of DL-PLA, and the effect of chitosan was stronger than that of chitin. A discussion on the mechanism of such inhibition is presented.
, 百拇医药
Key words DL-Polylactide Chitin Chitosan Degradation in vitro Retardation
1 前 言
聚乳酸(PLA)是一种具有很好生物相容性和可降解吸收的高分子材料,医学上可用于药物缓释、手术缝线、防粘连膜、神经保护和接合导管以及骨折内固定材料[1~9]。由于PLA降解过程中产生的酸性降解产物一方面起自催化作用,加速母体的降解,使材料的初始力学性能下降过快,另一方面又可能产生非感染性炎症。因此有报道[10]通过共聚或共混方法加入如水杨酸类的消炎药物,以克服非感染性炎症。但这种方法不能解决根本问题。考虑到甲壳素(CHI)和它的衍生物甲壳胺(CHS)具有良好的生物相容性,也是可降解吸收的医用天然高分子材料,其水解产物氨基葡萄糖的氨基具有碱性,可有效地与PLA的降解产物的酸性中和,抑制PLA的自催化水解和非感染性炎症。我们分别用CHI和CHS与DL-PLA共混,制备DL-PLA/CHI和DL-PLA/CHS复合材料,在生理盐水中进行体外降解试验,从生理盐水的pH值、试样的失重率和外观形态以及复合材料中DL-PLA分子量的变化,考察了CHI和CHS对DL-PLA降解的影响。
, 百拇医药
2 实验部分
2.1 材料
DL-PLA:自合成,Mv(分子量)=3.0×104。
CHI:工业品,Mv=6.12×105;CHS:工业品,Mv=4.65×105,脱乙酰度83.5%。它们使用前均经纯化处理[11],再研磨过筛,取过300目部分,70 ℃真空干燥48 h备用。
2.2 DL-PLA/CHI和DL-PLA/CHS复合物及试样的制备
在不锈钢的加热台上将DL-PLA加热至粘流态(约85℃),分别加入计量的CHI和CHS粉末,以获取不同比例的DL-PLA/CHI与DL-PLA/CHS复合物。用口宽约8 mm的不锈钢铲混炼5 min后取出,再模压成厚为2.0 mm的片材,最后裁成40 mm×10 mm×2.0 mm的样条供降解试验。
, 百拇医药
2.3 降解试验
降解试验在试管中进行。降解液为生理盐水,pH=6.22(实测),降解温度37 ℃。试验期间,样条(预先称重)完全浸泡在降解液中,每个试管浸泡1条样条。
2.4 表征
定期随机取出降解试验样条,并对降解液和样条进行如下表征:
降解液的pH值:用pHS-25型酸度计(上海雷磁仪器厂)测定。
试样的外观形态:通过肉眼观察确定。
失重率的测定:样条先用蒸馏水充分洗涤,40 ℃真空干燥48 h后,称重,计算其失重率。
DL-PLA分子量的测定:粘度法,温度25 ℃。测定时将洗涤干燥好的样条用氯仿溶解,滤去不溶物。DL-PLA的分子量按下式[12]计算:
, http://www.100md.com
[η]=5.45×10-4×Mv0.73
3 结果与讨论
3.1 DL-PLA和DL-PLA/CHI、DL-PLA/CHS复合物降解过程中降解液pH值的变化
DL-PLA和DL-PLA/CHI、DL-PLA/CHS复合物降解过程中降解液pH值的变化如图1、2所示。从图中可以看到,纯DL-PLA在降解的前12周,降解液的pH值基本不变,12周后pH值迅速降低,至16周时降至2.2。而对于DL-PLA/CHI复合物,在前12周,与纯DL-PLA相比,其降液的pH值却略有升高,并且随CHI含量增加而增高。降解至12周后,降解液的pH值也迅速下降,至16周时降至2.0~3.0。DL-PLA/CHS复合物降解液pH值的变化规律与DL-PLA/CHI系列相似,但相应的各个时期的pH值较高,且随复合物中CHS含量的增加而增大。当CHS含量为30%,降解至16周时降解液的pH值为5.5。

, http://www.100md.com
图1 DL-PLA/CHI的降解时间对生理盐水pH值的影响
Fig 1 Dependence of pH-values of physiological saline
on degradation time for DL-PLA/CHI
a.DL-PLA;b.DL-PLA/CHI=90/10;c.DL-PLA/CHI=
80/20;d.DL-PLA/CHI=70/30

图2 DL-PLA/CHS的降解时间对生理盐水pH值的影响
Fig 2 Depaendence of pH-values of physiological saline
, 百拇医药
on degradation time for DL-PLA/CHS
a.DL-PLA;b.DL-PLA/CHS=90/10;c.DL-PLA/CHS=
80/20;d.DL-PLA/CHS=70/30
3.2 CHI和CHS对DL-PLA降解过程中分子量的影响
表1是DL-PLA和DL-PLA/CHI、DL-PLA/CHS复合物在降解过程中DL-PLA分子量(Mv)随时间变化的结果。可以看到,复合物的DL-PLA在降解的各个时期的Mv都比同时期的纯DL-PLA的高,而且CHI或CHS的含量越高,其DL-PLA的Mv越高,说明复合物中DL-PLA的降解速度比纯DL-PLA的慢。CHI和CHS在不同程度上对DL-PLA的降解有抑制作用。表1的结果表明,纯DL-PLA分子量降解半衰期约4周,而两个复合系列中的DL-PLA分子量降解半衰期约为4~8周。
, http://www.100md.com
表1 DL-PLA和DL-PLA/CHI、DL-PLA/CHS中DL-PLA分子量(Mv)随降解时间的变化
Table 1 Variations of molecular weight(Mv) of DL-PLA with degradation time for DL-PLA, DL-PLA/CHI and DL-PLA/CHS Time
(wk)
DL-PLA
DL-PLA/CHI
DL-PLA/CHS
90/10
70/30
90/10
, http://www.100md.com
70/30
0
3.0×104
3.0×104
3.0×104
3.0×104
3.0×104
4
1.4×104
1.5×104
1.6×104
, 百拇医药
1.6×104
1.9×104
8
0.61×104
0.72×104
0.91×104
0.85×104
1.1×104
12
0.27×104
, 百拇医药
0.35×104
0.50×104
0.44×104
0.65×104
16
0.12×104
0.15×104
0.24×104
0.23×104
0.39×104
, 百拇医药
3.3 DL-PLA降解机理和CHI、CHS对DL-PLA降解的影响
3.3.1 DL-PLA降解机理 降解时间对DL-PLA、DL-PLA/CHI和DL-PLA/CHS的失重率的影响见表2。纯DL-PLA在降解的前12周,失重率很小且变化缓慢,降解液的pH值(图1、2曲线a)下降也很小,说明此时DL-PLA降解成可溶于水的小分子的数目仍很少。而在降解12周后的4周时间,失重率成倍增加,降解液的pH值也从12周起发生突变,至16周时下降至2.2,说明此时DL-PLA降解成可溶于水的小分子的数目增多。由此可见,DL-PLA在降解液中的降解是大分子链的随机断裂过程,分子量由大变小(见表1),而不是直接解聚成小分子乳酸。这与文献[13]报道聚乳酸的水解机理相符。表2 降解时间对DL-PLA、DL-PLA/CHI和DL-PLA/CHS的失重率的影响
Table 2 Dependence of weight-loss ratios(%) on degradation time for DL-PLA, DL-PLA/CHI and DL-PLA/CHS Time
, 百拇医药
(wk)
DL-PLA
DL-PLA/CHI
DL-PLA/CHS
90/10
80/20
70/30
90/10
80/20
70/30
4
0.00
0.16
, http://www.100md.com
0.28
0.32
0.40
0.90
1.14
8
0.16
0.25
0.36
0.48
0.73
1.40
1.87
, http://www.100md.com
12
0.18
0.31
0.42
0.63
1.38
2.22
2.15
16
0.37
a
a
a
, 百拇医药
3.64
3.60
a.Specimens broken and could not be determined/试样碎裂,未能测定
3.3.2 CHI和CHS对DL-PLA降解的影响 CHI和CHS对DL-PLA降解的影响可归结为两个方面:(1)CHI和CHS都具有较强的亲水性,它们与DL-PLA共混后,使水渗透到试样内部的速率增大(可从试样在降解液中浸泡4周后即变形,而DL-PLA对照样仍透明和外观无变化得到反映,见表3)而使DL-PLA分子链中的不稳定键即酯键的水解速率加快;(2)CHI和CHS的降解产物或其自身含有的氨基,能与DL-PLA降解的酸性产物起中和反应,可抑制DL-PLA的酸自催化加速水解作用。从实验结果(见图1、2和表1)看,后者作用更强于前者。这可能是CHI和CHS在降解一开始就可以水解成可溶于水的小分子甚至是氨基葡萄糖,而DL-PLA则没有一开始降解就有这种作用。由于可溶于水的小分子单糖及多糖的碱性使降解液的pH值升高。但降解时间超过12周后,CHI和CHS继续水解的同时,DL-PLA水解成可溶于水的酸性小分子物质开始产生并迅速增加,其引起的酸性超过了CHI和CHS水解产生的碱性的速度,因而降解液的pH值下降。
, 百拇医药
表3 降解时间对试样外观形态的影响
Table 3 Effects of degradation time on appearance and morpholgoy of specimens Time(wk)
DL-PLA
DL-PLA/CHI
DL-PLA/CHS
4
transparent and no change in
appearance
softening and deformed
, http://www.100md.com
softening and deformed
8
whitening and opaque
being pale in color, others
basically the smae as above
the same as the DL-PLA/CHI
specimens
12
softening but not sticking
basically the same as above
, 百拇医药
the same as the DL-PLA/CHI
specimens
16
softening and sticking
specimens broken and small
amount of CHI powder free
of the matrixes
the same as the DL-PLA/CHI
specimens
比较CHI和CHS对DL-PLA降解的影响,CHS更能抑制DL-PLA的降解。这主要是因为CHS较CHI具有更多的氨基所致。
, 百拇医药
4 结 论
DL-PLA降解过程是大分子链的随机断裂过程,其实质是聚酯分子链中酯键的水解,可由于降解产物的酸性催化作用而加速。CHI和CHS与DL-PLA复合后,虽然由于它们的较强的亲水性而使水渗透到材料内部的速率增大而可能使DL-PLA的降解加快,但CHI和CHS的水解产物或其自身所含有的氨基的碱性作用,中和了DL-PLA降解产物乳酸的酸性,在一定程度上抑制了DL-PLA的酸自催化加速水解作用,使DL-PLA的降解作用抑制。由于CHS有更多的氨基,CHS的这种抑制作用要强于CHI。
* 广东省自然科学基金资助项目(960020,970160)
参考文献
1 陈世龙,熊德举,赵应慧.可吸收骨折内固定材料.生物医学工程学杂志,1993;10(2)∶169
, 百拇医药
2 胡培成,吴兰亭,杨士林.医用生物降解材料―聚乳酸及其共聚物.生物医学工程学杂志,1993;10(2)∶183
3 王远亮,赵建华.生物可降解聚乳酸骨科材料研究进展.功能材料,1995;26(6)∶567
4 Suuronen R, Pohjonen T, Taurio R et al. Strength retention of self-reinforced poly-L-lactide screws and plates:an in vivo and in vitro study. J Mat Sci:Mat in Med, 1992; 3∶426
5 刘建国,徐莘香.骨科生物降解可吸收材料30年进展.中华创伤杂志,1996;12(1)∶64
6 Satish Pulapura, Joachim KoHn.医用生物可吸收性聚合物的发展趋势.国外医学生物医学分册,1992;15(5)∶281
, 百拇医药
7 B
 stman OM.Current concepts review:Absorbable implants for the fixation of fractures. J Bone and Joint Surg, 1991; 75-A(1)∶148
stman OM.Current concepts review:Absorbable implants for the fixation of fractures. J Bone and Joint Surg, 1991; 75-A(1)∶1488 Suuronen R. Biodegradable fracture-fixation devices in maxillofacial surgery. Int J Oral Maxillofac Surg, 1993; 22∶50
9 陈希哲,王永海.可吸收骨折内固定物及其在颌面外科的应用.国外医学口腔分册,1995;22(2)∶65
10 Super H, Grilpman DW, Pennings A. Incorporation of salicylates into poly(L-lactide).J Polym Bull, 1994; 32∶509
, 百拇医药
11 唐舫成.生物降解材料聚乳酸/甲壳素复合物的基础研究.中山大学硕士论文,1997
12 Schindler A, Harper D. Polylactide:Ⅱ.Viscosity-molecular weight relationships and unperturbed chain dimensions. J Polym Sci: Polym Chem Ed, 1979; 17∶2593
13 沈正荣,朱家蕙,吴兰亭等.DL-聚乳酸微球大鼠体内的降解.生物医学工程学杂志,1994;11(2)∶98
(收稿:1998-03-20 修回:1998-07-28), 百拇医药