���ѳ����������߶��ص����幹������Ч����
���ߣ��ȷ��� ��� ��ҹϼ Ǯ���� ��Ƽ Ҷѩ
��λ��������ѧ����ҽԺ��������ʵ���ң����� 100044
�ؼ��ʣ����壻���������߶����ࣻҩ�����壻��л���ѳ������������ںϵ������ࣻ��л
����ҽ�ƴ�ѧѧ��000419 [ժ Ҫ] Ŀ�ģ��������ѳ�����������183B2ScFv ��ٵ����ⶾ��(peudononas exotoxin, PE38)���ںϵ��ױ������岢�Ʊ������ѳ����������߶��ص���183B2ScFvPE38��Ϊ�ѳ����������ƴ��»��������������û��̼���������3���ǿ�¡�������뵥������Ļ����붾�صĻ����ǿ�¡��ԭ�˱�������pET30a(+)�ϣ�����IPTG���յ��½��б������ֱ��ELISA��ϸ��ɱ�˶Կ��弰���ز��ֵĻ��Խ��м�顣��������ﵰ��183B2ScFvPE38���нϺõĿ�����Լ����ػ��ԡ����ۣ����ѳ����������߶���183B2ScFvPE38 �������õ�����ѧ���Լ�����ѧ���ԣ����������õ�Ӧ��ǰ����
, http://www.100md.com
[��ͼ�����] R966 [���ױ�ʶ��] A [���±��] 1000-1530(2000)04-0347-04
Vector construction and high level expression of single chain
immunotoxin against ovarian carcinoma
YOU Fang-Lei
(Department of Gynecologic Oncology, Peking University People's Hospital,Beijing 100044, China)
FENG Jie
(Department of Gynecologic Oncology, Peking University People's Hospital,Beijing 100044, China)
, ��Ĵҽҩ
CHEN Ye-Xia
(Department of Gynecologic Oncology, Peking University People's Hospital,Beijing 100044, China)
QIAN He-Nian
(Department of Gynecologic Oncology, Peking University People's Hospital,Beijing 100044, China)
ZHOU Ping
(Department of Gynecologic Oncology, Peking University People's Hospital,Beijing 100044, China)
, ��Ĵҽҩ
YE Xue
(Department of Gynecologic Oncology, Peking University People's Hospital,Beijing 100044, China)
ABSTRACT Objective:
To construct an expression vector for co_expression of single chain Fv antibody (OC183B2) and peudomonas exotoxin(PE38). Methods: Clone the genes of ScFv (OC183B2) and PE38 into PET30a(+) and then express the immunotoxin after induced with IPTG. Results: Liable activity of antibody and toxic in were both observed in the fusion recombinant protein. Conclusion: The recombinant fusion protein 183B2ScFvPE38 keeps the activity of both components and may be of great use in the future to deal with ovarian carcinoma.
, ��Ĵҽҩ
KEY WORDS Antibodies, neoplasm; Immunotoxins; Drug carriers/metab; Ovarian neoplasms; Recombinant fusion proteins/metab
(J Beijing Med Univ, 2000,32:347-350)
�����������ŷ�������ѧ������ѧ�����ķ�չ������������ѧ�����Ѿ���Ϊ���������ơ����ơ�����֮����Ҫ�����Ʒ�ʽ�����Ҷ�����һֱ�����Ե���¡����Ϊ���壬����ͬλ�ء�ҩ����ص���,���ѳ����������ߵ�����Ϻ����ߵ������Ƶ��о������ѳɹ��Ʊ���С���ӵ���[1]����99mTc����½����������ģ�ͷ�������������о����������������ͼ���ڴ˻����ϣ���ʵ������Ӧ�ñ����Ʊ��ĵ������幹�����߶��أ��о��ڿ��嵼���£�Я�����ص����ѳ������а������ƵĿ����ԡ�
, ��Ĵҽҩ
���߶����������������Ƶ�һ���·������ڹ��⣬�������߶����ѽ�����ڼ������ٴ�ʵ���о��Ρ�ʵ��֤ʵ���߶��ؾ������õ�Ӧ��ǰ��[2��3]�����ڹ����ѳ��������Ե���¡���幹�����߶��ص��о����������ټ�,����δ���йر�����
1 �����뷽��
1.1 ���幹�������߶��صĸ�Ч����
1.1.1 �����;��� pET16-183B2 ScFvΪ���ҹ����ĺ���183B2�����������(183B2ScFv)�������� PAGITΪ���ж��ػ���(peudononas exotoxin, PE38)����������Ч��������pET30a(+)������pUC18���˾�Bl21��DH5��Ϊ���ұ��档����PAGIT������GI724 Ϊ�й���ѧԺ�Ŵ��о����ƻ����������͡�
, ��Ĵҽҩ
1.1.2 ����������ø����ø ����Promega��˾��ϸ��ϵ���ѳ���ϸ��ϵSKOV3��������ϸ��ϵHeLa Ϊ���ұ��档
1.1.3 ���߶��ر�������Ĺ���(ͼ1) (1) pUC18-183B2ScFv�Ĺ����� pET16-183B2ScFv��Nde��EcoR�������������µ������壬������СƬ�Σ�pUC18����ͬλ��ø�У����մ�Ƭ�Ρ���T4 DNA ����ø�������½����������ǿ�¡��pUC18�У�����֮ΪpUC18-183B2ScFv��(2) pUC18-ScFvPE38�Ĺ�����������pUC18-183B2ScFv��Sac��EcoR�����������մ�Ƭ�Σ�����PE38��PAGIT������ͬλ�����£����ղ������ǿ�¡���ѻ��յĴ�Ƭ���С���ʱ��������������ΪpUC18-ScFvPE38��(3) pET30-ScFvPE38�Ĺ�����pUC18-ScFvPE38 Nde��EcoR��ø���º������߶��ص�Ƭ�Σ�������ͬλ���ǿ�¡��pET30a(+)�У���ɸ�Ч��������pET30-ScFvPE38�Ĺ��������Ը���������ø�м�����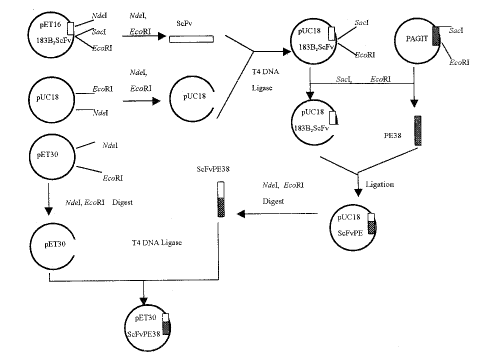
, ��Ĵҽҩ
ͼ1 ���幹��ͼʾ
Figure 1 Construction route of the vectors
1.1.4 �����������յ�����������ѽ⼰������ ����������������Bl21�˾���37����1��100(�����)ת�Ӻ����������600 nm���ܶ�ԼΪ0.4ʱ����IPTG����Ũ��Ϊ0.4 mmol.L-1���յ�4 h���ռ����壬��������ϸ�������ķ�������壬����������Һ������Һ��PBS����ҹ�������徭����ϴ�Ӻ�8mol.L-1�����ܽ⣬���븴��Һ(�ɷ֣�50 mmol.L-1 Tris-HCl,5mmol.L-1 EDTA,1mmol.L-1 �����ȹ���ģ�5mmol.L-1 ��ԭ�ȹ����)ϡ���ԣ�10�渴��48h��PEG 20000Ũ����20mmol.L-1��Tris-Cl����ͬŨ�ȵ��������ݶ�����
, ��Ĵҽҩ
1.1.5 ������� SDS-�۱�ϩ����������Ӿ�������β��P�䴿�ȡ�
1.2 ���ﵰ���Լ��
1.2.1 ��Ҫ���� ���ѳ�������¡����COC183B2Ϊ�������Ʊ����廯����Sephorose4B����Parmacia��˾��������������ø���Ա���ͬ�����\����չ��˾��
1.2.2 �������Ŀ�ԭ����ȡ����� (1)��ˮ��ϸ�����OC183B2��ԭ���ԵIJ��˸�ˮ����������林������Σ�Ȼ������Ͳ�����ȡ��ԭ���Ͳ������ϲ����廯����Sephorose4B���������ƽ����ȫ����������ż��2 h��װ�������Ҵ�����գ����Ỻ��Һ�����Ỻ��Һ���������ϴ�Ӻ�����������3 mol.L-1�������ϴ�ѣ���������Ǽ�⡣(2) ø�꿹ԭ�Ʊ��������Ͳ������õ���Ũ���������pH 9.2��0.001 mol.L-1̼���λ���Һ��ƽ�ⱸ�á�������������ø��ȩ�����������������ԭ���±ܹ����2 h���ټ����������Ƶ�4g.L-1���������ƣ�4�� 2 h��������������ɱ�ǹ��̡�
, http://www.100md.com
1.2.3 ���߶��صĻ��Բⶨ (1)������� ��ֱ��ELISA����⡣���Ե�����10 mg.L-1��4������ҹ��HRP-��ԭOC183B2��⣻�����ѽ�Һ����(�����Ա���ɷ�)�ð���Һ�ݶ�ϡ�ͺ�4������ҹ����HRP-��ԭ��⡣ʵ����ÿ�����pET30a(+)ƽ���Ʊ�������Ϊ���Զ��ա���������COC183B2��Ϊ���Զ��ա�(2) ���ػ��Բ���ϸ����ʵ��(MTT��)��⡣��ϸ��Ϊ����OC183B2��ԭ���ѳ���ϸ��ϵSKOV3������ϸ������Ϊ������ϸ��ϵHeLa(OC183B2 ��ԭ����)��������ϸ����1��105Ũ�Ƚ�����96���������С�����1 d���ݶȼ��뾭�������߶��س����ѽ����塣�Կ���������������SKOV3��Ϊ���ա�24��48 h��۲�ϸ����̬��48 h�����MTT��37���������4 h����������SDS��ֹ��Ӧ�����570 nm���ܶ�ֵ(D570nmֵ)������������ʽ����ɱ���ʡ�
, http://www.100md.com
ϸ��������%=(ʵ����D570nm-��ϸ��������D570nm)/(��ϸ������D570nm-��ϸ������D570nm)
2 ���
2.1 ��Ч���������ø�м���(ͼ2)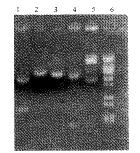
1, recombinants digested with NdeI,EcoRI; 2, recombinants digested with SpeI;
3, recombinants digested with Hind��; 4, recombinants digested with SacI;
, ��Ĵҽҩ 5, recombinants;6, molecular weight markers (��DNA/BstE��).
ͼ2 ��������pET30-ScFvPE38ø�в�����֬�ǵ�Ӿ���
Figure 2 Agarose electrophoresis of cloned vector pET30-ScFvPE38
digested with restriction enzymes.
��������pET30-ScFvPE38��Sac��ø�У���������Լ1 200 bp���Ҵ�С��Ƭ�Σ������ۼ���ֵ�����pET30-ScFv PE38 ��Nde��EcoR�� ø������СƬ�δ�С�����߶��ش�С����͡�Hind��Spe��ø�к�pET30-ScFvPE38�����ԡ�SpeIΪ��¡��������������λ�㡣Hind��ΪpET30a(+)�ϵ�ø��λ�㡣
, ��Ĵҽҩ
2.2 ����������߶��ص��ķ���(ͼ3)
1, molecular weight markers; 2, pET30a(+)/BL21(DE3),37�� 4 hours after induced with 0.4 mmol.L-1 IPTG;
3, pET30-ScFvPE38, 37�� 4 hours after induced with 0.4 mmol.L-1 IPTG;
4, sonicated supernatant; 5, inclusion body; 7,8, renatured fusion protein.
, ��Ĵҽҩ ͼ3 SDS-PAGE����pET30-ScFvPE38�ںϵ��ı���ʹ���
Figure 3 SDS-PAGE analysis of expression and purity
of pET30-ScFvPE38 fusion proteins
pET30-ScFvPE38 ת���˾�Bl21(DE3)��IPTG�յ������߶�����������ʽΪ����Ч��������ѽ�������������������ʽ���SDS-�۱�ϩ����������Ӿ�ɼ������弰ȫ������Է�������68 000����Ũ�������������ռȫ����30%���ϡ������ѽ�Һ�����У�����ڴ˴����������������������ܽ⸴�Ժ��ȴ�90%���ϡ�
2.3 ���ﵰ���ʵĻ��Լ��
(1) ֱ��ELISA�����490 nm���ܶ�ֵ: ���Զ��� 0.210�����Զ���1.191�����Ե��� 0.632�������ѽ�Һ���� 0.796������ֵ���������Զ���3�����ϡ��������á�(2) ϸ��ɱ�˽������������ͬ�����Ķ��ص��ף�SKOV3�����У�����24 h��ϸ�����⣬��̬��������������λ����ϸ���ۼ�������Һ��ϸ����Ƭ�ѻ�����ϸ������������48 h��ϸ����ȫ�������Ѽ�����ϸ����̬��HeLaϸ����̬����������pET30a(+)�������������ѽ������SKOV3������Ӱ�졣��1���˵�����߶��ض�SKOV3��������ɱ�����á�
, http://www.100md.com
��1 ���߶���183B2ScFvPE38��ɱ������(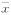 ��s)
��s)
Table 1 The cytotoxicity of immunotoxin 183B2ScFvPE38(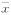 ��s) Immunotoxin
��s) Immunotoxin
volume
SKOV3
HeLa
D570nm
SR
, ��Ĵҽҩ
(%)��
D570nm
SR
(%)
5 ��l
0.359��0.257
54.5
0.954��0.090
102.0
8 ��l
0.242��0.037
36.8
, ��Ĵҽҩ
0.853��0.031
91.7
10 ��l
0.150��0.046
21.5
0.868��0.042
94.0
12 ��l
0.137��0.052
19.3
0.789��0.059
85.8
, ��Ĵҽҩ
15 ��l
0.051��0.019
3.5
0.904��0.008
89.3
Live cell
0.572��0.012
-
92.704��0.102
-
Dead cell
0.030��0.006
, ��Ĵҽҩ
-
0.081��0.040
-
*P<0.02 vs HeLa�� SR, survival rate.3 ����
���߶�����ָ�������붾�ص������ں϶�������һ�ִ���ӵ��ס����п��岿����Ҫ�����������ص�����п�ԭ�����Խ�ϣ����ز�������Ҫ��ʵʩ��ϸ����ɱ�����á����߶����ܹ�ѡ���Ե���Ա�����Ӧ��ԭ��ϸ��(������ϸ��)������ɱ������[4]��
��ʵ���������õļٵ����ⶾ��(PE)������ԭ��Ϊʹ���ϸ����������EF-2ʧ����°�ϸ���ĵ��ϳ�;�����裬�Ӷ�ʹϸ��������PE ����3���ṹ��(domain��D)���ɵ�[5]�� DI�� D�� D������DI �ַ�DIa��DIb��DIa���н��ϸ������������������PE���ϸ��Ĥ�������ϡ�DIb�����в������D����PE �Ŀ�Ĥ���䡣��D������к��ǻ�ת��ø���ԣ������EF-2��ADP-���ǻ�����
, ��Ĵҽҩ
��νP E 3 8���ǽ� P E�����б�������ʶ��ͽ�ϵ��Dz��ֻ���( Dla�Ͳ���Dlb)ɾ�������õ��Ļ����䵰�ײ���[6]����ȱʧ�˽������ P E�뿹�����������ÿ���������뿹ԭ�����Խ�ϵ��ص㽫���ص��������Ӧ��ԭ��ϸ���������������߶��ض�ϸ���������ԡ�
���⣬�����ѡ�����ϸ���������Ժ���������������Ҫ�����á�ѡ��һ�����˵Ŀ��������ѭһ��ԭ����������Ե�ϸ�����濹ԭ�ǰ�ϸ�����еĻ���������֯����Խ��١����ҹ����Ŀ��ѳ�����������183B2 ScFv Ϊ�ѳ���������[7]����������֯�����١���������������߶������Ƶ������ԡ�
��ʵ�������߶��صĿ��岿�ֲ��õ������壬���з���С������ǿ����Դ�Եͣ�������ǿ�����ڴ������������ܱ�����������������Ե��ŵ㡣���ң�����һЩ�����ڵ������Ƶ�ҩ������ѧ��������ϴ�����ڷֲ��ݻ�,�ϸߵ���֯�ڷֲ������ȡ�
, ��Ĵҽҩ
ʵ���У�����ԭ��ϸ�����\����ʹ���߶��صIJ����ﵽ30%���ϣ�������˸�Ч�����Ϊ���߶��صĴ����Ʊ������ڵ��ٴ�Ӧ�ô����˻�����
�ڿ�����Բⶨ�У����ڵ�������ȱ��Fc�Σ����Խ��Ѳⶨ����������������д����Ŀ�ԭ����HRP��ǣ�����ֱ��ELISA����������˽ϺõĽ����ELISA�����SDS-PAGE��Ӿ�����֤ʵpET30- ScFvPE38�����������Ա��ﲢ�������õĻ��ԡ�������ϸ������ʵ���У����Dz����˳����ѽ�Һ�������ɱ��ʵ�鲢��ʾ�˶�ϸ�������Ե�ɱ�����á����Ե��Ŀ��������õ���֤ʵ�����Ĺ��������ǽ���һ���������߶��ص��ף�������������Խ��и������̽�֡�
��֮�����dzɹ��ع����˿��ѳ����������߶��أ�������������ȷ���˱��ﵰ�Ļ��ԡ�Ϊ�ѳ������ߵ������Ƶ춨�˻�����
�����
1���� Ƽ���� �ݣ��� ��,��.�����ѳ�������¡����COC183-B2�����ɱ��������������������¡�����з���[J].����ҽ�ƴ�ѧѧ����1998��30��202-204
, http://www.100md.com
2��LoRusso PM, Lomen PL, Redman BG, et al. Phase I study of monoclonal antibody-ricin A chain immunoconjugate Xomazyme-791 in patients with metastatic colon cancer[J]. Am J Clin Oncol�� 1995 ,18(4):307-312
3��Kuan C, Pastan I. Recombinant immunotoxin Containing a Disulfide-Stabilized Fv Directed at erbB2 that does not require proteolytic activity[J]. Biochemistry,1996,36:2872-2877
4��Kuan C, Pastan I. Improved anti-tumor activity of a recombinant anti-Lewisy immunotoxin not requiring proteolytic activition[J]. Proc Natl Acad Sci USA, 1996 , 93:974-978
, http://www.100md.com
5��Allured VS, Collier RJ, Corroll SF, et al. Structure of exotoxin A of pseudomonas aeruginosa at 3.0-Angstrom resolution[J]. Proc Natl Acad Sci USA, 1986,83:1320-1324
6��Batra JK, Kasprizyk PG, Bird RE, et al. Recombinant anti-erbB2 immunotoxins containing pseudomonas exotoxin[J]. Proc Natl Acad Sci USA, 1992,89:5867-5871
7���� �ݣ�Ǯ���꣬�� �㣬��.���ֿ��ѳ���Ƥ������¡������Ʊ��������ܵ��о���Ƚ�[J].����ҽ�ƴ�ѧѧ����1989��21��11-13
(2000-04-20�ո�), http://www.100md.com
��λ��������ѧ����ҽԺ��������ʵ���ң����� 100044
�ؼ��ʣ����壻���������߶����ࣻҩ�����壻��л���ѳ������������ںϵ������ࣻ��л
����ҽ�ƴ�ѧѧ��000419 [ժ Ҫ] Ŀ�ģ��������ѳ�����������183B2ScFv ��ٵ����ⶾ��(peudononas exotoxin, PE38)���ںϵ��ױ������岢�Ʊ������ѳ����������߶��ص���183B2ScFvPE38��Ϊ�ѳ����������ƴ��»��������������û��̼���������3���ǿ�¡�������뵥������Ļ����붾�صĻ����ǿ�¡��ԭ�˱�������pET30a(+)�ϣ�����IPTG���յ��½��б������ֱ��ELISA��ϸ��ɱ�˶Կ��弰���ز��ֵĻ��Խ��м�顣��������ﵰ��183B2ScFvPE38���нϺõĿ�����Լ����ػ��ԡ����ۣ����ѳ����������߶���183B2ScFvPE38 �������õ�����ѧ���Լ�����ѧ���ԣ����������õ�Ӧ��ǰ����
, http://www.100md.com
[��ͼ�����] R966 [���ױ�ʶ��] A [���±��] 1000-1530(2000)04-0347-04
Vector construction and high level expression of single chain
immunotoxin against ovarian carcinoma
YOU Fang-Lei
(Department of Gynecologic Oncology, Peking University People's Hospital,Beijing 100044, China)
FENG Jie
(Department of Gynecologic Oncology, Peking University People's Hospital,Beijing 100044, China)
, ��Ĵҽҩ
CHEN Ye-Xia
(Department of Gynecologic Oncology, Peking University People's Hospital,Beijing 100044, China)
QIAN He-Nian
(Department of Gynecologic Oncology, Peking University People's Hospital,Beijing 100044, China)
ZHOU Ping
(Department of Gynecologic Oncology, Peking University People's Hospital,Beijing 100044, China)
, ��Ĵҽҩ
YE Xue
(Department of Gynecologic Oncology, Peking University People's Hospital,Beijing 100044, China)
ABSTRACT Objective:
To construct an expression vector for co_expression of single chain Fv antibody (OC183B2) and peudomonas exotoxin(PE38). Methods: Clone the genes of ScFv (OC183B2) and PE38 into PET30a(+) and then express the immunotoxin after induced with IPTG. Results: Liable activity of antibody and toxic in were both observed in the fusion recombinant protein. Conclusion: The recombinant fusion protein 183B2ScFvPE38 keeps the activity of both components and may be of great use in the future to deal with ovarian carcinoma.
, ��Ĵҽҩ
KEY WORDS Antibodies, neoplasm; Immunotoxins; Drug carriers/metab; Ovarian neoplasms; Recombinant fusion proteins/metab
(J Beijing Med Univ, 2000,32:347-350)
�����������ŷ�������ѧ������ѧ�����ķ�չ������������ѧ�����Ѿ���Ϊ���������ơ����ơ�����֮����Ҫ�����Ʒ�ʽ�����Ҷ�����һֱ�����Ե���¡����Ϊ���壬����ͬλ�ء�ҩ����ص���,���ѳ����������ߵ�����Ϻ����ߵ������Ƶ��о������ѳɹ��Ʊ���С���ӵ���[1]����99mTc����½����������ģ�ͷ�������������о����������������ͼ���ڴ˻����ϣ���ʵ������Ӧ�ñ����Ʊ��ĵ������幹�����߶��أ��о��ڿ��嵼���£�Я�����ص����ѳ������а������ƵĿ����ԡ�
, ��Ĵҽҩ
���߶����������������Ƶ�һ���·������ڹ��⣬�������߶����ѽ�����ڼ������ٴ�ʵ���о��Ρ�ʵ��֤ʵ���߶��ؾ������õ�Ӧ��ǰ��[2��3]�����ڹ����ѳ��������Ե���¡���幹�����߶��ص��о����������ټ�,����δ���йر�����
1 �����뷽��
1.1 ���幹�������߶��صĸ�Ч����
1.1.1 �����;��� pET16-183B2 ScFvΪ���ҹ����ĺ���183B2�����������(183B2ScFv)�������� PAGITΪ���ж��ػ���(peudononas exotoxin, PE38)����������Ч��������pET30a(+)������pUC18���˾�Bl21��DH5��Ϊ���ұ��档����PAGIT������GI724 Ϊ�й���ѧԺ�Ŵ��о����ƻ����������͡�
, ��Ĵҽҩ
1.1.2 ����������ø����ø ����Promega��˾��ϸ��ϵ���ѳ���ϸ��ϵSKOV3��������ϸ��ϵHeLa Ϊ���ұ��档
1.1.3 ���߶��ر�������Ĺ���(ͼ1) (1) pUC18-183B2ScFv�Ĺ����� pET16-183B2ScFv��Nde��EcoR�������������µ������壬������СƬ�Σ�pUC18����ͬλ��ø�У����մ�Ƭ�Ρ���T4 DNA ����ø�������½����������ǿ�¡��pUC18�У�����֮ΪpUC18-183B2ScFv��(2) pUC18-ScFvPE38�Ĺ�����������pUC18-183B2ScFv��Sac��EcoR�����������մ�Ƭ�Σ�����PE38��PAGIT������ͬλ�����£����ղ������ǿ�¡���ѻ��յĴ�Ƭ���С���ʱ��������������ΪpUC18-ScFvPE38��(3) pET30-ScFvPE38�Ĺ�����pUC18-ScFvPE38 Nde��EcoR��ø���º������߶��ص�Ƭ�Σ�������ͬλ���ǿ�¡��pET30a(+)�У���ɸ�Ч��������pET30-ScFvPE38�Ĺ��������Ը���������ø�м�����

, ��Ĵҽҩ
ͼ1 ���幹��ͼʾ
Figure 1 Construction route of the vectors
1.1.4 �����������յ�����������ѽ⼰������ ����������������Bl21�˾���37����1��100(�����)ת�Ӻ����������600 nm���ܶ�ԼΪ0.4ʱ����IPTG����Ũ��Ϊ0.4 mmol.L-1���յ�4 h���ռ����壬��������ϸ�������ķ�������壬����������Һ������Һ��PBS����ҹ�������徭����ϴ�Ӻ�8mol.L-1�����ܽ⣬���븴��Һ(�ɷ֣�50 mmol.L-1 Tris-HCl,5mmol.L-1 EDTA,1mmol.L-1 �����ȹ���ģ�5mmol.L-1 ��ԭ�ȹ����)ϡ���ԣ�10�渴��48h��PEG 20000Ũ����20mmol.L-1��Tris-Cl����ͬŨ�ȵ��������ݶ�����
, ��Ĵҽҩ
1.1.5 ������� SDS-�۱�ϩ����������Ӿ�������β��P�䴿�ȡ�
1.2 ���ﵰ���Լ��
1.2.1 ��Ҫ���� ���ѳ�������¡����COC183B2Ϊ�������Ʊ����廯����Sephorose4B����Parmacia��˾��������������ø���Ա���ͬ�����\����չ��˾��
1.2.2 �������Ŀ�ԭ����ȡ����� (1)��ˮ��ϸ�����OC183B2��ԭ���ԵIJ��˸�ˮ����������林������Σ�Ȼ������Ͳ�����ȡ��ԭ���Ͳ������ϲ����廯����Sephorose4B���������ƽ����ȫ����������ż��2 h��װ�������Ҵ�����գ����Ỻ��Һ�����Ỻ��Һ���������ϴ�Ӻ�����������3 mol.L-1�������ϴ�ѣ���������Ǽ�⡣(2) ø�꿹ԭ�Ʊ��������Ͳ������õ���Ũ���������pH 9.2��0.001 mol.L-1̼���λ���Һ��ƽ�ⱸ�á�������������ø��ȩ�����������������ԭ���±ܹ����2 h���ټ����������Ƶ�4g.L-1���������ƣ�4�� 2 h��������������ɱ�ǹ��̡�
, http://www.100md.com
1.2.3 ���߶��صĻ��Բⶨ (1)������� ��ֱ��ELISA����⡣���Ե�����10 mg.L-1��4������ҹ��HRP-��ԭOC183B2��⣻�����ѽ�Һ����(�����Ա���ɷ�)�ð���Һ�ݶ�ϡ�ͺ�4������ҹ����HRP-��ԭ��⡣ʵ����ÿ�����pET30a(+)ƽ���Ʊ�������Ϊ���Զ��ա���������COC183B2��Ϊ���Զ��ա�(2) ���ػ��Բ���ϸ����ʵ��(MTT��)��⡣��ϸ��Ϊ����OC183B2��ԭ���ѳ���ϸ��ϵSKOV3������ϸ������Ϊ������ϸ��ϵHeLa(OC183B2 ��ԭ����)��������ϸ����1��105Ũ�Ƚ�����96���������С�����1 d���ݶȼ��뾭�������߶��س����ѽ����塣�Կ���������������SKOV3��Ϊ���ա�24��48 h��۲�ϸ����̬��48 h�����MTT��37���������4 h����������SDS��ֹ��Ӧ�����570 nm���ܶ�ֵ(D570nmֵ)������������ʽ����ɱ���ʡ�
, http://www.100md.com
ϸ��������%=(ʵ����D570nm-��ϸ��������D570nm)/(��ϸ������D570nm-��ϸ������D570nm)
2 ���
2.1 ��Ч���������ø�м���(ͼ2)

1, recombinants digested with NdeI,EcoRI; 2, recombinants digested with SpeI;
3, recombinants digested with Hind��; 4, recombinants digested with SacI;
, ��Ĵҽҩ 5, recombinants;6, molecular weight markers (��DNA/BstE��).
ͼ2 ��������pET30-ScFvPE38ø�в�����֬�ǵ�Ӿ���
Figure 2 Agarose electrophoresis of cloned vector pET30-ScFvPE38
digested with restriction enzymes.
��������pET30-ScFvPE38��Sac��ø�У���������Լ1 200 bp���Ҵ�С��Ƭ�Σ������ۼ���ֵ�����pET30-ScFv PE38 ��Nde��EcoR�� ø������СƬ�δ�С�����߶��ش�С����͡�Hind��Spe��ø�к�pET30-ScFvPE38�����ԡ�SpeIΪ��¡��������������λ�㡣Hind��ΪpET30a(+)�ϵ�ø��λ�㡣
, ��Ĵҽҩ
2.2 ����������߶��ص��ķ���(ͼ3)

1, molecular weight markers; 2, pET30a(+)/BL21(DE3),37�� 4 hours after induced with 0.4 mmol.L-1 IPTG;
3, pET30-ScFvPE38, 37�� 4 hours after induced with 0.4 mmol.L-1 IPTG;
4, sonicated supernatant; 5, inclusion body; 7,8, renatured fusion protein.
, ��Ĵҽҩ ͼ3 SDS-PAGE����pET30-ScFvPE38�ںϵ��ı���ʹ���
Figure 3 SDS-PAGE analysis of expression and purity
of pET30-ScFvPE38 fusion proteins
pET30-ScFvPE38 ת���˾�Bl21(DE3)��IPTG�յ������߶�����������ʽΪ����Ч��������ѽ�������������������ʽ���SDS-�۱�ϩ����������Ӿ�ɼ������弰ȫ������Է�������68 000����Ũ�������������ռȫ����30%���ϡ������ѽ�Һ�����У�����ڴ˴����������������������ܽ⸴�Ժ��ȴ�90%���ϡ�
2.3 ���ﵰ���ʵĻ��Լ��
(1) ֱ��ELISA�����490 nm���ܶ�ֵ: ���Զ��� 0.210�����Զ���1.191�����Ե��� 0.632�������ѽ�Һ���� 0.796������ֵ���������Զ���3�����ϡ��������á�(2) ϸ��ɱ�˽������������ͬ�����Ķ��ص��ף�SKOV3�����У�����24 h��ϸ�����⣬��̬��������������λ����ϸ���ۼ�������Һ��ϸ����Ƭ�ѻ�����ϸ������������48 h��ϸ����ȫ�������Ѽ�����ϸ����̬��HeLaϸ����̬����������pET30a(+)�������������ѽ������SKOV3������Ӱ�졣��1���˵�����߶��ض�SKOV3��������ɱ�����á�
, http://www.100md.com
��1 ���߶���183B2ScFvPE38��ɱ������(
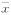 ��s)
��s)Table 1 The cytotoxicity of immunotoxin 183B2ScFvPE38(
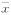 ��s) Immunotoxin
��s) Immunotoxinvolume
SKOV3
HeLa
D570nm
SR
, ��Ĵҽҩ
(%)��
D570nm
SR
(%)
5 ��l
0.359��0.257
54.5
0.954��0.090
102.0
8 ��l
0.242��0.037
36.8
, ��Ĵҽҩ
0.853��0.031
91.7
10 ��l
0.150��0.046
21.5
0.868��0.042
94.0
12 ��l
0.137��0.052
19.3
0.789��0.059
85.8
, ��Ĵҽҩ
15 ��l
0.051��0.019
3.5
0.904��0.008
89.3
Live cell
0.572��0.012
-
92.704��0.102
-
Dead cell
0.030��0.006
, ��Ĵҽҩ
-
0.081��0.040
-
*P<0.02 vs HeLa�� SR, survival rate.3 ����
���߶�����ָ�������붾�ص������ں϶�������һ�ִ���ӵ��ס����п��岿����Ҫ�����������ص�����п�ԭ�����Խ�ϣ����ز�������Ҫ��ʵʩ��ϸ����ɱ�����á����߶����ܹ�ѡ���Ե���Ա�����Ӧ��ԭ��ϸ��(������ϸ��)������ɱ������[4]��
��ʵ���������õļٵ����ⶾ��(PE)������ԭ��Ϊʹ���ϸ����������EF-2ʧ����°�ϸ���ĵ��ϳ�;�����裬�Ӷ�ʹϸ��������PE ����3���ṹ��(domain��D)���ɵ�[5]�� DI�� D�� D������DI �ַ�DIa��DIb��DIa���н��ϸ������������������PE���ϸ��Ĥ�������ϡ�DIb�����в������D����PE �Ŀ�Ĥ���䡣��D������к��ǻ�ת��ø���ԣ������EF-2��ADP-���ǻ�����
, ��Ĵҽҩ
��νP E 3 8���ǽ� P E�����б�������ʶ��ͽ�ϵ��Dz��ֻ���( Dla�Ͳ���Dlb)ɾ�������õ��Ļ����䵰�ײ���[6]����ȱʧ�˽������ P E�뿹�����������ÿ���������뿹ԭ�����Խ�ϵ��ص㽫���ص��������Ӧ��ԭ��ϸ���������������߶��ض�ϸ���������ԡ�
���⣬�����ѡ�����ϸ���������Ժ���������������Ҫ�����á�ѡ��һ�����˵Ŀ��������ѭһ��ԭ����������Ե�ϸ�����濹ԭ�ǰ�ϸ�����еĻ���������֯����Խ��١����ҹ����Ŀ��ѳ�����������183B2 ScFv Ϊ�ѳ���������[7]����������֯�����١���������������߶������Ƶ������ԡ�
��ʵ�������߶��صĿ��岿�ֲ��õ������壬���з���С������ǿ����Դ�Եͣ�������ǿ�����ڴ������������ܱ�����������������Ե��ŵ㡣���ң�����һЩ�����ڵ������Ƶ�ҩ������ѧ��������ϴ�����ڷֲ��ݻ�,�ϸߵ���֯�ڷֲ������ȡ�
, ��Ĵҽҩ
ʵ���У�����ԭ��ϸ�����\����ʹ���߶��صIJ����ﵽ30%���ϣ�������˸�Ч�����Ϊ���߶��صĴ����Ʊ������ڵ��ٴ�Ӧ�ô����˻�����
�ڿ�����Բⶨ�У����ڵ�������ȱ��Fc�Σ����Խ��Ѳⶨ����������������д����Ŀ�ԭ����HRP��ǣ�����ֱ��ELISA����������˽ϺõĽ����ELISA�����SDS-PAGE��Ӿ�����֤ʵpET30- ScFvPE38�����������Ա��ﲢ�������õĻ��ԡ�������ϸ������ʵ���У����Dz����˳����ѽ�Һ�������ɱ��ʵ�鲢��ʾ�˶�ϸ�������Ե�ɱ�����á����Ե��Ŀ��������õ���֤ʵ�����Ĺ��������ǽ���һ���������߶��ص��ף�������������Խ��и������̽�֡�
��֮�����dzɹ��ع����˿��ѳ����������߶��أ�������������ȷ���˱��ﵰ�Ļ��ԡ�Ϊ�ѳ������ߵ������Ƶ춨�˻�����
�����
1���� Ƽ���� �ݣ��� ��,��.�����ѳ�������¡����COC183-B2�����ɱ��������������������¡�����з���[J].����ҽ�ƴ�ѧѧ����1998��30��202-204
, http://www.100md.com
2��LoRusso PM, Lomen PL, Redman BG, et al. Phase I study of monoclonal antibody-ricin A chain immunoconjugate Xomazyme-791 in patients with metastatic colon cancer[J]. Am J Clin Oncol�� 1995 ,18(4):307-312
3��Kuan C, Pastan I. Recombinant immunotoxin Containing a Disulfide-Stabilized Fv Directed at erbB2 that does not require proteolytic activity[J]. Biochemistry,1996,36:2872-2877
4��Kuan C, Pastan I. Improved anti-tumor activity of a recombinant anti-Lewisy immunotoxin not requiring proteolytic activition[J]. Proc Natl Acad Sci USA, 1996 , 93:974-978
, http://www.100md.com
5��Allured VS, Collier RJ, Corroll SF, et al. Structure of exotoxin A of pseudomonas aeruginosa at 3.0-Angstrom resolution[J]. Proc Natl Acad Sci USA, 1986,83:1320-1324
6��Batra JK, Kasprizyk PG, Bird RE, et al. Recombinant anti-erbB2 immunotoxins containing pseudomonas exotoxin[J]. Proc Natl Acad Sci USA, 1992,89:5867-5871
7���� �ݣ�Ǯ���꣬�� �㣬��.���ֿ��ѳ���Ƥ������¡������Ʊ��������ܵ��о���Ƚ�[J].����ҽ�ƴ�ѧѧ����1989��21��11-13
(2000-04-20�ո�), http://www.100md.com