导数分光光度法测定注射用头孢哌酮钠和舒巴坦钠的含量
作者:姜 红 范艺腾*
单位:天津医科大学总医院 天津 300052
关键词:导数分光光度法;头孢哌酮钠;舒巴坦钠
华西药学杂志990540 提要 用导数分光光度法不经分离直接测定注射用头孢哌酮钠和舒巴坦钠的含量。用一阶导数分光光度法测定头孢哌酮钠的含量,平均回收率为99.31%,RSD为0.44%(n=6)。用二阶导数分光光度法测定舒巴坦钠的含量,平均回收率为100.05%,RSD为0.67%(n=6);方法简便快速,结果满意。
注射用头孢哌酮钠和舒巴坦钠(1∶1)是一种联合制剂,商品名舒普深,其中头孢哌酮钠为一抗G+菌和抗G-菌的广谱头孢菌素活性剂,舒巴坦钠为一强效β内酰胺酶抑制剂。两药联用,后者能增强前者的抗菌活性。舒普深的定量分析方法有高效液相色谱法,但需要特殊设备并且费用较高。现参照文献[1]建立了导数分光光度法测定头孢哌酮钠和舒巴坦钠的含量。
, 百拇医药
1 实验部分
1.1 仪器与试药
UV-260分光光度计(日本岛津);镀铬游标卡尺(江西工具厂,精密度0.02 mm)。头孢哌酮钠(92.4%)、舒巴坦钠(90.5%)、注射用头孢哌酮钠、舒巴坦钠均由中国大连辉瑞制药有限公司提供;蒸馏水(自制)。
1.2 条件的选择
1.2.1 贮备液的制备 精密称取经105℃干燥至恒重的头孢哌酮钠和舒巴坦钠适量,分别置250 ml量瓶中,水溶解并稀释至刻度,摇匀,使浓度分别为250 μg/ml的头孢哌酮钠和舒巴坦钠贮备液,置冰箱保存备用。
1.2.2 测定波长的选择 分别精密吸取上述贮备液各5 ml,置50 ml量瓶中,水溶解并稀释至刻度,摇匀。制备两种单一溶液和一种混合溶液。在200~300 nm波长范围内扫描,分别绘制导数吸收光谱(图1,2,3)。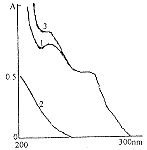
, 百拇医药
图1 零阶导数光谱图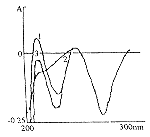
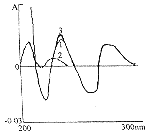
图2 一阶导数光谱图 图3 二阶导数光谱图
从图1看,头孢哌酮钠和舒巴坦钠在同一紫外区均有吸收,相互干扰;从图2看,头孢哌酮钠的一阶导数光谱在(279±1)nm有一谷吸收,此处舒巴坦钠无吸收,所以,(279±1)nm的零-谷导数半振幅值D可作为头孢哌酮钠的定量依据;从图3看,舒巴坦钠的二阶导数光谱在(234±1)nm有一最大吸收峰,此处头孢哌酮钠吸收为零,所以,(234±1)nm的峰-零导数半振幅值D可作为舒巴坦钠的定量依据。
1.2.3 测定信息选择 波长范围200~300 nm;波长标度为10 nm/cm;狭缝为2.0 nm;Δλ=4。
, http://www.100md.com
1.3 方法与结果
1.3.1 稳定性试验 分别配制适宜浓度的头孢哌酮钠和舒巴坦钠混合液3份,于室温下放置0、1、3、5 h,在200~300 nm波长范围内,分别绘制一阶、二阶导数吸收光谱,其振幅的位置和幅度在5 h内均无变化。
1.3.2 干扰试验 分别精密量取2、4、6、8 ml舒巴坦钠贮备液,置50 ml量瓶中,再精密加入5 ml头孢哌酮钠贮备液。另精密量取5 ml头孢哌酮钠贮备液,置50 ml量瓶中。上述均用水溶解并稀释至刻度,制备4份混合液和1份头孢哌酮钠溶液。在200~300 nm波长范围内,测定一阶导数光谱,在(279±1)nm量取半振幅D。结果5份D均为34.38 mm,说明不同浓度的舒巴坦钠对头孢哌酮钠的测定无干扰。4份混合液和1份舒巴坦钠溶液的制备同“4份混合液和1份头孢哌酮钠溶液”的制备。在200~300 nm波长范围内,测定二阶导数光谱,在(234±1)nm量取半振幅D。结果5份D均为13.52 mm。(234±1)nm是舒巴坦钠的定量波长,也是头孢哌酮钠的零交波长,说明不同浓度的头孢哌酮钠对舒巴坦钠的测定无干扰。
, http://www.100md.com
1.3.3 线性试验 分别精密称取经105℃干燥至恒重的头孢哌酮钠和舒巴坦钠适量,以水为溶媒稀释成浓度为5、10、20、30、40、50 μg/ml的溶液,在200~300 nm波长范围内,分别测定头孢哌酮钠一阶导数吸收光谱和舒巴坦钠二阶导数吸收光谱。在(279±1)nm和(234±1)nm量取头孢哌酮钠和舒巴坦钠的半振幅D。求得D对浓度C的回归方程:C头=0.6911D-0.6274 r=0.9999(n=3);C舒=2.2711D-2.8319 r=0.9999(n=3)。头孢哌酮钠和舒巴坦钠在5~50 μg/ml线性关系良好。
1.3.4 回收率试验 按处方配比,精密称取经105℃干燥至恒重的头孢哌酮钠和舒巴坦钠适量,置100 ml量瓶中,用水溶解并稀释至刻度,摇匀。精密吸取5 ml,置50 ml量瓶中,用水溶解并稀释至刻度,摇匀。在200~300 nm波长范围内,分别测定一阶、二阶导数吸收光谱,并量取(279±1)nm和(234±1)nm的半振幅D。分别代入以上两条标准曲线中,计算头孢哌酮钠和舒巴坦钠的测得量和回收率,结果见表1。
, 百拇医药
表1 回收率试验结果(n=6) No.
头孢哌酮钠
舒巴坦钠
投入量
(mg)
测得量
(mg)
回收率
(%)
投入量
(mg)
测得量
(mg)
, http://www.100md.com
回收率
(%)
1
25.30
25.13
99.33
25.10
24.85
99.00
2
25.20
25.17
99.88
, http://www.100md.com
24.70
24.92
100.89
3
24.60
24.53
99.71
26.00
26.08
100.31
4
24.80
24.55
, http://www.100md.com
98.99
25.30
25.33
100.12
5
26.10
25.76
98.70
24.80
24.91
100.44
6
26.30
, 百拇医药
26.10
99.24
26.10
25.99
99.58
99.31
100.05
RSD
0.44
0.67
1.3.5 供试品的测定 取本品5瓶,按中国药典1995年版二部附录5的方法,进行注射用无菌粉末的装量差异检查,求出平均装量。精密称取适量(约相当于头孢哌酮钠和舒巴坦钠25 mg),置100 ml量瓶中,按回收率试验项下同法操作。测定并计算头孢哌酮钠和舒巴坦钠的标示百分含量,结果见表2。表2 样品含量测定结果(n=5) 批号
, http://www.100md.com
平均装量
(g)
头孢哌酮钠
(%)
舒巴坦钠
(%)
75839006
1.1644
103.52
100.96
75839016
1.1617
102.61
, 百拇医药
102.57
75839027
1.1796
102.44
101.33
2 小结
本文采用一阶、二阶导数分光光度法,不经分离直接测定复方制剂中的头孢哌酮钠和舒巴坦钠的含量。该方法具有简便快速、准确可靠、稳定性和线性关系良好的特点,而且测定费用低廉,结果满意。适合本品的质量控制。
* 天津医科大学药学系1997届毕业生
参考文献
1 Chan CY, Chang K, French GL. Determination of cefoperazone and sulbactam in injections by high performance liquid chromatography. J Antimicrob Chemother, 1986, 18∶537
2 Alberto P, Javier GV, Vicente R, et al, First and second derivative spectrophotometric determination of cefoperazone and sulbactam in injections. J Pharm Biomed Anal, 1994, 12(5)∶653, 百拇医药(姜 红 范艺腾*)
单位:天津医科大学总医院 天津 300052
关键词:导数分光光度法;头孢哌酮钠;舒巴坦钠
华西药学杂志990540 提要 用导数分光光度法不经分离直接测定注射用头孢哌酮钠和舒巴坦钠的含量。用一阶导数分光光度法测定头孢哌酮钠的含量,平均回收率为99.31%,RSD为0.44%(n=6)。用二阶导数分光光度法测定舒巴坦钠的含量,平均回收率为100.05%,RSD为0.67%(n=6);方法简便快速,结果满意。
注射用头孢哌酮钠和舒巴坦钠(1∶1)是一种联合制剂,商品名舒普深,其中头孢哌酮钠为一抗G+菌和抗G-菌的广谱头孢菌素活性剂,舒巴坦钠为一强效β内酰胺酶抑制剂。两药联用,后者能增强前者的抗菌活性。舒普深的定量分析方法有高效液相色谱法,但需要特殊设备并且费用较高。现参照文献[1]建立了导数分光光度法测定头孢哌酮钠和舒巴坦钠的含量。
, 百拇医药
1 实验部分
1.1 仪器与试药
UV-260分光光度计(日本岛津);镀铬游标卡尺(江西工具厂,精密度0.02 mm)。头孢哌酮钠(92.4%)、舒巴坦钠(90.5%)、注射用头孢哌酮钠、舒巴坦钠均由中国大连辉瑞制药有限公司提供;蒸馏水(自制)。
1.2 条件的选择
1.2.1 贮备液的制备 精密称取经105℃干燥至恒重的头孢哌酮钠和舒巴坦钠适量,分别置250 ml量瓶中,水溶解并稀释至刻度,摇匀,使浓度分别为250 μg/ml的头孢哌酮钠和舒巴坦钠贮备液,置冰箱保存备用。
1.2.2 测定波长的选择 分别精密吸取上述贮备液各5 ml,置50 ml量瓶中,水溶解并稀释至刻度,摇匀。制备两种单一溶液和一种混合溶液。在200~300 nm波长范围内扫描,分别绘制导数吸收光谱(图1,2,3)。

, 百拇医药
图1 零阶导数光谱图


图2 一阶导数光谱图 图3 二阶导数光谱图
从图1看,头孢哌酮钠和舒巴坦钠在同一紫外区均有吸收,相互干扰;从图2看,头孢哌酮钠的一阶导数光谱在(279±1)nm有一谷吸收,此处舒巴坦钠无吸收,所以,(279±1)nm的零-谷导数半振幅值D可作为头孢哌酮钠的定量依据;从图3看,舒巴坦钠的二阶导数光谱在(234±1)nm有一最大吸收峰,此处头孢哌酮钠吸收为零,所以,(234±1)nm的峰-零导数半振幅值D可作为舒巴坦钠的定量依据。
1.2.3 测定信息选择 波长范围200~300 nm;波长标度为10 nm/cm;狭缝为2.0 nm;Δλ=4。
, http://www.100md.com
1.3 方法与结果
1.3.1 稳定性试验 分别配制适宜浓度的头孢哌酮钠和舒巴坦钠混合液3份,于室温下放置0、1、3、5 h,在200~300 nm波长范围内,分别绘制一阶、二阶导数吸收光谱,其振幅的位置和幅度在5 h内均无变化。
1.3.2 干扰试验 分别精密量取2、4、6、8 ml舒巴坦钠贮备液,置50 ml量瓶中,再精密加入5 ml头孢哌酮钠贮备液。另精密量取5 ml头孢哌酮钠贮备液,置50 ml量瓶中。上述均用水溶解并稀释至刻度,制备4份混合液和1份头孢哌酮钠溶液。在200~300 nm波长范围内,测定一阶导数光谱,在(279±1)nm量取半振幅D。结果5份D均为34.38 mm,说明不同浓度的舒巴坦钠对头孢哌酮钠的测定无干扰。4份混合液和1份舒巴坦钠溶液的制备同“4份混合液和1份头孢哌酮钠溶液”的制备。在200~300 nm波长范围内,测定二阶导数光谱,在(234±1)nm量取半振幅D。结果5份D均为13.52 mm。(234±1)nm是舒巴坦钠的定量波长,也是头孢哌酮钠的零交波长,说明不同浓度的头孢哌酮钠对舒巴坦钠的测定无干扰。
, http://www.100md.com
1.3.3 线性试验 分别精密称取经105℃干燥至恒重的头孢哌酮钠和舒巴坦钠适量,以水为溶媒稀释成浓度为5、10、20、30、40、50 μg/ml的溶液,在200~300 nm波长范围内,分别测定头孢哌酮钠一阶导数吸收光谱和舒巴坦钠二阶导数吸收光谱。在(279±1)nm和(234±1)nm量取头孢哌酮钠和舒巴坦钠的半振幅D。求得D对浓度C的回归方程:C头=0.6911D-0.6274 r=0.9999(n=3);C舒=2.2711D-2.8319 r=0.9999(n=3)。头孢哌酮钠和舒巴坦钠在5~50 μg/ml线性关系良好。
1.3.4 回收率试验 按处方配比,精密称取经105℃干燥至恒重的头孢哌酮钠和舒巴坦钠适量,置100 ml量瓶中,用水溶解并稀释至刻度,摇匀。精密吸取5 ml,置50 ml量瓶中,用水溶解并稀释至刻度,摇匀。在200~300 nm波长范围内,分别测定一阶、二阶导数吸收光谱,并量取(279±1)nm和(234±1)nm的半振幅D。分别代入以上两条标准曲线中,计算头孢哌酮钠和舒巴坦钠的测得量和回收率,结果见表1。
, 百拇医药
表1 回收率试验结果(n=6) No.
头孢哌酮钠
舒巴坦钠
投入量
(mg)
测得量
(mg)
回收率
(%)
投入量
(mg)
测得量
(mg)
, http://www.100md.com
回收率
(%)
1
25.30
25.13
99.33
25.10
24.85
99.00
2
25.20
25.17
99.88
, http://www.100md.com
24.70
24.92
100.89
3
24.60
24.53
99.71
26.00
26.08
100.31
4
24.80
24.55
, http://www.100md.com
98.99
25.30
25.33
100.12
5
26.10
25.76
98.70
24.80
24.91
100.44
6
26.30
, 百拇医药
26.10
99.24
26.10
25.99
99.58
99.31
100.05
RSD
0.44
0.67
1.3.5 供试品的测定 取本品5瓶,按中国药典1995年版二部附录5的方法,进行注射用无菌粉末的装量差异检查,求出平均装量。精密称取适量(约相当于头孢哌酮钠和舒巴坦钠25 mg),置100 ml量瓶中,按回收率试验项下同法操作。测定并计算头孢哌酮钠和舒巴坦钠的标示百分含量,结果见表2。表2 样品含量测定结果(n=5) 批号
, http://www.100md.com
平均装量
(g)
头孢哌酮钠
(%)
舒巴坦钠
(%)
75839006
1.1644
103.52
100.96
75839016
1.1617
102.61
, 百拇医药
102.57
75839027
1.1796
102.44
101.33
2 小结
本文采用一阶、二阶导数分光光度法,不经分离直接测定复方制剂中的头孢哌酮钠和舒巴坦钠的含量。该方法具有简便快速、准确可靠、稳定性和线性关系良好的特点,而且测定费用低廉,结果满意。适合本品的质量控制。
* 天津医科大学药学系1997届毕业生
参考文献
1 Chan CY, Chang K, French GL. Determination of cefoperazone and sulbactam in injections by high performance liquid chromatography. J Antimicrob Chemother, 1986, 18∶537
2 Alberto P, Javier GV, Vicente R, et al, First and second derivative spectrophotometric determination of cefoperazone and sulbactam in injections. J Pharm Biomed Anal, 1994, 12(5)∶653, 百拇医药(姜 红 范艺腾*)