A蛋白基因在枯草杆菌R25及地衣芽孢杆菌NM105中的表达
作者:张尤新 王桂忱 章银梅 汤懋盓
单位:中国科学院遗传研究所,北京100101
关键词:A蛋白基因;A蛋白;表达;枯草杆菌
中国免疫学杂志990407 中国图书分类号 R392.11
摘 要 目的:测定A蛋白基因在R25及NM105中的表达情况。方法:根据A蛋白基因产物——A蛋白能特异地与许多动物的免疫球蛋白的Fc段结合这一特性,采用ELISA检测法测定。结果:在细菌生长对数期,表达量与酶活性都在快速上升,在细菌生长平台期,表达量呈下降趋势。加中性蛋白酶抑制剂,使表达量提高了46%,低酶活性培养基的表达量是LB培养基的7.4倍,在碱性蛋白酶缺失的R25中的表达量是NM105的1.6倍。结论:A蛋白基因表达量与胞外蛋白酶活性关系极为密切。
Expression of protein A gene in R25 and NM105
, http://www.100md.com
ZHANG You-Xin,WANG Gui-Chen,ZHANG Yin-Mei et al.Institute of Genetics,Academia Sinica,Beijing 100101
Abstract Objective:Determined the expression condition of protein A in R25 and NM105.Methods:By ELISA and based on specific property that the protein A can be specifically combined with Fc fragment of immunoglobulin of many animals.Results:The protein A gene expression degree and protease activity both increased rapidly in logarithmic growth phase,and the protein A gene expression degree can raise 46% by adding neutral protease inhibitor.The quantative of protein A in the low enzyme activity medium was 7.4 fold of that in LB medium.And in R25,a alkaline protease deletion mutant,was 1.6 fold of that in NM105.Conclusion:The result of the expression condition of protein A gene in R25 and NM105 showed that the expression of protein A gene was connected with out-cell protease activity seriously.
, 百拇医药
Key words Protein A gene Protein A Expression Bacillus subtilis
基因工程的宿主系统大肠杆菌是现代分子生物学研究中最常用的材料之一。而枯草杆菌作为基因工程的另一个宿主具有许多优于大肠杆菌的特点。目前国际上用于基因工程宿主研究的枯草杆菌都来源于168菌株。枯草杆菌Ki-2由中国科学院遗传研究所汤懋盓等于1964年鉴定为可转化菌株,它与168株相比具有许多优点[1-3]。作为一个新建立的遗传工程系统,一系列研究工作都在进行之中。为了进一步检测该系统,同时也为了得到目前医学、免疫学及分子生物学广泛应用的外源基因表达产物——A蛋白,本实验开展了国内少报道的外源基因——A蛋白基因在Ki-2-132株R25中的表达,通过一系列实验结果的观察比较,对该系统在外源基因表达上的影响进行了初步探讨。
本实验表达的A蛋白是存在于某些金黄色葡萄球菌膜表面的一种蛋白质,在免疫学及分子生物学等方面有着广泛的应用价值[4-6],来源及产量有限。1984年Uhlen等利用重组DNA技术从金黄色葡萄球菌中克隆出A蛋白基因[7],以后又有人在大肠杆菌中实现了表达[8]。通过本实验的研究,经过不同条件的处理,得到不同产量的A蛋白。该遗传工程系统对外源基因表达的影响为今后的研究提供理论和技术上的积累。
, http://www.100md.com
1 材料与方法
1.1 菌株与质粒 枯草杆菌Ki-2-132株,来自中国科学院遗传所。携带A蛋白基因的质粒pRIT-5及大肠杆菌JM107由中科院生物物理所赠送。
1.2 质粒DNA提取[9] 基本上按Aandrew Mountain等的方法提取。
1.3 转化方法 pRIT-5通过细菌感受态转化至枯草杆菌R25菌株中[10],在10 μg/ml氯霉素的平皿上选择转化体,再通过原生质体转化至地衣芽孢杆菌NM105中[11]。因NM105菌无细胞感受态,所以必须经过原生质体转化,才能使质粒DNA进入菌体内。经氯霉素抗药性筛选,得到阳性转化体。
1.4 转化子的筛选鉴定 琼脂糖凝胶电泳和Cla I、Bcl I两种限制性内切酶消化反应按McDonel1等方法进行[12]。
, 百拇医药
1.5 A蛋白基因表达量与培养时间关系的观察 将鉴定后得到的携带pRIT-5质粒的阳性转化子、R25和NM105按相应时间进行培养,时间分别为2、4、6、8、12、16 h。每一管内为10 ml LB培养液[12],氯霉素为10 μg/ml,分别取相应菌株的一个单菌落加入试管中,37℃振荡培养,经饱和硫酸铵沉淀,得到培养液上清中的可溶性蛋白。
1.6 R25培养过程中中性蛋白酶抑制剂EDTA对表达量的影响 在培养高峰细菌达到对数后期时,加EDTA浓度至1 mmol/L,继续培养20 min,对照组不加,然后提取胞外可溶性蛋白。
1.7 应用低酶活性培养基与LB培养基分别培养的NM105表达量观察[11] 培养方法是接菌在低酶活性培养基普通CH/S培养基培养过夜,转接至无磷CH/S培养基中培养6 h,然后再经硫酸铵沉淀,透析得到胞外可溶性蛋白,留做ELISA检测。
, http://www.100md.com
1.8 ELISA测A蛋白基因的表达量及免疫活性 参见文献[13]。
1.9 胞外蛋白酶活性测定 参见文献[14]。
2 结果
2.1 携带外源基因——A蛋白基因的质粒的筛选与鉴定 携带A蛋白基因的质粒pRIT-5是一个大肠杆菌和枯草杆菌中的穿梭质粒,具有氨苄(Ap)抗性和氯霉素(Cm)抗性,但在不同的菌种中显示不同的抗性,在枯草杆菌及地衣芽孢杆菌中只显示Cm抗性。我们利用这一特性进行携带外源基因阳性转化子筛选,从得到的阳性转化子中提取质粒DNA,选择A蛋白基因上所带单酶切位点的Bcl I酶和双酶切位点的Cla I酶,进行酶切反应,与原大肠杆菌JM107中所提的质粒pRIT-5进行对照,经琼脂糖凝胶电泳,紫外灯下观察,酶切图谱一致证明质粒稳定,如图1所示。
, 百拇医药
图1 由JM107、R25和NM105分别提取质粒DNA酶切电泳图谱
Fig.1 The electrophoretic pattern of plasmid DNA digested by restrictive enzyme in JM107,R25 and NM105
Note:1.control zone of plasmid DNA;2~4.a line zone of plasmid DNA digested by restrictive enzyme (Bcl I) in JM107,R25 and NM105;5~7.two line zone plasmid DNA digested by restrictive enzyme (Cla I) in JM107,R25 and NM105
2.2 A蛋白基因表达量与培养时间关系曲线 将按不同时间培养得到的胞外可溶性蛋白经ELISA进行定性定量检测A蛋白,其关系如图2所示。
, http://www.100md.com
2.3 A蛋白基因表达量与胞外蛋白酶活性的关系 由于R25菌株是碱性蛋白酶缺失的突变菌株,所以在实验过程中观察A蛋白基因表达量与胞外蛋白酶的关系,还需限制中性蛋白酶的活性。实验组中加EDTA后培养得到的胞外可溶性蛋白与对照组经ELISA检测,其结果是,实验组使胞外蛋白酶活性降低50%,A蛋白表达量较对照组提高46%。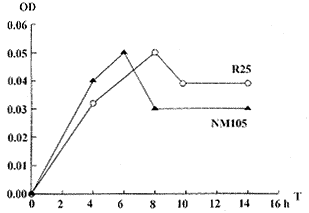
图2 A蛋白基因表达量与时间关系曲线
Fig.2 Curve of protein A gene expression amount relative to incubation time in R25 and NM105
2.4 不同培养基对A蛋白基因表达量的影响 应用低酶活性培养基与LB培养基对照培养,得到胞外可溶性蛋白,分别测胞外蛋白酶活性和胞外A蛋白含量。我们发现NM105在低酶活性培养基中A蛋白基因的表达量达到LB培养基表达量的7.4倍。
, http://www.100md.com
2.5 R25与NM105中A蛋白基因表达量对照(ELISA结果) 在不同菌种之间,我们测得Ki-2-132的突变菌株碱性蛋白酶缺失的R25 A蛋白基因的表达量是地衣芽孢杆菌NM105的1.6倍。
3 讨论
关于A蛋白基因的表达问题,Stephen等人所做的实验是通过在A蛋白基因上游序列整合上高效表达的强启动子,即枯草杆菌α-淀粉酶启动子,通过这一强启动子,实现高效表达[15]。另有实验则是在大肠杆菌中高效表达重组A蛋白。经SDS-PAGE及Western blotting结果显示pPA-3质粒在DH5α受体菌中,经热诱导后所表达的重组A蛋白约占菌体可溶性蛋白的20%,其分子量有4种,推测可能是由于重组A蛋白在菌体内被蛋白酶降解的缘故[8]。
本实验着重观察胞外蛋白酶对A蛋白基因表达的影响。我们发现A蛋白基因的表达量与胞外蛋白酶活性关系极为密切。首先在培养时间方面,细菌生长对数期时,菌体生长旺盛,所分泌的胞外蛋白酶及表达量也在快速上升;细菌生长平台期时,菌体生长数目饱和,酶活性趋于最高状态,而表达量反而呈下降趋势。此结果表明,当菌体数目饱和时,菌体分泌的胞外蛋白酶达峰值,而表达量也达最高值,三者趋于饱和状态。此时,胞外蛋白酶活性很高,而表达的A蛋白量不再增加,受到蛋白酶的降解作用反而减少。
, 百拇医药
本研究通过一系列的实验观察充分说明在外源基因表达上,胞外蛋白酶有着很大的影响。由此看来,在表达过程中确定最佳提取产物时间,采取抑制胞外蛋白酶活性的方法是非常必要的,而选择表达量高的宿主系统则是更关键的。
Ki-2-132这一遗传工程系统的研究有良好的前景,随着对这一系统遗传背景的深入了解及多侧面研究工作的深入,它将发展为很完备并优于168菌株的又一基因工程系统。
A蛋白基因在枯草杆菌R25及地衣芽孢杆菌NM105中的表达 国家自然科学基金资助项目(No.38970470)
张尤新 现在锦州医学院基础医学院生物化学教研室,锦州121001
章银梅 联系人
作者简介:张尤新,女,39岁,硕士生;
, http://www.100md.com
汤懋盓,男,60岁,研究员,硕士生导师,主要从事枯草杆菌系统研究
4 参考文献
[1] 汤懋盓,童克忠,陈 慎 et al.枯草杆菌转化的研究.微生物学报,1964;10(2):105
[2] 汤懋盓,魏荣宣,杨月琴 et al.pUBllo 质粒转化枯草杆菌Ki-2株及其突变体的研究.遗传学报,1981;8(1):8
[3] 范树田,杨 迪,孙永华 et al.一个拷贝数增加的枯草杆菌重组质粒.科学通报,1984;17(1):1070
[4] Forsgren A,Sjoquist J.\!Protein A "from S. aureus.I pseudoimmune reaction with human gamma-globuin.J Immunol,1966;97(6):822
, 百拇医药
[5] Bansal S C,Bansal B R,Thomas H L et al.Ex vivo removal of serum IgG in a patient with colon carcinoma,some biochemical,immunological and histological observations.Cancer,1978;42(1):1
[6] Nilsson B,Abrahmsen L,Uhlen M.Immobilization and purification of enzymes with staphylococcal protein A gene fusion vectors.EMBO J,1985;4(4):1075
[7] Uhlen M,Guss B,Nilsson B et al.Complete sequence of the staphylococcal gene encoding protein A,a gene evolved through multiple duplications.J Biol Chem,1984;259(3):1695
, 百拇医药
[8] 蔡仕英,刘亚霞,强伯勤 et al.在大肠杆菌中高效表达重组Protein A.生物工程学报,1992;8(2):123
[9] Sambrook J,Fritsch E F,Maniatis T.Extraction and purification of plasmid DNA.Molecular Cloning,1987;8(1):121
[10] Hybridigation lsonthern.Transformation of bacillus subtilis.G M I Chen,1975;248(1):6163
[11] Chang S,Cohen S N.High frequency transformation of bacillus subtilis protoplasts by plasmid DNA.Moi Gen Genet,1979;168(1):111
, 百拇医药
[12] 萨姆布鲁克 J,弗里奇 E F,曼尼阿蒂斯 T et al.分子克隆实验指南.第2版.北京:科学技术出版社,1992:316,908
[13] 李成文.现代免疫化学技术.上海:上海科学技术出版社,1992:117-120
[14] Markl S,Eugenio F.Replacement of the B.S subtilis in structural gene with an in vitro derived deletion mutation.J Bact,1984;158:411
[15] Stephen R,Fahnestock,Kathryn E et al.Expression of the staphylococcal protein A gene in bacillus subtilis by gene fusions utilizing the promoter from a bacillus amyloliquefaciens α anaylase gene.Bacteri,1986;12(1):796
〔收稿1997-05-26 二次修回1998-07-01〕, 百拇医药
单位:中国科学院遗传研究所,北京100101
关键词:A蛋白基因;A蛋白;表达;枯草杆菌
中国免疫学杂志990407 中国图书分类号 R392.11
摘 要 目的:测定A蛋白基因在R25及NM105中的表达情况。方法:根据A蛋白基因产物——A蛋白能特异地与许多动物的免疫球蛋白的Fc段结合这一特性,采用ELISA检测法测定。结果:在细菌生长对数期,表达量与酶活性都在快速上升,在细菌生长平台期,表达量呈下降趋势。加中性蛋白酶抑制剂,使表达量提高了46%,低酶活性培养基的表达量是LB培养基的7.4倍,在碱性蛋白酶缺失的R25中的表达量是NM105的1.6倍。结论:A蛋白基因表达量与胞外蛋白酶活性关系极为密切。
Expression of protein A gene in R25 and NM105
, http://www.100md.com
ZHANG You-Xin,WANG Gui-Chen,ZHANG Yin-Mei et al.Institute of Genetics,Academia Sinica,Beijing 100101
Abstract Objective:Determined the expression condition of protein A in R25 and NM105.Methods:By ELISA and based on specific property that the protein A can be specifically combined with Fc fragment of immunoglobulin of many animals.Results:The protein A gene expression degree and protease activity both increased rapidly in logarithmic growth phase,and the protein A gene expression degree can raise 46% by adding neutral protease inhibitor.The quantative of protein A in the low enzyme activity medium was 7.4 fold of that in LB medium.And in R25,a alkaline protease deletion mutant,was 1.6 fold of that in NM105.Conclusion:The result of the expression condition of protein A gene in R25 and NM105 showed that the expression of protein A gene was connected with out-cell protease activity seriously.
, 百拇医药
Key words Protein A gene Protein A Expression Bacillus subtilis
基因工程的宿主系统大肠杆菌是现代分子生物学研究中最常用的材料之一。而枯草杆菌作为基因工程的另一个宿主具有许多优于大肠杆菌的特点。目前国际上用于基因工程宿主研究的枯草杆菌都来源于168菌株。枯草杆菌Ki-2由中国科学院遗传研究所汤懋盓等于1964年鉴定为可转化菌株,它与168株相比具有许多优点[1-3]。作为一个新建立的遗传工程系统,一系列研究工作都在进行之中。为了进一步检测该系统,同时也为了得到目前医学、免疫学及分子生物学广泛应用的外源基因表达产物——A蛋白,本实验开展了国内少报道的外源基因——A蛋白基因在Ki-2-132株R25中的表达,通过一系列实验结果的观察比较,对该系统在外源基因表达上的影响进行了初步探讨。
本实验表达的A蛋白是存在于某些金黄色葡萄球菌膜表面的一种蛋白质,在免疫学及分子生物学等方面有着广泛的应用价值[4-6],来源及产量有限。1984年Uhlen等利用重组DNA技术从金黄色葡萄球菌中克隆出A蛋白基因[7],以后又有人在大肠杆菌中实现了表达[8]。通过本实验的研究,经过不同条件的处理,得到不同产量的A蛋白。该遗传工程系统对外源基因表达的影响为今后的研究提供理论和技术上的积累。
, http://www.100md.com
1 材料与方法
1.1 菌株与质粒 枯草杆菌Ki-2-132株,来自中国科学院遗传所。携带A蛋白基因的质粒pRIT-5及大肠杆菌JM107由中科院生物物理所赠送。
1.2 质粒DNA提取[9] 基本上按Aandrew Mountain等的方法提取。
1.3 转化方法 pRIT-5通过细菌感受态转化至枯草杆菌R25菌株中[10],在10 μg/ml氯霉素的平皿上选择转化体,再通过原生质体转化至地衣芽孢杆菌NM105中[11]。因NM105菌无细胞感受态,所以必须经过原生质体转化,才能使质粒DNA进入菌体内。经氯霉素抗药性筛选,得到阳性转化体。
1.4 转化子的筛选鉴定 琼脂糖凝胶电泳和Cla I、Bcl I两种限制性内切酶消化反应按McDonel1等方法进行[12]。
, 百拇医药
1.5 A蛋白基因表达量与培养时间关系的观察 将鉴定后得到的携带pRIT-5质粒的阳性转化子、R25和NM105按相应时间进行培养,时间分别为2、4、6、8、12、16 h。每一管内为10 ml LB培养液[12],氯霉素为10 μg/ml,分别取相应菌株的一个单菌落加入试管中,37℃振荡培养,经饱和硫酸铵沉淀,得到培养液上清中的可溶性蛋白。
1.6 R25培养过程中中性蛋白酶抑制剂EDTA对表达量的影响 在培养高峰细菌达到对数后期时,加EDTA浓度至1 mmol/L,继续培养20 min,对照组不加,然后提取胞外可溶性蛋白。
1.7 应用低酶活性培养基与LB培养基分别培养的NM105表达量观察[11] 培养方法是接菌在低酶活性培养基普通CH/S培养基培养过夜,转接至无磷CH/S培养基中培养6 h,然后再经硫酸铵沉淀,透析得到胞外可溶性蛋白,留做ELISA检测。
, http://www.100md.com
1.8 ELISA测A蛋白基因的表达量及免疫活性 参见文献[13]。
1.9 胞外蛋白酶活性测定 参见文献[14]。
2 结果
2.1 携带外源基因——A蛋白基因的质粒的筛选与鉴定 携带A蛋白基因的质粒pRIT-5是一个大肠杆菌和枯草杆菌中的穿梭质粒,具有氨苄(Ap)抗性和氯霉素(Cm)抗性,但在不同的菌种中显示不同的抗性,在枯草杆菌及地衣芽孢杆菌中只显示Cm抗性。我们利用这一特性进行携带外源基因阳性转化子筛选,从得到的阳性转化子中提取质粒DNA,选择A蛋白基因上所带单酶切位点的Bcl I酶和双酶切位点的Cla I酶,进行酶切反应,与原大肠杆菌JM107中所提的质粒pRIT-5进行对照,经琼脂糖凝胶电泳,紫外灯下观察,酶切图谱一致证明质粒稳定,如图1所示。

, 百拇医药
图1 由JM107、R25和NM105分别提取质粒DNA酶切电泳图谱
Fig.1 The electrophoretic pattern of plasmid DNA digested by restrictive enzyme in JM107,R25 and NM105
Note:1.control zone of plasmid DNA;2~4.a line zone of plasmid DNA digested by restrictive enzyme (Bcl I) in JM107,R25 and NM105;5~7.two line zone plasmid DNA digested by restrictive enzyme (Cla I) in JM107,R25 and NM105
2.2 A蛋白基因表达量与培养时间关系曲线 将按不同时间培养得到的胞外可溶性蛋白经ELISA进行定性定量检测A蛋白,其关系如图2所示。
, http://www.100md.com
2.3 A蛋白基因表达量与胞外蛋白酶活性的关系 由于R25菌株是碱性蛋白酶缺失的突变菌株,所以在实验过程中观察A蛋白基因表达量与胞外蛋白酶的关系,还需限制中性蛋白酶的活性。实验组中加EDTA后培养得到的胞外可溶性蛋白与对照组经ELISA检测,其结果是,实验组使胞外蛋白酶活性降低50%,A蛋白表达量较对照组提高46%。

图2 A蛋白基因表达量与时间关系曲线
Fig.2 Curve of protein A gene expression amount relative to incubation time in R25 and NM105
2.4 不同培养基对A蛋白基因表达量的影响 应用低酶活性培养基与LB培养基对照培养,得到胞外可溶性蛋白,分别测胞外蛋白酶活性和胞外A蛋白含量。我们发现NM105在低酶活性培养基中A蛋白基因的表达量达到LB培养基表达量的7.4倍。
, http://www.100md.com
2.5 R25与NM105中A蛋白基因表达量对照(ELISA结果) 在不同菌种之间,我们测得Ki-2-132的突变菌株碱性蛋白酶缺失的R25 A蛋白基因的表达量是地衣芽孢杆菌NM105的1.6倍。
3 讨论
关于A蛋白基因的表达问题,Stephen等人所做的实验是通过在A蛋白基因上游序列整合上高效表达的强启动子,即枯草杆菌α-淀粉酶启动子,通过这一强启动子,实现高效表达[15]。另有实验则是在大肠杆菌中高效表达重组A蛋白。经SDS-PAGE及Western blotting结果显示pPA-3质粒在DH5α受体菌中,经热诱导后所表达的重组A蛋白约占菌体可溶性蛋白的20%,其分子量有4种,推测可能是由于重组A蛋白在菌体内被蛋白酶降解的缘故[8]。
本实验着重观察胞外蛋白酶对A蛋白基因表达的影响。我们发现A蛋白基因的表达量与胞外蛋白酶活性关系极为密切。首先在培养时间方面,细菌生长对数期时,菌体生长旺盛,所分泌的胞外蛋白酶及表达量也在快速上升;细菌生长平台期时,菌体生长数目饱和,酶活性趋于最高状态,而表达量反而呈下降趋势。此结果表明,当菌体数目饱和时,菌体分泌的胞外蛋白酶达峰值,而表达量也达最高值,三者趋于饱和状态。此时,胞外蛋白酶活性很高,而表达的A蛋白量不再增加,受到蛋白酶的降解作用反而减少。
, 百拇医药
本研究通过一系列的实验观察充分说明在外源基因表达上,胞外蛋白酶有着很大的影响。由此看来,在表达过程中确定最佳提取产物时间,采取抑制胞外蛋白酶活性的方法是非常必要的,而选择表达量高的宿主系统则是更关键的。
Ki-2-132这一遗传工程系统的研究有良好的前景,随着对这一系统遗传背景的深入了解及多侧面研究工作的深入,它将发展为很完备并优于168菌株的又一基因工程系统。
A蛋白基因在枯草杆菌R25及地衣芽孢杆菌NM105中的表达 国家自然科学基金资助项目(No.38970470)
张尤新 现在锦州医学院基础医学院生物化学教研室,锦州121001
章银梅 联系人
作者简介:张尤新,女,39岁,硕士生;
, http://www.100md.com
汤懋盓,男,60岁,研究员,硕士生导师,主要从事枯草杆菌系统研究
4 参考文献
[1] 汤懋盓,童克忠,陈 慎 et al.枯草杆菌转化的研究.微生物学报,1964;10(2):105
[2] 汤懋盓,魏荣宣,杨月琴 et al.pUBllo 质粒转化枯草杆菌Ki-2株及其突变体的研究.遗传学报,1981;8(1):8
[3] 范树田,杨 迪,孙永华 et al.一个拷贝数增加的枯草杆菌重组质粒.科学通报,1984;17(1):1070
[4] Forsgren A,Sjoquist J.\!Protein A "from S. aureus.I pseudoimmune reaction with human gamma-globuin.J Immunol,1966;97(6):822
, 百拇医药
[5] Bansal S C,Bansal B R,Thomas H L et al.Ex vivo removal of serum IgG in a patient with colon carcinoma,some biochemical,immunological and histological observations.Cancer,1978;42(1):1
[6] Nilsson B,Abrahmsen L,Uhlen M.Immobilization and purification of enzymes with staphylococcal protein A gene fusion vectors.EMBO J,1985;4(4):1075
[7] Uhlen M,Guss B,Nilsson B et al.Complete sequence of the staphylococcal gene encoding protein A,a gene evolved through multiple duplications.J Biol Chem,1984;259(3):1695
, 百拇医药
[8] 蔡仕英,刘亚霞,强伯勤 et al.在大肠杆菌中高效表达重组Protein A.生物工程学报,1992;8(2):123
[9] Sambrook J,Fritsch E F,Maniatis T.Extraction and purification of plasmid DNA.Molecular Cloning,1987;8(1):121
[10] Hybridigation lsonthern.Transformation of bacillus subtilis.G M I Chen,1975;248(1):6163
[11] Chang S,Cohen S N.High frequency transformation of bacillus subtilis protoplasts by plasmid DNA.Moi Gen Genet,1979;168(1):111
, 百拇医药
[12] 萨姆布鲁克 J,弗里奇 E F,曼尼阿蒂斯 T et al.分子克隆实验指南.第2版.北京:科学技术出版社,1992:316,908
[13] 李成文.现代免疫化学技术.上海:上海科学技术出版社,1992:117-120
[14] Markl S,Eugenio F.Replacement of the B.S subtilis in structural gene with an in vitro derived deletion mutation.J Bact,1984;158:411
[15] Stephen R,Fahnestock,Kathryn E et al.Expression of the staphylococcal protein A gene in bacillus subtilis by gene fusions utilizing the promoter from a bacillus amyloliquefaciens α anaylase gene.Bacteri,1986;12(1):796
〔收稿1997-05-26 二次修回1998-07-01〕, 百拇医药