流式细胞术三色分析循环活化血小板及其在缺血性脑血管病中的临床意义
作者:王建中 曹凌 贺茂林 袁家颖
单位:100034 北京医科大学第一医院检验科
关键词:流式细胞术;血小板活化;纤维蛋白原受体;P-选择素;缺血性脑血管病
中华医学杂志000705【摘要】目的 探讨流式细胞术(FCM)三色分析血液中循环活化血小板(CAP)在缺血性脑血管病中的临床意义。方法 以纤维蛋白原受体(FIB-R)、P-选择素(CD62P)作为分子标志物,FCM三色免疫荧光分析CAP。结果 正常人静止血小板膜表面FIB-R和CD62P表达极低(阳性百分率的中位数分别为1.4%和0.7%)。0.1 μmol/L ADP可使血小板明显活化,10 μmol/L ADP使活化血小板膜表面FIB-R和CD62P表达至峰值,阳性百分率分别为87.8%和81.3%。合成肽(RGDS)可抑制抗FIB-R的单克隆抗体与ADP活化血小板结合。112例有血栓形成倾向疾病和120例缺血性脑血管病患者血液中表达FIB-R的CAP数量与正常人比较差异有显著意义(P<0.01),但表达CD62P的CAP数量增高不明显(P>0.05)。急性脑梗死患者治疗前后CAP的FIB-R表达呈连续下降趋势(P<0.05),而且CAP的FIB-R表达量与患者的ESS(欧洲脑卒中评分)呈负相关。结论 FIB-R可作为CAP检测的灵敏、特异的分子标志物,流式细胞术三色分析CAP能准确地反映体内血小板的活化水平,对缺血性脑血管病的发病机理研究、预后判断、疗效监测等有重要的临床意义。
, 百拇医药
Flow cytometric 3-color analysis of circulating activated platelets and its clinical significance in ischemic cerebrovascular diseases
WANG Jianzhong CAO Ling HE Maolin et al.
(The First Hospital, Beijing Medical University, Beijing 100034, China)
【Abstract】Objective To explore the flow cytometric 3-color analysis of circulating activated platelets (CAP) and its clinical significance in ischemic cerebrovascular diseases. Methods The fibrinogen receptor (FIB-R) and P-selectin (CD62P) were used for molecular marker of CAP, which were analyzed by flow cytometric 3-color immunofluorescence. Results Expression of FIB-R and CD62P on the resting platelet membrane surface was very lower in normal individuals, the median of FIB-R and CD62P positive percent was 1.40% and 0.70% respectively. Platelet can be obviously activated by 0.1 μmol/L ADP, and 10.0 μmol/L ADP leaded to the peak expression of FIB-R and CD62P on the activated platelet membrane surface, FIB-R and CD62P positive percent of 87.8% and 81.34% respectively. That monoclonal antibody of the FIB-R combined with ADP activating platelets was inhibited by synthetic peptide (RGDS). The quantity of CAP with FIB-R expression was markedly higher (P<0.01) and the amount of CAP with CD62P expression was not significantly higher (P>0.05) in blood of 112 patients with thrombotic tendency and 120 patients with ischemic cerebrovascular diseases than in healthy individuals. The expression of CAP with FIB-R of in front and behind treatment of acute cerebral infarction continuously decreased (P<0.05), and the quantity of CAP with FIB-R expression was related negatively to Europe stroke score (ESS) of patients with acute cerebral infarction. Conclusion The FIB-R may be regarded as sensitive and specific molecular marker in detection of CAP. The level of platelet activation in vivo can be reflected accurately by flow cytometric 3-color analysis of CAP, which has an important clinical significance for the study of pathogenesis, estimation of prognosis and supervision of curative effect in ischemic cerebrovascular diseases.
, 百拇医药
【Key words】Flow cytometry; Activated platelet;Fibrinogen receptor;P-selectin;Ischemic cerebrovascular diseases
血液中循环活化血小板(CAP)增高可作为动脉血管病,如缺血性中风、心肌梗死、周围血管病等疾病有局部血栓形成的标志物[1],CAP测定可能有助于中风等疾病的预后判断和治疗[2],然而由于CAP测定方法不同,常导致其检查结果有争议[3]。我们选择了血小板膜表面纤维蛋白原受体(FIB-R)、P-选择素(CD62P)作为CAP的分子标志物,用流式细胞术(FCM)三色免疫荧光标记法,测定了112例有血栓形成倾向疾病和120例缺血性脑血管病患者以及35例正常人血液中CAP数量变化,以探讨其在缺血性脑血管病中的临床意义。
对象与方法
, 百拇医药
一、对象
1.有血栓形成倾向疾病患者组112例:高脂蛋白血症27例,男13例、女14例,平均年龄62岁±11.5岁。糖尿病25例,男19例、女6例,平均年龄63岁±7.2岁。高血压病31例,男22例、女9例,平均年龄64岁±7岁。脑动脉硬化29例,男23例、女6例,平均年龄66岁±5.9岁。
2.缺血性脑血管病患者组120例:短暂性脑缺血发作(TIA)发病半年内患者25例,男17例、女8例,平均年龄66岁±8.8岁。发病3个月以上脑梗死(慢性期)患者26例,男19例、女7例,平均年龄65岁±6.6岁。急性期(发病2 d内)腔隙性脑梗死(腔梗)患者17例,男13例,女4例,平均年龄62岁±9岁。发病2 d内脑梗死(急性期皮质性脑梗死)患者52例,男34例、女18例,平均年龄63岁±10岁,患者病情轻重按欧洲脑卒中评分(ESS)标准进行评分,根据患者病情进行常规治疗(用低分子右旋糖苷、维脑路通、醒脑静等常规药物治疗)和溶栓治疗(发病6 h内,150万单位尿激酶溶栓)。以上患者均经临床、脑CT等检查,由神经内科专科医师确诊。
, 百拇医药
3.正常对照组35例:经体检正常,无心脑血管病的健康志愿者,男20例,女15例,平均年龄63岁±9.7岁。
4.主要试剂:(1)荧光色素标记单克隆抗体(McAb):PAC-1 FITC为异硫氰酸荧光素标记的抗血小板活化GPIIb-IIIa,即纤维蛋白原受体(FIB-R)的McAb。CD62P PE为藻红蛋白标记的抗P-选择素的McAb。CD61 PerCP为Peridinin chlorophyll protein(PerCP)标记的血小板糖蛋白IIIa的McAb。MIgG 为藻红蛋白标记的鼠IgG。以上均为美国Becton-Dickinson公司产品;(2)人工合成的精氨酰-甘氨酰-天冬氨酰-丝氨酰多肽(RGDS)为美国Sigma 公司产品;(3)二磷酸腺苷(ADP),Boehringer Mannheim公司产品;(4)多聚甲醛(PFA),美国E.Marke产品;(5)流式细胞仪三色校准微球(CaliBRITETM3 Kit),美国Becton-Dickinson公司产品。
, 百拇医药
5.主要仪器:(1)FACSort型流式细胞仪,美国Becton-Dickinson公司产品;(2)CA570全自动血细胞分析仪,瑞典MEDONIC公司产品;(3)LBY-NJ2四通道血小板聚集仪,中国普利生公司产品;(4)ACL Futura全自动凝血分析仪,美国Laboratory Instrument公司产品。
二、方法
1.样本采集:各组患者及正常人均静脉采血,经106 mmol/L枸橼酸钠抗凝,急性脑梗塞患者于治疗前、治疗后1 d、7 d采血3次。其它患者及正常人于清晨、空腹采血,且应停用抗血小板、抗凝血药7~10 d以上,采血1次。
2.流式细胞术三色分析活化血小板:(1)样本制备:分别取PAC-1 FITC、CD62P PE 、CD61 PerCP 各10 μl加入一塑料试管中混匀作为测定管;另取PAC-FITC、MIgG PE、CD61 PerCP、RGDS(5 mg/ml)各10 μl加入一塑料试管中混匀作为对照管,两管中分别加入10 min前采集的静脉抗凝血5 μl与试剂轻轻混匀、室温条件下避光作用20 min,立即加入预冷2~8℃的1%多聚甲醛1 ml并混匀,置2~8℃冰箱内2 h后、24 h内在流式细胞仪上进行测定;(2)流式细胞仪检测和数据分析:用荧光微球校准流式细胞仪后,在CellQuest软件环境中,将流式细胞仪的前向角散射(FSC)、侧向角散射(SSC)、三色荧光(FL1~FL3)的检测信号均设置为对数放大,以CD61 PerCP/SSC双参数设门,分别检测对照管和测定管中单个血小板的光散射及三色荧光强度,并分析FIB-R(PAC-1)和CD62P阳性CAP的百分率及平均荧光强度(MFI),以测定管与对照管MFI的比值(RMFI)代表血小板表达活化分子标志物的相对含量。
, 百拇医药
3.其它检查指标:(1)血小板计数(PLT)和血小板平均体积(MPV)测定,用抗凝全血在CA570血细胞分析仪上测定;(2)血小板聚集率(PAR),用ADP(3 μmol/L终浓度)作诱导剂,在血小板聚集仪上测定最大血小板聚集率(PAR);(3)血浆纤维蛋白含量(FIB)测定,在ACL Futura全自动凝血仪上以光学法测定FIB含量。
4.数据统计:实验结果以中位数(全距)或算术平均数±标准差( ±s)表示,多组间资料分析用方差分析或秩和检验,相关性用线性回归分析,各项统计均用SPSS统计软件在计算机上完成。
±s)表示,多组间资料分析用方差分析或秩和检验,相关性用线性回归分析,各项统计均用SPSS统计软件在计算机上完成。
结果
1.ADP活化血小板膜糖蛋白变化:用不同浓度ADP(0、0.1、0.2、0.5、1.0、2.0、5.0、10.0、20.0 μmol/L)加入正常人抗凝血液中、37℃激活5 min后在流式细胞仪上测定血小板膜表面FIB-R和CD62P阳性血小板百分率和平均荧光强度(MFI)见图1。在上述浓度ADP激活的血液标本测定管中分别加入10μl RGDS 后再测定血小板膜表面FIB-R和CD62P阳性血小板百分率和MFI,可见RGDS可竞争性抑制McAb PAC-1与FIB-R的结合(见图2)。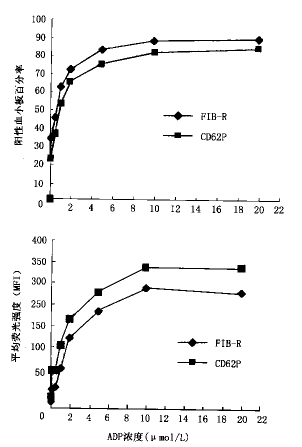
, 百拇医药
图1 不同浓度ADP激活的血小板表面膜FIB-R和
CD62P表达的动态变化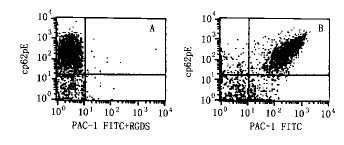
图2 RGDS对ADP(10.0 μmol/L)激活血小板FIB-R和CD62P表达的影响,FCM分析荧光点图:A―加RGDS,B―未加RGDS
2.各组人群各项结果比较:正常人群的PLT、MPV、PAR测定结果分别为(153±53)×109/L、8.7 fl±0.5 fl、57.9%±10.3%,PLT、MPV、PAR 3项结果与有血栓形成倾向疾病和缺血性脑血管病患者(治疗前)2组人群差异无显著意义(P>0.05)。FIB测定除腔隙性脑梗死(3.6 g/L±1.3 g/L)和急性脑梗死(3.7 g/L±0.7 g/L )患者组比正常对照组(3.1 g/L±0.7 g/L)显著增高(P<0.05)外,其它各患者组的FIB测定结果与正常对照组比较差异无显著意义(P>0.05)。正常人对照组、有血栓形成倾向疾病和缺血性脑血管病患者组(治疗前)3组人群血小板膜表面FIB-R和CD62P测定结果见表1。
, 百拇医药
3.急性脑梗死患者治疗前后各项指标动态变化:急性脑梗死患者治疗前后血小板膜FIB-R和CD62P表达量(RMFI)、纤维蛋白原含量(FIB)、欧洲卒中评分(ESS)动态变化分别见表2。
表1 不同人群血小板膜表面FIB-R和CD62P测定结果比较(中位数) 组别
例数
FIB-R(%)
FIB-R(RMFI)
CD62P(%)
CD62P(RMFI)
正常人
35
1.40(0~4.88)
, http://www.100md.com
29.70(19.1~48.12)
0.70(0~2.05)
34.93(25.58~59.26)
高脂血症
27
7.59(0.05~46.81)*
33.32(14.87~94.75)△
1.04(0~47.55)
37.13(23.12~97.75)
糖尿病
, 百拇医药
25
7.80(1.6~54.02)*
38.22(26.74~59.21)△
0.84(0~17.94)
33.99(19.77~50.83)
高血压病
31
8.87(1.79~43.26)*
37.43(23.31~51.41)△
0.95(0~10.62)
, 百拇医药
34.98(20.4~68.66)
脑动脉硬化
29
13.70(1.12~69.83)*
34.32(17.18~79.02)△
1.85(0~27.61)
34.28(20.91~120.12)
TIA
25
9.27(1.29~71.16)*
, 百拇医药
37.61(26.66~64.08)△
1.58(0~27.61)
39.29(21.58~74.45)
脑梗死(慢性期)
26
9.01(1.0~47.8)*
35.99(28.29~96.0)△
0.90(0~54.8)
31.44(17.71~113.68)
腔梗(急性期)
, 百拇医药
17
11.20(2.0~76.9)*
38.79(25.44~114.63)*
1.39(0~46.9)
33.19(22.17~51.92)
脑梗死(急性期)
52
13.90(0.1~91.8)*
46.64(25.51~161.12)*
1.33(0~46.29)
, http://www.100md.com
36.79(21.2~111.24)
注:与正常人群比较*P<0.01,△P<0.05表2 急性脑梗死患者治疗前后各项指标的动态变化比较 组别
例数
FIB-R(RMFI)☆
CD62P(RMFI)☆
FIB(g/L)
ESS
治疗前
52
46.64(25.51~161.12)
, 百拇医药
36.79(21.20~111.24)
3.7±0.7
63±18
治疗后1d
52
34.73(16.43~108.92)△
30.16(18.82~69.58)
3.3±0.9
75±21△
治疗后7d
52
, 百拇医药
31.40(16.35~115.08)*
39.40(24.35~82.22)
3.4±0.8
79±22*
注:☆数据以中位数(全距)表示,与治疗前比较△P<0.05,*P<0.01 4.部分检查指标的相关性分析:经相关性分析,急性脑梗死患者病情轻重评分(ESS)与血小板膜表面FIB-R表达量(RMFI)呈负相关(r=-0.910,P<0.01),与血小板膜表面CD62P表达量(RMFI)和纤维蛋白原含量(FIB)无相关性。体外试验中,ADP活化血小板表面FIB-R与CD62P表达量呈正相关(r=0.991,P<0.01)。讨论
1.流式细胞术三色分析活化血小板方法学:血小板活化在血栓形成过程中起着重要作用,活化血小板既是血栓的组成成分之一,又可循环于血液中[4],即循环活化血小板(CAP)。活化血小板与静止血小板相比,其膜糖蛋白(GP)分子的种类、数量、分布和构型等出现显著变化[4-6],FCM作为一种高效、快速、多参数分析的先进技术,可以非常灵敏地检测到活化血小板膜表面糖蛋白分子的变化,从而可以精确判断血小板的功能状态[5-7]。
, http://www.100md.com
本研究中采用抗凝全血标本且用量极少,影响血小板体外活化因素较少,比以往的方法[6,7]更为简便、快速。在实验中选择了PAC-1作为识别FIB-R的McAb[8],CD62P作为血小板α颗粒发生释放反应的标志物[3,6],进行三色免疫荧光标记,加上FSC和SSC共5项参数进行分析,从而提高了FCM检测活化血小板的灵敏度与准确性。研究结果表明,正常人血液中静止血小板膜表面FIB-R和CD62P表达极低。血小板在体外经ADP激活后,其膜表面FIB-R和CD62P表达明显增高,McAb PAC-1能特异性识别活化血小板膜表面的FIB-R。由此可见,FCM三色分析活化血小板具有高灵敏和高特异性。在体外试验中,ADP激活的血小板膜表面FIB-R和CD62P表达呈正相关(r>0.99,P<0.01),表明两者均可作为活化血小板的分子标志物,但这2种标志物反映的血小板活化途径完全不同[3,4,6]。
2.循环活化血小板(CAP)在缺血性脑血管病中的临床意义:缺血性脑血管病的发病机制较为复杂,有研究提示CAP增高与其发生有密切关系[1-3],但血小板活化如何导致缺血性脑血管病,尤其是引起急性脑梗死发作的机制尚不太清楚。血浆纤维蛋白原(FIB)含量仅在腔隙性梗死和急性期脑梗死时明显高于正常人(P<0.05),提示FIB与脑梗死发生有关。本研究结果表明,血小板膜表面FIB-R表达增高是缺血性脑血管病发生的重要因素,在高脂蛋白血症、糖尿病、高血压病和脑动脉硬化患者就已存在FIB-R表达增高,急性腔隙性梗死和急性脑梗死时,血浆FIB和血小板膜表面FIB-R均显著增高,必然促进血小板聚集性增强而导致白色血栓形成或红色血栓形成,最终引发急性脑梗死。CD62P在体外ADP活化血小板膜表面明显增高,但在有血栓倾向疾病和缺血性脑血管病患者血液中血小板膜表面却未见明显增高,其原因可能是循环血液中的活化血小板表面CD62P分子迅速从其表面清除所致[4,9]。Michelson等[5]还证实CD62P被清除的活化血小板仍能继续循环于血液中发挥其功能。因此CD62P并非一种循环中脱颗粒血小板(活化血小板)检测的理想标志物[8],本实验结果也得到验证。急性脑梗死患者治疗后,血小板膜表面FIB-R表达量比治疗前明显降低,其降低的程度与患者病情轻重的评价指标―ESS(欧洲脑卒中评分)呈负相关,提示血小板膜表面FIB-R 表达量与脑梗死患者病情轻重程度有关。研究中还发现治疗后病情好转的急性脑梗死患者发生再瘫痪时,其血小板膜表面FIB-R表达比瘫痪前明显增高,这对临床判断患者预后或是否发生病情加重有意义。
, 百拇医药
基金项目:国家卫生部科学研究基金资助项目(96-1-261)
参考文献
1,Ruf A, Patscheke H. Flow cytometric detection of activated platelets: comparison of determining shape change, fibrinogen binding and P-selectin expression. Semin Thromb Hemost, 1995,21:146-151.
2,Grau AJ, Ruf A, vogt A, et al. Increased fraction of circulating activated platelets in acute and previous cerebrovascular ischemia. Thromb haemost, 1998,80:298-301.
, 百拇医药
3,Michelson AD. Flow cytometry: a clinical test of platelet function. Blood, 1996, 87: 4925-4936.
4,Shattil SJ, Hoie JA, Cunning M, et al. Changes in the platelet membrane glycoprotein IIb-IIIa complex during platelet activation. J Biol chem, 1985, 260:11107-11114.
5,Michelson AD, Flow cytometry assessment of glycoprotein movements in platelets. Platelets, 1997,8:105-115.
6,王建中,孙芾,王淑娟,等.流式细胞术检测活化血小板.中华医学检验杂志,1994,17:232-235.
, 百拇医药
7,Abrams C, Shattil SJ. Immunological detection of activation platelets in clinical disorder. Thromb Haemost , 1991, 65:467-650.
8,Taub R, Gould RJ, Garsky VM, et al. A monoclonal antibody against the platelet fibrinogen receptor contains a sequence that minics a receptor recognition domain in fibrinogen. J Biol chem, 1989, 264:259-265.
9,Michelson AD, Barnard MR, Hechtman HB, et al. In vivo tracting of platelets: circulating degranulated platelets rapidly lose surface P-selectin but continue to circulate and function. Porch Natl Acad Sci USA, 1996, 93:11877-11882.
收稿日期:1999-07-12, http://www.100md.com
单位:100034 北京医科大学第一医院检验科
关键词:流式细胞术;血小板活化;纤维蛋白原受体;P-选择素;缺血性脑血管病
中华医学杂志000705【摘要】目的 探讨流式细胞术(FCM)三色分析血液中循环活化血小板(CAP)在缺血性脑血管病中的临床意义。方法 以纤维蛋白原受体(FIB-R)、P-选择素(CD62P)作为分子标志物,FCM三色免疫荧光分析CAP。结果 正常人静止血小板膜表面FIB-R和CD62P表达极低(阳性百分率的中位数分别为1.4%和0.7%)。0.1 μmol/L ADP可使血小板明显活化,10 μmol/L ADP使活化血小板膜表面FIB-R和CD62P表达至峰值,阳性百分率分别为87.8%和81.3%。合成肽(RGDS)可抑制抗FIB-R的单克隆抗体与ADP活化血小板结合。112例有血栓形成倾向疾病和120例缺血性脑血管病患者血液中表达FIB-R的CAP数量与正常人比较差异有显著意义(P<0.01),但表达CD62P的CAP数量增高不明显(P>0.05)。急性脑梗死患者治疗前后CAP的FIB-R表达呈连续下降趋势(P<0.05),而且CAP的FIB-R表达量与患者的ESS(欧洲脑卒中评分)呈负相关。结论 FIB-R可作为CAP检测的灵敏、特异的分子标志物,流式细胞术三色分析CAP能准确地反映体内血小板的活化水平,对缺血性脑血管病的发病机理研究、预后判断、疗效监测等有重要的临床意义。
, 百拇医药
Flow cytometric 3-color analysis of circulating activated platelets and its clinical significance in ischemic cerebrovascular diseases
WANG Jianzhong CAO Ling HE Maolin et al.
(The First Hospital, Beijing Medical University, Beijing 100034, China)
【Abstract】Objective To explore the flow cytometric 3-color analysis of circulating activated platelets (CAP) and its clinical significance in ischemic cerebrovascular diseases. Methods The fibrinogen receptor (FIB-R) and P-selectin (CD62P) were used for molecular marker of CAP, which were analyzed by flow cytometric 3-color immunofluorescence. Results Expression of FIB-R and CD62P on the resting platelet membrane surface was very lower in normal individuals, the median of FIB-R and CD62P positive percent was 1.40% and 0.70% respectively. Platelet can be obviously activated by 0.1 μmol/L ADP, and 10.0 μmol/L ADP leaded to the peak expression of FIB-R and CD62P on the activated platelet membrane surface, FIB-R and CD62P positive percent of 87.8% and 81.34% respectively. That monoclonal antibody of the FIB-R combined with ADP activating platelets was inhibited by synthetic peptide (RGDS). The quantity of CAP with FIB-R expression was markedly higher (P<0.01) and the amount of CAP with CD62P expression was not significantly higher (P>0.05) in blood of 112 patients with thrombotic tendency and 120 patients with ischemic cerebrovascular diseases than in healthy individuals. The expression of CAP with FIB-R of in front and behind treatment of acute cerebral infarction continuously decreased (P<0.05), and the quantity of CAP with FIB-R expression was related negatively to Europe stroke score (ESS) of patients with acute cerebral infarction. Conclusion The FIB-R may be regarded as sensitive and specific molecular marker in detection of CAP. The level of platelet activation in vivo can be reflected accurately by flow cytometric 3-color analysis of CAP, which has an important clinical significance for the study of pathogenesis, estimation of prognosis and supervision of curative effect in ischemic cerebrovascular diseases.
, 百拇医药
【Key words】Flow cytometry; Activated platelet;Fibrinogen receptor;P-selectin;Ischemic cerebrovascular diseases
血液中循环活化血小板(CAP)增高可作为动脉血管病,如缺血性中风、心肌梗死、周围血管病等疾病有局部血栓形成的标志物[1],CAP测定可能有助于中风等疾病的预后判断和治疗[2],然而由于CAP测定方法不同,常导致其检查结果有争议[3]。我们选择了血小板膜表面纤维蛋白原受体(FIB-R)、P-选择素(CD62P)作为CAP的分子标志物,用流式细胞术(FCM)三色免疫荧光标记法,测定了112例有血栓形成倾向疾病和120例缺血性脑血管病患者以及35例正常人血液中CAP数量变化,以探讨其在缺血性脑血管病中的临床意义。
对象与方法
, 百拇医药
一、对象
1.有血栓形成倾向疾病患者组112例:高脂蛋白血症27例,男13例、女14例,平均年龄62岁±11.5岁。糖尿病25例,男19例、女6例,平均年龄63岁±7.2岁。高血压病31例,男22例、女9例,平均年龄64岁±7岁。脑动脉硬化29例,男23例、女6例,平均年龄66岁±5.9岁。
2.缺血性脑血管病患者组120例:短暂性脑缺血发作(TIA)发病半年内患者25例,男17例、女8例,平均年龄66岁±8.8岁。发病3个月以上脑梗死(慢性期)患者26例,男19例、女7例,平均年龄65岁±6.6岁。急性期(发病2 d内)腔隙性脑梗死(腔梗)患者17例,男13例,女4例,平均年龄62岁±9岁。发病2 d内脑梗死(急性期皮质性脑梗死)患者52例,男34例、女18例,平均年龄63岁±10岁,患者病情轻重按欧洲脑卒中评分(ESS)标准进行评分,根据患者病情进行常规治疗(用低分子右旋糖苷、维脑路通、醒脑静等常规药物治疗)和溶栓治疗(发病6 h内,150万单位尿激酶溶栓)。以上患者均经临床、脑CT等检查,由神经内科专科医师确诊。
, 百拇医药
3.正常对照组35例:经体检正常,无心脑血管病的健康志愿者,男20例,女15例,平均年龄63岁±9.7岁。
4.主要试剂:(1)荧光色素标记单克隆抗体(McAb):PAC-1 FITC为异硫氰酸荧光素标记的抗血小板活化GPIIb-IIIa,即纤维蛋白原受体(FIB-R)的McAb。CD62P PE为藻红蛋白标记的抗P-选择素的McAb。CD61 PerCP为Peridinin chlorophyll protein(PerCP)标记的血小板糖蛋白IIIa的McAb。MIgG 为藻红蛋白标记的鼠IgG。以上均为美国Becton-Dickinson公司产品;(2)人工合成的精氨酰-甘氨酰-天冬氨酰-丝氨酰多肽(RGDS)为美国Sigma 公司产品;(3)二磷酸腺苷(ADP),Boehringer Mannheim公司产品;(4)多聚甲醛(PFA),美国E.Marke产品;(5)流式细胞仪三色校准微球(CaliBRITETM3 Kit),美国Becton-Dickinson公司产品。
, 百拇医药
5.主要仪器:(1)FACSort型流式细胞仪,美国Becton-Dickinson公司产品;(2)CA570全自动血细胞分析仪,瑞典MEDONIC公司产品;(3)LBY-NJ2四通道血小板聚集仪,中国普利生公司产品;(4)ACL Futura全自动凝血分析仪,美国Laboratory Instrument公司产品。
二、方法
1.样本采集:各组患者及正常人均静脉采血,经106 mmol/L枸橼酸钠抗凝,急性脑梗塞患者于治疗前、治疗后1 d、7 d采血3次。其它患者及正常人于清晨、空腹采血,且应停用抗血小板、抗凝血药7~10 d以上,采血1次。
2.流式细胞术三色分析活化血小板:(1)样本制备:分别取PAC-1 FITC、CD62P PE 、CD61 PerCP 各10 μl加入一塑料试管中混匀作为测定管;另取PAC-FITC、MIgG PE、CD61 PerCP、RGDS(5 mg/ml)各10 μl加入一塑料试管中混匀作为对照管,两管中分别加入10 min前采集的静脉抗凝血5 μl与试剂轻轻混匀、室温条件下避光作用20 min,立即加入预冷2~8℃的1%多聚甲醛1 ml并混匀,置2~8℃冰箱内2 h后、24 h内在流式细胞仪上进行测定;(2)流式细胞仪检测和数据分析:用荧光微球校准流式细胞仪后,在CellQuest软件环境中,将流式细胞仪的前向角散射(FSC)、侧向角散射(SSC)、三色荧光(FL1~FL3)的检测信号均设置为对数放大,以CD61 PerCP/SSC双参数设门,分别检测对照管和测定管中单个血小板的光散射及三色荧光强度,并分析FIB-R(PAC-1)和CD62P阳性CAP的百分率及平均荧光强度(MFI),以测定管与对照管MFI的比值(RMFI)代表血小板表达活化分子标志物的相对含量。
, 百拇医药
3.其它检查指标:(1)血小板计数(PLT)和血小板平均体积(MPV)测定,用抗凝全血在CA570血细胞分析仪上测定;(2)血小板聚集率(PAR),用ADP(3 μmol/L终浓度)作诱导剂,在血小板聚集仪上测定最大血小板聚集率(PAR);(3)血浆纤维蛋白含量(FIB)测定,在ACL Futura全自动凝血仪上以光学法测定FIB含量。
4.数据统计:实验结果以中位数(全距)或算术平均数±标准差(
 ±s)表示,多组间资料分析用方差分析或秩和检验,相关性用线性回归分析,各项统计均用SPSS统计软件在计算机上完成。
±s)表示,多组间资料分析用方差分析或秩和检验,相关性用线性回归分析,各项统计均用SPSS统计软件在计算机上完成。结果
1.ADP活化血小板膜糖蛋白变化:用不同浓度ADP(0、0.1、0.2、0.5、1.0、2.0、5.0、10.0、20.0 μmol/L)加入正常人抗凝血液中、37℃激活5 min后在流式细胞仪上测定血小板膜表面FIB-R和CD62P阳性血小板百分率和平均荧光强度(MFI)见图1。在上述浓度ADP激活的血液标本测定管中分别加入10μl RGDS 后再测定血小板膜表面FIB-R和CD62P阳性血小板百分率和MFI,可见RGDS可竞争性抑制McAb PAC-1与FIB-R的结合(见图2)。

, 百拇医药
图1 不同浓度ADP激活的血小板表面膜FIB-R和
CD62P表达的动态变化

图2 RGDS对ADP(10.0 μmol/L)激活血小板FIB-R和CD62P表达的影响,FCM分析荧光点图:A―加RGDS,B―未加RGDS
2.各组人群各项结果比较:正常人群的PLT、MPV、PAR测定结果分别为(153±53)×109/L、8.7 fl±0.5 fl、57.9%±10.3%,PLT、MPV、PAR 3项结果与有血栓形成倾向疾病和缺血性脑血管病患者(治疗前)2组人群差异无显著意义(P>0.05)。FIB测定除腔隙性脑梗死(3.6 g/L±1.3 g/L)和急性脑梗死(3.7 g/L±0.7 g/L )患者组比正常对照组(3.1 g/L±0.7 g/L)显著增高(P<0.05)外,其它各患者组的FIB测定结果与正常对照组比较差异无显著意义(P>0.05)。正常人对照组、有血栓形成倾向疾病和缺血性脑血管病患者组(治疗前)3组人群血小板膜表面FIB-R和CD62P测定结果见表1。
, 百拇医药
3.急性脑梗死患者治疗前后各项指标动态变化:急性脑梗死患者治疗前后血小板膜FIB-R和CD62P表达量(RMFI)、纤维蛋白原含量(FIB)、欧洲卒中评分(ESS)动态变化分别见表2。
表1 不同人群血小板膜表面FIB-R和CD62P测定结果比较(中位数) 组别
例数
FIB-R(%)
FIB-R(RMFI)
CD62P(%)
CD62P(RMFI)
正常人
35
1.40(0~4.88)
, http://www.100md.com
29.70(19.1~48.12)
0.70(0~2.05)
34.93(25.58~59.26)
高脂血症
27
7.59(0.05~46.81)*
33.32(14.87~94.75)△
1.04(0~47.55)
37.13(23.12~97.75)
糖尿病
, 百拇医药
25
7.80(1.6~54.02)*
38.22(26.74~59.21)△
0.84(0~17.94)
33.99(19.77~50.83)
高血压病
31
8.87(1.79~43.26)*
37.43(23.31~51.41)△
0.95(0~10.62)
, 百拇医药
34.98(20.4~68.66)
脑动脉硬化
29
13.70(1.12~69.83)*
34.32(17.18~79.02)△
1.85(0~27.61)
34.28(20.91~120.12)
TIA
25
9.27(1.29~71.16)*
, 百拇医药
37.61(26.66~64.08)△
1.58(0~27.61)
39.29(21.58~74.45)
脑梗死(慢性期)
26
9.01(1.0~47.8)*
35.99(28.29~96.0)△
0.90(0~54.8)
31.44(17.71~113.68)
腔梗(急性期)
, 百拇医药
17
11.20(2.0~76.9)*
38.79(25.44~114.63)*
1.39(0~46.9)
33.19(22.17~51.92)
脑梗死(急性期)
52
13.90(0.1~91.8)*
46.64(25.51~161.12)*
1.33(0~46.29)
, http://www.100md.com
36.79(21.2~111.24)
注:与正常人群比较*P<0.01,△P<0.05表2 急性脑梗死患者治疗前后各项指标的动态变化比较 组别
例数
FIB-R(RMFI)☆
CD62P(RMFI)☆
FIB(g/L)
ESS
治疗前
52
46.64(25.51~161.12)
, 百拇医药
36.79(21.20~111.24)
3.7±0.7
63±18
治疗后1d
52
34.73(16.43~108.92)△
30.16(18.82~69.58)
3.3±0.9
75±21△
治疗后7d
52
, 百拇医药
31.40(16.35~115.08)*
39.40(24.35~82.22)
3.4±0.8
79±22*
注:☆数据以中位数(全距)表示,与治疗前比较△P<0.05,*P<0.01 4.部分检查指标的相关性分析:经相关性分析,急性脑梗死患者病情轻重评分(ESS)与血小板膜表面FIB-R表达量(RMFI)呈负相关(r=-0.910,P<0.01),与血小板膜表面CD62P表达量(RMFI)和纤维蛋白原含量(FIB)无相关性。体外试验中,ADP活化血小板表面FIB-R与CD62P表达量呈正相关(r=0.991,P<0.01)。讨论
1.流式细胞术三色分析活化血小板方法学:血小板活化在血栓形成过程中起着重要作用,活化血小板既是血栓的组成成分之一,又可循环于血液中[4],即循环活化血小板(CAP)。活化血小板与静止血小板相比,其膜糖蛋白(GP)分子的种类、数量、分布和构型等出现显著变化[4-6],FCM作为一种高效、快速、多参数分析的先进技术,可以非常灵敏地检测到活化血小板膜表面糖蛋白分子的变化,从而可以精确判断血小板的功能状态[5-7]。
, http://www.100md.com
本研究中采用抗凝全血标本且用量极少,影响血小板体外活化因素较少,比以往的方法[6,7]更为简便、快速。在实验中选择了PAC-1作为识别FIB-R的McAb[8],CD62P作为血小板α颗粒发生释放反应的标志物[3,6],进行三色免疫荧光标记,加上FSC和SSC共5项参数进行分析,从而提高了FCM检测活化血小板的灵敏度与准确性。研究结果表明,正常人血液中静止血小板膜表面FIB-R和CD62P表达极低。血小板在体外经ADP激活后,其膜表面FIB-R和CD62P表达明显增高,McAb PAC-1能特异性识别活化血小板膜表面的FIB-R。由此可见,FCM三色分析活化血小板具有高灵敏和高特异性。在体外试验中,ADP激活的血小板膜表面FIB-R和CD62P表达呈正相关(r>0.99,P<0.01),表明两者均可作为活化血小板的分子标志物,但这2种标志物反映的血小板活化途径完全不同[3,4,6]。
2.循环活化血小板(CAP)在缺血性脑血管病中的临床意义:缺血性脑血管病的发病机制较为复杂,有研究提示CAP增高与其发生有密切关系[1-3],但血小板活化如何导致缺血性脑血管病,尤其是引起急性脑梗死发作的机制尚不太清楚。血浆纤维蛋白原(FIB)含量仅在腔隙性梗死和急性期脑梗死时明显高于正常人(P<0.05),提示FIB与脑梗死发生有关。本研究结果表明,血小板膜表面FIB-R表达增高是缺血性脑血管病发生的重要因素,在高脂蛋白血症、糖尿病、高血压病和脑动脉硬化患者就已存在FIB-R表达增高,急性腔隙性梗死和急性脑梗死时,血浆FIB和血小板膜表面FIB-R均显著增高,必然促进血小板聚集性增强而导致白色血栓形成或红色血栓形成,最终引发急性脑梗死。CD62P在体外ADP活化血小板膜表面明显增高,但在有血栓倾向疾病和缺血性脑血管病患者血液中血小板膜表面却未见明显增高,其原因可能是循环血液中的活化血小板表面CD62P分子迅速从其表面清除所致[4,9]。Michelson等[5]还证实CD62P被清除的活化血小板仍能继续循环于血液中发挥其功能。因此CD62P并非一种循环中脱颗粒血小板(活化血小板)检测的理想标志物[8],本实验结果也得到验证。急性脑梗死患者治疗后,血小板膜表面FIB-R表达量比治疗前明显降低,其降低的程度与患者病情轻重的评价指标―ESS(欧洲脑卒中评分)呈负相关,提示血小板膜表面FIB-R 表达量与脑梗死患者病情轻重程度有关。研究中还发现治疗后病情好转的急性脑梗死患者发生再瘫痪时,其血小板膜表面FIB-R表达比瘫痪前明显增高,这对临床判断患者预后或是否发生病情加重有意义。
, 百拇医药
基金项目:国家卫生部科学研究基金资助项目(96-1-261)
参考文献
1,Ruf A, Patscheke H. Flow cytometric detection of activated platelets: comparison of determining shape change, fibrinogen binding and P-selectin expression. Semin Thromb Hemost, 1995,21:146-151.
2,Grau AJ, Ruf A, vogt A, et al. Increased fraction of circulating activated platelets in acute and previous cerebrovascular ischemia. Thromb haemost, 1998,80:298-301.
, 百拇医药
3,Michelson AD. Flow cytometry: a clinical test of platelet function. Blood, 1996, 87: 4925-4936.
4,Shattil SJ, Hoie JA, Cunning M, et al. Changes in the platelet membrane glycoprotein IIb-IIIa complex during platelet activation. J Biol chem, 1985, 260:11107-11114.
5,Michelson AD, Flow cytometry assessment of glycoprotein movements in platelets. Platelets, 1997,8:105-115.
6,王建中,孙芾,王淑娟,等.流式细胞术检测活化血小板.中华医学检验杂志,1994,17:232-235.
, 百拇医药
7,Abrams C, Shattil SJ. Immunological detection of activation platelets in clinical disorder. Thromb Haemost , 1991, 65:467-650.
8,Taub R, Gould RJ, Garsky VM, et al. A monoclonal antibody against the platelet fibrinogen receptor contains a sequence that minics a receptor recognition domain in fibrinogen. J Biol chem, 1989, 264:259-265.
9,Michelson AD, Barnard MR, Hechtman HB, et al. In vivo tracting of platelets: circulating degranulated platelets rapidly lose surface P-selectin but continue to circulate and function. Porch Natl Acad Sci USA, 1996, 93:11877-11882.
收稿日期:1999-07-12, http://www.100md.com