HSP90β蛋白低调肿瘤细胞系的建立
作者:刘宪玲 徐立 郭建成 肖冰 俞召才 樊代明
单位:刘宪玲 徐立 郭建成 肖冰 俞召才 樊代明(第四军医大学西京医院消化病研究所 西安 710032)
关键词:HSP90β;反义核酸;基因转染;RNA酶保护分析;Western blot
中国肿瘤生物治疗杂志000207
摘 要 目的: 通过转染HSP90β反义核酸重组子pcDNA-HSP90于4株人消化系肿瘤细胞系,以建立HSP90β蛋白低调肿瘤细胞系, 并研究HSP90β蛋白低调后细胞的生长情况。方法: 用Lipofectamine介导将pcDNA-HSP90转染人胃癌细胞系SGC7901、人胃癌多药耐药细胞系SGC7901/VCR、人肝癌细胞系HCC7402及人食道癌细胞系Ec109,用G418进行筛选,用RNA酶保护分析法鉴定HSP90β反义核酸的表达,用 Western blot 法检测HSP90β蛋白的表达。用细胞生长曲线研究基因转染细胞的生长情况。结果: pcDNA-HSP90转染细胞AH-SGC7901,AH-SGC7901/VCR,AH-HCC7402及AH-Ec109有HSP90β反义RNA表达, 这些细胞HSP90β蛋白表达低调。研究还发现这些细胞的生长受到不同程度的抑制,其中AH-SGC7901/VCR及AH-Ec109细胞受抑程度更明显。结论: pcDNA-HSP90转染细胞AH-SGC7901,AH-SGC7901/VCR,AH-HCC7402及AH-Ec109 HSP90β蛋白表达降低,细胞的生长受到不同程度的抑制。
, 百拇医药
《中国图书资料分类法》分类号 Q78
Construction of HSP90β Protein Down-Regulated Tumor Cell Lines
Liu Xianling Xu Li Guo Jiancheng Xiao Bing Yu Zhaocai Fan Daiming
(Institute of Digestive Disease, XiJing Hospital, Fourth Military Medical University, Xi'an 710032)
Abstract Objective: To set up HSP90β Protein down-regulated digestive tumor cell lines and study the influence of HSP90β to tumor cells. Methods: pcDNA-HSP90 of HSP90β anti-sense RNA reconstructs was transfected into SGC7901 of human gastric cancer cell line, SGC7901/VCR of MDR-type human gastric cancer cell line, HCC7402 of human hepatic cancer cell line and Ec109 of human esophageal cancer cell line by lipofectamine. Positive clones were selected by G418. Antisense RNA of HSP90β of the positive clones was detected by RNase protection assay and the expression of HSP90β protein was assayed by Western blot. Cell growth was studied by cell growth curve. Results: pcDNA-HSP90 transfected cells were named AH-SGC7901, AH-SGC7901/VCR, AH-HCC7402 and AH-Ec109 respectively and there were antisense RNA of HSP90β in them. HSP90β protein in them was lower than in their parental cells. Cell growth was inhibited to different degrees, and the growth of AH-SGC7901/VCR and AH-Ec109 cells were most greatly inhibited. Conclusion: The expression of HSP90β protein in AH-SGC7901, AH-SGC7901/VCR, AH-HCC7402 and AH-Ec109 cell lines was decreased and the study also showed that decreasing the expression of HSP90β could inhibit tumor cell growth.
, 百拇医药
Key words HSP90β; anti-sense RNA; gene transfection; RNase protection assay; Western blot
近年来,发现HSP90与肿瘤的关系比较密切[1~3]。HSP90α可通过调节细胞周期促进细胞增殖,HSP90β能够抑制细胞凋亡与分化[4,5],且最近有人报道HSP90β与P-gp的表达有关[6]。本研究拟用HSP90β反义核酸转染人4株消化系肿瘤细胞系,以建立HSP90β蛋白低调细胞系, 为进一步研究HSP90β对肿瘤细胞的生物学意义提供实验材料,并研究HSP90β蛋白对消化系肿瘤细胞生长的影响。
1 材料与方法
1.1 材料
人胃癌细胞系SGC7901, 人胃癌多药耐药细胞系SGC7901/VCR, 人肝癌细胞系HCC7402, 人食道癌细胞系Ec109。HSP90β反义核酸重组子pcDNA-HSP90由刘宪玲等[7]构建。 pcDNA 3.1(+)由美国扬静华提供。主要试剂(略)。
, http://www.100md.com
1.2 方法
1.2.1 重组质粒的转染及阳性克隆的筛选
实验组转染pcDNA-HSP90, 空载体对照组转染pcDNA3.1(+), SGC7901,SGC7901/VCR,HCC7402,Ec109细胞作为相应的空白对照组。碱裂解法提取重组质粒pcDNA-HSP90。用Lipofectamine介导基因的转染(按说明书进行),G418(400 μg/ml)进行抗性筛选。3~4周后见抗性细胞集落形成,挑选细胞克隆,用含100 μg/ml G418的10%FBS-PRMI 1640液扩大培养。
1.2.2 RNA酶保护分析法检测基因转染细胞HSP90反义核酸的表达[9]
从HSP90β cDNA序列的第1 641 bp起,读取30个bp作为探针,送上海生物工程公司合成。末端标记法标记寡核苷酸探针[8]。提取RNA同时做含量测定后,取RNA 10 μg, 加1.0×105 cpm的[γ-32P]标记的寡核苷酸探针及β-actin探针,加无水乙醇、糖原、3 mol/L 乙酸钠,于-20℃放置20 min,离心、乙醇洗涤、真空干燥,加30 μl甲酰胺杂交缓冲液重悬;85℃ 变性5~10 min,37℃杂交过夜。 加RNase S1 buffer 2 μl, 水16 μl, RNase S1 2 μl(2 μg/ml), 37℃消化1 h;乙醇沉淀;加20 μl终止液(10%SDS, 20 mg/ml 蛋白酶κ)37℃ 15 min;酚/氯仿抽提、乙醇沉淀、真空干燥;重溶于10 μl RNA 上样缓冲液中,上样,做18%聚丙烯酰胺/尿素凝胶电泳(200 v, 120 min)和放射自显影。
, 百拇医药
1.2.3 Western blot检测基因转染细胞HSP90β蛋白的表达
用三去污剂裂解缓冲液裂解细胞,获取细胞裂解液经蛋白质定量后行SDS-PAGE,电转膜及免疫印迹。山羊抗人HSP90β一抗(1∶100)室温作用2 h;辣根过氧化酶标记的驴抗山羊IgG(1∶500)室温作用1 h;PBS洗涤,四氯萘酚显色并拍照。用Quantimet 570 (Germany, Leica Inc.) 图象分析仪(QUIC图象系统)对免疫印迹结果进行半定量分析。条带的染色强度以灰度值表示(256级灰度,条带越深,灰度值越小)。
1.2.4 转染细胞的形态和生长速度观察
分别取基因转染细胞及其相应的亲本细胞(细胞浓度为1×104/孔,每孔2 ml体积)接种于24孔板,常规培养,观察细胞形态及生长状况,绘制细胞生长曲线。并按Patterson公式计算细胞在对数生长期的倍增时间。Td = T*lg2/lg(Nt/N0)。其中Td为细胞倍增时间(h),T为细胞由N0增至Nt所需时间(h)。
, 百拇医药
2 结 果
2.1 G418筛选出的阳性克隆
pcDNA-HSP90转染SGC7901,SGC7901/VCR,HCC-7402及Ec109细胞后,筛选出其相应的阳性克隆,被分别命名为AH-SGC7901,AH-SGC7901/VCR,AH-HCC74O2及AH-Ec109。空载体pcDNA转染细胞被命名为SGC7901-pcDNA,SGC7901/VCR-pcDNA,HCC7402-pcDNA及Ec109-pcDNA。
2.2 RNA酶保护分析法 结果见图1。
图1 RNA酶保护分析法检测HSP90反义RNA转染细胞、空载体转染细胞
及其亲本细胞中HSP90反义RNA的表达
, http://www.100md.com
Fig. 1 The expression of anti-sense RNA of HSP90 in pcDNA-HSP90 transfected cell lines, pcDNA transfected
cell lines and their parental cell lines by RNase protection assay
M: PBR322 DNA/HaeⅢ Marker; C1: Positive control,β-actin(20 bp) and HSP90 probe (30 bp); C2: Negative control, probe plus
RNase S1, no RNA. 1: AH-SGC7901/VCR; 2: SGC7901-pcDNA/VCR; 3: SGC7901/VCR; 4: AH-SGC7901; 5: SGC7901-pcDAN;
, http://www.100md.com
6: SGC7901; 7: AH-HCC7402; 8: HCC7402-pcDNA; 9: HCC7402; 10: AH-Ec109; 11: Ec109-pcDNA; 12: Ec109
HSP90β反义核酸转染细胞AH-SGC7901/VCR(1),AH-SGC7901(4),AH-HCC7402(7)及AH-Ec109(10)组有两条电泳带,依据分子量Marker,可确定它们分别为β-actin内参照及HSP90 反义RNA;转染pcDNA3.1(+)组及空白对照组可见1条带为β-actin。表明pcDNA-HSP90已转染入细胞,并有HSP90β反义RNA的表达。
2.3 HSP90β反义核酸转染细胞HSP90β蛋白低调
Western blot 结果见图2。用Quanuimet 570 图象分析仪进行分析,结果见表1。
, http://www.100md.com
pcDNA-HSP90转染细胞系HSP90β蛋白的表达明显低于其亲本细胞系及其空白对照细胞系。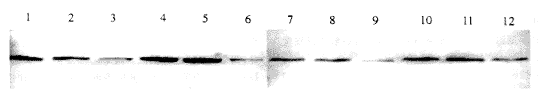
图2 pcDNA-HSP90转染细胞HSP90β蛋白的表达
Fig. 2 The expression of HSP90β protein in pcDNA-HSP90 transfected cell lines
1: SGC7901; 2: SGC7901-pcDNA; 3:AH-SGC7901; 4: SGC7901/VCR; 5: SGC7901/VCR-pcDNA;
6: AH-SGC7901/VCR; 7: HCC7402; 8: HCC7402-pcDNA; 9: AH-HCC7402; 10: Ec109; 11: Ec109-pcDNA; 12: AH-Ec109
, 百拇医药
表1 基因转染细胞及其对照细胞
Hsp90β蛋白表达的半定量分析
Tab. 1 The grey scales of HSP90β in pcDNA-HSP90
transfected cell lines and their parental cell lines Cell lines
Grey scales
P
1.SGC7901
61.44±2.45
2.SGC7901-pcDNA
, 百拇医药
61.15±3.33
3.AH-SGC7901
83.17±2.89
P<0.05△
4.SGC7901/VCR
37.52±3.67
5.SGC7901/VCR-pcDNA
38.91±3.31
6.AH-SGC7901/VCR
80.50±3.60
P<0.05▲
, 百拇医药
7.HCC7402
93.47±3.41
8.HCC7402-pcDNA
89.13±3.51
9.AH-HCC7402
156.8±2.75
P<0.05□
10.Ec109
81.75±4.02
11.Ec109-pcDNA
81.21±3.26
, 百拇医药
12.103.21±4.24
103.21±4.24
P<0.05■
△ 3 vs 1,2; ▲ 6 vs 4,5; □ 9 vs 7,8; ■ 12 vs 10, 11
2.4 转染细胞的生长曲线
基因转染后的AH-SGC7901,AH-SGC7901/VCR, AH-HCC7402及AH-Ec109细胞与其相应的亲本细胞SGC7901, SGC7901/VCR, HCC7402及Ec109相比,细胞生长受到不同程度的抑制(见图3)。
由细胞生长曲线求得各细胞倍增时间Td,AH-SGC7901,AH-SGC7901/VCR, AH-HCC7402及AH-Ec109细胞的Td较其亲本细胞分别延长了1.12 h,16.69 h,2.74 h及15.97 h。可见 AH-SGC7901/VCR细胞及AH-Ec109细胞的倍增时间Td较其相应的亲本细胞的Td明显延长 (P<0.05), AH-SGC7901及AH-HCC7402细胞较其相应的亲本细胞的Td改变不明显 (P>0.05)。AH-SGC7901,AH-SGC7901/VCR, AH-HCC7402及AH-Ec109细胞与其相应的亲本细胞相比,他们在第10天的抑制率分别为24.28%, 27.58%, 10.51%及66.91%。
, 百拇医药
3 讨 论
依据反义核酸技术的原理,我们构建成HSP90β反义核酸重组子pcDNA-HSP90[7]。并转染SGC7901,SGC7901/VCR,HCC7402及Ec109细胞,用G418进行抗性筛选,挑选出相应的阳性克隆AH-SGC7901, AH-SGC7901/VCR, AH-HCC7402及AG-Ec109。
我们用RNA酶保护分析方法鉴定经G418筛选出的克隆是否有HSP90β反义RNA的表达,RNase保护分析的原理[9,10]为, 将标记的寡核苷酸探针与细胞总RNA或mRNA杂交,再用RNase S1消化单链未杂交的RNA,则杂交的双链被保护不被RNase S1消化。经丙烯酰胺/尿素凝胶电泳可分离出来,放射自显影后可显示杂交的条带;通过标准分子量marker可确定其大小。此方法的特异性及敏感性远远超过Northern杂交,且较Northern blot 简单, 较Dot blot精确。RNA酶保护分析结果表明,pcDNA-HSP90转染细胞有HSP90β反义RNA的表达。
, http://www.100md.com
Western blot检测结果表明,与亲本细胞及转染空载体的细胞相比, HSP90β反义核酸转染细胞AH-SGC7901,AH-SGC7901/VCR,HCC7402及Ec109 HSP90β蛋白的表达明显减低, 说明HSP90β反义RNA对HSP90βmRNA有部分封闭作用, 从而使其翻译为HSP90β蛋白减少。
通过对转染细胞生长曲线的研究发现,基因转染细胞的生长受到不同程度的抑制,其中AH-SGC7901/VCR细胞及AH-Ec109细胞受抑程度更明显。热休克蛋白HSP90β为细胞内的主要分子伴侣蛋白,参与蛋白质的装配、折叠与成熟,稳定蛋白质的构象,本研究表明HSP90β对肿瘤细胞的生长具有一定的作用。降低HSP90β蛋白的表达可抑制消化系肿瘤细胞的生长。提示可通过抑制HSP90β蛋白的表达而抑制肿瘤细胞的生长。
图3 pcDNA-HSP90转染细胞的生长曲线(A,B,C,D)
, 百拇医药
Fig. 3 The growth curve of pcDNA-HSP90 transfected cell lines (A,B,C,D)
总之,HSP90β反义核酸重组子pcDNA-HSP90转染的 AH-SGC7901,AH-SGC7901/VCR,AH-HCC7402及AH-Ec109细胞,均有HSP90β反义RNA的表达,且部分封闭了HSP90β蛋白的表达,此为进一步研究HSP90β对消化系肿瘤细胞的生物学作用建立了细胞模型。
国家自然科学基金第39570806号及国家杰出青年基金第3952020号资助
刘宪玲,女,36岁,主治医师,讲师博士
参 考 文 献
1,Jameel A, Skilton RA, Campbell TA, et al. Clinical and biological significance of HSP90α in human breast cancer. Int J Cancer, 1992, 50: 409
, 百拇医药
2,Mileo AM, Fanuele M, Battaglia F, et al. Selective overexpression of mRNA coding for 90 kDa stress protein in human overian cancer. Anticancer Res, 1990, 10: 903
3,Nanbu K, Konshi I, Komatsu T, et al. Expression of heat shock proteins HSP70 and HSP90 in endometrial carcinomas. Cancer, 1996, 77: 330
4,Yano M, Naito Z, Tanaka S, et al. Expression and roles of heat shock proteins in human breast cancer. Jpn J Cancer Res, 1996, 87: 908
, 百拇医药
5,Yamada T, Nakamura R, Kido K, et al. Function of hsp90 in differentiation and apoptosis of human EC cells. Trans Soc Pathol Jpn, 1995, 84: 217
6,Bertram J, Palfner K, Hiddemann W, et al. Increase of P-glycoprotein-mediated drug resistance by hsp90 beta. Anticancer Drug, 1996, 7: 838
7,刘宪玲, 肖 冰, 俞召才, 等. HSP90β反义RNA真核表达载体pcDNA-HSP90的构建与鉴定. 细胞与分子免疫学杂志, 1999, 15: 207
8,姜 泊, 张亚历, 周殿元 主编. 分子生物学常用实验方法. 北京: 人民军医出版社, 1995. 42
9,Lau ET, Kong RY, Cheah KSE. A critical assessment of the RNase protection assay as a means of determining exon sizes. Anal Biochem, 1993, 209: 360
10,萨姆布鱼克 J, 弗里奇 EF, 曼尼阿蒂斯 T. 分子克隆实验指南. 金冬雁,黎孟枫 等译. 第2版, 北京: 科学出版社, 1995. 374
(1999-07-14收稿; 1999-10-03修回), 百拇医药
单位:刘宪玲 徐立 郭建成 肖冰 俞召才 樊代明(第四军医大学西京医院消化病研究所 西安 710032)
关键词:HSP90β;反义核酸;基因转染;RNA酶保护分析;Western blot
中国肿瘤生物治疗杂志000207
摘 要 目的: 通过转染HSP90β反义核酸重组子pcDNA-HSP90于4株人消化系肿瘤细胞系,以建立HSP90β蛋白低调肿瘤细胞系, 并研究HSP90β蛋白低调后细胞的生长情况。方法: 用Lipofectamine介导将pcDNA-HSP90转染人胃癌细胞系SGC7901、人胃癌多药耐药细胞系SGC7901/VCR、人肝癌细胞系HCC7402及人食道癌细胞系Ec109,用G418进行筛选,用RNA酶保护分析法鉴定HSP90β反义核酸的表达,用 Western blot 法检测HSP90β蛋白的表达。用细胞生长曲线研究基因转染细胞的生长情况。结果: pcDNA-HSP90转染细胞AH-SGC7901,AH-SGC7901/VCR,AH-HCC7402及AH-Ec109有HSP90β反义RNA表达, 这些细胞HSP90β蛋白表达低调。研究还发现这些细胞的生长受到不同程度的抑制,其中AH-SGC7901/VCR及AH-Ec109细胞受抑程度更明显。结论: pcDNA-HSP90转染细胞AH-SGC7901,AH-SGC7901/VCR,AH-HCC7402及AH-Ec109 HSP90β蛋白表达降低,细胞的生长受到不同程度的抑制。
, 百拇医药
《中国图书资料分类法》分类号 Q78
Construction of HSP90β Protein Down-Regulated Tumor Cell Lines
Liu Xianling Xu Li Guo Jiancheng Xiao Bing Yu Zhaocai Fan Daiming
(Institute of Digestive Disease, XiJing Hospital, Fourth Military Medical University, Xi'an 710032)
Abstract Objective: To set up HSP90β Protein down-regulated digestive tumor cell lines and study the influence of HSP90β to tumor cells. Methods: pcDNA-HSP90 of HSP90β anti-sense RNA reconstructs was transfected into SGC7901 of human gastric cancer cell line, SGC7901/VCR of MDR-type human gastric cancer cell line, HCC7402 of human hepatic cancer cell line and Ec109 of human esophageal cancer cell line by lipofectamine. Positive clones were selected by G418. Antisense RNA of HSP90β of the positive clones was detected by RNase protection assay and the expression of HSP90β protein was assayed by Western blot. Cell growth was studied by cell growth curve. Results: pcDNA-HSP90 transfected cells were named AH-SGC7901, AH-SGC7901/VCR, AH-HCC7402 and AH-Ec109 respectively and there were antisense RNA of HSP90β in them. HSP90β protein in them was lower than in their parental cells. Cell growth was inhibited to different degrees, and the growth of AH-SGC7901/VCR and AH-Ec109 cells were most greatly inhibited. Conclusion: The expression of HSP90β protein in AH-SGC7901, AH-SGC7901/VCR, AH-HCC7402 and AH-Ec109 cell lines was decreased and the study also showed that decreasing the expression of HSP90β could inhibit tumor cell growth.
, 百拇医药
Key words HSP90β; anti-sense RNA; gene transfection; RNase protection assay; Western blot
近年来,发现HSP90与肿瘤的关系比较密切[1~3]。HSP90α可通过调节细胞周期促进细胞增殖,HSP90β能够抑制细胞凋亡与分化[4,5],且最近有人报道HSP90β与P-gp的表达有关[6]。本研究拟用HSP90β反义核酸转染人4株消化系肿瘤细胞系,以建立HSP90β蛋白低调细胞系, 为进一步研究HSP90β对肿瘤细胞的生物学意义提供实验材料,并研究HSP90β蛋白对消化系肿瘤细胞生长的影响。
1 材料与方法
1.1 材料
人胃癌细胞系SGC7901, 人胃癌多药耐药细胞系SGC7901/VCR, 人肝癌细胞系HCC7402, 人食道癌细胞系Ec109。HSP90β反义核酸重组子pcDNA-HSP90由刘宪玲等[7]构建。 pcDNA 3.1(+)由美国扬静华提供。主要试剂(略)。
, http://www.100md.com
1.2 方法
1.2.1 重组质粒的转染及阳性克隆的筛选
实验组转染pcDNA-HSP90, 空载体对照组转染pcDNA3.1(+), SGC7901,SGC7901/VCR,HCC7402,Ec109细胞作为相应的空白对照组。碱裂解法提取重组质粒pcDNA-HSP90。用Lipofectamine介导基因的转染(按说明书进行),G418(400 μg/ml)进行抗性筛选。3~4周后见抗性细胞集落形成,挑选细胞克隆,用含100 μg/ml G418的10%FBS-PRMI 1640液扩大培养。
1.2.2 RNA酶保护分析法检测基因转染细胞HSP90反义核酸的表达[9]
从HSP90β cDNA序列的第1 641 bp起,读取30个bp作为探针,送上海生物工程公司合成。末端标记法标记寡核苷酸探针[8]。提取RNA同时做含量测定后,取RNA 10 μg, 加1.0×105 cpm的[γ-32P]标记的寡核苷酸探针及β-actin探针,加无水乙醇、糖原、3 mol/L 乙酸钠,于-20℃放置20 min,离心、乙醇洗涤、真空干燥,加30 μl甲酰胺杂交缓冲液重悬;85℃ 变性5~10 min,37℃杂交过夜。 加RNase S1 buffer 2 μl, 水16 μl, RNase S1 2 μl(2 μg/ml), 37℃消化1 h;乙醇沉淀;加20 μl终止液(10%SDS, 20 mg/ml 蛋白酶κ)37℃ 15 min;酚/氯仿抽提、乙醇沉淀、真空干燥;重溶于10 μl RNA 上样缓冲液中,上样,做18%聚丙烯酰胺/尿素凝胶电泳(200 v, 120 min)和放射自显影。
, 百拇医药
1.2.3 Western blot检测基因转染细胞HSP90β蛋白的表达
用三去污剂裂解缓冲液裂解细胞,获取细胞裂解液经蛋白质定量后行SDS-PAGE,电转膜及免疫印迹。山羊抗人HSP90β一抗(1∶100)室温作用2 h;辣根过氧化酶标记的驴抗山羊IgG(1∶500)室温作用1 h;PBS洗涤,四氯萘酚显色并拍照。用Quantimet 570 (Germany, Leica Inc.) 图象分析仪(QUIC图象系统)对免疫印迹结果进行半定量分析。条带的染色强度以灰度值表示(256级灰度,条带越深,灰度值越小)。
1.2.4 转染细胞的形态和生长速度观察
分别取基因转染细胞及其相应的亲本细胞(细胞浓度为1×104/孔,每孔2 ml体积)接种于24孔板,常规培养,观察细胞形态及生长状况,绘制细胞生长曲线。并按Patterson公式计算细胞在对数生长期的倍增时间。Td = T*lg2/lg(Nt/N0)。其中Td为细胞倍增时间(h),T为细胞由N0增至Nt所需时间(h)。
, 百拇医药
2 结 果
2.1 G418筛选出的阳性克隆
pcDNA-HSP90转染SGC7901,SGC7901/VCR,HCC-7402及Ec109细胞后,筛选出其相应的阳性克隆,被分别命名为AH-SGC7901,AH-SGC7901/VCR,AH-HCC74O2及AH-Ec109。空载体pcDNA转染细胞被命名为SGC7901-pcDNA,SGC7901/VCR-pcDNA,HCC7402-pcDNA及Ec109-pcDNA。
2.2 RNA酶保护分析法 结果见图1。

图1 RNA酶保护分析法检测HSP90反义RNA转染细胞、空载体转染细胞
及其亲本细胞中HSP90反义RNA的表达
, http://www.100md.com
Fig. 1 The expression of anti-sense RNA of HSP90 in pcDNA-HSP90 transfected cell lines, pcDNA transfected
cell lines and their parental cell lines by RNase protection assay
M: PBR322 DNA/HaeⅢ Marker; C1: Positive control,β-actin(20 bp) and HSP90 probe (30 bp); C2: Negative control, probe plus
RNase S1, no RNA. 1: AH-SGC7901/VCR; 2: SGC7901-pcDNA/VCR; 3: SGC7901/VCR; 4: AH-SGC7901; 5: SGC7901-pcDAN;
, http://www.100md.com
6: SGC7901; 7: AH-HCC7402; 8: HCC7402-pcDNA; 9: HCC7402; 10: AH-Ec109; 11: Ec109-pcDNA; 12: Ec109
HSP90β反义核酸转染细胞AH-SGC7901/VCR(1),AH-SGC7901(4),AH-HCC7402(7)及AH-Ec109(10)组有两条电泳带,依据分子量Marker,可确定它们分别为β-actin内参照及HSP90 反义RNA;转染pcDNA3.1(+)组及空白对照组可见1条带为β-actin。表明pcDNA-HSP90已转染入细胞,并有HSP90β反义RNA的表达。
2.3 HSP90β反义核酸转染细胞HSP90β蛋白低调
Western blot 结果见图2。用Quanuimet 570 图象分析仪进行分析,结果见表1。
, http://www.100md.com
pcDNA-HSP90转染细胞系HSP90β蛋白的表达明显低于其亲本细胞系及其空白对照细胞系。

图2 pcDNA-HSP90转染细胞HSP90β蛋白的表达
Fig. 2 The expression of HSP90β protein in pcDNA-HSP90 transfected cell lines
1: SGC7901; 2: SGC7901-pcDNA; 3:AH-SGC7901; 4: SGC7901/VCR; 5: SGC7901/VCR-pcDNA;
6: AH-SGC7901/VCR; 7: HCC7402; 8: HCC7402-pcDNA; 9: AH-HCC7402; 10: Ec109; 11: Ec109-pcDNA; 12: AH-Ec109
, 百拇医药
表1 基因转染细胞及其对照细胞
Hsp90β蛋白表达的半定量分析
Tab. 1 The grey scales of HSP90β in pcDNA-HSP90
transfected cell lines and their parental cell lines Cell lines
Grey scales
P
1.SGC7901
61.44±2.45
2.SGC7901-pcDNA
, 百拇医药
61.15±3.33
3.AH-SGC7901
83.17±2.89
P<0.05△
4.SGC7901/VCR
37.52±3.67
5.SGC7901/VCR-pcDNA
38.91±3.31
6.AH-SGC7901/VCR
80.50±3.60
P<0.05▲
, 百拇医药
7.HCC7402
93.47±3.41
8.HCC7402-pcDNA
89.13±3.51
9.AH-HCC7402
156.8±2.75
P<0.05□
10.Ec109
81.75±4.02
11.Ec109-pcDNA
81.21±3.26
, 百拇医药
12.103.21±4.24
103.21±4.24
P<0.05■
△ 3 vs 1,2; ▲ 6 vs 4,5; □ 9 vs 7,8; ■ 12 vs 10, 11
2.4 转染细胞的生长曲线
基因转染后的AH-SGC7901,AH-SGC7901/VCR, AH-HCC7402及AH-Ec109细胞与其相应的亲本细胞SGC7901, SGC7901/VCR, HCC7402及Ec109相比,细胞生长受到不同程度的抑制(见图3)。
由细胞生长曲线求得各细胞倍增时间Td,AH-SGC7901,AH-SGC7901/VCR, AH-HCC7402及AH-Ec109细胞的Td较其亲本细胞分别延长了1.12 h,16.69 h,2.74 h及15.97 h。可见 AH-SGC7901/VCR细胞及AH-Ec109细胞的倍增时间Td较其相应的亲本细胞的Td明显延长 (P<0.05), AH-SGC7901及AH-HCC7402细胞较其相应的亲本细胞的Td改变不明显 (P>0.05)。AH-SGC7901,AH-SGC7901/VCR, AH-HCC7402及AH-Ec109细胞与其相应的亲本细胞相比,他们在第10天的抑制率分别为24.28%, 27.58%, 10.51%及66.91%。
, 百拇医药
3 讨 论
依据反义核酸技术的原理,我们构建成HSP90β反义核酸重组子pcDNA-HSP90[7]。并转染SGC7901,SGC7901/VCR,HCC7402及Ec109细胞,用G418进行抗性筛选,挑选出相应的阳性克隆AH-SGC7901, AH-SGC7901/VCR, AH-HCC7402及AG-Ec109。
我们用RNA酶保护分析方法鉴定经G418筛选出的克隆是否有HSP90β反义RNA的表达,RNase保护分析的原理[9,10]为, 将标记的寡核苷酸探针与细胞总RNA或mRNA杂交,再用RNase S1消化单链未杂交的RNA,则杂交的双链被保护不被RNase S1消化。经丙烯酰胺/尿素凝胶电泳可分离出来,放射自显影后可显示杂交的条带;通过标准分子量marker可确定其大小。此方法的特异性及敏感性远远超过Northern杂交,且较Northern blot 简单, 较Dot blot精确。RNA酶保护分析结果表明,pcDNA-HSP90转染细胞有HSP90β反义RNA的表达。
, http://www.100md.com
Western blot检测结果表明,与亲本细胞及转染空载体的细胞相比, HSP90β反义核酸转染细胞AH-SGC7901,AH-SGC7901/VCR,HCC7402及Ec109 HSP90β蛋白的表达明显减低, 说明HSP90β反义RNA对HSP90βmRNA有部分封闭作用, 从而使其翻译为HSP90β蛋白减少。
通过对转染细胞生长曲线的研究发现,基因转染细胞的生长受到不同程度的抑制,其中AH-SGC7901/VCR细胞及AH-Ec109细胞受抑程度更明显。热休克蛋白HSP90β为细胞内的主要分子伴侣蛋白,参与蛋白质的装配、折叠与成熟,稳定蛋白质的构象,本研究表明HSP90β对肿瘤细胞的生长具有一定的作用。降低HSP90β蛋白的表达可抑制消化系肿瘤细胞的生长。提示可通过抑制HSP90β蛋白的表达而抑制肿瘤细胞的生长。

图3 pcDNA-HSP90转染细胞的生长曲线(A,B,C,D)
, 百拇医药
Fig. 3 The growth curve of pcDNA-HSP90 transfected cell lines (A,B,C,D)
总之,HSP90β反义核酸重组子pcDNA-HSP90转染的 AH-SGC7901,AH-SGC7901/VCR,AH-HCC7402及AH-Ec109细胞,均有HSP90β反义RNA的表达,且部分封闭了HSP90β蛋白的表达,此为进一步研究HSP90β对消化系肿瘤细胞的生物学作用建立了细胞模型。
国家自然科学基金第39570806号及国家杰出青年基金第3952020号资助
刘宪玲,女,36岁,主治医师,讲师博士
参 考 文 献
1,Jameel A, Skilton RA, Campbell TA, et al. Clinical and biological significance of HSP90α in human breast cancer. Int J Cancer, 1992, 50: 409
, 百拇医药
2,Mileo AM, Fanuele M, Battaglia F, et al. Selective overexpression of mRNA coding for 90 kDa stress protein in human overian cancer. Anticancer Res, 1990, 10: 903
3,Nanbu K, Konshi I, Komatsu T, et al. Expression of heat shock proteins HSP70 and HSP90 in endometrial carcinomas. Cancer, 1996, 77: 330
4,Yano M, Naito Z, Tanaka S, et al. Expression and roles of heat shock proteins in human breast cancer. Jpn J Cancer Res, 1996, 87: 908
, 百拇医药
5,Yamada T, Nakamura R, Kido K, et al. Function of hsp90 in differentiation and apoptosis of human EC cells. Trans Soc Pathol Jpn, 1995, 84: 217
6,Bertram J, Palfner K, Hiddemann W, et al. Increase of P-glycoprotein-mediated drug resistance by hsp90 beta. Anticancer Drug, 1996, 7: 838
7,刘宪玲, 肖 冰, 俞召才, 等. HSP90β反义RNA真核表达载体pcDNA-HSP90的构建与鉴定. 细胞与分子免疫学杂志, 1999, 15: 207
8,姜 泊, 张亚历, 周殿元 主编. 分子生物学常用实验方法. 北京: 人民军医出版社, 1995. 42
9,Lau ET, Kong RY, Cheah KSE. A critical assessment of the RNase protection assay as a means of determining exon sizes. Anal Biochem, 1993, 209: 360
10,萨姆布鱼克 J, 弗里奇 EF, 曼尼阿蒂斯 T. 分子克隆实验指南. 金冬雁,黎孟枫 等译. 第2版, 北京: 科学出版社, 1995. 374
(1999-07-14收稿; 1999-10-03修回), 百拇医药