жизщЦЯМЄУИЭЛБфЬх(r-SAKІЄN)ЕФДПЛЏ
зїепЃКвЖСЂЮФ ШЮ Оќ ЫЮКѓбр
ЕЅЮЛЃКЩЯКЃвНПЦДѓбЇЗжзгвХДЋбаОПЪвЃЌЩЯКЃ 200032
ЙиМќДЪЃКЦЯМЄУИЭЛБфЬхЃЛАќКЬхЃЛИДадЃЛДПЛЏ
еЊ вЊ жизщЦЯМЄУИЭЛБфЬхЛљвђдкДѓГІИЫОњжаИпаЇБэДя
еЊ вЊ жизщЦЯМЄУИЭЛБфЬхЛљвђдкДѓГІИЫОњжаИпаЇБэДяЃЌВњЮявдАќКЬхЕФаЮЪНДцдкгкАћНЌжаЁЃЭЈЙ§ЗЂНЭЃЌРЉдіЙЄГЬОњЃЌЛњаЕЦЦОњЃЌРыаФЗжРыДжжЦАќКЬхЃЌКѓепОДПЛЏКѓгУбЮЫсывШмНтЃЌr-SAKІЄNЗжзгИДадКѓгУРызгНЛЛЛВуЮіКЭЗжзгЩИЭббЮЃЌДПЖШДя97%ЃЌБШЛюад5ЁС104HU/mgЃЌMr14000ЃЌЕШЕчЕуЮЊpH6.8ЁЃ
Purificaion of Recombinant Staphylokinase Mutant(r-SAKІЄN)
, АйФДвНвЉ
Ye Liwen, Ren Jun, Song Houyan
(Department of Molecular Genetics, Shanghai Medical University, Shanghai 200032)
Abstract Recombinant staphylokinase mutant (r-SAKІЄN) was efficientl y ex pressed in E. coli in the form of inclusion body. By the methods of fermen tation, inclusion body extraction, refolding of r-SAKІЄN molecular, Q-seph aros e FF ion-exchange chromatography and gel filtration of Sephadex G-25. The pur ity of r-SAKІЄN was reached 97% and with specific activity 5ЁС104 HU/mg. The Mr and isoelectro point were 14000 and pH6.8 respectively.
, АйФДвНвЉ
Key Words r-Staphylokinase mutant (r-SAKІЄN), Inclusion body, Purification
ЦЯМЄУИ(Staphylokinase)ЪЧгЩФГаЉИаШОШмдадЪЩОњЬхЕФН№ЛЦЩЋЦЯЬбЧђОњВњЩњЕФЭтЗжУкЕААзЃЌгЩ136ИіАБЛљЫсзщГЩЃЌMr15500ЁЃЦЯМЄУИгыЯЫШмУИдНсКЯКѓзЊЛЏЮЊЦЯМЄУИЯЫШмУИИДКЯЮяЃЌОпгаМЄЛюЯЫШмУИдЕФФмСІЁЃдкЬхФкгаЯЫЮЌЕААзДцдкЪБЃЌЦЯМЄУИЖдШЫЯЫШмУИдЕФМЄЛюзїгУОпгаЯЫЮЌЕААзЬивьадЃЌвђДЫЦЯМЄУИПЩЭћПЊЗЂГЩаТвЛДњИпаЇЬивьШмЫЈвЉЮя[1]ЁЃЦЯМЄУИЗжзгСПНЯаЁЃЌЪЧНЯЮЊРэЯыЕФбаОПЕААзжЪНсЙЙгыЙІФмЕФВФСЯЁЃАДееНсЙЙгыЙІФмЕФЙиЯЕЩшМЦЭЛБфЬхЗжзгЃЌЭЈЙ§ЕААзжЪЙЄГЬЃЌПЊЗЂГіаТЕФШмЫЈвЉЮяЁЃCollenЕШЖдЦЯМЄУИЗжзгжаЖрИіДјЕчКЩЕФЯрСкАБЛљЫсЭЛБфЮЊБћАБЫсЃЌВЂЖдИїЭЛБфЬхгывАЩњаЭЦЯМЄУИадФмНјааСЫБШНЯЃЌБэУїЗжзгжаВПЗжАБЛљЫсЭЛБфФмИФБфЦЯМЄУИЕФадФмЁЃЮвУЧРћгУPCRММЪѕвдБОбаОПЪвПЫТЁЕФвАЩњаЭЦЯМЄУИЛљвђЮЊФЃАх[2]РЉдіN-ФЉЖЫШБЪЇ18ИіАБЛљЫсЕФЦЯМЄУИЭЛБфЬхЛљвђЃЌдкДѓГІИЫОњжаЕУЕНСЫИпаЇБэДяЃЌБэДяВњЮяаЮГЩСЫАќКЬх[3]ЁЃБОЮФБЈИцСЫИУЭЛБфЬхЛљвђБэДяВњЮя(r-SAKІЄN)ЕФЬсШЁЁЂИДадЁЂДПЛЏЗНЗЈЃЌвдМАИУЭЛБфЬхЕФВПЗжЬиадЁЃ
, АйФДвНвЉ
1 ВФСЯМАЩшБИ
1.1 жизщЦЯМЄУИШБЪЇЭЛБфЬх(r-SAKІЄN)ИпаЇБэДяОњжъ
ЮЊБОЪвЙЙНЈЃЌКЌЭЛБфЬхЛљвђЃЌPRЃЌPLЦєЖЏзгЃЌClts857зшвжЕААзЛљвђЃЌ5sRNAt1t2жежЙаХКХЕїПиЁЃr-SAKІЄNБэДяЫЎЦНеМОњЬхзмЕААзЕФ32%вдЩЯЁЃ
1.2 ЪдМС
РвЕААзЫЎНтВњЮяЃЌЕШЕчОлНЙБъзМpHЕААзЃЌОљЙКздSigmaЙЋЫОЁЃЦЯЬбЬЧЃЌЮоЛњбЮЃЌАБЫЎЃЌАБмаЧрУЙЫиЃЌбЮЫсСђАЗЫиЕШОљЮЊЗћКЯвЉгУБъзМЕФЙњВњЪдМСЁЃЯЫШмУИдКЭЭУПЙSAKПЙЬхЃЌгЩБОЪвжЦБИЁЃРБИљЙ§бѕЛЏЮяУИБъМЧЕФбђПЙЭУПЙЬхКЭЖўАБЛљСЊБНАЗЙКздЛЊУРЙЋЫОЁЃдиЬхСНадЕчНтжЪ(pH3.5ЁЋ10)ЮЊЩЯКЃРіжщЖЋЗчЩњЮяММЪѕгаЯоЙЋЫОВњЦЗЁЃ
, http://www.100md.com 1.3 вЧЦї
ЗЂНЭЙоЃЌУРЙњNBSЙЋЫОГіЦЗЃЌBiofloЂѓ 5LЁЃSemi-dry transfer cell,ЕААзДПЛЏEconoЯЕ ЭГЃЌЙКздУРЙњBio-RadЙЋЫОЁЃ
Image Master МАЩЋЦзЬюСЯSephadex G25, Q-Sepharose FFЮЊPharmacia BiotechВњЦЗЁЃ
2 ЗН ЗЈ
2.1 SDS-PAGEЕчгО
АДSambrookЗНЗЈ[4]ЃЌЗжРыНКХЈЖШ15%ЃЌПМТэЪЯССРЖШОЩЋЁЃ
2.2 ЕААзЖЈСПВтЖЈ
АДLowryЗгЪдМСЗЈЁЃ
, АйФДвНвЉ
2.3 ЗЂНЭ
жжзгОњгУLBХрбјЛљдквЁЦПжаНјааЖўМЖЗХДѓХрбјЃЌХрбјЮТЖШЮЊ30ЁцЁЃЖўМЖЗХДѓКѓНЋжжзгОњвКМгШыИФСМЕФM9ХрбјЛљжаЃЌдкЗЂНЭЙожаХрбјЁЃдкЗЂНЭХрбјЙ§ГЬжаЃЌИїжжВЮЪ§гЩЮЂЛњздЖЏПижЦЃЌpHПижЦдк6.8ЃЌгЩАБЫЎЕїећЃЛШмбѕПижЦгк60%ЃЌ30ЁцХрбј5hЃЌЯИОњУмЖШДя3ЁЋ5ODКѓЩ§ЮТжС42ЁцЃЌЮТЖШгеЕМХрбј3hКѓ5000r/min10minРыаФЪеОњЁЃдкХрбјЙ§ГЬжаЃЌВЙГфРвЕААзЫЎНтЮяКЭЦЯЬбЬЧЁЃ
2.4 АќКЬхжЦБИМАДПЛЏ
НЋРыаФЫљЪеОњгУPBSЯДЕг1ДЮЃЌРыаФЃЌ5000r/min10min,4ЁцЃЌдйНЋОњаќИЁгк4ЁцPBSжаЃЌгУИпбЙдШНЌБУЦЦОњЃЌ35MPaЁЃ5000r/min10min4ЁцРыаФЪеМЏГСЕэЃЌЭЌбљЛКГхвКЯДЕгГСЕэЃЌЪеМЏЯДЕгКѓЕФАќКЬхЃЌ-70ЁцБИгУЁЃгУSDS-PAGEЕчгОЃЌПМТэЪЯССРЖШОЩЋКѓImageMasterЩЈУшМьВтЯДЕгЧАКѓАќКЬхжаr-SAKІЄNЕФДПЖШЁЃ
, http://www.100md.com
2.5 r-SAKІЄNАќКЬхШмНтЁЂИДадгыДПЛЏ
ДПЛЏКѓЕФАќКЬхгУ6mol/LбЮЫсыввд1ЁУ20ШмНтЃЌЪвЮТЗХжУ1hЃЌРыаФ10000r/min30minЃЌНЋЩЯЧхжУЭИЮіДќжаЃЌвд0.05mol/LpH7.4PBЗжВНЭИЮіЃЌЙВ48hЃЌ4ЁцЁЃРыаФ10000r/min3minЃЌНЋЩЯЧхЯЁЪЭ50БЖЃЌ4ЁцЙ§вЙЃЌИДадКѓЕФбљЦЗвд4ml/minЫйЖШЩЯQ-Sepharose FFжљЃЌжљЬхЛ§2cmЁС20cmЃЌгУЩЯЪіPBЛКГхвКЯДжљКѓгУ0ЁЋ1mol/LNaClЬнЖШЯДЭбЃЌЪеМЏКЌr-SAKІЄNЛюадВПЗжЃЌОХЈЫѕКѓгУSephadexG-25ЗжзгЩИНјвЛВНДПЛЏВЂЭббЮЁЃжљЬхЛ§2.5cmЁС80cmЃЌСїЫй2ml/minЁЃ
ЪеМЏКЌr-SAKІЄNВПЗжЃЌВЂгУSDS-PAGE,Image MasterЩЈУшЗжЮіЃЌМјЖЈДПЖШЁЃ
2.6 ЛюадВтЖЈЃЌЗжзгСПВтЖЈЃЌУтвпЗДгІадМјЖЈЃЌЕШЕчЕуВтЖЈ
, http://www.100md.com ЛюадВтЖЈВЩгУРвЕААзАхШмШІЗЈЃЌЦЯМЄУИБъзМЦЗДгжаЙњЩњЮяжЦЦЗМјЖЈЫљЙКТђЁЃ
ЗжзгСПМАУтвпЗДгІадМјЖЈЃКбљЦЗОSDS-PAGEКѓЧаЮЊСНАыЃЌЗжБ№вдПМТэЪЯССРЖШОЩЋКЭзЊвЦЕНPVDFФЄЃЌАДSambrookЗЈ[5]ЃЌНјааWestern blotЁЃЕквЛПЙЬхЮЊЭУПЙSAKЃЌЕкЖўПЙЬхЮЊРБИљЙ§бѕЛЏЮяУИБъМЧЕФбђПЙЭУПЙЬхЃЌЯдЩЋЕзЮяЮЊЖўАБЛљСЊБНАЗЁЃ
ЕШЕчОлНЙЕчгОЃКАДЗНЗЈ[6]ЁЃ
3 Нс Йћ
3.1 ЗЂНЭ
5LЗЂНЭЙоЗЂНЭЯИОњЩњГЄЧњЯпМћЭМ(1)ЃЌУПИє0.5hШЁбљЦЗвЛДЮЃЌНјааSDS-PAGEКЭlmage MasterЩЈУшЃЌМьВтr-SAKІЄNеМОњЬхзмЕААзЕФАйЗжБШЃЌШЗЖЈr-SAKІЄNБэДяЧњЯпМћЭМ(2)ЁЃЗЂНЭНсЪјКѓРыаФЪеЪЊОњ90gЁЃ
, http://www.100md.com
Fig 1 Fermentation process of E. coli harboring pEMN
Fig 2 Expression of r-SAKІЄN in fermentation process
3.2 ЦЦОњМААќКЬхДПЛЏ
гУЕЭЩјPBаќИЁБэДяОњЃЌИпбЙдШНЌБУдШНЌКѓЃЌОЙтбЇЯдЮЂОЕМьВщЦЦОњТЪДѓгк95%ЁЃРыаФЪеМЏГСЕэЃЌМДЮЊДжжЦЪЊАќКЬхдМ10gЁЃАќКЬхОЯДЕгДПЛЏЃЌЕУДПЛЏЕФАќКЬхдМЮЊ8gЁЃАќКЬхЯДЕгЧАКѓSDS-PAGEНсЙћМћЭМ(3)ЃЌImage MasterЗжЮіr-SAKІЄNДПЖШгЩ68%діМгЕН81%ЁЃ

, АйФДвНвЉ
A Marker (ЁС103)
B Inclusion body before washing
C Inclusion body after washing
D r-SAKІЄNafter renaturation
E r-SAKІЄNafter Q-Sepharose FF chromatography
F r-SAKІЄNafter Sephadex G-25 chromatography
Fig 3 SDS-PAGE analysis r-SAKІЄN in process of purification
, http://www.100md.com
3.3 r-SAKІЄNИДадЃЌДПЛЏМАЦфЬиадМьВт
ДѓГІИЫОњБэДяЕФr-SAKІЄNвдЮоЛюадЕФАќКЬхДцдкЃЌОШмНтКЭИДадДІРэКѓВХБэЯжЛюадЁЃМћБэ1ЁЃ
Tab 1 Purification of r-SAK-ІЄN
Weight
(gram)
Protein
(mg)
Total
activity
Specific
, http://www.100md.com activity
Purity
(%)
Bacteria
90
11000
-
-
32
Inclusion body
10
3310
-
, АйФДвНвЉ
-
68
Purified inclusion body
8
2100
-
-
81
Refolded protein
1000
4ЁС107
4ЁС104
, АйФДвНвЉ
88
After Q-sepharose
320
1.47ЁС107
4.6ЁС104
96
After gel filtration
288
1.44ЁС107
5ЁС104
97
, http://www.100md.com
Purity: ratio of r-SAK-ІЄN to total bacteria protein
ДПЛЏЙ§ГЬИїВНВњЮяЕФSDS-PAGEЕчгОЭММћЭМ(3.4.5)ЁЃДПЖШЗжБ№ЮЊ88%ЃЌ96%КЭ97%ЃЛБШЛюадЗжБ№ЮЊ4.0ЁС104ЃЌ4.6ЁС104КЭ5ЁС104HU/mgЁЃ
Fig 4 Q-Sepharose FF chromatography of r-SAKІЄN
, http://www.100md.com
A Marker;B r-SAKІЄN;C Westen Blot
Fig 5 Gel filtration of r-SAKІЄN on Sephadex G-25
Western bolt:r-SAKІЄNгыr-SAKгаЯрЭЌЕФУтвпадЃЌМћЭМ(6)ЃЌФ§НКЕШЕчОлНЙНсЙћМћЭМ(7)ЃЌr-SAKІЄNЕФЕШЕчЕуЮЊpH6.8ЁЃ

Fig 6 Western blot identify the purified r-SAKІЄN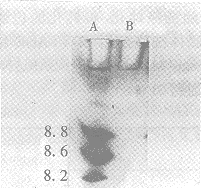

, АйФДвНвЉ
Fig 7 Isoelectrophoresis of purified r-SAKІЄN
4 Ьж Тл
1995ФъБОбаОПЪвГЩЙІЕиЭъГЩСЫвАЩњаЭrSAKЕФПЫТЁКЭдкДѓГІИЫОњжаЕФИпаЇБэДявдМАВњЮяЕФЗжРыКЭДПЛЏ[7ЁЋ9]ЁЃвАЩњаЭr-SAKдкДѓГІИЫОњжаЕФБэДяГЪПЩШмЁЂЛюадзДЬЌЃЌДцдкгкАћНЌжаЁЃЮЊСЫбаОПSAKЕФНсЙЙгыЙІФмЕФЙиЯЕЃЌЮвУЧПЫТЁСЫN-ЖЫШБЪЇ18ИіАБЛљЫсЕФЭЛБфЬхЛљвђЃЌВЂгУЭЌбљЕФдиЬхPLY-4ЙЙНЈСЫБэДяжЪСЃЃЌгывАЩњаЭЛљвђЕФБэДяВЛЭЌЃЌЦфБэДяВњЮяаЮГЩАќКЬхЃЌr-SAKІЄNБиаыИДадКѓВХФмбаОПЫќЕФЬиадЃЌашвЊДДНЈвЛЬзВЛЭЌгквАЩњаЭr-SAKЕФаТЕФДПЛЏЗНЗЈЁЃжизщЦЯМЄУИШБЪЇЭЛБфЬхЛљвђЁЃдкPLЃЌPRЦєЖЏзгCIts857ОЕїПиКЭЮТЖШгеЕМФмдкДѓГІИЫОњжаИпаЇБэДяr-SAKІЄNЃЌБэДяЫЎЦНЮЊ32ЁЋ38%ЁЃвРЭМ(1)КЭЭМ(2)ПЩжЊЮТЖШгеЕМ1.5hКѓБэДяСПвбНгНќзюИпжЕЁЃЕЋОњЬхзмСПШддкдіМгЃЌжБжС3hвдКѓВХМѕТ§ЃЌЫљвдЮвУЧдкЮТЖШгеЕМ3hКѓЪеОњЃЌаЇТЪзюИпЁЃгУИпбЙдШНЌЗЈЦЦОњЃЌЦЦОњаЇТЪДя95%вдЩЯЁЃВЩгУ6mol/LбЮЫсывШмНтАќКЬхЃЌгаРћгкБЃЛЄжизщЕААзжЪЁЃr-SAKNЕФИДадЪЧвЛИіЛКТ§Й§ГЬЃЌдкЭИЮіМАВуЮіЙ§ГЬжаБШЛюадОљгаЩЯЩ§ЃЌБэУїБфадЕФЕААзжЪж№НЅЛжИДе§ГЃелЕўЁЃЭЈЙ§ИДадЃЌr-SAKІЄNЕФДПЖШгжЕУЕНСЫНјвЛВНЕФЬсИпЁЃЭЈЙ§вЛДЮРызгНЛЛЛДПЖШПЩДя96%ЁЃБОбаОПЯдЪОSAKЕФN-ЖЫ18ИіАБЛљЫсгыБэДяЙ§ГЬжаЕААзжЪЕФелЕўгаЙиЃЌШБЪЇЕФАБЛљЫсжаКЌгаЖрИіРЕАБЫсађСагАЯьr-SAKІЄNдкОњЬхжаелЕўЮЊЛюадЙЙЯѓЁЃОЙ§бЮЫсывШмНтЃЌИДадМАРызгНЛЛЛКЭФ§НКЙ§ТЫЃЌДПЛЏЕФr-SAKІЄNБШЛюадЮЊ5ЁС104IU/mgЃЌMrЮЊ14000ЃЌЕШЕчЕуpH6.8ЁЃЮвУЧНЈСЂЕФДПЛЏЗНЗЈВйзїМђЕЅЃЌЩЯбљЖрЃЌДПЖШИпЃЌЮЊвдКѓSAKЕААзжЪЙЄГЬбаОПМАЦфЫќЭЛБфЬхЕФДПЛЏДђКУСЫЛљДЁЁЃгЩгкЗжзгСПЕЭЃЌШєФмЩшЗЈНЕЕЭЭЛБфЬхЗжзгЕФУтвпдадЃЌдђПЩФмжЦГЩr-SAKІЄNПкЗўжЦМСЃЌгУгкЗРжЮаФМЁЙЃШћКЭФдЙЃШћЕШЁЃ
, АйФДвНвЉ
ВЮПМЮФЯз
1 Vanderschueren S, Barrios L, Kerdsinchat P, et al. A randomized trial of recombinant staphylokinase versus alteplase for coronary artery patency in acute myocardial infarction. Circulation, 1995ЃЌ92ЁУ2044
2 вЖСЂЮФЃЌЬРЦфШКЃЌЫЮКѓбр.ЦЯМЄУИЭЛБфЬхЛљвђЕФПЫТЁгыБэДя.вЉЮяЩњЮяММЪѕЃЌ1999ЃЌ6(1)ЁУ9
3 Sambrook J, Fritsch EF, Maniatis T. Molecular cloning. 2nd. Cold spring ha rbor laboratory press 1989,18
, http://www.100md.com
4 Ding H, Zhu YS, Song HY, et al. Acta Academiae Medicinae. Shanghai. 19 92;19(Suppl)ЁУ38
5 ЬРЦфШКЃЌеХаЁшЏЃЌгкУєЃЌЕШ.жизщЦЯМЄУИ(r-SAK)ЕФЗжРыДПЛЏКЭНсОЇ.вЉЮяЩњЮя ММЪѕЃЌ1997ЃЌ4(1)ЁУ1
6 гкУєЃЌШЮОќЃЌЫЮКѓбрЃЌЕШ.зЂЩфгУжизщЦЯМЄУИЕФжаЪдбаОП.ИпММЪѕЭЈбЖ ЃЌ1998ЃЌ8(1)ЁУ45
7 ЫЮКѓбр.вЛжжжизщЦЯМЄУИЕФжЦБИЗНЗЈ.ZL94 1 12105.4
ЪеИхШеЦк:1998-05-22, АйФДвНвЉ
ЕЅЮЛЃКЩЯКЃвНПЦДѓбЇЗжзгвХДЋбаОПЪвЃЌЩЯКЃ 200032
ЙиМќДЪЃКЦЯМЄУИЭЛБфЬхЃЛАќКЬхЃЛИДадЃЛДПЛЏ
еЊ вЊ жизщЦЯМЄУИЭЛБфЬхЛљвђдкДѓГІИЫОњжаИпаЇБэДя
еЊ вЊ жизщЦЯМЄУИЭЛБфЬхЛљвђдкДѓГІИЫОњжаИпаЇБэДяЃЌВњЮявдАќКЬхЕФаЮЪНДцдкгкАћНЌжаЁЃЭЈЙ§ЗЂНЭЃЌРЉдіЙЄГЬОњЃЌЛњаЕЦЦОњЃЌРыаФЗжРыДжжЦАќКЬхЃЌКѓепОДПЛЏКѓгУбЮЫсывШмНтЃЌr-SAKІЄNЗжзгИДадКѓгУРызгНЛЛЛВуЮіКЭЗжзгЩИЭббЮЃЌДПЖШДя97%ЃЌБШЛюад5ЁС104HU/mgЃЌMr14000ЃЌЕШЕчЕуЮЊpH6.8ЁЃ
Purificaion of Recombinant Staphylokinase Mutant(r-SAKІЄN)
, АйФДвНвЉ
Ye Liwen, Ren Jun, Song Houyan
(Department of Molecular Genetics, Shanghai Medical University, Shanghai 200032)
Abstract Recombinant staphylokinase mutant (r-SAKІЄN) was efficientl y ex pressed in E. coli in the form of inclusion body. By the methods of fermen tation, inclusion body extraction, refolding of r-SAKІЄN molecular, Q-seph aros e FF ion-exchange chromatography and gel filtration of Sephadex G-25. The pur ity of r-SAKІЄN was reached 97% and with specific activity 5ЁС104 HU/mg. The Mr and isoelectro point were 14000 and pH6.8 respectively.
, АйФДвНвЉ
Key Words r-Staphylokinase mutant (r-SAKІЄN), Inclusion body, Purification
ЦЯМЄУИ(Staphylokinase)ЪЧгЩФГаЉИаШОШмдадЪЩОњЬхЕФН№ЛЦЩЋЦЯЬбЧђОњВњЩњЕФЭтЗжУкЕААзЃЌгЩ136ИіАБЛљЫсзщГЩЃЌMr15500ЁЃЦЯМЄУИгыЯЫШмУИдНсКЯКѓзЊЛЏЮЊЦЯМЄУИЯЫШмУИИДКЯЮяЃЌОпгаМЄЛюЯЫШмУИдЕФФмСІЁЃдкЬхФкгаЯЫЮЌЕААзДцдкЪБЃЌЦЯМЄУИЖдШЫЯЫШмУИдЕФМЄЛюзїгУОпгаЯЫЮЌЕААзЬивьадЃЌвђДЫЦЯМЄУИПЩЭћПЊЗЂГЩаТвЛДњИпаЇЬивьШмЫЈвЉЮя[1]ЁЃЦЯМЄУИЗжзгСПНЯаЁЃЌЪЧНЯЮЊРэЯыЕФбаОПЕААзжЪНсЙЙгыЙІФмЕФВФСЯЁЃАДееНсЙЙгыЙІФмЕФЙиЯЕЩшМЦЭЛБфЬхЗжзгЃЌЭЈЙ§ЕААзжЪЙЄГЬЃЌПЊЗЂГіаТЕФШмЫЈвЉЮяЁЃCollenЕШЖдЦЯМЄУИЗжзгжаЖрИіДјЕчКЩЕФЯрСкАБЛљЫсЭЛБфЮЊБћАБЫсЃЌВЂЖдИїЭЛБфЬхгывАЩњаЭЦЯМЄУИадФмНјааСЫБШНЯЃЌБэУїЗжзгжаВПЗжАБЛљЫсЭЛБфФмИФБфЦЯМЄУИЕФадФмЁЃЮвУЧРћгУPCRММЪѕвдБОбаОПЪвПЫТЁЕФвАЩњаЭЦЯМЄУИЛљвђЮЊФЃАх[2]РЉдіN-ФЉЖЫШБЪЇ18ИіАБЛљЫсЕФЦЯМЄУИЭЛБфЬхЛљвђЃЌдкДѓГІИЫОњжаЕУЕНСЫИпаЇБэДяЃЌБэДяВњЮяаЮГЩСЫАќКЬх[3]ЁЃБОЮФБЈИцСЫИУЭЛБфЬхЛљвђБэДяВњЮя(r-SAKІЄN)ЕФЬсШЁЁЂИДадЁЂДПЛЏЗНЗЈЃЌвдМАИУЭЛБфЬхЕФВПЗжЬиадЁЃ
, АйФДвНвЉ
1 ВФСЯМАЩшБИ
1.1 жизщЦЯМЄУИШБЪЇЭЛБфЬх(r-SAKІЄN)ИпаЇБэДяОњжъ
ЮЊБОЪвЙЙНЈЃЌКЌЭЛБфЬхЛљвђЃЌPRЃЌPLЦєЖЏзгЃЌClts857зшвжЕААзЛљвђЃЌ5sRNAt1t2жежЙаХКХЕїПиЁЃr-SAKІЄNБэДяЫЎЦНеМОњЬхзмЕААзЕФ32%вдЩЯЁЃ
1.2 ЪдМС
РвЕААзЫЎНтВњЮяЃЌЕШЕчОлНЙБъзМpHЕААзЃЌОљЙКздSigmaЙЋЫОЁЃЦЯЬбЬЧЃЌЮоЛњбЮЃЌАБЫЎЃЌАБмаЧрУЙЫиЃЌбЮЫсСђАЗЫиЕШОљЮЊЗћКЯвЉгУБъзМЕФЙњВњЪдМСЁЃЯЫШмУИдКЭЭУПЙSAKПЙЬхЃЌгЩБОЪвжЦБИЁЃРБИљЙ§бѕЛЏЮяУИБъМЧЕФбђПЙЭУПЙЬхКЭЖўАБЛљСЊБНАЗЙКздЛЊУРЙЋЫОЁЃдиЬхСНадЕчНтжЪ(pH3.5ЁЋ10)ЮЊЩЯКЃРіжщЖЋЗчЩњЮяММЪѕгаЯоЙЋЫОВњЦЗЁЃ
, http://www.100md.com 1.3 вЧЦї
ЗЂНЭЙоЃЌУРЙњNBSЙЋЫОГіЦЗЃЌBiofloЂѓ 5LЁЃSemi-dry transfer cell,ЕААзДПЛЏEconoЯЕ ЭГЃЌЙКздУРЙњBio-RadЙЋЫОЁЃ
Image Master МАЩЋЦзЬюСЯSephadex G25, Q-Sepharose FFЮЊPharmacia BiotechВњЦЗЁЃ
2 ЗН ЗЈ
2.1 SDS-PAGEЕчгО
АДSambrookЗНЗЈ[4]ЃЌЗжРыНКХЈЖШ15%ЃЌПМТэЪЯССРЖШОЩЋЁЃ
2.2 ЕААзЖЈСПВтЖЈ
АДLowryЗгЪдМСЗЈЁЃ
, АйФДвНвЉ
2.3 ЗЂНЭ
жжзгОњгУLBХрбјЛљдквЁЦПжаНјааЖўМЖЗХДѓХрбјЃЌХрбјЮТЖШЮЊ30ЁцЁЃЖўМЖЗХДѓКѓНЋжжзгОњвКМгШыИФСМЕФM9ХрбјЛљжаЃЌдкЗЂНЭЙожаХрбјЁЃдкЗЂНЭХрбјЙ§ГЬжаЃЌИїжжВЮЪ§гЩЮЂЛњздЖЏПижЦЃЌpHПижЦдк6.8ЃЌгЩАБЫЎЕїећЃЛШмбѕПижЦгк60%ЃЌ30ЁцХрбј5hЃЌЯИОњУмЖШДя3ЁЋ5ODКѓЩ§ЮТжС42ЁцЃЌЮТЖШгеЕМХрбј3hКѓ5000r/min10minРыаФЪеОњЁЃдкХрбјЙ§ГЬжаЃЌВЙГфРвЕААзЫЎНтЮяКЭЦЯЬбЬЧЁЃ
2.4 АќКЬхжЦБИМАДПЛЏ
НЋРыаФЫљЪеОњгУPBSЯДЕг1ДЮЃЌРыаФЃЌ5000r/min10min,4ЁцЃЌдйНЋОњаќИЁгк4ЁцPBSжаЃЌгУИпбЙдШНЌБУЦЦОњЃЌ35MPaЁЃ5000r/min10min4ЁцРыаФЪеМЏГСЕэЃЌЭЌбљЛКГхвКЯДЕгГСЕэЃЌЪеМЏЯДЕгКѓЕФАќКЬхЃЌ-70ЁцБИгУЁЃгУSDS-PAGEЕчгОЃЌПМТэЪЯССРЖШОЩЋКѓImageMasterЩЈУшМьВтЯДЕгЧАКѓАќКЬхжаr-SAKІЄNЕФДПЖШЁЃ
, http://www.100md.com
2.5 r-SAKІЄNАќКЬхШмНтЁЂИДадгыДПЛЏ
ДПЛЏКѓЕФАќКЬхгУ6mol/LбЮЫсыввд1ЁУ20ШмНтЃЌЪвЮТЗХжУ1hЃЌРыаФ10000r/min30minЃЌНЋЩЯЧхжУЭИЮіДќжаЃЌвд0.05mol/LpH7.4PBЗжВНЭИЮіЃЌЙВ48hЃЌ4ЁцЁЃРыаФ10000r/min3minЃЌНЋЩЯЧхЯЁЪЭ50БЖЃЌ4ЁцЙ§вЙЃЌИДадКѓЕФбљЦЗвд4ml/minЫйЖШЩЯQ-Sepharose FFжљЃЌжљЬхЛ§2cmЁС20cmЃЌгУЩЯЪіPBЛКГхвКЯДжљКѓгУ0ЁЋ1mol/LNaClЬнЖШЯДЭбЃЌЪеМЏКЌr-SAKІЄNЛюадВПЗжЃЌОХЈЫѕКѓгУSephadexG-25ЗжзгЩИНјвЛВНДПЛЏВЂЭббЮЁЃжљЬхЛ§2.5cmЁС80cmЃЌСїЫй2ml/minЁЃ
ЪеМЏКЌr-SAKІЄNВПЗжЃЌВЂгУSDS-PAGE,Image MasterЩЈУшЗжЮіЃЌМјЖЈДПЖШЁЃ
2.6 ЛюадВтЖЈЃЌЗжзгСПВтЖЈЃЌУтвпЗДгІадМјЖЈЃЌЕШЕчЕуВтЖЈ
, http://www.100md.com ЛюадВтЖЈВЩгУРвЕААзАхШмШІЗЈЃЌЦЯМЄУИБъзМЦЗДгжаЙњЩњЮяжЦЦЗМјЖЈЫљЙКТђЁЃ
ЗжзгСПМАУтвпЗДгІадМјЖЈЃКбљЦЗОSDS-PAGEКѓЧаЮЊСНАыЃЌЗжБ№вдПМТэЪЯССРЖШОЩЋКЭзЊвЦЕНPVDFФЄЃЌАДSambrookЗЈ[5]ЃЌНјааWestern blotЁЃЕквЛПЙЬхЮЊЭУПЙSAKЃЌЕкЖўПЙЬхЮЊРБИљЙ§бѕЛЏЮяУИБъМЧЕФбђПЙЭУПЙЬхЃЌЯдЩЋЕзЮяЮЊЖўАБЛљСЊБНАЗЁЃ
ЕШЕчОлНЙЕчгОЃКАДЗНЗЈ[6]ЁЃ
3 Нс Йћ
3.1 ЗЂНЭ
5LЗЂНЭЙоЗЂНЭЯИОњЩњГЄЧњЯпМћЭМ(1)ЃЌУПИє0.5hШЁбљЦЗвЛДЮЃЌНјааSDS-PAGEКЭlmage MasterЩЈУшЃЌМьВтr-SAKІЄNеМОњЬхзмЕААзЕФАйЗжБШЃЌШЗЖЈr-SAKІЄNБэДяЧњЯпМћЭМ(2)ЁЃЗЂНЭНсЪјКѓРыаФЪеЪЊОњ90gЁЃ

, http://www.100md.com
Fig 1 Fermentation process of E. coli harboring pEMN

Fig 2 Expression of r-SAKІЄN in fermentation process
3.2 ЦЦОњМААќКЬхДПЛЏ
гУЕЭЩјPBаќИЁБэДяОњЃЌИпбЙдШНЌБУдШНЌКѓЃЌОЙтбЇЯдЮЂОЕМьВщЦЦОњТЪДѓгк95%ЁЃРыаФЪеМЏГСЕэЃЌМДЮЊДжжЦЪЊАќКЬхдМ10gЁЃАќКЬхОЯДЕгДПЛЏЃЌЕУДПЛЏЕФАќКЬхдМЮЊ8gЁЃАќКЬхЯДЕгЧАКѓSDS-PAGEНсЙћМћЭМ(3)ЃЌImage MasterЗжЮіr-SAKІЄNДПЖШгЩ68%діМгЕН81%ЁЃ


, АйФДвНвЉ
A Marker (ЁС103)
B Inclusion body before washing
C Inclusion body after washing
D r-SAKІЄNafter renaturation
E r-SAKІЄNafter Q-Sepharose FF chromatography
F r-SAKІЄNafter Sephadex G-25 chromatography
Fig 3 SDS-PAGE analysis r-SAKІЄN in process of purification
, http://www.100md.com
3.3 r-SAKІЄNИДадЃЌДПЛЏМАЦфЬиадМьВт
ДѓГІИЫОњБэДяЕФr-SAKІЄNвдЮоЛюадЕФАќКЬхДцдкЃЌОШмНтКЭИДадДІРэКѓВХБэЯжЛюадЁЃМћБэ1ЁЃ
Tab 1 Purification of r-SAK-ІЄN
Weight
(gram)
Protein
(mg)
Total
activity
Specific
, http://www.100md.com activity
Purity
(%)
Bacteria
90
11000
-
-
32
Inclusion body
10
3310
-
, АйФДвНвЉ
-
68
Purified inclusion body
8
2100
-
-
81
Refolded protein
1000
4ЁС107
4ЁС104
, АйФДвНвЉ
88
After Q-sepharose
320
1.47ЁС107
4.6ЁС104
96
After gel filtration
288
1.44ЁС107
5ЁС104
97
, http://www.100md.com
Purity: ratio of r-SAK-ІЄN to total bacteria protein
ДПЛЏЙ§ГЬИїВНВњЮяЕФSDS-PAGEЕчгОЭММћЭМ(3.4.5)ЁЃДПЖШЗжБ№ЮЊ88%ЃЌ96%КЭ97%ЃЛБШЛюадЗжБ№ЮЊ4.0ЁС104ЃЌ4.6ЁС104КЭ5ЁС104HU/mgЁЃ

Fig 4 Q-Sepharose FF chromatography of r-SAKІЄN

, http://www.100md.com
A Marker;B r-SAKІЄN;C Westen Blot
Fig 5 Gel filtration of r-SAKІЄN on Sephadex G-25
Western bolt:r-SAKІЄNгыr-SAKгаЯрЭЌЕФУтвпадЃЌМћЭМ(6)ЃЌФ§НКЕШЕчОлНЙНсЙћМћЭМ(7)ЃЌr-SAKІЄNЕФЕШЕчЕуЮЊpH6.8ЁЃ


Fig 6 Western blot identify the purified r-SAKІЄN


, АйФДвНвЉ
Fig 7 Isoelectrophoresis of purified r-SAKІЄN
4 Ьж Тл
1995ФъБОбаОПЪвГЩЙІЕиЭъГЩСЫвАЩњаЭrSAKЕФПЫТЁКЭдкДѓГІИЫОњжаЕФИпаЇБэДявдМАВњЮяЕФЗжРыКЭДПЛЏ[7ЁЋ9]ЁЃвАЩњаЭr-SAKдкДѓГІИЫОњжаЕФБэДяГЪПЩШмЁЂЛюадзДЬЌЃЌДцдкгкАћНЌжаЁЃЮЊСЫбаОПSAKЕФНсЙЙгыЙІФмЕФЙиЯЕЃЌЮвУЧПЫТЁСЫN-ЖЫШБЪЇ18ИіАБЛљЫсЕФЭЛБфЬхЛљвђЃЌВЂгУЭЌбљЕФдиЬхPLY-4ЙЙНЈСЫБэДяжЪСЃЃЌгывАЩњаЭЛљвђЕФБэДяВЛЭЌЃЌЦфБэДяВњЮяаЮГЩАќКЬхЃЌr-SAKІЄNБиаыИДадКѓВХФмбаОПЫќЕФЬиадЃЌашвЊДДНЈвЛЬзВЛЭЌгквАЩњаЭr-SAKЕФаТЕФДПЛЏЗНЗЈЁЃжизщЦЯМЄУИШБЪЇЭЛБфЬхЛљвђЁЃдкPLЃЌPRЦєЖЏзгCIts857ОЕїПиКЭЮТЖШгеЕМФмдкДѓГІИЫОњжаИпаЇБэДяr-SAKІЄNЃЌБэДяЫЎЦНЮЊ32ЁЋ38%ЁЃвРЭМ(1)КЭЭМ(2)ПЩжЊЮТЖШгеЕМ1.5hКѓБэДяСПвбНгНќзюИпжЕЁЃЕЋОњЬхзмСПШддкдіМгЃЌжБжС3hвдКѓВХМѕТ§ЃЌЫљвдЮвУЧдкЮТЖШгеЕМ3hКѓЪеОњЃЌаЇТЪзюИпЁЃгУИпбЙдШНЌЗЈЦЦОњЃЌЦЦОњаЇТЪДя95%вдЩЯЁЃВЩгУ6mol/LбЮЫсывШмНтАќКЬхЃЌгаРћгкБЃЛЄжизщЕААзжЪЁЃr-SAKNЕФИДадЪЧвЛИіЛКТ§Й§ГЬЃЌдкЭИЮіМАВуЮіЙ§ГЬжаБШЛюадОљгаЩЯЩ§ЃЌБэУїБфадЕФЕААзжЪж№НЅЛжИДе§ГЃелЕўЁЃЭЈЙ§ИДадЃЌr-SAKІЄNЕФДПЖШгжЕУЕНСЫНјвЛВНЕФЬсИпЁЃЭЈЙ§вЛДЮРызгНЛЛЛДПЖШПЩДя96%ЁЃБОбаОПЯдЪОSAKЕФN-ЖЫ18ИіАБЛљЫсгыБэДяЙ§ГЬжаЕААзжЪЕФелЕўгаЙиЃЌШБЪЇЕФАБЛљЫсжаКЌгаЖрИіРЕАБЫсађСагАЯьr-SAKІЄNдкОњЬхжаелЕўЮЊЛюадЙЙЯѓЁЃОЙ§бЮЫсывШмНтЃЌИДадМАРызгНЛЛЛКЭФ§НКЙ§ТЫЃЌДПЛЏЕФr-SAKІЄNБШЛюадЮЊ5ЁС104IU/mgЃЌMrЮЊ14000ЃЌЕШЕчЕуpH6.8ЁЃЮвУЧНЈСЂЕФДПЛЏЗНЗЈВйзїМђЕЅЃЌЩЯбљЖрЃЌДПЖШИпЃЌЮЊвдКѓSAKЕААзжЪЙЄГЬбаОПМАЦфЫќЭЛБфЬхЕФДПЛЏДђКУСЫЛљДЁЁЃгЩгкЗжзгСПЕЭЃЌШєФмЩшЗЈНЕЕЭЭЛБфЬхЗжзгЕФУтвпдадЃЌдђПЩФмжЦГЩr-SAKІЄNПкЗўжЦМСЃЌгУгкЗРжЮаФМЁЙЃШћКЭФдЙЃШћЕШЁЃ
, АйФДвНвЉ
ВЮПМЮФЯз
1 Vanderschueren S, Barrios L, Kerdsinchat P, et al. A randomized trial of recombinant staphylokinase versus alteplase for coronary artery patency in acute myocardial infarction. Circulation, 1995ЃЌ92ЁУ2044
2 вЖСЂЮФЃЌЬРЦфШКЃЌЫЮКѓбр.ЦЯМЄУИЭЛБфЬхЛљвђЕФПЫТЁгыБэДя.вЉЮяЩњЮяММЪѕЃЌ1999ЃЌ6(1)ЁУ9
3 Sambrook J, Fritsch EF, Maniatis T. Molecular cloning. 2nd. Cold spring ha rbor laboratory press 1989,18
, http://www.100md.com
4 Ding H, Zhu YS, Song HY, et al. Acta Academiae Medicinae. Shanghai. 19 92;19(Suppl)ЁУ38
5 ЬРЦфШКЃЌеХаЁшЏЃЌгкУєЃЌЕШ.жизщЦЯМЄУИ(r-SAK)ЕФЗжРыДПЛЏКЭНсОЇ.вЉЮяЩњЮя ММЪѕЃЌ1997ЃЌ4(1)ЁУ1
6 гкУєЃЌШЮОќЃЌЫЮКѓбрЃЌЕШ.зЂЩфгУжизщЦЯМЄУИЕФжаЪдбаОП.ИпММЪѕЭЈбЖ ЃЌ1998ЃЌ8(1)ЁУ45
7 ЫЮКѓбр.вЛжжжизщЦЯМЄУИЕФжЦБИЗНЗЈ.ZL94 1 12105.4
ЪеИхШеЦк:1998-05-22, АйФДвНвЉ