β-淀粉样蛋白对大鼠脑神经细胞凋亡及白介素2表达的影响
作者:戴永萍 刘春风 包仕尧
单位:(215004 苏州医学院附属第二医院神经内科)
关键词:Alzheimer病;β淀粉样蛋白;细胞凋亡;尼莫的平
江苏医药000516 【摘要】 目的 研究β-淀粉样蛋白(Aβ)的神经毒性机制,特别是对大鼠海马和额叶皮层细胞凋亡相关基因bcl-2表达的影响,以及尼莫的平的作用。方法 将SD大鼠随机分模型组、治疗组和对照组。在立体定位下于迈内特基底核(NBM)注入Aβ10μg建立Alzheimer病模型,治疗组在建立模型后每天腹腔注射尼莫的平至实验结束。对照组NBM注入等容积生理盐水。流式细胞仪DNA含量分析和免疫荧光法检测来测定细胞群中细胞凋亡的比例和Bcl-2蛋白的含量,并结合常规病理和透射电镜观察组织学改变。结果 组织学可见早期凋亡的形态学改变。模型组大鼠海马、额叶神经细胞凋亡和Bcl-2蛋白含量较对照组升高;尼莫的平治疗后凋亡细胞减少,但海马区仍高于对照组,Bcl-2蛋白水平有所下调,接近正常对照组。结论 Aβ的神经毒性与细胞凋亡有关,尼莫的平有一定的治疗作用。
, 百拇医药
Alzheimer病(AD)的主要病理特征是患者脑内的神经炎性斑块和血管淀粉样变性。神经炎性斑块的主要成分是含40个氨基酸残基的β-淀粉样蛋白(Aβ),人们对它的作用进行了大量的研究,提出了AD病因的Aβ学说,但Aβ的神经毒性机制尚不明确。本文以Aβ注入大鼠NBM建立大鼠AD模型,采用流式细胞仪(FCM)研究Aβ对大鼠海马和额叶皮层细胞凋亡相关基因bcl-2表达的影响,以及尼莫的平的作用。
材料与方法
一、实验动物及分组:健康雄性SD大鼠3~4月龄,体重180~250g,由苏州医学院动物实验中心提供。随机分模型组(n=9)、尼莫的平治疗组(n=9)和对照组(n=10)。
二、模型制备和给药方法:按我们已报告的方法[1]参照大鼠脑立体定位图谱,将10μl的Aβ(RBI,美国)在立体定位仪下注入大鼠迈内特基底核(NBM)坐标为前囟后1.4mm,旁2.5mm,深7.2mm。对照组在NBM处注入等容积生理盐水,尼莫的平治疗组在建立模型后即刻给予腹腔注射尼莫的平50μg/100g体重,以后每天注射1次至实验结束,共2周。
, 百拇医药
三、病理组织学观察方法:模型组大鼠注入Aβ后2周断头取鼠脑海马、额叶脑组织,HE染色显微镜和醋酯铀-枸橼酸铅染色透射电镜进行组织学观察。
四、海马、额叶神经细胞凋亡和Bcl-2蛋白的检测:制备后细胞悬液操作在流式细胞仪(FCM,EPICS XL型,Coulter,美国)先后作凋亡细胞和Bcl-2蛋白免疫荧光检测分析。
细胞凋亡检测分析:细胞悬液经处理后,上机作DNA含量的测定,每个样本测100个细胞,经计算机处理得出该细胞群体的DNA含量分布,绘出其直方图。在G1峰的左侧可以见到凋亡细胞(亚G1期)峰群,计算出该群细胞所占百分数。
Bcl-2蛋白的检测:细胞悬液用细胞膜打孔剂处理,按操作说明书操作。加入第一抗体(bcl-2兔IgG,),37℃中孵育60分钟,按操作说明书操作。PBS清洗后再加第二抗体异硫氰酸荧光素(FITC)标记的羊抗兔IgG反应60分钟,再用PBS清洗3次。上机作免疫荧光强度的检测,以荧光指数(FI)表示Bcl-2蛋白的相对含量。
, http://www.100md.com
五、统计学处理:
数据以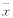 ±s表示。用t检验进行比较。
±s表示。用t检验进行比较。
结果
一、组织学改变:HE染色可见海马和额叶变性的神经细胞和少量胶质细胞增生。透射电镜下可见一些细胞膜出现皱缩,细胞体积正常或稍缩小,细胞核膜完整,染色质浓缩,并见边聚现象。额叶神经细胞也有类似现象。本组未见典型凋亡小体。
二、凋亡细胞和Bcl-2蛋白测定:各组大鼠海马、额叶神经细胞亚G1期细胞百分数和Bcl-2蛋白含量改变见表1。模型组大鼠海马、额叶神经细胞亚G1期细胞和Bcl-2蛋白含量较对照组升高;尼莫的平治疗后亚G1期细胞下降,但海马区仍高于对照组,Bcl-2水平均有所下调,接近正常对照组。
, 百拇医药
表1 各组大鼠海马和额叶凋亡细胞百分数和Bcl-2蛋白含量改变 组别
额 叶
海 马
凋亡细胞百分数
Bcl-2蛋白
凋亡细胞百分数
Bcl-2蛋白
模型组
9.8±2.9*△
2.87±0.34*△
12.7±4.1**△
, 百拇医药
2.68±0.41**△
治疗组
6.1±2.4
1.89±0.27
7.8±3.4*
1.86±0.28
对照组
5.1±2.1
2.23±0.27
4.8±1.2
2.15±0.28
, http://www.100md.com 与对照组比较*P<0.01,**P<0.05;与治疗组比,△P<0.01
讨论
研究表明AD的大多数症状与脑内沉积的Aβ毒性作用所造成的神经退行性变有关,研究发现Aβ是一种有明显神经毒性的短肽,但Aβ致神经细胞丧失是通过凋亡还是通过坏死机制,尚未有明确的结论[2]。为研究Aβ的神经损伤机制和药物的干预作用,我们将Aβ注入大鼠NBM以建立大鼠AD模型,在已进行的行为学测试表明了该模型很好地复制了AD的学习记忆缺损,并能引起海马、额叶局部脑血流量降低[1]。近年来研究表明Alzheimer病(AD)与细胞凋亡及相关基因关系密切[3,4]。在培养的神经细胞、AD动物模型和AD患者脑内均发现了细胞凋亡的证据[3]。但也有不同的意见,认为细胞凋亡并非是AD神经细胞死亡的主要方式[4]。为此我们采用流式细胞仪亚“G1”峰检测法研究了Aβ对大鼠海马、额叶神经细胞的影响。亚G1期细胞在整个细胞群中所占的百分数,可以用来比较不同细胞群之间凋亡细胞的多少。我们发现无论海马还是额叶的神经细胞凋亡都增加,海马区更明显。同样在组织学研究中也发现了早期凋亡的证据。在Aβ致细胞损害过程中,有作者发现Aβ通过干扰细胞Ca2+的平衡产生细胞毒性,并诱导细胞凋亡[5]。Arispe等[6]的体外试验发现合成的Aβ可形成一种跨越脂双层的离子通道,这些通道可以有效地转运钙离子,而且这种改变早于淀粉样斑块的形成。由于发现Aβ可以在脂质体上形成钙离子通道,破坏细胞内外的Ca2+平衡,因此细胞内游离钙的增加被认为可能是凋亡的早期触发因素之一。我们采用尼莫的平抑制了部分细胞凋亡的发生,也证实了Ca2+的重要作用。而不能完全抑制海马区细胞凋亡原因,可能与治疗的时间、药物剂量以及同时存在其它机制有关。
, http://www.100md.com
细胞凋亡受到多种基因的调节,其中bcl-2是一个重要的与凋亡相关的基因。我们发现注入Aβ后2周模型组大鼠海马和额叶bcl-2基因表达增强,应用尼莫的平后其表达的水平有所下调。这与O’Barr等[7]在AD患者中的观察结果基本一致,他们发现AD患者Bcl-2蛋白表达水平是非痴呆老年人蛋白表达的3倍以上;而Su等[8]应用免疫组化技术在AD患者发现在老年斑周围Bcl-2表达上调,在纤维缠结神经元中其表达水平下调。Paradis等[9]用100nM浓度的Aβ加入培养的人海马神经细胞中所发现的结果却相反,Bcl-2表达水平下降而Bax升高。这说明bcl-2基因在对AD中神经细胞凋亡有一定的调节作用,对抗Aβ所诱导的细胞凋亡,并可能与Aβ浓度或含量有关。
由此可见,在动物模型、细胞培养以及AD患者的研究中大多数的结果都表明Aβ的神经毒性与细胞凋亡以及相关的基因关系密切。
参考文献
, http://www.100md.com
1,刘春风,戴永萍,包仕尧,等.Alzheimer病大鼠局部脑血流量与行为学改变的研究.临床神经病学杂志,1999,12:160-162.
2,Wisniewski T,Ghiso J,Frangine B.Alzheimer’s disease and solubleAβ.Neurobiology of aging,1994,15:143-152.
3,Savitz SI,Rosenbaum DM.Apoptosis in neurological disease.Neurosurgery,1998,42:555-574.
4,Stadelmann C,Bruck W,Bancher C,et al.Alzheimer disease:DNA fragmentation indicates increased neuronal vulnerability,but not apoptosis.J Neuropathol Exp Neurol,1998,57:456-464.
, 百拇医药
5,Fu W,Luo H,Parthasarathy S,et al.Catecholamines potentiate amyloid beta-peptide neurotoxicity:involve-ment of oxidative stress,mitochondrial dysfunction,and perturbed calcium homeostasis.Neurobiol Dis,1998,5:229-243.
6,Arispe N,Rojas E,Pollard H.Alzheimer’s disease amyloid beta protein forms calcium channeles in bilayer membranes:blockade by tromethamine and aluminum.Proc Natl Acad Sci USA,1993,90:567-571.
7,O’Barr S,Schultz J,Rogers J.Expression of the protoncogene bcl-2 in Alzheimer’s disease brain.Neurobiol Aging,1996,17:131-136.
, 百拇医药
8,Su JH,Deng G,Cotman CW.Bax protein expression is increased in Alzheimer’s brain:correlations with DNA damage,Bcl-2 expression,and brain pathology.J Neuropathol Exp Neurol,1997,56:86-93.
9,Paradis E,Douillard H,Koutroumanis M,et al.Amyloid beta peptide of Alzheimer’s disease downregulates Bcl-2 and upregulates bax expression in human neurons.J Neurosci,1996,16:7533-7539.
(收稿:1999-09-20 修回:1999-11-09), 百拇医药
单位:(215004 苏州医学院附属第二医院神经内科)
关键词:Alzheimer病;β淀粉样蛋白;细胞凋亡;尼莫的平
江苏医药000516 【摘要】 目的 研究β-淀粉样蛋白(Aβ)的神经毒性机制,特别是对大鼠海马和额叶皮层细胞凋亡相关基因bcl-2表达的影响,以及尼莫的平的作用。方法 将SD大鼠随机分模型组、治疗组和对照组。在立体定位下于迈内特基底核(NBM)注入Aβ10μg建立Alzheimer病模型,治疗组在建立模型后每天腹腔注射尼莫的平至实验结束。对照组NBM注入等容积生理盐水。流式细胞仪DNA含量分析和免疫荧光法检测来测定细胞群中细胞凋亡的比例和Bcl-2蛋白的含量,并结合常规病理和透射电镜观察组织学改变。结果 组织学可见早期凋亡的形态学改变。模型组大鼠海马、额叶神经细胞凋亡和Bcl-2蛋白含量较对照组升高;尼莫的平治疗后凋亡细胞减少,但海马区仍高于对照组,Bcl-2蛋白水平有所下调,接近正常对照组。结论 Aβ的神经毒性与细胞凋亡有关,尼莫的平有一定的治疗作用。
, 百拇医药
Alzheimer病(AD)的主要病理特征是患者脑内的神经炎性斑块和血管淀粉样变性。神经炎性斑块的主要成分是含40个氨基酸残基的β-淀粉样蛋白(Aβ),人们对它的作用进行了大量的研究,提出了AD病因的Aβ学说,但Aβ的神经毒性机制尚不明确。本文以Aβ注入大鼠NBM建立大鼠AD模型,采用流式细胞仪(FCM)研究Aβ对大鼠海马和额叶皮层细胞凋亡相关基因bcl-2表达的影响,以及尼莫的平的作用。
材料与方法
一、实验动物及分组:健康雄性SD大鼠3~4月龄,体重180~250g,由苏州医学院动物实验中心提供。随机分模型组(n=9)、尼莫的平治疗组(n=9)和对照组(n=10)。
二、模型制备和给药方法:按我们已报告的方法[1]参照大鼠脑立体定位图谱,将10μl的Aβ(RBI,美国)在立体定位仪下注入大鼠迈内特基底核(NBM)坐标为前囟后1.4mm,旁2.5mm,深7.2mm。对照组在NBM处注入等容积生理盐水,尼莫的平治疗组在建立模型后即刻给予腹腔注射尼莫的平50μg/100g体重,以后每天注射1次至实验结束,共2周。
, 百拇医药
三、病理组织学观察方法:模型组大鼠注入Aβ后2周断头取鼠脑海马、额叶脑组织,HE染色显微镜和醋酯铀-枸橼酸铅染色透射电镜进行组织学观察。
四、海马、额叶神经细胞凋亡和Bcl-2蛋白的检测:制备后细胞悬液操作在流式细胞仪(FCM,EPICS XL型,Coulter,美国)先后作凋亡细胞和Bcl-2蛋白免疫荧光检测分析。
细胞凋亡检测分析:细胞悬液经处理后,上机作DNA含量的测定,每个样本测100个细胞,经计算机处理得出该细胞群体的DNA含量分布,绘出其直方图。在G1峰的左侧可以见到凋亡细胞(亚G1期)峰群,计算出该群细胞所占百分数。
Bcl-2蛋白的检测:细胞悬液用细胞膜打孔剂处理,按操作说明书操作。加入第一抗体(bcl-2兔IgG,),37℃中孵育60分钟,按操作说明书操作。PBS清洗后再加第二抗体异硫氰酸荧光素(FITC)标记的羊抗兔IgG反应60分钟,再用PBS清洗3次。上机作免疫荧光强度的检测,以荧光指数(FI)表示Bcl-2蛋白的相对含量。
, http://www.100md.com
五、统计学处理:
数据以
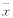 ±s表示。用t检验进行比较。
±s表示。用t检验进行比较。结果
一、组织学改变:HE染色可见海马和额叶变性的神经细胞和少量胶质细胞增生。透射电镜下可见一些细胞膜出现皱缩,细胞体积正常或稍缩小,细胞核膜完整,染色质浓缩,并见边聚现象。额叶神经细胞也有类似现象。本组未见典型凋亡小体。
二、凋亡细胞和Bcl-2蛋白测定:各组大鼠海马、额叶神经细胞亚G1期细胞百分数和Bcl-2蛋白含量改变见表1。模型组大鼠海马、额叶神经细胞亚G1期细胞和Bcl-2蛋白含量较对照组升高;尼莫的平治疗后亚G1期细胞下降,但海马区仍高于对照组,Bcl-2水平均有所下调,接近正常对照组。
, 百拇医药
表1 各组大鼠海马和额叶凋亡细胞百分数和Bcl-2蛋白含量改变 组别
额 叶
海 马
凋亡细胞百分数
Bcl-2蛋白
凋亡细胞百分数
Bcl-2蛋白
模型组
9.8±2.9*△
2.87±0.34*△
12.7±4.1**△
, 百拇医药
2.68±0.41**△
治疗组
6.1±2.4
1.89±0.27
7.8±3.4*
1.86±0.28
对照组
5.1±2.1
2.23±0.27
4.8±1.2
2.15±0.28
, http://www.100md.com 与对照组比较*P<0.01,**P<0.05;与治疗组比,△P<0.01
讨论
研究表明AD的大多数症状与脑内沉积的Aβ毒性作用所造成的神经退行性变有关,研究发现Aβ是一种有明显神经毒性的短肽,但Aβ致神经细胞丧失是通过凋亡还是通过坏死机制,尚未有明确的结论[2]。为研究Aβ的神经损伤机制和药物的干预作用,我们将Aβ注入大鼠NBM以建立大鼠AD模型,在已进行的行为学测试表明了该模型很好地复制了AD的学习记忆缺损,并能引起海马、额叶局部脑血流量降低[1]。近年来研究表明Alzheimer病(AD)与细胞凋亡及相关基因关系密切[3,4]。在培养的神经细胞、AD动物模型和AD患者脑内均发现了细胞凋亡的证据[3]。但也有不同的意见,认为细胞凋亡并非是AD神经细胞死亡的主要方式[4]。为此我们采用流式细胞仪亚“G1”峰检测法研究了Aβ对大鼠海马、额叶神经细胞的影响。亚G1期细胞在整个细胞群中所占的百分数,可以用来比较不同细胞群之间凋亡细胞的多少。我们发现无论海马还是额叶的神经细胞凋亡都增加,海马区更明显。同样在组织学研究中也发现了早期凋亡的证据。在Aβ致细胞损害过程中,有作者发现Aβ通过干扰细胞Ca2+的平衡产生细胞毒性,并诱导细胞凋亡[5]。Arispe等[6]的体外试验发现合成的Aβ可形成一种跨越脂双层的离子通道,这些通道可以有效地转运钙离子,而且这种改变早于淀粉样斑块的形成。由于发现Aβ可以在脂质体上形成钙离子通道,破坏细胞内外的Ca2+平衡,因此细胞内游离钙的增加被认为可能是凋亡的早期触发因素之一。我们采用尼莫的平抑制了部分细胞凋亡的发生,也证实了Ca2+的重要作用。而不能完全抑制海马区细胞凋亡原因,可能与治疗的时间、药物剂量以及同时存在其它机制有关。
, http://www.100md.com
细胞凋亡受到多种基因的调节,其中bcl-2是一个重要的与凋亡相关的基因。我们发现注入Aβ后2周模型组大鼠海马和额叶bcl-2基因表达增强,应用尼莫的平后其表达的水平有所下调。这与O’Barr等[7]在AD患者中的观察结果基本一致,他们发现AD患者Bcl-2蛋白表达水平是非痴呆老年人蛋白表达的3倍以上;而Su等[8]应用免疫组化技术在AD患者发现在老年斑周围Bcl-2表达上调,在纤维缠结神经元中其表达水平下调。Paradis等[9]用100nM浓度的Aβ加入培养的人海马神经细胞中所发现的结果却相反,Bcl-2表达水平下降而Bax升高。这说明bcl-2基因在对AD中神经细胞凋亡有一定的调节作用,对抗Aβ所诱导的细胞凋亡,并可能与Aβ浓度或含量有关。
由此可见,在动物模型、细胞培养以及AD患者的研究中大多数的结果都表明Aβ的神经毒性与细胞凋亡以及相关的基因关系密切。
参考文献
, http://www.100md.com
1,刘春风,戴永萍,包仕尧,等.Alzheimer病大鼠局部脑血流量与行为学改变的研究.临床神经病学杂志,1999,12:160-162.
2,Wisniewski T,Ghiso J,Frangine B.Alzheimer’s disease and solubleAβ.Neurobiology of aging,1994,15:143-152.
3,Savitz SI,Rosenbaum DM.Apoptosis in neurological disease.Neurosurgery,1998,42:555-574.
4,Stadelmann C,Bruck W,Bancher C,et al.Alzheimer disease:DNA fragmentation indicates increased neuronal vulnerability,but not apoptosis.J Neuropathol Exp Neurol,1998,57:456-464.
, 百拇医药
5,Fu W,Luo H,Parthasarathy S,et al.Catecholamines potentiate amyloid beta-peptide neurotoxicity:involve-ment of oxidative stress,mitochondrial dysfunction,and perturbed calcium homeostasis.Neurobiol Dis,1998,5:229-243.
6,Arispe N,Rojas E,Pollard H.Alzheimer’s disease amyloid beta protein forms calcium channeles in bilayer membranes:blockade by tromethamine and aluminum.Proc Natl Acad Sci USA,1993,90:567-571.
7,O’Barr S,Schultz J,Rogers J.Expression of the protoncogene bcl-2 in Alzheimer’s disease brain.Neurobiol Aging,1996,17:131-136.
, 百拇医药
8,Su JH,Deng G,Cotman CW.Bax protein expression is increased in Alzheimer’s brain:correlations with DNA damage,Bcl-2 expression,and brain pathology.J Neuropathol Exp Neurol,1997,56:86-93.
9,Paradis E,Douillard H,Koutroumanis M,et al.Amyloid beta peptide of Alzheimer’s disease downregulates Bcl-2 and upregulates bax expression in human neurons.J Neurosci,1996,16:7533-7539.
(收稿:1999-09-20 修回:1999-11-09), 百拇医药