褪黑激素的化学合成方法
作者:林晨 张婉春
单位:福建医科大学化学教研室,福州 350004
关键词:褪黑激素;松果体;N-乙酰基-5-甲氧色胺;5-甲氧色胺;激素类;合成
福建医科大学学报000249
中图分类号:R977.1;R322.55 文献标识码:A
文章编号:1000-2235(2000)02-0205-04
褪黑激素(melatonin,MT)是松果体腺(pineal gland,PG)分泌的生物活性最高的内源性激素。1930年,Spath和Lederer最早在合成中发现了MT[1],其结构式如下 ,化学名为N-乙酰基-5-甲氧基色胺。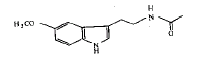
, http://www.100md.com
1958年皮肤病学家Aaron Lener[2]等人从牛松果腺中提取出MT,其在苯中析出呈淡黄色叶片状结晶。从MT被分离以来,世界上有上千个实验室在研究它的作用,对动物及人体几乎不产生毒性[3]的MT能参与中枢神经系统[4,5]、生殖系统[6,7]、免疫系统、个体发育[8]等多种生理活动。目前,MT及其衍生物已试用于催眠、抗癌[9]、心血管病[10]、避孕、抗衰老[11]、食品添加等方面。
利用生物提取仅能获得微量的MT,甚至无法对其进行结构测定。动物来源有限、成本高等因素也决定目前只能用化学合成的方法来制备MT。首先对文献中报道过的各种合成方法及线路进行分析比较是很有必要的。
1 造环合成
通过含苯环的简单原料合成出含吲哚环的中间体。
, http://www.100md.com
1.1 以5-甲氧基吲哚为合成第一目标。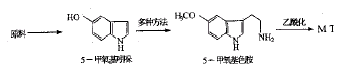
例1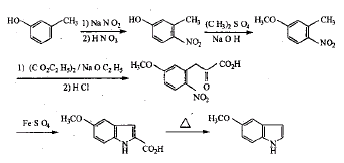
段传凤[12]以间甲酚为原料经九步合成出MT,其中间甲酚先硝化,再氧化引入硝基的办法比用硝酸直接硝化收率提高一倍,且无需后处理,可直接甲氧基化得到邻甲氧基邻硝基甲苯,通过除去溶剂中微量水份,并调整反应温度,使产率有所提高。关环后达到第一目标时产率为29%。该合成路线步骤长,其中对甲氧基邻硝基苯丙酮酸乙酯的还原环合及脱羧反应的条件较为苛刻,不易控制。 例2
Horst[13]将3-甲基-4-硝基苯酚经硫酸二甲酯甲基化后,再与N,N-二甲基甲酰胺的二甲缩醛反应,最后还原达到第一目标。 例3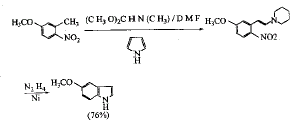
, http://www.100md.com
Batcho[14]及马灵台[15]的思路与Horst相似,直接将邻甲氧基邻硝基甲苯与DMF/二甲缩醛反应形成2-硝基-5-甲氧基-β-四氢吡咯基苯乙烯,再经还原环合可较好地达到第一目标。
第一目标到5-甲氧基色胺的转化有多条途径,其基本思路是在第一目标的吲哚环的C-3上引入合适的侧链并对其修饰达到第二目标。最常用的是例6。 例6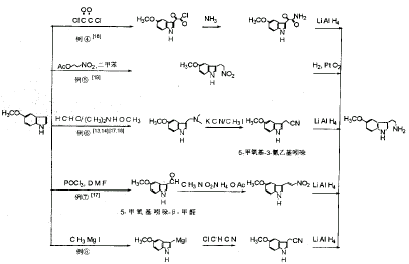
1.2 直接以5-甲氧基色胺为第一目标。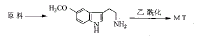
与以5-甲氧基吲哚为合成第一目标不同的是后者在成环的同时完成了环上3位侧链的枝接。 例9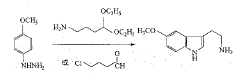
, http://www.100md.com
本例[16,19,20]采用的是Fischer吲哚合成法。苯腙经重排得到了吲哚衍生物。早些时候,国外主要是由对甲氧基苯肼与3-氨基丁醛二乙缩醛在氯化锌催化下合成5-甲氧基色胺,产率15%。若改用4-氯丁醛制备,产率约为45%。原料3-氨基丁醛二乙缩醛或4-氯丁醛的制备[21],繁琐是主要的缺点。 例10
环化效率不高使得第二目标得率仅有13%[22]。乙酰乙酸乙酯与1-氯-3-溴烷在钠环境中制备原料也属不易。例11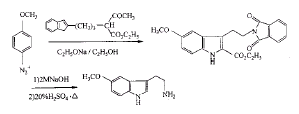
经环化、水解、脱羧后,第二目标的产率为40%。3-乙酰基-2-哌啶酮[23]需由丙二酸二乙脂和丙烯腈反应,再经Raney Ni催化氢化制得。 例12[24~26]
, 百拇医药
Franco[25]利用Japp-Klingemann反应设计出一条使用简易原料的反应路线。因为在制备N-3-溴丙基邻苯二甲酰亚胺的回流操作时需要大量的丙酮作为反应溶剂,致使此步反应时间较长(24 h),而且在5-甲氧基色胺的精制中使用了高成本的六甲基二硅烷胺。王加旺、蔡晓宏等参考文献[25]并改进简化了工艺,设计了一种主体反应为五步的合成方法。2-乙酰基-5-邻苯二甲酰亚胺基戊酸乙酯可由邻苯二甲酰亚胺钾与1,3-二溴丙烷反应生成的N-3-溴丙基邻苯二甲亚胺与乙酰乙酸乙酯在乙醇钠的乙醇溶液中缩合而成。反应中每一步产率都较高(>70%)。达到5-甲氧基色胺时产率为26%。改进的实验中,1,3-二溴丙烷代替了丙酮,使反应温度为155~160℃,这不仅使反应时间缩短为6~7 h,而且减少了反应中生成二聚物的量,提高了收率。在2-羧乙基-3-(2-邻苯二甲酰亚胺乙基)戊酸乙酯-5-甲氧基吲哚的制备中较文献[25]省略了精制步骤;在5-甲氧基色胺的精制中避免了使用高成本的六甲基二硅烷胺,采用的萃取和反萃取法精制,简化了工艺,降低了成本,提高了收率,为工业化生产奠定了基础。
, http://www.100md.com
最后,5-甲氧基色胺经乙酰化能顺利得到MT。在造环合成中,对原料、操作、产率的深入研究对工业化生产有重要的意义。例9和例11的产率较高,但有的反应原料需经起始原料的合成,增加了操作步骤,成本同时也提高了。例10、例26及某些文献[27,28]中都存在反应原料复杂、昂贵、产率低、重复性不好等缺陷。以5-甲氧基吲哚为第一目标的合成路线中,原料虽简单,但合成步骤多、操作麻烦、产率低。文献[29,30]中因为成本高及可操作性差等因素而未能推广。
2 借环合成
吲哚环是MT的核心部分。以吲哚环为原料的借环合成比造环合成简化了实验步骤,有相对的优越性。例13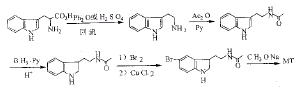
例14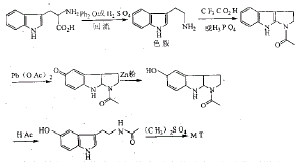
, http://www.100md.com
色氨酸是一种价廉易得的常用生化试剂,它易热脱羧得到色胺。合成中需对环5H进行甲氧基化,直接卤代或甲氧基化,产率很低,所以Kunio Saito[31]先对环2、3位进行还原,卤代环5H后再甲氧基化。例13,14中都不采用直接甲氧基化。例15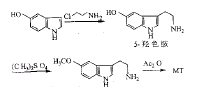
Luigi[32]利用 ClCH2CH2NH2引入氨基,避免了使用较昂贵的氢化铝锂还原剂。例16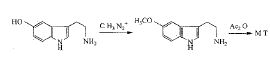
直接以例15中环3位上已接驳乙胺基的5-羟色胺为原料[33]进行重氮甲烷甲基化,产率较高。例17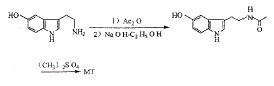
, 百拇医药
从咖啡蜡中可提取5-羟色胺,但植物来源有限和分离纯化的困难限制了它的推广。 例18[34]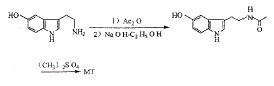
在例6及例7中,也可以用5-甲氧基吲哚、5-甲氧基吲哚-β-甲醛、5-甲氧-3-氰乙基吲哚为原料进行合成,它们都省去了甲氧基取代环5H的操作。
3 结 语
作为人体生物节律的自然调节物的褪黑激素所拥有的广阔前景正成为相关学科界研究的热点。综观文献资料可以看出,在造环合成中例[11]显示了原料简单、价格低廉、线路简明、收率较高等优点,其具体的合成工艺也得到了较好的改进。在借环合成中,以含有吲哚环的色氨酸为原料的合成线路不失为一条捷径,但是如何提高环5位的甲氧基化的选择性及取代效率仍是科学工作者进一步研究的课题。
, 百拇医药
对色氨酸产品进行深加工,开发MT及其衍生物不仅能带来高附加值,而且对MT的工业化生产具有重要的科学和应用价值。寻找高产率、低成本、操作简易的合成线路还需进一步探索。微波等物理催化手段[35]的应用已成为一种全新、优越的方法。Caddick用微波照射催化Fischer吲哚合成反应,仅几分钟就定量完成了反应。文献[25]中采用的5-甲氧基吲哚这一不易得到的原料也能通过微波催化定量完成。这将为诸如2-甲基-6,7-二氯MT[36]、葡萄醛酸-6-羟MT[37]等高稳定性、高活性衍生物的合成带来新的启示。另外,从松果体腺细胞内以色氨酸为原料,经过羟化、脱羧及N-乙酰转移酶等的催化最终形成MT的生物合成过程[38]中也许能得到这样的灵感,如果能测出人PG细胞中的基因序列,则可以通过基因工程生产出有大量生物活性的MT。
作者简介:林 晨(1970~),男,讲师.
参考文献:
, 百拇医药
[1]Spath E,Lederer E.Synthesen von 4-carbolinen[J].Ber,1930,63:2102.
[2]Lerner AB,Case JD,Yoshiyata Takahashi,et al.Isolation of melatonin,the pineal gland factor that lightens melanocytes[J].J Am Chem Soc,1958,80:2587.
[3]Neville S,Arent J,Ioannides C.Evidence for melatonin synthesis in rodent harderian gland:a dynamic invitro sudy[J].J Pineal Res,1989,6:73.
[4]Vaughan GM.Melatonin in human[A].In:Reited RJ(Ed).Pineal Research Review[C].New York:Alan Riss,1984.142.
, http://www.100md.com
[5]Sandyk R.Melatonin supplements for aging[J].Int J Neurosci,1996,87(3/4):219.
[6]马明新.褪黑激素对哺乳动物繁殖生理的作用[J].国外蓄牧科技,1989,16(4):19.
[7]Sirotkin AV,Schaeffer HJ.Direct regulation of mammalian reproductive organs by serotonin and melatonin[J].J Endocrinol,1997,154(1):1.
[8]孙庆松,刘志平.褪黑激素促进水貂毛皮与早熟的研究[J].野生动物,1995,(4):22
[9]Ronco AL,Halberg F.The pineal and cancer[J].Anticancer Res,1996,16(4A):2033.
, http://www.100md.com
[10]Sandyk R,Awerbuch GI.The relationship between melatonin secretion and serum cholesterol in patients with multiple sclerosis[J].Int J Neurosci,1994,76(1/2):81.
[11]Reiter RJ.Interactions of the pineal hormone melatonin with oxygen centered free radicals:a brief review[J].Brazb J Med Biol Res,1993,26(11):1141.
[12]段传凤,杨依军.褪黑激素(N-乙酰基-5-甲氧基色胺)的合成[J].药学学报,1991,23(3):182.
[13]Horst HJ.Compound and composition for treating tumors[J].CA,1982,97:215988s.
, 百拇医药
[14]Batcho AD,Leimgruber W.Extrapineal melatonin and N-acetylsertonin[J].Organic Synthesis,1990,7:34.
[15]马灵台,林桂椿,张礼和,等.褪黑激素的合成研究[J].北京医科大学学报,1991,23(3):214.
[16]Szmuszkovicz J,Authony WC,Heinzelman RV.Synthesis of N-acetyl-5- methoxytryptamine[J].J Org Chem,1960,25:857.
[17]Supienski J,Misztal S.Synthesis of melatonin(5-methoxy-N-acetyltryptamine)[J].Bull Acad Rolon Sci Ser Biol,1960,8:479.
, 百拇医药
[18]Michael EF,Thomas AC,James AC,et al.Synthesis and evaluation of the antiovulatory activity of a variety of melatonin analogues[J].J Med Chem,1979,22(1):63.
[19]Grandberg II,Afronina NI,Zuyanova,TI,et al.Indoles Ⅱ.Synthesis of 1-substituted tryptamines[J].CA,1969,70:68046V.
[20]Grandberg II,Zuganova TI,Afronina NI,et al.New method of synthesizing important biogenic amines[J].Dokl Akod Nauk SSSR,1967,176(3):583.
, http://www.100md.com
[21]Jin Soon Cha.Exceptionally facile reduction of acid chlorides to aldehydes by sodium tri-tert-butoxyaluminohydride[J].J Org Chem,1993,58:4732.
[22]Szantay C,Szabo L,Kalans Gy.A new route to tryptamines[J].Synthesis,1974,(5):354
[23]Abramovitch RA,Shapiro DJ.A convenint synthesis of tryptamines and β-carbolines[J].J Chem Soc,1956,(11/12):4589.
[24]王家旺,张 惠,吴纯启,等.一种简便的松果腺素的合成方法[J].精细化工,1999,16(2):16.
, 百拇医药
[25]Franco F,Luigi D,Ermanno D.The total synthesis of melatonin as a drug for therapy of AIDS[P].Eur Pat 330625,1981-08-30.
[26]蔡晓宏,刘 鸿,赵 晏,等.褪黑素的合成研究[J].陕西化工,1998,27(2):25.
[27]Bertaccini G,Vitali T.Synthesis and pharmacological activity of some 5-methoxyindole derivatives occuring in nature[J].Farmaco Ed Sci,1967,22(4):229.
[28]Supriewski J,Misztal S,Marczynski T.Synthesis and biological properties of melatonin[J].Dissertations Pharm,1961,13:25.
, 百拇医药
[29]Kita Y,Tohma H,Inagaki M,et al.Synthesis and evaluation of the antiovulatory activity of a variety of melatonin analogues[J].Heterocycles,1992,33:503.
[30]Buzas A,Herrison C.Electrophilic substitution in indoles.Part 18.Cyclisation of N-acyltryptamines[J].ibid,1977,(2):129.
[31]Kunio Saito,Yasuo Kikubawa.Introduction of a methoxyl group into indoles and 2,3-dihydroindoles.A new synthesis of 5-hydroxytryptamine(Serotonin)[J].J Heterocyclic Chem,1979,16:1325.
, 百拇医药
[32]DiBella Luigi.Pharmaceutical prepartion containing N-acetyl-5-methoxytrptamine for treating leucoses and neurotic syndromes[P].Belg,824022,1975-04-16.
[33]Bertaccini G,Vitali T.Synthesis and pharmacological activity of some 5-methoxyindole derivatives occurring in nature[J].Farmaco Ed Sci,1967,22(4):229.
[34]Supniewski J,Misztal S.Synthesis of melatonin[J].CA,1960,82:15457.
[35]Caddick S.Microwave assisted organic reactions[J].Tetrahedron,1995,51(8):10403.
, http://www.100md.com
[36]Clemens JA.Synthetic methodes to indoles derivatives[J].Neural Transm,1986,21(Suppl):451.
[37]Leone AM.Hydroxylatonin of tryptamine derivatives[J].Neuroendocrinol Lett,1987,9(5):289.
[38]汪晓飞,刘志民,彭树勋,等.褪黑素:一个多功能的光周期信号[J].生理科学进展,1998,29(3):281.
收稿日期:1999-11-08, http://www.100md.com
单位:福建医科大学化学教研室,福州 350004
关键词:褪黑激素;松果体;N-乙酰基-5-甲氧色胺;5-甲氧色胺;激素类;合成
福建医科大学学报000249
中图分类号:R977.1;R322.55 文献标识码:A
文章编号:1000-2235(2000)02-0205-04
褪黑激素(melatonin,MT)是松果体腺(pineal gland,PG)分泌的生物活性最高的内源性激素。1930年,Spath和Lederer最早在合成中发现了MT[1],其结构式如下 ,化学名为N-乙酰基-5-甲氧基色胺。

, http://www.100md.com
1958年皮肤病学家Aaron Lener[2]等人从牛松果腺中提取出MT,其在苯中析出呈淡黄色叶片状结晶。从MT被分离以来,世界上有上千个实验室在研究它的作用,对动物及人体几乎不产生毒性[3]的MT能参与中枢神经系统[4,5]、生殖系统[6,7]、免疫系统、个体发育[8]等多种生理活动。目前,MT及其衍生物已试用于催眠、抗癌[9]、心血管病[10]、避孕、抗衰老[11]、食品添加等方面。
利用生物提取仅能获得微量的MT,甚至无法对其进行结构测定。动物来源有限、成本高等因素也决定目前只能用化学合成的方法来制备MT。首先对文献中报道过的各种合成方法及线路进行分析比较是很有必要的。
1 造环合成
通过含苯环的简单原料合成出含吲哚环的中间体。
, http://www.100md.com
1.1 以5-甲氧基吲哚为合成第一目标。
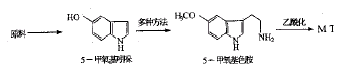
例1

段传凤[12]以间甲酚为原料经九步合成出MT,其中间甲酚先硝化,再氧化引入硝基的办法比用硝酸直接硝化收率提高一倍,且无需后处理,可直接甲氧基化得到邻甲氧基邻硝基甲苯,通过除去溶剂中微量水份,并调整反应温度,使产率有所提高。关环后达到第一目标时产率为29%。该合成路线步骤长,其中对甲氧基邻硝基苯丙酮酸乙酯的还原环合及脱羧反应的条件较为苛刻,不易控制。 例2

Horst[13]将3-甲基-4-硝基苯酚经硫酸二甲酯甲基化后,再与N,N-二甲基甲酰胺的二甲缩醛反应,最后还原达到第一目标。 例3

, http://www.100md.com
Batcho[14]及马灵台[15]的思路与Horst相似,直接将邻甲氧基邻硝基甲苯与DMF/二甲缩醛反应形成2-硝基-5-甲氧基-β-四氢吡咯基苯乙烯,再经还原环合可较好地达到第一目标。
第一目标到5-甲氧基色胺的转化有多条途径,其基本思路是在第一目标的吲哚环的C-3上引入合适的侧链并对其修饰达到第二目标。最常用的是例6。 例6

1.2 直接以5-甲氧基色胺为第一目标。
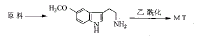
与以5-甲氧基吲哚为合成第一目标不同的是后者在成环的同时完成了环上3位侧链的枝接。 例9
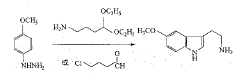
, http://www.100md.com
本例[16,19,20]采用的是Fischer吲哚合成法。苯腙经重排得到了吲哚衍生物。早些时候,国外主要是由对甲氧基苯肼与3-氨基丁醛二乙缩醛在氯化锌催化下合成5-甲氧基色胺,产率15%。若改用4-氯丁醛制备,产率约为45%。原料3-氨基丁醛二乙缩醛或4-氯丁醛的制备[21],繁琐是主要的缺点。 例10

环化效率不高使得第二目标得率仅有13%[22]。乙酰乙酸乙酯与1-氯-3-溴烷在钠环境中制备原料也属不易。例11

经环化、水解、脱羧后,第二目标的产率为40%。3-乙酰基-2-哌啶酮[23]需由丙二酸二乙脂和丙烯腈反应,再经Raney Ni催化氢化制得。 例12[24~26]

, 百拇医药
Franco[25]利用Japp-Klingemann反应设计出一条使用简易原料的反应路线。因为在制备N-3-溴丙基邻苯二甲酰亚胺的回流操作时需要大量的丙酮作为反应溶剂,致使此步反应时间较长(24 h),而且在5-甲氧基色胺的精制中使用了高成本的六甲基二硅烷胺。王加旺、蔡晓宏等参考文献[25]并改进简化了工艺,设计了一种主体反应为五步的合成方法。2-乙酰基-5-邻苯二甲酰亚胺基戊酸乙酯可由邻苯二甲酰亚胺钾与1,3-二溴丙烷反应生成的N-3-溴丙基邻苯二甲亚胺与乙酰乙酸乙酯在乙醇钠的乙醇溶液中缩合而成。反应中每一步产率都较高(>70%)。达到5-甲氧基色胺时产率为26%。改进的实验中,1,3-二溴丙烷代替了丙酮,使反应温度为155~160℃,这不仅使反应时间缩短为6~7 h,而且减少了反应中生成二聚物的量,提高了收率。在2-羧乙基-3-(2-邻苯二甲酰亚胺乙基)戊酸乙酯-5-甲氧基吲哚的制备中较文献[25]省略了精制步骤;在5-甲氧基色胺的精制中避免了使用高成本的六甲基二硅烷胺,采用的萃取和反萃取法精制,简化了工艺,降低了成本,提高了收率,为工业化生产奠定了基础。
, http://www.100md.com
最后,5-甲氧基色胺经乙酰化能顺利得到MT。在造环合成中,对原料、操作、产率的深入研究对工业化生产有重要的意义。例9和例11的产率较高,但有的反应原料需经起始原料的合成,增加了操作步骤,成本同时也提高了。例10、例26及某些文献[27,28]中都存在反应原料复杂、昂贵、产率低、重复性不好等缺陷。以5-甲氧基吲哚为第一目标的合成路线中,原料虽简单,但合成步骤多、操作麻烦、产率低。文献[29,30]中因为成本高及可操作性差等因素而未能推广。
2 借环合成
吲哚环是MT的核心部分。以吲哚环为原料的借环合成比造环合成简化了实验步骤,有相对的优越性。例13

例14

, http://www.100md.com
色氨酸是一种价廉易得的常用生化试剂,它易热脱羧得到色胺。合成中需对环5H进行甲氧基化,直接卤代或甲氧基化,产率很低,所以Kunio Saito[31]先对环2、3位进行还原,卤代环5H后再甲氧基化。例13,14中都不采用直接甲氧基化。例15

Luigi[32]利用 ClCH2CH2NH2引入氨基,避免了使用较昂贵的氢化铝锂还原剂。例16
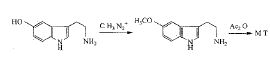
直接以例15中环3位上已接驳乙胺基的5-羟色胺为原料[33]进行重氮甲烷甲基化,产率较高。例17
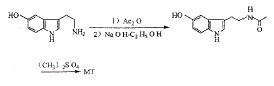
, 百拇医药
从咖啡蜡中可提取5-羟色胺,但植物来源有限和分离纯化的困难限制了它的推广。 例18[34]
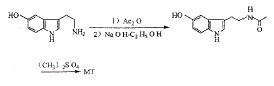
在例6及例7中,也可以用5-甲氧基吲哚、5-甲氧基吲哚-β-甲醛、5-甲氧-3-氰乙基吲哚为原料进行合成,它们都省去了甲氧基取代环5H的操作。
3 结 语
作为人体生物节律的自然调节物的褪黑激素所拥有的广阔前景正成为相关学科界研究的热点。综观文献资料可以看出,在造环合成中例[11]显示了原料简单、价格低廉、线路简明、收率较高等优点,其具体的合成工艺也得到了较好的改进。在借环合成中,以含有吲哚环的色氨酸为原料的合成线路不失为一条捷径,但是如何提高环5位的甲氧基化的选择性及取代效率仍是科学工作者进一步研究的课题。
, 百拇医药
对色氨酸产品进行深加工,开发MT及其衍生物不仅能带来高附加值,而且对MT的工业化生产具有重要的科学和应用价值。寻找高产率、低成本、操作简易的合成线路还需进一步探索。微波等物理催化手段[35]的应用已成为一种全新、优越的方法。Caddick用微波照射催化Fischer吲哚合成反应,仅几分钟就定量完成了反应。文献[25]中采用的5-甲氧基吲哚这一不易得到的原料也能通过微波催化定量完成。这将为诸如2-甲基-6,7-二氯MT[36]、葡萄醛酸-6-羟MT[37]等高稳定性、高活性衍生物的合成带来新的启示。另外,从松果体腺细胞内以色氨酸为原料,经过羟化、脱羧及N-乙酰转移酶等的催化最终形成MT的生物合成过程[38]中也许能得到这样的灵感,如果能测出人PG细胞中的基因序列,则可以通过基因工程生产出有大量生物活性的MT。
作者简介:林 晨(1970~),男,讲师.
参考文献:
, 百拇医药
[1]Spath E,Lederer E.Synthesen von 4-carbolinen[J].Ber,1930,63:2102.
[2]Lerner AB,Case JD,Yoshiyata Takahashi,et al.Isolation of melatonin,the pineal gland factor that lightens melanocytes[J].J Am Chem Soc,1958,80:2587.
[3]Neville S,Arent J,Ioannides C.Evidence for melatonin synthesis in rodent harderian gland:a dynamic invitro sudy[J].J Pineal Res,1989,6:73.
[4]Vaughan GM.Melatonin in human[A].In:Reited RJ(Ed).Pineal Research Review[C].New York:Alan Riss,1984.142.
, http://www.100md.com
[5]Sandyk R.Melatonin supplements for aging[J].Int J Neurosci,1996,87(3/4):219.
[6]马明新.褪黑激素对哺乳动物繁殖生理的作用[J].国外蓄牧科技,1989,16(4):19.
[7]Sirotkin AV,Schaeffer HJ.Direct regulation of mammalian reproductive organs by serotonin and melatonin[J].J Endocrinol,1997,154(1):1.
[8]孙庆松,刘志平.褪黑激素促进水貂毛皮与早熟的研究[J].野生动物,1995,(4):22
[9]Ronco AL,Halberg F.The pineal and cancer[J].Anticancer Res,1996,16(4A):2033.
, http://www.100md.com
[10]Sandyk R,Awerbuch GI.The relationship between melatonin secretion and serum cholesterol in patients with multiple sclerosis[J].Int J Neurosci,1994,76(1/2):81.
[11]Reiter RJ.Interactions of the pineal hormone melatonin with oxygen centered free radicals:a brief review[J].Brazb J Med Biol Res,1993,26(11):1141.
[12]段传凤,杨依军.褪黑激素(N-乙酰基-5-甲氧基色胺)的合成[J].药学学报,1991,23(3):182.
[13]Horst HJ.Compound and composition for treating tumors[J].CA,1982,97:215988s.
, 百拇医药
[14]Batcho AD,Leimgruber W.Extrapineal melatonin and N-acetylsertonin[J].Organic Synthesis,1990,7:34.
[15]马灵台,林桂椿,张礼和,等.褪黑激素的合成研究[J].北京医科大学学报,1991,23(3):214.
[16]Szmuszkovicz J,Authony WC,Heinzelman RV.Synthesis of N-acetyl-5- methoxytryptamine[J].J Org Chem,1960,25:857.
[17]Supienski J,Misztal S.Synthesis of melatonin(5-methoxy-N-acetyltryptamine)[J].Bull Acad Rolon Sci Ser Biol,1960,8:479.
, 百拇医药
[18]Michael EF,Thomas AC,James AC,et al.Synthesis and evaluation of the antiovulatory activity of a variety of melatonin analogues[J].J Med Chem,1979,22(1):63.
[19]Grandberg II,Afronina NI,Zuyanova,TI,et al.Indoles Ⅱ.Synthesis of 1-substituted tryptamines[J].CA,1969,70:68046V.
[20]Grandberg II,Zuganova TI,Afronina NI,et al.New method of synthesizing important biogenic amines[J].Dokl Akod Nauk SSSR,1967,176(3):583.
, http://www.100md.com
[21]Jin Soon Cha.Exceptionally facile reduction of acid chlorides to aldehydes by sodium tri-tert-butoxyaluminohydride[J].J Org Chem,1993,58:4732.
[22]Szantay C,Szabo L,Kalans Gy.A new route to tryptamines[J].Synthesis,1974,(5):354
[23]Abramovitch RA,Shapiro DJ.A convenint synthesis of tryptamines and β-carbolines[J].J Chem Soc,1956,(11/12):4589.
[24]王家旺,张 惠,吴纯启,等.一种简便的松果腺素的合成方法[J].精细化工,1999,16(2):16.
, 百拇医药
[25]Franco F,Luigi D,Ermanno D.The total synthesis of melatonin as a drug for therapy of AIDS[P].Eur Pat 330625,1981-08-30.
[26]蔡晓宏,刘 鸿,赵 晏,等.褪黑素的合成研究[J].陕西化工,1998,27(2):25.
[27]Bertaccini G,Vitali T.Synthesis and pharmacological activity of some 5-methoxyindole derivatives occuring in nature[J].Farmaco Ed Sci,1967,22(4):229.
[28]Supriewski J,Misztal S,Marczynski T.Synthesis and biological properties of melatonin[J].Dissertations Pharm,1961,13:25.
, 百拇医药
[29]Kita Y,Tohma H,Inagaki M,et al.Synthesis and evaluation of the antiovulatory activity of a variety of melatonin analogues[J].Heterocycles,1992,33:503.
[30]Buzas A,Herrison C.Electrophilic substitution in indoles.Part 18.Cyclisation of N-acyltryptamines[J].ibid,1977,(2):129.
[31]Kunio Saito,Yasuo Kikubawa.Introduction of a methoxyl group into indoles and 2,3-dihydroindoles.A new synthesis of 5-hydroxytryptamine(Serotonin)[J].J Heterocyclic Chem,1979,16:1325.
, 百拇医药
[32]DiBella Luigi.Pharmaceutical prepartion containing N-acetyl-5-methoxytrptamine for treating leucoses and neurotic syndromes[P].Belg,824022,1975-04-16.
[33]Bertaccini G,Vitali T.Synthesis and pharmacological activity of some 5-methoxyindole derivatives occurring in nature[J].Farmaco Ed Sci,1967,22(4):229.
[34]Supniewski J,Misztal S.Synthesis of melatonin[J].CA,1960,82:15457.
[35]Caddick S.Microwave assisted organic reactions[J].Tetrahedron,1995,51(8):10403.
, http://www.100md.com
[36]Clemens JA.Synthetic methodes to indoles derivatives[J].Neural Transm,1986,21(Suppl):451.
[37]Leone AM.Hydroxylatonin of tryptamine derivatives[J].Neuroendocrinol Lett,1987,9(5):289.
[38]汪晓飞,刘志民,彭树勋,等.褪黑素:一个多功能的光周期信号[J].生理科学进展,1998,29(3):281.
收稿日期:1999-11-08, http://www.100md.com