神经营养因子NGF、BDNF对鼠胚基底前脑胆碱能神经元发育生长的协同作用
作者:金国华 徐慧君 田美玲 秦建兵 黄镇 张新化
单位:南通医学院神经生物学研究室,南通226001
关键词:神经生长因子;脑源性神经营养因子;胚基底前脑;胆碱能神经元;细胞培养;脑内移植;大鼠
南通医学院学报000104[摘 要] 目的:探讨神经营养因子NGF、BDNF联合使用时对鼠胚基底前脑胆碱能神经元发育生长的协同作用。方法:实验分成NGF、BDNF、NGF+BDNF和对照4组。采用细胞培养和脑内移植手段及AChE组化染色、显微测量和图象分析等技术。检测各组胚基底前脑培养4天和8天时的AChE阳性神经元数、胞体直径、胞体发出的突起数及最长突起长度以及胚基底前脑移植至脑内4.5个月时移植区内AChE阳性神经元数、细胞面积和纤维密度。结果:NGF主要有利于AChE阳性神经元存活,并有轻微促进突起发育生长的作用,BDNF促进胞体和突起发育生长的作用较强;培养4天时,BDNF+NGF组的指标优于NGF组,但和BDNF组比较无显著性差异。培养8天时,NGF+BDNF组的指标优于NGF组或BDNF组。脑移植区中,应用神经营养因子动物AChE阳性神经元的形态学指标好于对照组,而NGF+BDNF组的指标又优于NGF组或BDNF组。结论:细胞培养中BDNF对胚基底前脑胆碱能神经元的作用较NGF早;NGF和BDNF在胚基底前脑胆碱能神经元早期发育生长中的作用各有侧重,两者联合使用在体内、外均可发挥协同作用。
, http://www.100md.com
[中图分类号] R338 [文献标识码] A
[文章编号]1000-2057(2000)01-0009-04
SYNERGIC EFFECTS OF NEUROTROPHINS NGF AND BDNF ON THE DEVELOPMENT
OF THE FETAL FOREBRAIN CHOLINERGIC NEURONS IN VITRO AND IN VIVO
JIN Guohua XU Huijun TIAN Meiling
(Department of Anatomy and Neurobiology, Nantong Medical College, Nantong 226001)
, http://www.100md.com
[Abstract] Objective:In the present study, the combination of two neurotrophic factors, i.e., NGF and BDNF were used to investigate the synergitic effects of these factors on the development of fetal forebrain cholinergic neurons. Methods: The experiments were divided into NGF, BDNF, NGF+BDNF and control groups. Using the techniques of cell culture, brain transplantation, AChE histochemical staining, micromeasure and image analysis, the number of AChE positive neurons of fetal forebrain, the diameter of cell bodies, the number of processes and the length of the longest processes were detected respectively on the 4th and 8th day after culture and the number of AChE positive neurons, the size of neurons and the density of fibers in the grafts were also investigated 4.5 months after grafting.Results: In the cell culture, NGF mainly increased the number of AChE positive neurons and slightly promoted the development of the processes, while BDNF strongly stimulated the development of the cell bodies and processes. On 4 day after cell culture, the data of NGF+BDNF group were superior to that of NGF group, but no difference between BDNF+NGF group and NGF group. On the 8th day, the data of NGF+BDNF group were better than that of NGF or BDNF group. In brain grafts, the morphological data using neurotrophic factors were superior to that of control group, while data of NGF+BDNF group were better than NGF or BDNF group.Conclusion: The effective time of BDNF were earlier than that of NGF for the development of cholinergic neurons in embryonic basal forebrain in vitro. The effects of NGF and BDNF had its own strong points and combined use of NGF and BDNF may play the synergic role in vivo and vitro during the earlier development of the cholinergic neurons in embryonic basal forebrain.
, http://www.100md.com
[Key words] nerve growth factor;brain-derired neurotrophic factor;embryonic basal forebrain;cholinergic neuron;cell culture;brain transplantation;rats
研究证据表明神经营养因子对不同种类中枢神经元的存活、胞体发育和突起延伸具有促进作用[1~3]。但神经元在发育分化增殖过程中存活的微环境及参与调控的因子十分复杂, 决非仅受一种神经营养因子的影响。迄今对神经营养因子之间的联合作用还不甚清楚。本研究用体外培养方法和脑内移植手段,借助于AChE组化染色、显微测量和图象分析等方法研究了神经生长因子(Nerve growth factor, NGF)和脑源性神经营养因子(Brain-derived Neurotrophic Factor, BDNF)在体内、外联合使用时对鼠胚基底前脑胆碱能神经元发育生长的影响。
, http://www.100md.com
1 材料和方法
1.1 细胞培养 分NGF、BDNF、NGF+BDNF及对照4组。用1.07%DMEM(Sigma公司),另加10%小牛血清、3.5mmol/L NaHCO3、25mmol/L KCl、2mmol/L谷氨酰胺和50U/ml庆大霉素,前3组在培养液中分别加入NGF(7s,宝灵曼公司)、BDNF(周嘉伟博士惠赠)、NGF+BDNF,使浓度分别达到100ng/ml,对照组培养液中不加神经营养因子。表面涂以100μg/ml多聚赖氨酸的1cm2盖玻片分别放入2块24孔培养板各孔中,每板每组6孔。置37℃培养箱干燥备用。
无菌条件下取E17 SD鼠基底前脑原基,剪碎置0.125%胰酶37℃消化20分钟,终止消化后吸管反复吹打制成细胞悬液,200目不锈钢筛网过滤、悬液与台盼蓝按1∶1混合后计数成活细胞,然后将细胞悬液接种于培养板各孔中,使其密度为2×105/cm2。每孔中加入2ml含不同神经营养因子的培养液或单纯培养液。培养板置饱和湿度5%CO2培养箱37℃培养,分别于4d和8d后中止培养,取出盖玻片,4%多聚甲醛固定,参照Tago[4]方法行AChE组化染色,孵育时加入盐酸爱普吧嗪和氟丙磷以去除非特异性酯酶影响,最后脱水、透明、封片。显微镜下计数AChE阳性细胞数,每组每孔随机选25个AChE阳性细胞,测量或计数胞体平均直径、胞体发出突起数和每个细胞最长突起的长度。
, 百拇医药
1.2 脑内移植 220~250g SD大鼠用复合麻醉剂Chlorpent经腹腔麻醉(2ml/kg)后,固定于立体定位仪,参照Paxinos图谱,将0.14mol/L的使君子酸(QA,Sigma公司)分两点注入基底大细胞核(NBM),以损毁NBM、阻断胆碱能神经元对大脑皮层的投射,以利于观察植入的胚胆碱能神经元在皮层的发育情况。
取E15-17的同种大鼠胚基底前脑原基,根据Bjorklund[5]的方法制成每10μl含1块胚基底前脑原基的细胞悬液,按分组要求在悬液中分别加入NGF、BDNF和NGF+BDNF,浓度为0.25g/L,对照组不加神经营养因子。取24只损毁基底大细胞核的SD大鼠,随机分成NGF、BDNF、NGF+BDNF和对照4组,每组6只。动物麻醉后固定于立体定位仪,取左侧额、顶叶皮质为移植点。额叶坐标为A=1.7mm,L=3.0mm,V=2.2mm(脑膜下);顶叶坐标为A=-1.3mm,L=4.6mm,V=2.4mm(脑膜下)。每点在10min内用微量进样器注入7.5μl细胞悬液,留针10min后缓慢退针。移植完毕将长5mm带芯套管插入同侧侧脑室,用聚甲基丙烯酸甲酯将其快速固定于颅骨。按分组将用人工脑脊液配制的相应神经营养因子4μl(5g/L)注入侧脑室,1次/2d,共7次,于最后1次灌注的次日拔管,对照组灌注同量人工脑脊液。
, http://www.100md.com
动物饲养4.5个月,麻醉后经升主动脉灌注100ml生理盐水和400ml 4%多聚甲醛0.1mol/L PB(pH7.4)。在立体定位仪上取前囟前后4mm一段脑后固定入蔗糖平衡,次日行冰冻连续切片,厚40μm,共收集4套。第1套尼氏染色;第2套乙酰胆碱酯酶(AChE)组化染色[4];另2套作其它免疫组化染色用。AChE组化染色切片的移植区计数存活的AChE阳性神经元数;每张有移植区的切片随机抽取4只AChE阳性神经元,每只动物共40只细胞,用MIAS-300计算机图象处理系统进行细胞面积分析;参照Lewis[6]方法,在600×显微镜下,在移植区随机抽取3个视野,计数移植区中AChE阳性纤维在16900μm2网格中与纵横线的平均交点数,作为纤维密度的指标。
1.3 统计分析 以上所有统计资料用方差分析和SNK检验进行统计学处理。
2 结 果
, http://www.100md.com
2.1 细胞培养 培养4d时NGF组AChE阳性细胞较稀疏,胞体以梭形为主,胞体较小,染色较浅。见部分细胞发出突起,但以单突起或双突起多见,且突起较短(图1)。BDNF组见分散的AChE阳性神经元,胞体较大呈圆形、梭形或多角形,部分胞体已长出突起,双突起和多突起较多见(图2)。NGF+BDNF组AChE阳性细胞密度、胞体和突起状况与BDNF组类似。对照组各孔中均未见到AChE阳性细胞。培养8d时,NGF组AChE阳性神经元数量多,胞体以梭形、三角形或多角形为主,以单、双突起者为多,三突起或多突起者相对少见,最长突起约500μm,突起较细(图3)。BDNF组AChE阳性神经元数量较多,胞体也较大,呈梭形、圆形或多角形,双突起、三突起或多突起多见,突起较长,最长突起可达780μm,突起也较粗(图4)。NGF+BDNF组AChE阳性神经元数量也多,胞体亦大,三突起和多突起较多见,最长突起700μm,突起粗(图5)。对照组AChE阳性神经元较少,胞体也较小,呈圆形、梭形或三角形,以单、双突起为主,偶见三突起或多突起,且突起较短、较细,最长突起约200μm。培养4d和8d时各组AChE阳性神经元数、胞体平均直径、胞体发出的突起数及最长突起长度结果详见表1。
, 百拇医药
方差分析和SNK检验发现培养4d时4项指标BDNF组、NGF+BDNF组与NGF组之间差异均有显著性,而BDNF组与NGF+BDNF组之间差异无显著性。培养8d时,AChE阳性神经元数除NGF组与NGF+BDNF组之间差异无显著性外,其余各组间差异均有显著性;胞体平均直径除BDNF组与NGF+BDNF组及NGF组与对照组之间差异无显著性外,其余各组间差异均有显著性;细胞发出的突起数和最长突起长度除BDNF组与NGF+BDNF组之间差异无显著性外,其余各组间差异均有显著性。 表1 培养4d和8d时AChE阳性神经元生长情况(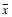 ±s)
±s)
NGF组
BDNF组
NGF+BDNF组
对照组
, 百拇医药
4d
8d
4d
8d
4d
8d
4d
8d
AChE阳性细胞数
胞体平均直径(μm)
突起数/细胞
最长突起长度(μm)
155.7±21.6
, 百拇医药
9.83±0.43
1.17±0.14
6.37±0.82
248.0±33.3
11.61±0.69
2.17±0.16
117.04±26.27
187.2±18.1
11.40±0.67
2.00±0.33
11.97±3.91
, http://www.100md.com 198.0±25.1
13.97±1.06
2.81±0.16
188.6±31.2
193.7±32.5
11.99±0.48
2.18±0.51
14.37±1.25
257.5±58.7
13.73±1.98
2.77±0.17
182.07±31.21
, http://www.100md.com
/
/
/
/
105.2±25.9
10.81±1.79
1.82±0.18
69.12±8.56
2.2 脑内移植区AChE阳性神经元情况 尼氏染色片见4组动物移植区细胞均能存活,移植区镶嵌在皮质中。移植区细胞成群分布,以中等大小细胞多见。和对照组相比可看出应用神经营养因子动物移植区细胞多,胶质细胞少,部分边界消失(图6)。AChE组化染色片中,各组移植区AChE阳性神经元散在或成群分布,以移植区和宿主交界处多见;深染的纤维呈网状或斑片状,部分AChE阳性纤维伸入到宿主皮质,以应用神经营养因子的动物多见。应用神经营养因子的各组和对照组比较,移植区较大,AChE阳性神经元较多、面积较大,纤维密度较高,在应用神经营养因子的各组中又以NGF+BDNF组的结果较好(图7-9)。4组实验动物移植区AChE阳性神经元有关统计指标结果详见表2。
, 百拇医药
SNK检验结果显示,AChE阳性神经元数各组间比较,其差异均有显著性(P<0.05或0.01),AChE阳性神经元面积和AChE阳性纤维交点数各组间比较,除NGF组与BDNF组之间差异无显著性外,其余各组间差异均有显著性(P<0.05或0.01)。 表2 4组实验动物移植区AChE阳性神经元有关指标统计结果(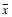 ±s)
±s)
有关指标
NGF组
BDNF组
NGF+BDNF组
对照组
方差分析
F3.20
, 百拇医药
P
AChE阳性神经元数
AChE阳性神经元面积(μm2)
AChE阳性纤维交点数
252±27
1960±129
61±8
205±31
1762±168
60±9
295±42
2181±279
, http://www.100md.com
76±13
158±28
1410±167
44±7
17.20
16.03
11.79
<0.01
<0.01
<0.01
图1 NGF组培养4天时,AChE阳性神经元较小,染色较淡,发出单突起或双突起。×132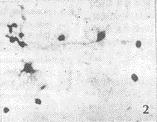
, 百拇医药
图2 BDNF组培养4天时,AChE阳性神经元较大,发出双突起或多突起。×132
图3 NGF组培养8天时,AChE阳性神经元较小,双突起较细。×132
图4 BDNF组培养8天时,AChE阳性神经元胞体较大,多突起较粗较长。×132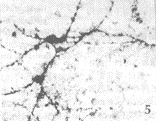
图5 NGF+BDNF组培养8天时,两只大胞体的AChE阳性神经元,其多突起较粗较长。×132
图6 尼氏染色,示移植区中(G)和宿主皮质(H)交界(↑)已不明显。×10
, 百拇医药
图7 NGF组移植区中成簇的AChE阳性神经元。×100
图8 BDNF组移植区中成簇的AChE阳性神经元。×100
图9 NGF+BDNF组移植区中一群大胞体、突起丰富的AChE阳性神经元。×100
3 讨 论
神经营养因子对神经元发育生长的作用及在神经元受到损害时对神经元的保护和促进神经再生的作用已成为当前神经科学领域研究的热点课题。以往资料表明NGF、BDNF等神经营养因子,对胚基底前脑胆碱能神经元的存活和分化具有促进作用[1~3]。但对这些神经元分化的研究,大多着重于胆碱乙酰转移酶(choline acetyltransferase, ChAT)的活力研究。而不同神经营养因子对神经元发育分化和突起发育生长的作用是否相同,以及神经营养因子间有否协同作用的研究较少。
, 百拇医药
本研究发现,在胚基底前脑胆碱能神经元的早期培养中,NGF的主要作用是提高胚胆碱能神经元的存活率,对突起发育有轻微作用且作用较迟,对胞体的作用不显著。而BDNF则在早期即表现为对胞体和突起的发育有较强的作用。这与Knusel[1]在检测培养的胚基底前脑胆碱能神经元ChAT活力时发现BDNF在培养的头几天特别有效,而NGF在后期具有较大刺激作用的结果相似。这些结果提示NGF和BDNF所起的作用时期不同。而且BDNF对突起的延伸作用优于NGF。NGF和BDNF联合使用时,在第4d与BDNF组比较,形态学发育的优势还不明显,但到第8d时,形态学发育的优势很显著,明显地好于单独使用NGF或BDNF组的指标。提示NGF和BDNF联合使用对胚胆碱能神经元发育生长具有协同作用。
脑内移植研究的形态学结果也揭示,应用神经营养因子动物的移植区中,AChE阳性神经元明显增多、胞体面积和纤维密度明显增大。联合使用NGF和BDNF时,上述的指标均好于单独使用NGF或BDNF的动物,这与体外细胞培养所得结果是一致的。表明NGF和BDNF的协同作用不仅在体外有效,在体内也产生同样的效应。
, http://www.100md.com
NGF和BDNF对体内、外的胚基底前脑胆碱能神经元发育生长发挥协同作用的机制可能是:(1)NGF和BDNF对胚胆碱能神经元的作用具有不同的时间窗,从而在时程上互补而发挥了协同作用。Knusel等[1]曾提出这一假设,本研究的结果又予以进一步证实。(2)NGF和BDNF两种神经营养因子的高亲和力受体不同。现已知P75NGFR既是NGF又是BDNF的低亲和力受体[7],但它们的高亲和力受体则不同,分别为trk(trkA)和trkB[8]。有研究资料证实,这种高亲和力受体在神经营养因子介导的细胞内反应中发挥主要作用[9,10]。Lachyankar等[11]提出,体外培养的神经元早期即能表达trk和trkB等受体。NGF和BDNF可能分别通过同一胚胆碱能神经元上的高亲和力受体trk和trkB两条信号传递途径介导细胞的生物反应,从而产生作用的不完全叠加而发挥协同作用。
神经元的存活与发育生长受许多不同分子的影响。脑内的神经元都处于特定的复杂微环境中,这种微环境中可能含有多种神经营养因子和其它分子物质。因此在神经细胞分化的研究中使用两种或多种因子,使之接近脑内复杂的微环境,会更有利于神经元的发育生长。
, http://www.100md.com
Nishi提出了几种神经营养因子联合使用可发挥协同作用的观点[12]。Knusel等[1]和Kato等[13]分别在胚基底前脑胆碱能神经元和胚脊髓运动神经元的培养中发现,神经营养因子的联合使用在提高这些神经元的ChAT活力方面可发挥协同作用。而我们这一研究结果又进一步从形态学方面证实了这种协同作用。本文仅是研究了同一家族中的两个神经营养因子联合使用时,对胚基底前脑胆碱能神经元发育生长的协同作用。而对这一家族中的其它神经营养因子或其它家族中的神经营养因子不同组合的作用有待于进一步研究。
[参考文献]
[1] Knusel B, Winslow JW, Rosenthal A, et al. Promotion of central cholinergic and dopaminergic neuron differentiation by brain-derived neurotrophic factor but not neurotrophin 3[J]. Proc Natl Acad Sci USA, 1991,88∶961.
, 百拇医药
[2] Aldersen RF, Alterman AL, Barde YA, et al. Brain-derived neurotrophic factor increases survival and differentiated functions of rat septal cholinergic neurons in culture[J]. Neuron,1990,5∶297.
[3] Meuton PR and Olson L. Nerve growth factor increases the size of intracortical cholinergic transplants[J]. Acta Neurol Scand,1993,87∶376.
[4] Tago H, Kimura H and Maeda T. Visualization of detailed acetylcholinesterase fiber and neuron staining in rat brain by a sensitive histochemical procedure[J]. J Histochem Cytochem, 1986,34∶1431.
, 百拇医药
[5] Bjorklund A, Stenevi V, Schmidt RH, et al. Intracerebral grafting of neuronal cell suspensions. I. Introduction and general methods of preparation[J]. Acta Physiol Scand, 1983,522(suppl)∶1.
[6] Lewis DA. Distribution of choline acetyltransferase immunoreactive axons in monkey frontal cortex[J]. Neurosci,1991,40∶363.
[7] Rodrigues-Tebar A, Dechant G and Barde YA. Binding of brain-derived neurotrophic factor to the nerve growth factor receptor[J]. Neuron, 1990,4∶487.
, 百拇医药
[8] Chao MV. Neurotrophin receptors: A window into neuronal differentiation[J]. Neuron,1992,9∶583.
[9] Kaplan DR, Hempstead BL Marti-Zanca D, et al. The trk proto-oncogene product: a signal transducing receptor for nerve growth factor[J]. Science, 1991, 252∶ 554.
[10] Ringstedt T, Lagercrantz H and Persson H. Expression of members of the trk family in the developing postnatal rat brain[J]. Dev Brain Res, 1993,72∶119.
, 百拇医药
[11] Lachyankar MB, Condon PJ, Quesenberry PJ, et al. Embryonic precursor cells that express trk receptors: induction of different cell fates by NGF, BDNF, NT-3, and CNTF[J]. Exp Neurol, 1997,144∶350.
[12] Nishi R.Neurotrophic factors: Two are better than one[J]. Science, 1994,265∶1052.
[13] Kato AC and Lindsay RM. Overlapping and additive effects of neurotrophins and CNTF on cultured human spinal cord neurons[J]. Exp Neurol, 1994,130∶196.
(1999-11-03收稿), 百拇医药
单位:南通医学院神经生物学研究室,南通226001
关键词:神经生长因子;脑源性神经营养因子;胚基底前脑;胆碱能神经元;细胞培养;脑内移植;大鼠
南通医学院学报000104[摘 要] 目的:探讨神经营养因子NGF、BDNF联合使用时对鼠胚基底前脑胆碱能神经元发育生长的协同作用。方法:实验分成NGF、BDNF、NGF+BDNF和对照4组。采用细胞培养和脑内移植手段及AChE组化染色、显微测量和图象分析等技术。检测各组胚基底前脑培养4天和8天时的AChE阳性神经元数、胞体直径、胞体发出的突起数及最长突起长度以及胚基底前脑移植至脑内4.5个月时移植区内AChE阳性神经元数、细胞面积和纤维密度。结果:NGF主要有利于AChE阳性神经元存活,并有轻微促进突起发育生长的作用,BDNF促进胞体和突起发育生长的作用较强;培养4天时,BDNF+NGF组的指标优于NGF组,但和BDNF组比较无显著性差异。培养8天时,NGF+BDNF组的指标优于NGF组或BDNF组。脑移植区中,应用神经营养因子动物AChE阳性神经元的形态学指标好于对照组,而NGF+BDNF组的指标又优于NGF组或BDNF组。结论:细胞培养中BDNF对胚基底前脑胆碱能神经元的作用较NGF早;NGF和BDNF在胚基底前脑胆碱能神经元早期发育生长中的作用各有侧重,两者联合使用在体内、外均可发挥协同作用。
, http://www.100md.com
[中图分类号] R338 [文献标识码] A
[文章编号]1000-2057(2000)01-0009-04
SYNERGIC EFFECTS OF NEUROTROPHINS NGF AND BDNF ON THE DEVELOPMENT
OF THE FETAL FOREBRAIN CHOLINERGIC NEURONS IN VITRO AND IN VIVO
JIN Guohua XU Huijun TIAN Meiling
(Department of Anatomy and Neurobiology, Nantong Medical College, Nantong 226001)
, http://www.100md.com
[Abstract] Objective:In the present study, the combination of two neurotrophic factors, i.e., NGF and BDNF were used to investigate the synergitic effects of these factors on the development of fetal forebrain cholinergic neurons. Methods: The experiments were divided into NGF, BDNF, NGF+BDNF and control groups. Using the techniques of cell culture, brain transplantation, AChE histochemical staining, micromeasure and image analysis, the number of AChE positive neurons of fetal forebrain, the diameter of cell bodies, the number of processes and the length of the longest processes were detected respectively on the 4th and 8th day after culture and the number of AChE positive neurons, the size of neurons and the density of fibers in the grafts were also investigated 4.5 months after grafting.Results: In the cell culture, NGF mainly increased the number of AChE positive neurons and slightly promoted the development of the processes, while BDNF strongly stimulated the development of the cell bodies and processes. On 4 day after cell culture, the data of NGF+BDNF group were superior to that of NGF group, but no difference between BDNF+NGF group and NGF group. On the 8th day, the data of NGF+BDNF group were better than that of NGF or BDNF group. In brain grafts, the morphological data using neurotrophic factors were superior to that of control group, while data of NGF+BDNF group were better than NGF or BDNF group.Conclusion: The effective time of BDNF were earlier than that of NGF for the development of cholinergic neurons in embryonic basal forebrain in vitro. The effects of NGF and BDNF had its own strong points and combined use of NGF and BDNF may play the synergic role in vivo and vitro during the earlier development of the cholinergic neurons in embryonic basal forebrain.
, http://www.100md.com
[Key words] nerve growth factor;brain-derired neurotrophic factor;embryonic basal forebrain;cholinergic neuron;cell culture;brain transplantation;rats
研究证据表明神经营养因子对不同种类中枢神经元的存活、胞体发育和突起延伸具有促进作用[1~3]。但神经元在发育分化增殖过程中存活的微环境及参与调控的因子十分复杂, 决非仅受一种神经营养因子的影响。迄今对神经营养因子之间的联合作用还不甚清楚。本研究用体外培养方法和脑内移植手段,借助于AChE组化染色、显微测量和图象分析等方法研究了神经生长因子(Nerve growth factor, NGF)和脑源性神经营养因子(Brain-derived Neurotrophic Factor, BDNF)在体内、外联合使用时对鼠胚基底前脑胆碱能神经元发育生长的影响。
, http://www.100md.com
1 材料和方法
1.1 细胞培养 分NGF、BDNF、NGF+BDNF及对照4组。用1.07%DMEM(Sigma公司),另加10%小牛血清、3.5mmol/L NaHCO3、25mmol/L KCl、2mmol/L谷氨酰胺和50U/ml庆大霉素,前3组在培养液中分别加入NGF(7s,宝灵曼公司)、BDNF(周嘉伟博士惠赠)、NGF+BDNF,使浓度分别达到100ng/ml,对照组培养液中不加神经营养因子。表面涂以100μg/ml多聚赖氨酸的1cm2盖玻片分别放入2块24孔培养板各孔中,每板每组6孔。置37℃培养箱干燥备用。
无菌条件下取E17 SD鼠基底前脑原基,剪碎置0.125%胰酶37℃消化20分钟,终止消化后吸管反复吹打制成细胞悬液,200目不锈钢筛网过滤、悬液与台盼蓝按1∶1混合后计数成活细胞,然后将细胞悬液接种于培养板各孔中,使其密度为2×105/cm2。每孔中加入2ml含不同神经营养因子的培养液或单纯培养液。培养板置饱和湿度5%CO2培养箱37℃培养,分别于4d和8d后中止培养,取出盖玻片,4%多聚甲醛固定,参照Tago[4]方法行AChE组化染色,孵育时加入盐酸爱普吧嗪和氟丙磷以去除非特异性酯酶影响,最后脱水、透明、封片。显微镜下计数AChE阳性细胞数,每组每孔随机选25个AChE阳性细胞,测量或计数胞体平均直径、胞体发出突起数和每个细胞最长突起的长度。
, 百拇医药
1.2 脑内移植 220~250g SD大鼠用复合麻醉剂Chlorpent经腹腔麻醉(2ml/kg)后,固定于立体定位仪,参照Paxinos图谱,将0.14mol/L的使君子酸(QA,Sigma公司)分两点注入基底大细胞核(NBM),以损毁NBM、阻断胆碱能神经元对大脑皮层的投射,以利于观察植入的胚胆碱能神经元在皮层的发育情况。
取E15-17的同种大鼠胚基底前脑原基,根据Bjorklund[5]的方法制成每10μl含1块胚基底前脑原基的细胞悬液,按分组要求在悬液中分别加入NGF、BDNF和NGF+BDNF,浓度为0.25g/L,对照组不加神经营养因子。取24只损毁基底大细胞核的SD大鼠,随机分成NGF、BDNF、NGF+BDNF和对照4组,每组6只。动物麻醉后固定于立体定位仪,取左侧额、顶叶皮质为移植点。额叶坐标为A=1.7mm,L=3.0mm,V=2.2mm(脑膜下);顶叶坐标为A=-1.3mm,L=4.6mm,V=2.4mm(脑膜下)。每点在10min内用微量进样器注入7.5μl细胞悬液,留针10min后缓慢退针。移植完毕将长5mm带芯套管插入同侧侧脑室,用聚甲基丙烯酸甲酯将其快速固定于颅骨。按分组将用人工脑脊液配制的相应神经营养因子4μl(5g/L)注入侧脑室,1次/2d,共7次,于最后1次灌注的次日拔管,对照组灌注同量人工脑脊液。
, http://www.100md.com
动物饲养4.5个月,麻醉后经升主动脉灌注100ml生理盐水和400ml 4%多聚甲醛0.1mol/L PB(pH7.4)。在立体定位仪上取前囟前后4mm一段脑后固定入蔗糖平衡,次日行冰冻连续切片,厚40μm,共收集4套。第1套尼氏染色;第2套乙酰胆碱酯酶(AChE)组化染色[4];另2套作其它免疫组化染色用。AChE组化染色切片的移植区计数存活的AChE阳性神经元数;每张有移植区的切片随机抽取4只AChE阳性神经元,每只动物共40只细胞,用MIAS-300计算机图象处理系统进行细胞面积分析;参照Lewis[6]方法,在600×显微镜下,在移植区随机抽取3个视野,计数移植区中AChE阳性纤维在16900μm2网格中与纵横线的平均交点数,作为纤维密度的指标。
1.3 统计分析 以上所有统计资料用方差分析和SNK检验进行统计学处理。
2 结 果
, http://www.100md.com
2.1 细胞培养 培养4d时NGF组AChE阳性细胞较稀疏,胞体以梭形为主,胞体较小,染色较浅。见部分细胞发出突起,但以单突起或双突起多见,且突起较短(图1)。BDNF组见分散的AChE阳性神经元,胞体较大呈圆形、梭形或多角形,部分胞体已长出突起,双突起和多突起较多见(图2)。NGF+BDNF组AChE阳性细胞密度、胞体和突起状况与BDNF组类似。对照组各孔中均未见到AChE阳性细胞。培养8d时,NGF组AChE阳性神经元数量多,胞体以梭形、三角形或多角形为主,以单、双突起者为多,三突起或多突起者相对少见,最长突起约500μm,突起较细(图3)。BDNF组AChE阳性神经元数量较多,胞体也较大,呈梭形、圆形或多角形,双突起、三突起或多突起多见,突起较长,最长突起可达780μm,突起也较粗(图4)。NGF+BDNF组AChE阳性神经元数量也多,胞体亦大,三突起和多突起较多见,最长突起700μm,突起粗(图5)。对照组AChE阳性神经元较少,胞体也较小,呈圆形、梭形或三角形,以单、双突起为主,偶见三突起或多突起,且突起较短、较细,最长突起约200μm。培养4d和8d时各组AChE阳性神经元数、胞体平均直径、胞体发出的突起数及最长突起长度结果详见表1。
, 百拇医药
方差分析和SNK检验发现培养4d时4项指标BDNF组、NGF+BDNF组与NGF组之间差异均有显著性,而BDNF组与NGF+BDNF组之间差异无显著性。培养8d时,AChE阳性神经元数除NGF组与NGF+BDNF组之间差异无显著性外,其余各组间差异均有显著性;胞体平均直径除BDNF组与NGF+BDNF组及NGF组与对照组之间差异无显著性外,其余各组间差异均有显著性;细胞发出的突起数和最长突起长度除BDNF组与NGF+BDNF组之间差异无显著性外,其余各组间差异均有显著性。 表1 培养4d和8d时AChE阳性神经元生长情况(
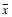 ±s)
±s)NGF组
BDNF组
NGF+BDNF组
对照组
, 百拇医药
4d
8d
4d
8d
4d
8d
4d
8d
AChE阳性细胞数
胞体平均直径(μm)
突起数/细胞
最长突起长度(μm)
155.7±21.6
, 百拇医药
9.83±0.43
1.17±0.14
6.37±0.82
248.0±33.3
11.61±0.69
2.17±0.16
117.04±26.27
187.2±18.1
11.40±0.67
2.00±0.33
11.97±3.91
, http://www.100md.com 198.0±25.1
13.97±1.06
2.81±0.16
188.6±31.2
193.7±32.5
11.99±0.48
2.18±0.51
14.37±1.25
257.5±58.7
13.73±1.98
2.77±0.17
182.07±31.21
, http://www.100md.com
/
/
/
/
105.2±25.9
10.81±1.79
1.82±0.18
69.12±8.56
2.2 脑内移植区AChE阳性神经元情况 尼氏染色片见4组动物移植区细胞均能存活,移植区镶嵌在皮质中。移植区细胞成群分布,以中等大小细胞多见。和对照组相比可看出应用神经营养因子动物移植区细胞多,胶质细胞少,部分边界消失(图6)。AChE组化染色片中,各组移植区AChE阳性神经元散在或成群分布,以移植区和宿主交界处多见;深染的纤维呈网状或斑片状,部分AChE阳性纤维伸入到宿主皮质,以应用神经营养因子的动物多见。应用神经营养因子的各组和对照组比较,移植区较大,AChE阳性神经元较多、面积较大,纤维密度较高,在应用神经营养因子的各组中又以NGF+BDNF组的结果较好(图7-9)。4组实验动物移植区AChE阳性神经元有关统计指标结果详见表2。
, 百拇医药
SNK检验结果显示,AChE阳性神经元数各组间比较,其差异均有显著性(P<0.05或0.01),AChE阳性神经元面积和AChE阳性纤维交点数各组间比较,除NGF组与BDNF组之间差异无显著性外,其余各组间差异均有显著性(P<0.05或0.01)。 表2 4组实验动物移植区AChE阳性神经元有关指标统计结果(
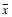 ±s)
±s)有关指标
NGF组
BDNF组
NGF+BDNF组
对照组
方差分析
F3.20
, 百拇医药
P
AChE阳性神经元数
AChE阳性神经元面积(μm2)
AChE阳性纤维交点数
252±27
1960±129
61±8
205±31
1762±168
60±9
295±42
2181±279
, http://www.100md.com
76±13
158±28
1410±167
44±7
17.20
16.03
11.79
<0.01
<0.01
<0.01

图1 NGF组培养4天时,AChE阳性神经元较小,染色较淡,发出单突起或双突起。×132

, 百拇医药
图2 BDNF组培养4天时,AChE阳性神经元较大,发出双突起或多突起。×132

图3 NGF组培养8天时,AChE阳性神经元较小,双突起较细。×132

图4 BDNF组培养8天时,AChE阳性神经元胞体较大,多突起较粗较长。×132

图5 NGF+BDNF组培养8天时,两只大胞体的AChE阳性神经元,其多突起较粗较长。×132

图6 尼氏染色,示移植区中(G)和宿主皮质(H)交界(↑)已不明显。×10

, 百拇医药
图7 NGF组移植区中成簇的AChE阳性神经元。×100

图8 BDNF组移植区中成簇的AChE阳性神经元。×100

图9 NGF+BDNF组移植区中一群大胞体、突起丰富的AChE阳性神经元。×100
3 讨 论
神经营养因子对神经元发育生长的作用及在神经元受到损害时对神经元的保护和促进神经再生的作用已成为当前神经科学领域研究的热点课题。以往资料表明NGF、BDNF等神经营养因子,对胚基底前脑胆碱能神经元的存活和分化具有促进作用[1~3]。但对这些神经元分化的研究,大多着重于胆碱乙酰转移酶(choline acetyltransferase, ChAT)的活力研究。而不同神经营养因子对神经元发育分化和突起发育生长的作用是否相同,以及神经营养因子间有否协同作用的研究较少。
, 百拇医药
本研究发现,在胚基底前脑胆碱能神经元的早期培养中,NGF的主要作用是提高胚胆碱能神经元的存活率,对突起发育有轻微作用且作用较迟,对胞体的作用不显著。而BDNF则在早期即表现为对胞体和突起的发育有较强的作用。这与Knusel[1]在检测培养的胚基底前脑胆碱能神经元ChAT活力时发现BDNF在培养的头几天特别有效,而NGF在后期具有较大刺激作用的结果相似。这些结果提示NGF和BDNF所起的作用时期不同。而且BDNF对突起的延伸作用优于NGF。NGF和BDNF联合使用时,在第4d与BDNF组比较,形态学发育的优势还不明显,但到第8d时,形态学发育的优势很显著,明显地好于单独使用NGF或BDNF组的指标。提示NGF和BDNF联合使用对胚胆碱能神经元发育生长具有协同作用。
脑内移植研究的形态学结果也揭示,应用神经营养因子动物的移植区中,AChE阳性神经元明显增多、胞体面积和纤维密度明显增大。联合使用NGF和BDNF时,上述的指标均好于单独使用NGF或BDNF的动物,这与体外细胞培养所得结果是一致的。表明NGF和BDNF的协同作用不仅在体外有效,在体内也产生同样的效应。
, http://www.100md.com
NGF和BDNF对体内、外的胚基底前脑胆碱能神经元发育生长发挥协同作用的机制可能是:(1)NGF和BDNF对胚胆碱能神经元的作用具有不同的时间窗,从而在时程上互补而发挥了协同作用。Knusel等[1]曾提出这一假设,本研究的结果又予以进一步证实。(2)NGF和BDNF两种神经营养因子的高亲和力受体不同。现已知P75NGFR既是NGF又是BDNF的低亲和力受体[7],但它们的高亲和力受体则不同,分别为trk(trkA)和trkB[8]。有研究资料证实,这种高亲和力受体在神经营养因子介导的细胞内反应中发挥主要作用[9,10]。Lachyankar等[11]提出,体外培养的神经元早期即能表达trk和trkB等受体。NGF和BDNF可能分别通过同一胚胆碱能神经元上的高亲和力受体trk和trkB两条信号传递途径介导细胞的生物反应,从而产生作用的不完全叠加而发挥协同作用。
神经元的存活与发育生长受许多不同分子的影响。脑内的神经元都处于特定的复杂微环境中,这种微环境中可能含有多种神经营养因子和其它分子物质。因此在神经细胞分化的研究中使用两种或多种因子,使之接近脑内复杂的微环境,会更有利于神经元的发育生长。
, http://www.100md.com
Nishi提出了几种神经营养因子联合使用可发挥协同作用的观点[12]。Knusel等[1]和Kato等[13]分别在胚基底前脑胆碱能神经元和胚脊髓运动神经元的培养中发现,神经营养因子的联合使用在提高这些神经元的ChAT活力方面可发挥协同作用。而我们这一研究结果又进一步从形态学方面证实了这种协同作用。本文仅是研究了同一家族中的两个神经营养因子联合使用时,对胚基底前脑胆碱能神经元发育生长的协同作用。而对这一家族中的其它神经营养因子或其它家族中的神经营养因子不同组合的作用有待于进一步研究。
[参考文献]
[1] Knusel B, Winslow JW, Rosenthal A, et al. Promotion of central cholinergic and dopaminergic neuron differentiation by brain-derived neurotrophic factor but not neurotrophin 3[J]. Proc Natl Acad Sci USA, 1991,88∶961.
, 百拇医药
[2] Aldersen RF, Alterman AL, Barde YA, et al. Brain-derived neurotrophic factor increases survival and differentiated functions of rat septal cholinergic neurons in culture[J]. Neuron,1990,5∶297.
[3] Meuton PR and Olson L. Nerve growth factor increases the size of intracortical cholinergic transplants[J]. Acta Neurol Scand,1993,87∶376.
[4] Tago H, Kimura H and Maeda T. Visualization of detailed acetylcholinesterase fiber and neuron staining in rat brain by a sensitive histochemical procedure[J]. J Histochem Cytochem, 1986,34∶1431.
, 百拇医药
[5] Bjorklund A, Stenevi V, Schmidt RH, et al. Intracerebral grafting of neuronal cell suspensions. I. Introduction and general methods of preparation[J]. Acta Physiol Scand, 1983,522(suppl)∶1.
[6] Lewis DA. Distribution of choline acetyltransferase immunoreactive axons in monkey frontal cortex[J]. Neurosci,1991,40∶363.
[7] Rodrigues-Tebar A, Dechant G and Barde YA. Binding of brain-derived neurotrophic factor to the nerve growth factor receptor[J]. Neuron, 1990,4∶487.
, 百拇医药
[8] Chao MV. Neurotrophin receptors: A window into neuronal differentiation[J]. Neuron,1992,9∶583.
[9] Kaplan DR, Hempstead BL Marti-Zanca D, et al. The trk proto-oncogene product: a signal transducing receptor for nerve growth factor[J]. Science, 1991, 252∶ 554.
[10] Ringstedt T, Lagercrantz H and Persson H. Expression of members of the trk family in the developing postnatal rat brain[J]. Dev Brain Res, 1993,72∶119.
, 百拇医药
[11] Lachyankar MB, Condon PJ, Quesenberry PJ, et al. Embryonic precursor cells that express trk receptors: induction of different cell fates by NGF, BDNF, NT-3, and CNTF[J]. Exp Neurol, 1997,144∶350.
[12] Nishi R.Neurotrophic factors: Two are better than one[J]. Science, 1994,265∶1052.
[13] Kato AC and Lindsay RM. Overlapping and additive effects of neurotrophins and CNTF on cultured human spinal cord neurons[J]. Exp Neurol, 1994,130∶196.
(1999-11-03收稿), 百拇医药