成人骨髓红细胞中胎儿珠蛋白基因在培养条件下重新活化△
作者:阳学贤 张俊武* 赵华路 黄小东 潘阳杏
单位:中国医学科学院 中国协和医科大学 基础医学研究所,北京100005
关键词:人胎儿珠蛋白基因;重新活化 ;细胞因子; 贫血治疗
基础医学与临床990510 摘要 本文研究转化生长因子β1(TGF-β1)和P53对致癌物转化的大鼠气管上皮(RTE)细胞的影响。结果表明早期转化的RTE细胞(尚未具致瘤性)和恶性转化的RTE细胞(已具致瘤性)的条件培养基可以抑制原代RTE细胞的集落形成率(CFE),部分抑制早期转化RTE细胞的CFE,但对恶性转化的RTE细胞无抑制作用。TGF-β1中和抗体可以阻断这种抑制作用,表明条件培养基中可能有TGF-β1。转化RTE细胞分泌TGF-β1可使对后者有抗性作用的细胞具有生长优势。为了评价P53对RTE细胞转化的作用,将野生型,突变型P53分别导入早期转化的RTE,研究表明,野生型P53抑制,而突变型P53促进转染细胞的CFE。突变型P53可能增强TGF-β1的分泌,从而促进转染细胞在裸鼠中癌变。本研究表明突变型P53可能通过TGF-β1
, 百拇医药
Effect of TGF β1 and p53 on the Transformation of
Rat Tracheal Epithelial Cells
Wang Hong Chen Lei Han Naijun Dai Jinwen Zhao Chunxia Cheng Shujun
(Cancer Institute,Chinese Academy of Medcal Sciences,Peking Union Medical College,Beijing100021)
The present study was carried out to investigate the role of TGF β1 and p53 on carcinogen-transformed rat tracheal epithelial (RTE) cells.The results showed that the colony forming efficiency (CFE) of primary and early tranformed RTE cells (nontumorigenic) was inhibited or partialy inhibited respectively by the conditioned medium (CM) from early transformed and malignant transfomed RTE cells (tumorigenic in nude mice).No such inhibition of CM on malignant transformed RTE was observed.The inhibition of CM was blocked by TGF β1 neutralized antibody,indicating the possible presence of TGF β1 in the CM.The secretion of TGF β1 produced by early and malignant transformed RTE cells may provide a selective advantage for the growth of transformed RTE cells which are resistant to TGF β1.In order to evalute the role of p53 during RTE transformation,wild or mutant p53 was transfected into early transformed RTE cells.It was observed that wild p53 could suppress and mutant p53 could increase CEF of the transfected cells.Mutant p53 probably increased TGF β1 secretion in CM,and enhanced malignant transformation of the transfected cells,when inoculated into nude mice.The results indicate that mutant p53 may promote tranformation of RTE cells through a TGF β1 autocrine/paracrine pathway.
, http://www.100md.com
Key words TGF β1 p53 Rat tracheal epithelial cell transformation
转化生长因子TGF-β1是个具有多重调节细胞生长功能的多肽,它可以抑制上皮细胞的生长,但很多肿瘤丧失了对TGF-β1抑制作用的应答[1]。TGF-β1是调节细胞周期的一个重要因子,在化学致癌的多步骤进程中,也起着重要的作用。在转化进程中,TGF-β1常表现出双重型,转化早期起着抑制的作用;随着转化的进程,转化细胞丧失了对TGF-β1抑制作用的效应[2]。P53基因是研究较为广泛的一个抑癌基因,几乎所有人类恶性肿瘤均发现有P53基因的突变或丢失[3]。P53和TGF-β1可能参与一条共同的途径调节细胞的生长和转化[4]。
, http://www.100md.com
本研究利用本室建立的RTE细胞转化模型,探讨P53及TGF-β1在气管上皮细胞转化中的作用及它们之间可能存在的关系。
1 材料与方法
1.1 材料
1.1.1 细胞系:致癌物甲基亚硝胺基吡啶基丁酮(NNK)和苯并(a)芘[B(a)P]转化的大鼠气管上皮(RTE)细胞系,由本室自建,以NNK转化的传至第15、21和45代(分别称NNK15、NNK21、NNK45),用B(a)P转化的传至第37代和41代(称B(a)P37和B(a)P41),其中NNK45和B(a)P37或B(a)P41已具有裸鼠致瘤性,而NNK15或NNK21还不具备裸鼠致瘤性[5]。
1.1.2 抗体:TGF-β1中和抗体为R&D公司产品,可特异性中和TGF-β1。
, 百拇医药
1.1.3 质粒:具有CMV启动子的人P53 cDNA真核表达型质粒PC53SN3,突变型p53(143val→ala)cDNA真核表达型质粒PC53CX3,为荷兰肿瘤研究所Dr. Rene Bernard惠赠。
1.1.4 条件培养基的制备:将NNK和B(a)P转化的RTE细胞,在选择培养基(成分为F12,含2%胎牛血清、5μg/mL胰岛素和0、1μg/mL氢化可的松)中培养,接种后48h去掉选择培养基,加入无血清的选择培养基,继续培养48h,收集培养基,离心去细胞碎片,所得的上清即为条件培养基。
1.2 方法
1.2.1 细胞集落形成实验:将原代RTE细胞、及NNK15、NNK45、B(a)P39细胞,以1×104细胞量接种于60mm平皿中,实验组培养基由去掉EGF的无血清完全培养基(完全培养基成分见文献6)分别和制备的NNK15、NNK45及B(a)P37条件培养基以1:1的比例混合组成,对照组培养基则由去EGF的无血清完全培养基和无血清的选择培养基以1:1的比例混合组成。培养7~10天,计数具有20个以上细胞的集落,计算细胞集落形成率(CFE)。
, 百拇医药
1.2.2 TGF-β1抗体中和实验:参照有关文献的方法[7],先将不同量TGF-β1抗体与收集的B(a)P41条件培养基共同孵育2h,然后将收获的原代RTE细胞以1×103/孔接种于24孔板,培养基由去EGF的完全培养基和TGF-β1抗体孵育的B(a)P41条件培养基以1:1比例混合组成。对照组分别为去血清的选择培养基和B(a)P41条件培养基,均相应与去EGF的完全培养基以1:1比例混合。继续培养7~10天,计数具有20个以上细胞的集落,并计算CFE及各组的相对CFE。
1.2.3 DNA转染及筛选:NNK21细胞培养到70%细胞密度时,换新鲜培养基,12h后转染。将10μg质粒DNA,与DOTAP混匀,缓慢加入,培养24h,换成新鲜培养基,有限稀释传代,并加入300μg/mL的G418连续筛选阳性细胞。
1.2.4 裸鼠致瘤实验:将转染野生型P53基因的NNK21 P53WT和突变型P53基因的NNK21P53MT及未转染细胞NNK21体外扩增,以5×106的细胞量接种于3~4周龄的裸鼠腹股沟,每组接种4只,无菌饲养观察。
, http://www.100md.com
2 结果
2.1 条件培养基对原代RTE细胞及转化细胞的作用
NNK15、NNK45、B(a)P37条件培养基均能强烈抑制原代RTE细胞的生长,部分抑制NNK早期转化的RTE细胞NNK15(无致瘤性)的生长,而对已恶性转化的细胞的生长无影响(表1)。
表1 条件培养基对原代及转化RTE细胞集落形成的影响
Table1 Effect of conditioned medium on the colony forming efficiency(CFE) of primary and transformed RTE cells(%, ±s)
±s)
Groups
, 百拇医药
CFF(100%)
Primary
NNK16
NNK47
B(a)P39
Control
0.99±0.04
8.94±0.18
9.84±0.56
9.90±0.48
NNK15
CM
, 百拇医药
0.02±0.09*
3.07±0.28*
9.46±0.14
9.43±0.09
NNK45
CM
0.04±0.01*
3.66±0.08*
9.85±0.01
9.85±0.43
B(a)P37
, 百拇医药
CM
0.02±0.01*
3.30±0.18*
9.83±0.26
9.75±0.38
*VS. control P<0.01; CM: Conditinoed medium
2.2 TGF-β1抗体阻断B(a)P41条件培养基对原代RTE细胞的抑制作用
随着TGF-β1抗体量的增加,原代RTE细胞的CFE上升,条件培养基对原代RTE细胞的抑制率下降(见表2)。
, 百拇医药
表2 TGF-β1抗体阻断B(a)P41条件培养基对原代RTE细胞集落形成的抑制作用
Table2 TGF-β1 neutralized antibody-induced blocking effect on the inhibition of colony forming efficiency(CEE)of primary RTE cells by conditioned medium from B(a)P41 cells
Groups
Primary RTE
CFE(%)±s
Relative CFE(%)
Control
, 百拇医药
2.62±0.06
100
a.B(a)P41CM
0.82±0.04**
31.3
b.B(a)P41CM+β1Ab(6μg/mL)
1.19±0.07
45.4
c.B(a)P41CM+β1Ab(15μg/mL)
1.73±0.03*
, 百拇医药
66.0
**a.vs.control P<0.01; *c.vs.a P<0.05; CM: Conditioned medium; β1:THF-β1 neutralized antibody.
2.3 转染野生型和突变型P53及未转染细胞集落形成实验
转染野生型P53的NNK21 P53WT细胞的集落形成率最低,与未转染的NNK21细胞相比差异显著(P<0.05),转染突变型P53的NNK21P53MT细胞集落形成率较高,但与NNK21细胞相比无统计学差异(见表3)。
表3 野生型、突变型P53基因转染对NNK21细胞的集落形成率的影响
Table3 Effect of the transfection of p53 wild or mutant type gene on the colony forming efficiency(CEE) of NNK21 cells(%, ±s)
±s)
, http://www.100md.com
Groups
CFE(%)
NNK21
6.60±0.62
NNK21P53WT
5.44±0.43*
NNK21P53MT
7.13±0.26
*vs. NNK21 p<0.05
2.4 转染野生型和突变型P53及未转染细胞条件培养基对原代RTE细胞生长的抑制作用
NNK21、NNK21P53WT和NNK21P53MT条件培养基均能抑制原代RTE细胞的生长,转染野生型P53质粒的NNK21P53WT细胞条件培养基的抑制率与未转染的NNK21细胞差别不大,而转染突变型P53质粒的NNK21P53MT细胞条件培养基对原代RTE细胞抑制较强(P<0.01)(见表4)。
, http://www.100md.com
图4 NNK21、NNK21P53WT、NNK21P53MT细胞条件培养基对原代RTE细胞集落形成的影响
Table4 Effect of the conditioned medium from NNK21,NNK210P53WT and NNK210P53MT on the colony forming efficiency(CFE) of primary RTE cells (%, ±s)
±s)
Groups
CFE(%)
a.Control
1.12±0.08
, http://www.100md.com
b.NNK21 CM
0.48±0.03
c.NNK21P53WT CM
0.55±0.06
d.NNK21P53MT CM
0.30±0.06
a.vs.b.c.d.P<0.01; b.vs.d.P<0.01 CM:Conditioned medium
2.5 裸鼠致瘤实验
转染野生型和突变型P53基因及未转染的NNK21细胞,接种裸鼠后均在接种处长出了肿块。分别取裸鼠长出肿块后20、60和200天的肿块,经病理诊断发现,未转染的NNK21细胞和NNK21P53WT细胞接种的裸鼠长出的是囊肿,未见有上皮细胞的增生。而NNK21P53MT细胞接种的裸鼠,20天时观察到了鳞状上皮细胞的增生,细胞核质比增大,呈复层鳞状排列;到60天细胞排列紊乱,病理诊断为不典型增生;200天时形成典型的鳞癌(见图1)。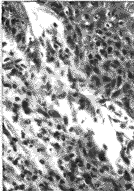

, 百拇医药
图1 NNK21p53MT细胞接种裸鼠200天后形成鳞状上皮细胞癌的组织切片,HE染色,示鳞状上皮细胞癌
Fig1 Histological section showing squamous cell carcinoma formd 200 days after the inoculation of NNK21p53MT cells into nude mice HE Staining (400×)
3 讨论
通过集落形成率的测定,发现化学致癌物早期转化和恶性转化的RTE细胞条件培养基可抑制正常RTE细胞的生长,部分抑制早期转化RTE细胞的生长,但对已具有致瘤性的恶性转化RTE细胞则无作用。Thomassen等报道TGF-β1可抑制正常原代RTE细胞的生长,部分抑制早期转化RTE细胞的生长,而已转化的RTE细胞则可拮抗TGF-β1的作用[8]。而我们的结果证明TGF-β1抗体可中和条件培养基对原代RTE细胞的抑制作用,表明转化RTE细胞可能分泌TGF-β1。Hagae等报道在大肠癌发生过程中,TGF-β1的分泌可以抑制正常细胞的生长,为对TGF-β1抑制作用已不敏感的恶性大肠癌细胞的生长选择一个优越的环境[9]。我们的研究表明在气管上皮细胞的转化过程中,TGF-β1也起着类似的选择性作用,从而促进气管上皮细胞的转化。
, 百拇医药
P53在气管上皮细胞的转化中也起着重要的作用。将野生型和突变型P53转染到尚未具有致瘤性的早期转化的NNK细胞中,发现野生型P53可以降低转染细胞的集落形成率。而野生型P53似可以增加NNK21细胞的集落形成率。Chen曾报道将野生型和突变型P53分别导入完全丢失内源性P53及内源性为突变型P53的骨肉瘤细胞系Saos-2,发现野生型P53的转染抑制了这两种细胞的恶性表型和致瘤性,同时突变型P53的转染略为增加了这两种细胞的生长速度[10]。我们的结果表明,突变型P53的转染可能会促进TGF-β1的分泌,并导致早期转化的NNK21细胞获得裸鼠致瘤性,成为恶性转化的RTE细胞,这不仅表明突变型P53是促进气管上皮细胞转化的一个重要因素,还表明了P53可能通过提高TGF-β1的分泌这条途径来促进气管上皮细胞的转化。但也不能排除另一种可能性,即导入突变型P53的气管上皮细胞降低了对TGF-β1的敏感性。由于TGF-β1作用的复杂性,在不同组织类型中TGF-β1的作用变化也很大,故P53与TGF-β1的关系值得进一步探讨。
, 百拇医药
△本研究经费由教委博点基金资助
1 Reiss M,Cowan JM,Vellucci VF,et al.Resistance of human squamous carcinoma cells to the antiproliferative effet of transforming growth factor b is a recessive phenotype.J Cell Biochem,1992,(Supple.16B):127
2 Gold LI,Saxena B,Mittal KR,et al.Increase expression of transforming growth factor β isoforms and basic fibroblast growth factor in complex hyperplasia and adenocarcionma of the endometrium: evdience for paracrine and autocrine.Cancer Research,1994,54:4855
, http://www.100md.com
3 Greenblatt MS,Bennett WP,Hollstein M,et al.Mutations in the p53 tumor suppresser gene: clues to cancer etiology and molecular pathogenesis.Cancer Research,1994,54:4855
4 Reiss M,Vellucci VF,Zhou ZL,et al.Mutant p53 tumor suppresser gene causes resistance to transforming growth factor beta 1 in murine keratinocytes.Cancer Research,1993,53:899
5 安兵,程书钧.NNK及X射线诱导大鼠气管上皮细胞的研究.癌变畸变突变,1993,5:9
6 高燕宁,程书钧,安兵,等.化学致癌物体外转化大鼠气管上皮细胞的研究.中国医学科学院学报,1990,12:325
, http://www.100md.com
7 Nettsheim P.Invitro analysis of multistage carcinogensis.Environ.Health prospect,1987,116:1109
8 Thomassen DG.Changes in cellular responses to inducers of differentiation,Growth factors,and oncogenes during neopastic progression of respiratory epithellial cells.In: Thomassen DG,and Nettesheim P,eds.Biology,toxicology and Carcinogenesis of respiratory epithelium.1st ed.USA.1990,205
9 Hague A,Manning A M,Van Der Stappen T W,et al.Escape from negative regulation of growth by transforming growth factor β and froms the imduction of apoptosis by the dictary agentsodium butyrate may be important in colorectal carcinogenesis.Cancer & Metastasis Reviews.1993,12:227
10 Chen PL,Molecular basis of cancer supression by the retinoblastoma and p53 genes.Diss Abstr Int [B],1993,53:1190, http://www.100md.com
单位:中国医学科学院 中国协和医科大学 基础医学研究所,北京100005
关键词:人胎儿珠蛋白基因;重新活化 ;细胞因子; 贫血治疗
基础医学与临床990510 摘要 本文研究转化生长因子β1(TGF-β1)和P53对致癌物转化的大鼠气管上皮(RTE)细胞的影响。结果表明早期转化的RTE细胞(尚未具致瘤性)和恶性转化的RTE细胞(已具致瘤性)的条件培养基可以抑制原代RTE细胞的集落形成率(CFE),部分抑制早期转化RTE细胞的CFE,但对恶性转化的RTE细胞无抑制作用。TGF-β1中和抗体可以阻断这种抑制作用,表明条件培养基中可能有TGF-β1。转化RTE细胞分泌TGF-β1可使对后者有抗性作用的细胞具有生长优势。为了评价P53对RTE细胞转化的作用,将野生型,突变型P53分别导入早期转化的RTE,研究表明,野生型P53抑制,而突变型P53促进转染细胞的CFE。突变型P53可能增强TGF-β1的分泌,从而促进转染细胞在裸鼠中癌变。本研究表明突变型P53可能通过TGF-β1
, 百拇医药
Effect of TGF β1 and p53 on the Transformation of
Rat Tracheal Epithelial Cells
Wang Hong Chen Lei Han Naijun Dai Jinwen Zhao Chunxia Cheng Shujun
(Cancer Institute,Chinese Academy of Medcal Sciences,Peking Union Medical College,Beijing100021)
The present study was carried out to investigate the role of TGF β1 and p53 on carcinogen-transformed rat tracheal epithelial (RTE) cells.The results showed that the colony forming efficiency (CFE) of primary and early tranformed RTE cells (nontumorigenic) was inhibited or partialy inhibited respectively by the conditioned medium (CM) from early transformed and malignant transfomed RTE cells (tumorigenic in nude mice).No such inhibition of CM on malignant transformed RTE was observed.The inhibition of CM was blocked by TGF β1 neutralized antibody,indicating the possible presence of TGF β1 in the CM.The secretion of TGF β1 produced by early and malignant transformed RTE cells may provide a selective advantage for the growth of transformed RTE cells which are resistant to TGF β1.In order to evalute the role of p53 during RTE transformation,wild or mutant p53 was transfected into early transformed RTE cells.It was observed that wild p53 could suppress and mutant p53 could increase CEF of the transfected cells.Mutant p53 probably increased TGF β1 secretion in CM,and enhanced malignant transformation of the transfected cells,when inoculated into nude mice.The results indicate that mutant p53 may promote tranformation of RTE cells through a TGF β1 autocrine/paracrine pathway.
, http://www.100md.com
Key words TGF β1 p53 Rat tracheal epithelial cell transformation
转化生长因子TGF-β1是个具有多重调节细胞生长功能的多肽,它可以抑制上皮细胞的生长,但很多肿瘤丧失了对TGF-β1抑制作用的应答[1]。TGF-β1是调节细胞周期的一个重要因子,在化学致癌的多步骤进程中,也起着重要的作用。在转化进程中,TGF-β1常表现出双重型,转化早期起着抑制的作用;随着转化的进程,转化细胞丧失了对TGF-β1抑制作用的效应[2]。P53基因是研究较为广泛的一个抑癌基因,几乎所有人类恶性肿瘤均发现有P53基因的突变或丢失[3]。P53和TGF-β1可能参与一条共同的途径调节细胞的生长和转化[4]。
, http://www.100md.com
本研究利用本室建立的RTE细胞转化模型,探讨P53及TGF-β1在气管上皮细胞转化中的作用及它们之间可能存在的关系。
1 材料与方法
1.1 材料
1.1.1 细胞系:致癌物甲基亚硝胺基吡啶基丁酮(NNK)和苯并(a)芘[B(a)P]转化的大鼠气管上皮(RTE)细胞系,由本室自建,以NNK转化的传至第15、21和45代(分别称NNK15、NNK21、NNK45),用B(a)P转化的传至第37代和41代(称B(a)P37和B(a)P41),其中NNK45和B(a)P37或B(a)P41已具有裸鼠致瘤性,而NNK15或NNK21还不具备裸鼠致瘤性[5]。
1.1.2 抗体:TGF-β1中和抗体为R&D公司产品,可特异性中和TGF-β1。
, 百拇医药
1.1.3 质粒:具有CMV启动子的人P53 cDNA真核表达型质粒PC53SN3,突变型p53(143val→ala)cDNA真核表达型质粒PC53CX3,为荷兰肿瘤研究所Dr. Rene Bernard惠赠。
1.1.4 条件培养基的制备:将NNK和B(a)P转化的RTE细胞,在选择培养基(成分为F12,含2%胎牛血清、5μg/mL胰岛素和0、1μg/mL氢化可的松)中培养,接种后48h去掉选择培养基,加入无血清的选择培养基,继续培养48h,收集培养基,离心去细胞碎片,所得的上清即为条件培养基。
1.2 方法
1.2.1 细胞集落形成实验:将原代RTE细胞、及NNK15、NNK45、B(a)P39细胞,以1×104细胞量接种于60mm平皿中,实验组培养基由去掉EGF的无血清完全培养基(完全培养基成分见文献6)分别和制备的NNK15、NNK45及B(a)P37条件培养基以1:1的比例混合组成,对照组培养基则由去EGF的无血清完全培养基和无血清的选择培养基以1:1的比例混合组成。培养7~10天,计数具有20个以上细胞的集落,计算细胞集落形成率(CFE)。
, 百拇医药
1.2.2 TGF-β1抗体中和实验:参照有关文献的方法[7],先将不同量TGF-β1抗体与收集的B(a)P41条件培养基共同孵育2h,然后将收获的原代RTE细胞以1×103/孔接种于24孔板,培养基由去EGF的完全培养基和TGF-β1抗体孵育的B(a)P41条件培养基以1:1比例混合组成。对照组分别为去血清的选择培养基和B(a)P41条件培养基,均相应与去EGF的完全培养基以1:1比例混合。继续培养7~10天,计数具有20个以上细胞的集落,并计算CFE及各组的相对CFE。
1.2.3 DNA转染及筛选:NNK21细胞培养到70%细胞密度时,换新鲜培养基,12h后转染。将10μg质粒DNA,与DOTAP混匀,缓慢加入,培养24h,换成新鲜培养基,有限稀释传代,并加入300μg/mL的G418连续筛选阳性细胞。
1.2.4 裸鼠致瘤实验:将转染野生型P53基因的NNK21 P53WT和突变型P53基因的NNK21P53MT及未转染细胞NNK21体外扩增,以5×106的细胞量接种于3~4周龄的裸鼠腹股沟,每组接种4只,无菌饲养观察。
, http://www.100md.com
2 结果
2.1 条件培养基对原代RTE细胞及转化细胞的作用
NNK15、NNK45、B(a)P37条件培养基均能强烈抑制原代RTE细胞的生长,部分抑制NNK早期转化的RTE细胞NNK15(无致瘤性)的生长,而对已恶性转化的细胞的生长无影响(表1)。
表1 条件培养基对原代及转化RTE细胞集落形成的影响
Table1 Effect of conditioned medium on the colony forming efficiency(CFE) of primary and transformed RTE cells(%,
 ±s)
±s)Groups
, 百拇医药
CFF(100%)
Primary
NNK16
NNK47
B(a)P39
Control
0.99±0.04
8.94±0.18
9.84±0.56
9.90±0.48
NNK15
CM
, 百拇医药
0.02±0.09*
3.07±0.28*
9.46±0.14
9.43±0.09
NNK45
CM
0.04±0.01*
3.66±0.08*
9.85±0.01
9.85±0.43
B(a)P37
, 百拇医药
CM
0.02±0.01*
3.30±0.18*
9.83±0.26
9.75±0.38
*VS. control P<0.01; CM: Conditinoed medium
2.2 TGF-β1抗体阻断B(a)P41条件培养基对原代RTE细胞的抑制作用
随着TGF-β1抗体量的增加,原代RTE细胞的CFE上升,条件培养基对原代RTE细胞的抑制率下降(见表2)。
, 百拇医药
表2 TGF-β1抗体阻断B(a)P41条件培养基对原代RTE细胞集落形成的抑制作用
Table2 TGF-β1 neutralized antibody-induced blocking effect on the inhibition of colony forming efficiency(CEE)of primary RTE cells by conditioned medium from B(a)P41 cells
Groups
Primary RTE
CFE(%)±s
Relative CFE(%)
Control
, 百拇医药
2.62±0.06
100
a.B(a)P41CM
0.82±0.04**
31.3
b.B(a)P41CM+β1Ab(6μg/mL)
1.19±0.07
45.4
c.B(a)P41CM+β1Ab(15μg/mL)
1.73±0.03*
, 百拇医药
66.0
**a.vs.control P<0.01; *c.vs.a P<0.05; CM: Conditioned medium; β1:THF-β1 neutralized antibody.
2.3 转染野生型和突变型P53及未转染细胞集落形成实验
转染野生型P53的NNK21 P53WT细胞的集落形成率最低,与未转染的NNK21细胞相比差异显著(P<0.05),转染突变型P53的NNK21P53MT细胞集落形成率较高,但与NNK21细胞相比无统计学差异(见表3)。
表3 野生型、突变型P53基因转染对NNK21细胞的集落形成率的影响
Table3 Effect of the transfection of p53 wild or mutant type gene on the colony forming efficiency(CEE) of NNK21 cells(%,
, http://www.100md.com
Groups
CFE(%)
NNK21
6.60±0.62
NNK21P53WT
5.44±0.43*
NNK21P53MT
7.13±0.26
*vs. NNK21 p<0.05
2.4 转染野生型和突变型P53及未转染细胞条件培养基对原代RTE细胞生长的抑制作用
NNK21、NNK21P53WT和NNK21P53MT条件培养基均能抑制原代RTE细胞的生长,转染野生型P53质粒的NNK21P53WT细胞条件培养基的抑制率与未转染的NNK21细胞差别不大,而转染突变型P53质粒的NNK21P53MT细胞条件培养基对原代RTE细胞抑制较强(P<0.01)(见表4)。
, http://www.100md.com
图4 NNK21、NNK21P53WT、NNK21P53MT细胞条件培养基对原代RTE细胞集落形成的影响
Table4 Effect of the conditioned medium from NNK21,NNK210P53WT and NNK210P53MT on the colony forming efficiency(CFE) of primary RTE cells (%,
Groups
CFE(%)
a.Control
1.12±0.08
, http://www.100md.com
b.NNK21 CM
0.48±0.03
c.NNK21P53WT CM
0.55±0.06
d.NNK21P53MT CM
0.30±0.06
a.vs.b.c.d.P<0.01; b.vs.d.P<0.01 CM:Conditioned medium
2.5 裸鼠致瘤实验
转染野生型和突变型P53基因及未转染的NNK21细胞,接种裸鼠后均在接种处长出了肿块。分别取裸鼠长出肿块后20、60和200天的肿块,经病理诊断发现,未转染的NNK21细胞和NNK21P53WT细胞接种的裸鼠长出的是囊肿,未见有上皮细胞的增生。而NNK21P53MT细胞接种的裸鼠,20天时观察到了鳞状上皮细胞的增生,细胞核质比增大,呈复层鳞状排列;到60天细胞排列紊乱,病理诊断为不典型增生;200天时形成典型的鳞癌(见图1)。


, 百拇医药
图1 NNK21p53MT细胞接种裸鼠200天后形成鳞状上皮细胞癌的组织切片,HE染色,示鳞状上皮细胞癌
Fig1 Histological section showing squamous cell carcinoma formd 200 days after the inoculation of NNK21p53MT cells into nude mice HE Staining (400×)
3 讨论
通过集落形成率的测定,发现化学致癌物早期转化和恶性转化的RTE细胞条件培养基可抑制正常RTE细胞的生长,部分抑制早期转化RTE细胞的生长,但对已具有致瘤性的恶性转化RTE细胞则无作用。Thomassen等报道TGF-β1可抑制正常原代RTE细胞的生长,部分抑制早期转化RTE细胞的生长,而已转化的RTE细胞则可拮抗TGF-β1的作用[8]。而我们的结果证明TGF-β1抗体可中和条件培养基对原代RTE细胞的抑制作用,表明转化RTE细胞可能分泌TGF-β1。Hagae等报道在大肠癌发生过程中,TGF-β1的分泌可以抑制正常细胞的生长,为对TGF-β1抑制作用已不敏感的恶性大肠癌细胞的生长选择一个优越的环境[9]。我们的研究表明在气管上皮细胞的转化过程中,TGF-β1也起着类似的选择性作用,从而促进气管上皮细胞的转化。
, 百拇医药
P53在气管上皮细胞的转化中也起着重要的作用。将野生型和突变型P53转染到尚未具有致瘤性的早期转化的NNK细胞中,发现野生型P53可以降低转染细胞的集落形成率。而野生型P53似可以增加NNK21细胞的集落形成率。Chen曾报道将野生型和突变型P53分别导入完全丢失内源性P53及内源性为突变型P53的骨肉瘤细胞系Saos-2,发现野生型P53的转染抑制了这两种细胞的恶性表型和致瘤性,同时突变型P53的转染略为增加了这两种细胞的生长速度[10]。我们的结果表明,突变型P53的转染可能会促进TGF-β1的分泌,并导致早期转化的NNK21细胞获得裸鼠致瘤性,成为恶性转化的RTE细胞,这不仅表明突变型P53是促进气管上皮细胞转化的一个重要因素,还表明了P53可能通过提高TGF-β1的分泌这条途径来促进气管上皮细胞的转化。但也不能排除另一种可能性,即导入突变型P53的气管上皮细胞降低了对TGF-β1的敏感性。由于TGF-β1作用的复杂性,在不同组织类型中TGF-β1的作用变化也很大,故P53与TGF-β1的关系值得进一步探讨。
, 百拇医药
△本研究经费由教委博点基金资助
1 Reiss M,Cowan JM,Vellucci VF,et al.Resistance of human squamous carcinoma cells to the antiproliferative effet of transforming growth factor b is a recessive phenotype.J Cell Biochem,1992,(Supple.16B):127
2 Gold LI,Saxena B,Mittal KR,et al.Increase expression of transforming growth factor β isoforms and basic fibroblast growth factor in complex hyperplasia and adenocarcionma of the endometrium: evdience for paracrine and autocrine.Cancer Research,1994,54:4855
, http://www.100md.com
3 Greenblatt MS,Bennett WP,Hollstein M,et al.Mutations in the p53 tumor suppresser gene: clues to cancer etiology and molecular pathogenesis.Cancer Research,1994,54:4855
4 Reiss M,Vellucci VF,Zhou ZL,et al.Mutant p53 tumor suppresser gene causes resistance to transforming growth factor beta 1 in murine keratinocytes.Cancer Research,1993,53:899
5 安兵,程书钧.NNK及X射线诱导大鼠气管上皮细胞的研究.癌变畸变突变,1993,5:9
6 高燕宁,程书钧,安兵,等.化学致癌物体外转化大鼠气管上皮细胞的研究.中国医学科学院学报,1990,12:325
, http://www.100md.com
7 Nettsheim P.Invitro analysis of multistage carcinogensis.Environ.Health prospect,1987,116:1109
8 Thomassen DG.Changes in cellular responses to inducers of differentiation,Growth factors,and oncogenes during neopastic progression of respiratory epithellial cells.In: Thomassen DG,and Nettesheim P,eds.Biology,toxicology and Carcinogenesis of respiratory epithelium.1st ed.USA.1990,205
9 Hague A,Manning A M,Van Der Stappen T W,et al.Escape from negative regulation of growth by transforming growth factor β and froms the imduction of apoptosis by the dictary agentsodium butyrate may be important in colorectal carcinogenesis.Cancer & Metastasis Reviews.1993,12:227
10 Chen PL,Molecular basis of cancer supression by the retinoblastoma and p53 genes.Diss Abstr Int [B],1993,53:1190, http://www.100md.com