抗癌药物磺巯嘌呤钠的电化学控制释放
http://www.100md.com
37c医学网
作者:邵方 李明春 刘毅敏 赵先英
单位:邵方(第三军医大学基础医学部化学教研室,重庆 400038);李明春(第三军医大学基础医学部化学教研室,重庆 400038);刘毅敏(第三军医大学基础医学部化学教研室,重庆 400038);赵先英(第三军医大学基础医学部化学教研室,重庆 400038)
关键词:电化学;控制释放;聚吡咯膜;磺巯嘌呤钠
第三军医大学学报000638 中图法分类号: R944.9 文献标识码: B
文章编号:1000-5404(2000)06-0577-01
Study on electrochemically controlled release of antineoplastic agent tisupurine
, http://www.100md.com
磺巯嘌呤钠﹙(AT-1438)是我国创制的一种水溶性的抗代谢类抗癌药物,它对绒毛膜上皮癌和恶性葡萄胎、急性白血病和头颈部肿瘤等均有良好疗效[1]。电化学控制药物释放是Miller等人于80年代初提出的一种药物释放方法。据药物在载体聚合物上的负载方式不同分为共价键合法与离子键合法两类。其中离子键合法由于具有电极制备简单,释放率高,便于定量控制等优点,近年来引起了广泛的关注[4]。目前已成功地进行电化学控制释放的物质有:多巴胺、谷氨酸、γ-氨基丁酸、ATP、二甲基多巴胺、苄基烟酰胺、氟尿嘧啶等[5~7]。本实验首次用聚吡咯修饰电极研究了FT-1438控制释放。并对其释放量与还原电位、膜厚等因素的关系进行了探讨。
1 材料与方法
1.1 仪器与试剂
HDV-7C晶体管恒电位仪(福建省三明市无线电二厂);DCD-3D低频超低频函数发生器、3086X-Y函‘数记录仪(四川仪表四厂);650紫外-可见光谱仪(美国Beckman公司);550富里叶红外光谱仪(美国Nicolet公司)。实验采用三电极体系。聚四氟嵌装圆铂片(4 cm2)为工作电极,同样大小铂片为对电极,饱和甘汞电极为参比电极。
, http://www.100md.com
巯嘌呤(6-MP)为Sigma产品;吡咯为fluka产品,每次使用前经氮气氛蒸馏纯化。AT-1438经6-MP合成[1,2],溴化钾压片法红外光谱与文献[3]一致,分光光度法测定其含量为95.2%
(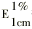 按351计算[3])。
按351计算[3])。
1.2 方法
磺巯嘌呤钠(AT-1438) 极易溶于水,且其药效部位为阴离子,便于采用阳离子聚合物(聚吡咯)离子键合法进行控制释放。我们选用与AT-1438分子量相近的对甲苯磺酸钠(NaToS)作为聚吡咯的支持电解质,以增大膜的表面积与孔径,从而增大AT-1438的负载量。
极易溶于水,且其药效部位为阴离子,便于采用阳离子聚合物(聚吡咯)离子键合法进行控制释放。我们选用与AT-1438分子量相近的对甲苯磺酸钠(NaToS)作为聚吡咯的支持电解质,以增大膜的表面积与孔径,从而增大AT-1438的负载量。
, http://www.100md.com
聚吡咯(PPy/ToS)修饰电极由恒电位聚合而得。电解液为0.1 mol//L 吡咯和0.1 mol/L NaToS的水溶液,聚合电位+0.6V,聚合前通氮20 min.,以除去溶液中的氧。膜厚由聚合过程中通过的电量来计算。聚合后,电极在0.1 mol/L NaCl溶液中于-1.0~+0.6V内扫描进行预处理,直至得到稳定循环伏安图,使Cl-尽可能与膜中ToS- 交换。然后将电位置于-0.6V直到电流减小到稳定值(约几个μA), 使膜中Cl-尽可能逸出。再将洗净的电极移入0.1 mol/L AT-1438水溶液中,在+0.6V电位下,使AT-1438掺入膜内。二次蒸馏水彻底冲洗电极后,在0.1 mol/L NaCl溶液中,控制电位为-0.6V以释放AT-1438。释放液中AT-1438浓度由紫外-可见光谱法进行测定,其最大吸收波长为287 nm 。
2 结果
2.1 AT-1438稳定性 AT-1438水溶液在-1.0~+0.6V电位范围内循环伏安无氧化还原峰;且该水溶液经循环伏安处理后其AT-1438紫外峰位置、高度不变,表明AT-1438在本实验条件下性质稳定。
, 百拇医药
2.2 AT-1438负载与释放
本实验得到的PPy/ToS膜呈发亮的棕黑色。0.5 μm厚的膜电极(PPy/ToS)与预处理后膜电极 (PPy/Cl-)负载、释放AT-1438所需时间分别为20 min、3 min与8 min、3 min;AT-1438释放量分别为2.65×10-7 mol/L与 1.46×10-6 mol/L。表明经Cl-交换ToS预处理,可显著提高AT-1438负载量、缩短负载时间。
2.3 释放量与还原电位、膜厚的关系
实验发现随还原电位由正向负移,AT-1438释放量由零逐渐增加。为保证PPy膜良好的循环伏安可逆性与AT-1438的稳定性,我们选定-0.6V为释放电位。在相同的负载与释放条件下,不同厚度的PPy膜AT-1438释放量不同,见表1。释放量随膜厚度增加而增大且呈现良好的线形关系,表明AT-1438的搀杂可深入到膜的内部。
, http://www.100md.com
表1 膜厚与释放量的关系 实验组
膜厚(l/μm)
释放量(CB/mol.L-1)
1
0.5
1.46×10-6
2
0.7
2.13×10-6
3
0.9
, http://www.100md.com
2.69×10-6
4
1.2
3.48×10-6
研究结果表明,利用PPy膜具有可逆的氧化还原态性质可以对阴离子抗癌药物AT-1438实现电化学控制释放,且释放速度和释放量可由还原电位、还原电量进行控制。有关膜的孔穴结构对负载量的影响,以及如何增大负载量以提高其实用性尚待进一步研究。 作者简介:邵方(1963-),男,河南省南阳市人,硕士,副教授,主要从事生物电化学方面的研究,发表论文18篇。电话:(023)68752807
参考文献:
[1] 上海药物研究所,中国科学院上海生物化学研究所,上海第十二制药厂,等.溶癌呤(AT-1438)抗癌作用的研究[J].中国科学,1977,3:281-288.
, http://www.100md.com
[2] Doarr I L, Wempen I, Clarke D A, et al. Thiation of nucleosides.Ⅲ.oxidation of 6-mercaptopurines[J]. J Org chem,1961,26(10):3 401-3 409.
[3] 中华人民共和国卫生部药典委员会.中华人民共和国药典[M].一九七七年版二部.北京:人民卫生出版社,1979.692-694及附录:163.
[4] 张文斌,李一峻,董绍俊.电化学控制药物释放[J].分析化学,1991,19(70):843-848.
[5] 李一峻,董绍俊.电化学控制释放三磷酸腺苷[J].化学学报,1995,53(2):163-167.
[6] 黄 华,刘柏峰,董绍俊.氟尿嘧啶的电化学控制释放[J].分析化学,1996,24(2):130-134.
[7] Robert Langer. New methods of drug delivery[J].Science,1990,249:1 527-1 533.
收稿日期:1999-08-20;修回日期:2000-03-11, 百拇医药
单位:邵方(第三军医大学基础医学部化学教研室,重庆 400038);李明春(第三军医大学基础医学部化学教研室,重庆 400038);刘毅敏(第三军医大学基础医学部化学教研室,重庆 400038);赵先英(第三军医大学基础医学部化学教研室,重庆 400038)
关键词:电化学;控制释放;聚吡咯膜;磺巯嘌呤钠
第三军医大学学报000638 中图法分类号: R944.9 文献标识码: B
文章编号:1000-5404(2000)06-0577-01
Study on electrochemically controlled release of antineoplastic agent tisupurine
, http://www.100md.com
磺巯嘌呤钠﹙(AT-1438)是我国创制的一种水溶性的抗代谢类抗癌药物,它对绒毛膜上皮癌和恶性葡萄胎、急性白血病和头颈部肿瘤等均有良好疗效[1]。电化学控制药物释放是Miller等人于80年代初提出的一种药物释放方法。据药物在载体聚合物上的负载方式不同分为共价键合法与离子键合法两类。其中离子键合法由于具有电极制备简单,释放率高,便于定量控制等优点,近年来引起了广泛的关注[4]。目前已成功地进行电化学控制释放的物质有:多巴胺、谷氨酸、γ-氨基丁酸、ATP、二甲基多巴胺、苄基烟酰胺、氟尿嘧啶等[5~7]。本实验首次用聚吡咯修饰电极研究了FT-1438控制释放。并对其释放量与还原电位、膜厚等因素的关系进行了探讨。
1 材料与方法
1.1 仪器与试剂
HDV-7C晶体管恒电位仪(福建省三明市无线电二厂);DCD-3D低频超低频函数发生器、3086X-Y函‘数记录仪(四川仪表四厂);650紫外-可见光谱仪(美国Beckman公司);550富里叶红外光谱仪(美国Nicolet公司)。实验采用三电极体系。聚四氟嵌装圆铂片(4 cm2)为工作电极,同样大小铂片为对电极,饱和甘汞电极为参比电极。
, http://www.100md.com
巯嘌呤(6-MP)为Sigma产品;吡咯为fluka产品,每次使用前经氮气氛蒸馏纯化。AT-1438经6-MP合成[1,2],溴化钾压片法红外光谱与文献[3]一致,分光光度法测定其含量为95.2%
(
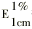 按351计算[3])。
按351计算[3])。1.2 方法
磺巯嘌呤钠(AT-1438)
 极易溶于水,且其药效部位为阴离子,便于采用阳离子聚合物(聚吡咯)离子键合法进行控制释放。我们选用与AT-1438分子量相近的对甲苯磺酸钠(NaToS)作为聚吡咯的支持电解质,以增大膜的表面积与孔径,从而增大AT-1438的负载量。
极易溶于水,且其药效部位为阴离子,便于采用阳离子聚合物(聚吡咯)离子键合法进行控制释放。我们选用与AT-1438分子量相近的对甲苯磺酸钠(NaToS)作为聚吡咯的支持电解质,以增大膜的表面积与孔径,从而增大AT-1438的负载量。, http://www.100md.com
聚吡咯(PPy/ToS)修饰电极由恒电位聚合而得。电解液为0.1 mol//L 吡咯和0.1 mol/L NaToS的水溶液,聚合电位+0.6V,聚合前通氮20 min.,以除去溶液中的氧。膜厚由聚合过程中通过的电量来计算。聚合后,电极在0.1 mol/L NaCl溶液中于-1.0~+0.6V内扫描进行预处理,直至得到稳定循环伏安图,使Cl-尽可能与膜中ToS- 交换。然后将电位置于-0.6V直到电流减小到稳定值(约几个μA), 使膜中Cl-尽可能逸出。再将洗净的电极移入0.1 mol/L AT-1438水溶液中,在+0.6V电位下,使AT-1438掺入膜内。二次蒸馏水彻底冲洗电极后,在0.1 mol/L NaCl溶液中,控制电位为-0.6V以释放AT-1438。释放液中AT-1438浓度由紫外-可见光谱法进行测定,其最大吸收波长为287 nm 。
2 结果
2.1 AT-1438稳定性 AT-1438水溶液在-1.0~+0.6V电位范围内循环伏安无氧化还原峰;且该水溶液经循环伏安处理后其AT-1438紫外峰位置、高度不变,表明AT-1438在本实验条件下性质稳定。
, 百拇医药
2.2 AT-1438负载与释放
本实验得到的PPy/ToS膜呈发亮的棕黑色。0.5 μm厚的膜电极(PPy/ToS)与预处理后膜电极 (PPy/Cl-)负载、释放AT-1438所需时间分别为20 min、3 min与8 min、3 min;AT-1438释放量分别为2.65×10-7 mol/L与 1.46×10-6 mol/L。表明经Cl-交换ToS预处理,可显著提高AT-1438负载量、缩短负载时间。
2.3 释放量与还原电位、膜厚的关系
实验发现随还原电位由正向负移,AT-1438释放量由零逐渐增加。为保证PPy膜良好的循环伏安可逆性与AT-1438的稳定性,我们选定-0.6V为释放电位。在相同的负载与释放条件下,不同厚度的PPy膜AT-1438释放量不同,见表1。释放量随膜厚度增加而增大且呈现良好的线形关系,表明AT-1438的搀杂可深入到膜的内部。
, http://www.100md.com
表1 膜厚与释放量的关系 实验组
膜厚(l/μm)
释放量(CB/mol.L-1)
1
0.5
1.46×10-6
2
0.7
2.13×10-6
3
0.9
, http://www.100md.com
2.69×10-6
4
1.2
3.48×10-6
研究结果表明,利用PPy膜具有可逆的氧化还原态性质可以对阴离子抗癌药物AT-1438实现电化学控制释放,且释放速度和释放量可由还原电位、还原电量进行控制。有关膜的孔穴结构对负载量的影响,以及如何增大负载量以提高其实用性尚待进一步研究。 作者简介:邵方(1963-),男,河南省南阳市人,硕士,副教授,主要从事生物电化学方面的研究,发表论文18篇。电话:(023)68752807
参考文献:
[1] 上海药物研究所,中国科学院上海生物化学研究所,上海第十二制药厂,等.溶癌呤(AT-1438)抗癌作用的研究[J].中国科学,1977,3:281-288.
, http://www.100md.com
[2] Doarr I L, Wempen I, Clarke D A, et al. Thiation of nucleosides.Ⅲ.oxidation of 6-mercaptopurines[J]. J Org chem,1961,26(10):3 401-3 409.
[3] 中华人民共和国卫生部药典委员会.中华人民共和国药典[M].一九七七年版二部.北京:人民卫生出版社,1979.692-694及附录:163.
[4] 张文斌,李一峻,董绍俊.电化学控制药物释放[J].分析化学,1991,19(70):843-848.
[5] 李一峻,董绍俊.电化学控制释放三磷酸腺苷[J].化学学报,1995,53(2):163-167.
[6] 黄 华,刘柏峰,董绍俊.氟尿嘧啶的电化学控制释放[J].分析化学,1996,24(2):130-134.
[7] Robert Langer. New methods of drug delivery[J].Science,1990,249:1 527-1 533.
收稿日期:1999-08-20;修回日期:2000-03-11, 百拇医药