TLC结合HPLC法检测保健食品及中成药中掺加化学降糖药物的研究(2)
 |
 |
 |
 |
3.4.1检测波长的选择取上述各对照品母液加甲醇稀释成约10μg・ml-1的溶液,在190 nm~370 nm的波长范围内进行扫描,测得格列本脲、格列齐特、格列喹酮、格列吡嗪的最大吸收波长为235 nm左右。故本实验选择235 nm作为检测波长,以便同时测定上述5种药物。
3.4.2流动相的选择根据文献报道,分别配制了5 mmoL・L-1庚烷磺酸钠溶液-乙腈、5 mmoL・L-1四丁基溴化铵溶液-乙腈、50 mmoL・L-1磷酸二氢钾溶液-乙腈、20mmoL・L-1乙酸铵溶液(+0.1%乙酸)-乙腈、20mmoL・L-1枸橼酸盐缓冲液-乙腈、20mmoL・L-1乙酸胺溶液-0.1%的乙酸-乙腈、0.5%醋酸-乙腈、0.5%醋酸-乙醇-乙腈,在本研究中考察了上述流动相对各物质色谱行为的影响,发现5 mmoL・L-1庚烷磺酸钠溶液-乙腈、5 mmoL・L-1四丁基溴化铵溶液-乙腈分别作为流动相时,其色谱峰拖尾,有很多杂质峰,且在室温低的时候容易出现浑浊;50 mmoL・L-1磷酸二氢钾溶液-乙腈、30 mmoL・L-1醋酸铵溶液-乙腈分别作为流动相时,各物质色谱峰峰形好,且能够完全分离开来,但为了保护柱子,因有磷酸盐的流动相,故选择20 mmoL・L-1乙酸铵溶液(+0.1%乙酸)-乙腈作为流动相。
, 百拇医药
3.4.3 流速的影响 考察了0.8 ,1.0 ,1.2ml・min -1三个流速,流速太小,出峰时间长且拖尾严重,色谱峰扩宽;流速太大,各组分保留时间均减小,导致峰分离不好,尤其是替硝唑和塞克硝唑分离不好,故本研究选用出峰时间和峰形较理想的流速为1.0ml・min -1。
3.4.4柱温的影响 考察了20,30,40,50 ℃四种温度,温度越高,出峰越快,且柱效高,但高于30℃后变化不明显,但温度太高对色谱柱不利,故本研究柱温设定为30 ℃。
3.5 实验结果
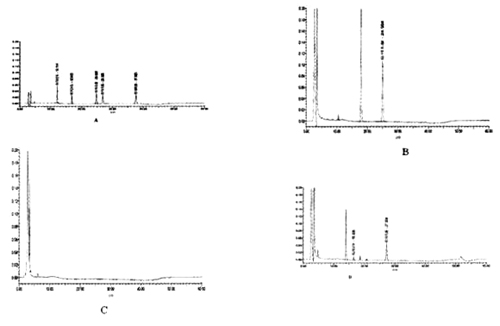
3.5.1 HPLC色谱分离情况取上述各对照品母液加甲醇分别配制成约20μg・ml -1的溶液及其混合液浓度为20 μg・ml -1,依选定的色谱条件,上机进行分析,记录色谱图,在选择好的实验条件下,格列本脲、格列齐特、格列吡嗪、格列喹酮、格列美脲5种药物与干扰完全分开,且峰形良好,其保留时间(tR)分别为:24.8 min,16.9min,12.1min,37.7min,26.7min。具体色谱图见图3。
, 百拇医药
图3A :格列本脲、格列齐特、格列喹酮、格列吡嗪、格列美脲混合对照品的HPLC图
B :中成药糖胶囊S5的HPLC图 C :阴性样品S1的HPLC图D:食品样品S12的HPLC图
Fig 3A :Chromatograms of Glibenclamide,Gliclazide,Glipizide,Gliquidone,Glimepiride
B :Chromatograms ofthe sampleC :Chromatograms ofthe blankD: Chromatograms ofthe food
3.5.2标准曲线的制备分别精密量取上述对照品溶液各1.0ml,2.0ml,3.0ml,4.0ml,5.0ml分置50ml容量瓶中,加甲醇稀释至刻度,摇匀,按上述选择好的色谱条件进样,记录色谱图,以峰面积(A)对浓度(C)进行线性拟合,得到格列本脲、格列齐特、格列吡嗪、格列喹酮、格列美脲的回归方程分别为: A格列本脲= 1.11×105 C-3.85×105,r=0.9993,(n=3);A格列齐特= 0.71×105 C-5.15×105,r=0.9998,(n=3); A格列吡嗪= 0.90×105C-2.90×105,r=0.9993,(n=3); A格列喹酮= 9.38×104 C+0.66×104,r=0.9993,(n=3); A格列美脲= 7.18×104 C+0.72×104,r=0.9995,(n=3);线性范围分别为:12.50~62.50μg・ml -1,8.40~42.00 μg・ml -1,13.28~66.40μg・ ml -1,9..96~49.80 μg・ml -1, 8.96~44.80 μg・ml -1。
, 百拇医药
3.5.3 最低检测限的确定根据检出限(S/N≥3)定义为产生相应于三倍背景噪音的标准差分析信号的分析物浓度值。据此定义计算出格列本脲、格列齐特、格列吡嗪、格列喹酮、格列美脲的检出限分别为0.160 ,0.641 ,0.071,0.085,0.102μg。
3.5.4精密度考察 取标准曲线项下浓度为30 μg・ml -1的对照品溶液进样分析,每天处理5份数据,连续做3 d,求得其日内日间的RSD,具体见表1。
3.5.5重复性试验取标准曲线项下浓度约为30μg・ml -1的对照品溶液连续进样5次,记录色谱图,其峰面积的相对标准偏差RSD分别为1.9%,2.1%,2.9%,1.1%、1.2%。
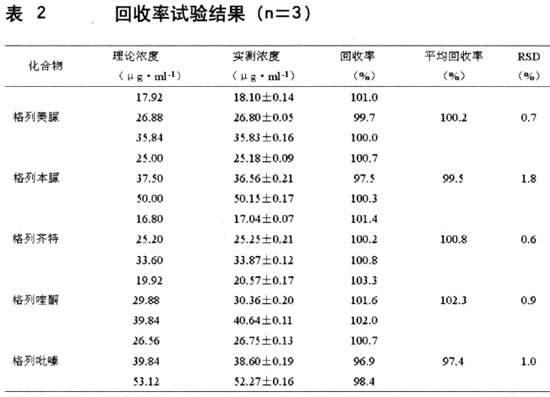
3.5.6 回收率实验精密量取上述配制好的阴性中成药胶囊S4溶液3 ml置50 ml容量瓶中,再精密加入上述配制好的对照品溶液各2.0 ,3.0 ,4.0 ml分置上述50 ml容量瓶中(各平行试验5份),加甲醇稀释至刻度,摇匀,按标准曲线项下操作,代入标准曲线方程求出各自的回收率,具体见表2。
, http://www.100md.com
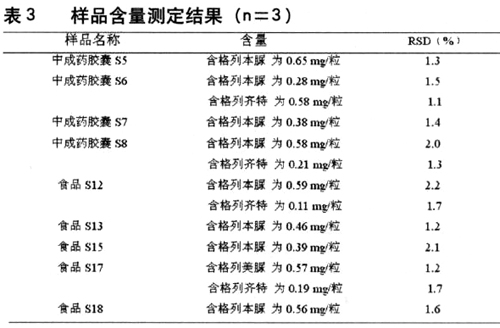
3.5.7样品测定结果采用上述选择好的色谱条件,取配制好的对照品溶液和样品溶液上机进行分析,记录色谱图,根据外标法,求出其含量,结果见表3。
4讨论
4.1 采用三氯甲烷作为溶剂时,提取较完全且干扰物质少。
4.2选择石油醚-乙酸乙酯-氯仿-无水乙醇-甲酸(10:5:2:1:0.1)为最佳展开剂。
4.3HPLC法试验中样品提取的溶剂的选择,分别采用了甲醇、氯仿、乙酸乙酯、甲醇-氯仿(1:1),通过实验得到,当溶剂采用甲醇时,其萃取率最好(95%)且峰型最好,故选用甲醇作为溶剂。
4.4 本试验建立的实验条件可以把格列本脲、格列齐特、格列吡嗪、格列喹酮、格列美脲在同一色谱条件下同时完全分离开来,为检测中成药中是否非法加入这5种化学药品,奠定了技术基础,为保障人们的用药安全,将会有很大的实际应用意义。同时对本试验检测所得的阳性样本用HPLC-MS进行了验证实验,结果液相色谱法和用质谱法检测的结果一致,说明该法具有良好的准确性。
, 百拇医药
参考文献
1黄瑛,易秋艳,杨蕾等.格列美脲胶囊有关物质.检查方法的研究[J].药物分析杂志,2003, 23(5):351.
2王泽民,康葵,冯梅.当代结构药物全集[M].北京科学技术出版社,1993,7月: 1962;1965.
3《中国药典》2005年版二部[S]:594-599.
4刘会臣.国产格列齐特片的相对生物利用度研究[J].中国医药工业杂志,1995,26(2):63.
5董宇,孔璋,钟大放.液相色谱-质谱联用法检测中药降糖制剂中非法掺入的苯乙双胍和格列本脲[J].沈阳药科大学学报,2005,22(1):19.
6孙玉明,孙苓苓,钟大放.液相-质谱联用法检测某些中药制剂中的格列本脲[J].药物分析杂志,2005,25(3):326., http://www.100md.com(吴美香 黄丽彬 谭贤英 欧阳吉德)