白细胞介素-1β诱导人椎间盘髓核细胞凋亡(2)
 |
| 第1页 |
参见附件(3430KB,4页)。
1.2 椎间盘细胞的分离和培养
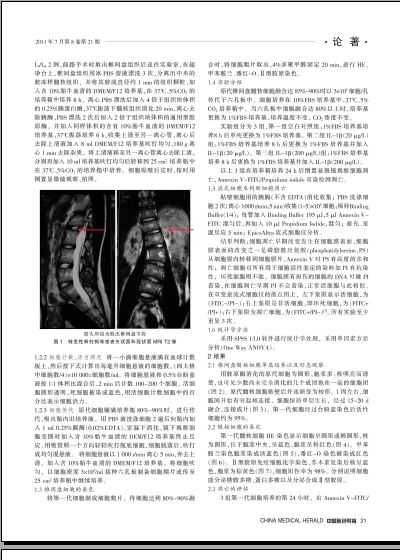
1.2.1 原代椎间盘髓核细胞的分离和培养[5-6]标本来自特发性脊柱侧弯患者(图1),男女各2例,年龄13~15岁,L2/L3 2例,L3/L4 2例,前路手术时取出椎间盘组织后送往实验室,在超净台上,椎间盘组织用冰PBS溶液漂洗3次,分离出中央的胶冻样髓核组织,并将其剪成直径约1 mm的组织颗粒,加入含10%胎牛血清的DMEM/F12培养基,在37℃、5%CO2 的培养箱中培养8 h,离心PBS漂洗后加入4倍于组织块体积的0.25%胰蛋白酶,37℃振荡下髓核组织消化20 min,离心去除胰酶,PBS漂洗2次后加入2倍于组织块体积的通用型胶原酶,并加入同样体积的含有10%胎牛血清的DMEM/F12培养基,37℃振荡培养6 h,收集上清至另一离心管,离心后去除上清液加入8 ml DMEM/F12培养基吹打均匀,180 g离心1 min去除杂质,将上清液移至另一离心管离心去除上清,分别再加入10 ml培养基吹打均匀后转移到25 cm2 培养瓶中在37℃、5%CO2 的培养箱中培养。细胞贴壁后定时,按时用倒置显微镜观察、拍照。
1.2.2 细胞计数、活力测定将一小滴细胞悬液滴在血球计数板上,然后按下式计算出每毫升细胞悬液的细胞数。(四大格中细胞数/4)×10 000=细胞数/ml。将细胞悬液和0.5%台盼蓝液按1∶1体积比混合后,2 min后计数100~200个细胞。活细胞圆形透明,死细胞被染成蓝色,用活细胞计数细胞中的百分比表示细胞活力。
1.2.3 细胞传代原代细胞铺满培养瓶80%~90%时,进行传代,吸出瓶内旧培养液。用PBS液洗涤细胞2遍后向瓶内加入1 ml 0.25%胰酶(0.02%EDTA),室温下消化,镜下观察细胞变圆时加入含10%胎牛血清的DEM/F12培养基终止反应。用吸管顺一个方向轻轻吹打瓶底细胞,细胞脱落后,吹打成均匀混悬液。 将细胞悬液以1 000 r/min离心5 min,弃去上清,加入含10%胎牛血清的DMEM/F12培养基,将细胞吹匀,以细胞密度3×105/ml接种六孔板制备细胞爬片或传至25 cm2培养瓶中继续培养。
1.3 椎间盘细胞的染色
将第一代细胞制成细胞爬片,待细胞达到80%~90%融合时,将细胞爬片取出,4%多聚甲醛固定20 min,进行HE、甲苯胺兰、番红-O、Ⅱ型胶原染色。
1.4 实验分组
原代椎间盘髓核细胞融合达85%~90%时以3×105细胞/孔传代于六孔板中。细胞培养在10%FBS培养基中,37℃、5% CO2培养箱中。当六孔板中细胞融合达80%以上时,培养基更换为1%FBS培养基,培养温度不变, CO2浓度不变。
实验组分为3组,第一组空白对照组:1%FBS培养基培养8 h后单纯更换为1%FBS培养基。第二组IL-1β(20 μg/L)组:1%FBS培养基培养8 h后更换为1%FBS培养基并加入IL-1β(20 μg/L)。第三组IL-1β(200 μg/L)组:1%FBS培养基培养8 h后更换为1%FBS培养基并加入IL-1β(200 μg/L)。
以上3组在培养箱培养24 h后倒置显微镜观察细胞凋亡,Annexin V-FITC/Propidium iodide双染检测凋亡。
1.5 流式细胞术判断细胞凋亡
贴壁细胞用的胰酶(不含EDTA)消化收集; PBS 洗涤细胞2次(离心1000 r/min,5 min)收集(1~5)×105细胞;稀释Binding Buffer(1∶4); 每管加入Binding Buffer 195 μl,5 μl Annexin V-FITC 混匀后,再加入10 μl Propidium Iodide,混匀; 避光、室温反应5 min; EpicsAltra流式细胞仪分析。
结果判断:细胞凋亡早期改变发生在细胞膜表面,细胞膜表面的改变之一是磷脂酰丝氨酸(phosphatidylserine,PS)从细胞膜内转移到细胞膜外,Annexin V对PS有高度的亲和性;凋亡细胞对所有用于细胞活性鉴定的染料如PI有抗染性,坏死细胞则不能。细胞膜有损伤的细胞的DNA可被PI着染,在细胞凋亡早期PI不会着染,正常活细胞与此相似。在双变量流式细胞仪的散点图上,左下象限显示活细胞,为(FITC-/PI-);右上象限是非活细胞,即坏死细胞,为(FITC+/PI+);右下象限为凋亡细胞,为(FITC+/PI-)[7]。所有实验至少重复3次。
1.6 统计学方法
采用SPSS 13.0软件进行统计学处理,采用单因素方差分析(One Way ANOVA)。
2 结果
2.1 椎间盘髓核细胞单层培养以及形态观察
用胶原酶消化的原代细胞为圆形,胞浆多,核明亮而清楚,也可见少数尚未完全消化的几个成团抱在一起的细胞团(图2)。原代髓核细胞贴壁后并逐渐变为梭形。1周左右,细胞间开始有突起相连接,细胞保持单层生长,经过15~20 d融合,连接成片(图3)。第一代细胞经过台盼蓝染色后活性细胞约为95%。
2.2 髓核细胞的鉴定
第一代髓核细胞HE 染色显示细胞呈圆形或椭圆形,核为圆形,位于胞浆中央,呈蓝色,胞浆呈粉红色(图4)。甲苯胺兰染色胞浆染成淡蓝色(图5),番红-O 染色被染成红色(图6)。Ⅱ型胶原免疫细胞化学染色、苏木素复染后核呈蓝色,胞浆为棕黄色(图7),细胞阳性率为98%。分别说明细胞能分泌糖胺多糖、蛋白多糖以及分泌合成Ⅱ型胶原。
2.3 凋亡的评估
3组第一代细胞培养的第24小时,由Annexin V-FITC/propidium iodide双染,FCM分析细胞凋亡。细胞凋亡率由公式计算得出(细胞凋亡率=凋亡细胞数/细胞总数×100%)。流式细胞术结果如图,右下象限表示细胞早期凋亡率(图8),细胞凋亡率评估 ......
您现在查看是摘要介绍页,详见PDF附件(3430KB,4页)。