止痒搽剂微生物限度检查方法的验证(1)
 |
[摘要] 目的 建立止痒搽剂微生物限度检查方法。方法 用常规法、培养基稀释法、薄膜过滤法进行细菌、霉菌及控制菌计数方法的验证。结果 采用常规法后白色念珠菌及黑霉菌的试验组及稀释剂对照组的回收率均大于70% ,采用薄膜过滤法后的大肠埃希菌、金黄色葡萄球菌、枯草芽孢杆菌的试验组及稀释剂对照组的回收率也可达到70%以上;采用培养基稀释法可检出金黄色葡萄球菌,采用薄膜过滤法可检出铜绿假单胞菌。结论 经方法学验证,结果符合现行《中国药典》2005年版的要求。
[关键词] 止痒搽剂; 微生物限度; 验证
[中图分类号] R927 [文献标识码] A [文章编号] 1673-9701(2009)23-56-03
Study on the Microbial Limit Test of Zhiyangchaji
QIU Kaifeng ZHU Jun
, http://www.100md.com
The Second Affiliated Hospital of Zhongshan University,Guangzhou,510120,China
[Abstract] ObjectiveTo establish a method for the determination of microbial limits in Zhiyangchaji. MethodsThe bacteria ,molds ,yeasts and controlled bacteria were counted by the common methods ,dilution method and membrane adhering method. ResultsThe recoveries of Candida albicans,Aspergillus niger in test group and diluted control group were above 70% when common method were used. The recoveries of Escherichiacoli,Staphy lococcus aureus,B acillus subtilis in test group and diluted control group were above 70% when membrane filtration method was used. Staphy lococcus aureus can be detected by dilution method and Pseudomonas aeruginosa can be detected by membrane filtration method. ConclusionThrough t he technological validation ,the result is consistent with the requirement of ChP.in force.
, 百拇医药
[Key Words]Zhiyangchaji; Microbial limit; Validation
止痒搽剂为我院传统医院制剂,其主要成分为五指柑、大风艾、地肤子,此3味中药在体外有不同的抑菌作用。现根据《中国药典》2005版,对其微生物限度检查方法进行验证,以保证测定结果的可靠性。
1 材料与方法
1.1 试剂
培养基:营养琼脂培养基,玫瑰红钠琼脂培养基,胆盐乳糖培养基(BL),营养肉汤培养基,改良马丁培养基,改良马丁琼脂培养基。稀释剂:pH7.0无菌氯化钠-蛋白胨缓冲液(以上均来源于广东环凯微生物科技有限公司)。
1.2 菌种
大肠埃希菌[CMCC(B)(44102)],金黄色葡萄球菌[CMCC(B)(26003)],枯草芽孢杆菌[CMCC(B)(63501)],白色念珠菌[CMCC(F)(98001)],铜绿假单胞菌[CMCC(B)(10104)],黑曲霉菌[CMCC(F)(98003)](以上均来源于中国药品生物制品检验所)。
, http://www.100md.com
1.3 样品
止痒搽剂,本院自制制剂,批号分别为:0802018、0802278、0803201。
2 方法与结果
2.1 供试液制备
取样品10mL,加入pH7.0的无菌氯化钠-蛋白胨缓冲液至100mL,使成1∶10的供试液。
2.2 菌液制备[1]
①取大肠埃希菌、金黄色葡萄球菌、枯草芽孢杆菌、铜绿假单胞菌的新鲜培养物接种至营养肉汤培养基,经37℃培养18~24h,取白色念珠菌的新鲜培养物接种至改良马丁培养基,经25℃培养24~48h,上述培养物分别用0.9%无菌氯化钠溶液制备成每1mL 含菌数为50~100cfu 的菌悬液,备用。
, 百拇医药
②取经25 ℃培养5~7d的黑曲霉菌改良马丁琼脂斜面培养物,加3~7mL0.9 %无菌氯化钠溶液洗下霉菌孢子。吸取胞子悬液(用管口带有薄的无菌或纱布能过滤菌丝的无菌毛细吸管)至无菌试管内,加0.9%无菌氯化钠溶液制备成每1mL 含菌数为50~100cfu的菌悬液,备用。
2.3 细菌、霉菌计数方法的验证
①试验组分别取1∶10供试液1mL、0.5mL、0.2mL,加上述菌悬液1mL,置直径90mm的无菌平皿中,倾注温度不超过45℃的溶化的琼脂培养基15mL,待凝固后置35℃培养48h,白色念珠菌置25℃培养72h,点计菌落数。②菌液组分别取菌悬液1mL 置平皿中不加供试液,余下方法及结果判断同试验组。③供试品对照组取1∶10供试液1mL,除不加菌液外,余下方法及结果判断同试验组。④稀释液对照组取pH7.0氯化钠-蛋白胨缓冲液1mL替代供试液,余下方法及结果判断同试验组。⑤回收率计算回收率应不低于70%试验组菌回收率=[(试验组平均菌落数- 供试品对照组平均菌落数)/菌液组平均菌落数]×100%稀释液组菌回收率=(稀释液组平均菌落数/菌液组平均菌落数)×100%
, http://www.100md.com
3 试验结果
3.1 常规法及培养基稀释法
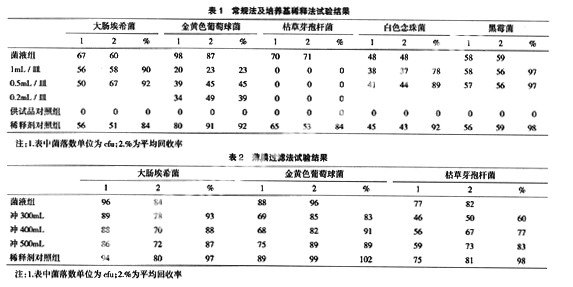
由表1结果可见,用常规法试验,白色念珠菌和黑霉菌的回收率都高于70%,而金黄色葡萄球菌和枯草芽孢杆菌的回收率均未达到70%。用培养基稀释(0.5mL/皿)和(0.2mL/皿)试验各菌株的回收率,稀释至0.2mL/皿时,枯草芽孢杆菌的回收率还是为0。因此,霉菌及酵母菌计数检查可用常规法,细菌检查不适合用常规法及培养基稀释法。
3.2 薄膜过滤法[2]
取1∶10供试液1mL,加入100mLpH7.0的氯化钠-蛋白胨缓冲液,过滤,再用300mL、400mL、500mLpH7.0的氯化钠-蛋白胨缓冲液分3次、4次、5次冲洗滤膜,在最后1次冲洗至剩约30mL冲洗液时加入相应的菌液1mL,摇匀,滤干。然后取出滤膜,菌面朝上贴于营养琼脂培养基平板上培养48h,点计菌落数。本组为试验组,除分别不加菌悬液、供试液外,同法制备供试品对照组、稀释剂对照组。
由表2结果可见,当冲洗液为400mL时,各个菌株的回收率均可达到70%以上,因此可用薄膜过滤法进行细菌数检查。
4 各种检查方法验证
4.1 控制菌检查方法验证
本品为外用制剂,按药典规定,控制菌应检铜绿假单胞菌和金黄色葡萄球菌。验证菌株的菌液制备同细菌数、霉菌及酵母菌计数方法的菌液制备。, http://www.100md.com(邱凯锋 朱 军)