水溶性罗红霉素微胶囊的制备及评价
 |
【摘要】目的:分别制备普通罗红霉素和水溶性罗红霉素的微胶囊缓释制剂,并进行了体外释放性能的比较。方法:通过锐孔-干燥浴法进行包封。结果:经过二次包封的水溶性罗红霉素的微胶囊,载药量和包封率分别达到32%和74%,经10h药物体外释放基本完全。结论:上述方法制备的水溶性罗红霉素微胶囊产品具有较好的缓释效果。
【关键词】锐孔法;罗红霉素;微胶囊
preparation and evaluation of microcapsule water-soluble Roxithromycin
ZHAO Peijin1,WANG Lei1, ZHANG Shufeng1, JIA Fang2
(1.Cangzhou Medical College,Cangzhou Hebei,061001 ;
, 百拇医药
2.Cangzhou Entry-ExitInspection and Quarantine Bureau,Cangzhou Hebei,061001)
【Abstract】 Objective:Water-soluble Roxithromycin mictocapsule sustained release preparation were prepared and the release in vitro of which were compared with common dosage form. Methods:The technics of microcapsulation was sealed by using piercing-drying bath. RESULT With the second entrapment, the loading capacity of water-soluble Roxithromycin amount to 32% and entrapment efficiency amount to 74%. After 8h, the release in vitro was completely. Conclusion:The sustained releasing efficiency of water-soluble Roxithromycin mictocapsule product is higher.
, 百拇医药
【Keywords】piercing; Roxithromycin; microcapsulation
罗红霉素属半合成大环内酯类抗生素,其抗菌谱与抗菌作用与红霉素相似,常用于治疗因细菌引起的全身各处的感染。普通罗红霉素为白色结晶性粉末,几乎不溶于水。本文首先以普通罗红霉素作为中心药物,采用海藻酸钠作为囊壁材料,用微胶囊化的方法来制备缓释制剂;而后又以水溶性罗红霉素作为中心药物,采用乙基纤维素作为囊壁,进行初次包封,再以海藻酸钠进行再次包封,最后对得到的微胶囊产品进行了释放指标的评价。
1实验部分
1.1仪器和试剂电子分析天平(AUY 220,日本岛津)、电热恒温水浴锅(北京科伟永兴仪器有限公司)、78-1型磁力加热搅拌器(杭州仪表电机厂)、TU-1201紫外可见分光光度计(北京通用仪器设备公司)。
海藻酸钠(青岛鹰飞化工有限公司)、氯化钙(天津化学试剂厂)、罗红霉素(河北沧州制药厂)、水溶性罗红霉素70%(浙江朗博药业有限公司)、乙基纤维素(上海化学试剂公司、甲苯(山西化工厂)、乙醇(天津化学试剂厂)、聚丁二烯(上海佛秒化工有限公司)、明胶(上海鲁博明胶公司)、甲苯二异氰酸酯(天津胜滨化工有限公司)。
, 百拇医药
1.2实验方法
1.2.1普通罗红霉素的微胶囊制备水温控制在55℃,边快速搅拌边将海藻酸钠少量均匀撒入,以防结成团块,使溶解速度迅速降低。溶解完后,加水稀释至所需浓度。将事先称量好的罗红霉素与海藻酸钠溶液混溶,磁力搅拌10min。乳化液在一定压力下,通过锐孔注射器滴入氯化钙液固化。当达到定量后,用滤网从固化液中取出,用水清洗,经冷却干燥,得到产品1。
1.2.2水溶性罗红霉素的微胶囊制备室温下,将甲苯和乙醇混合,形成一定量的5%的甲苯-乙醇分散液, 然后将一定质量的乙基纤维素加入分散液中,使乙氧基含量为47%,粘度为20mPa•s,将7g水溶性罗红霉素加入分散液中,再加入15g聚丁二烯作为引发相分离的辅助物质。将上述液体用磁力搅拌器搅30min。液膜形成后,在1~2min内向体系中加入10g甲苯二异氰酸酯,与膜沉淀材料中的乙醇迅速反应,形成不溶于水的乙基纤维素膜,最后在真空干燥器中干燥,除去多余的溶剂。
, 百拇医药
随后采用与1.2.1相同的方法,用海藻酸钠进行再次包封,得到产品2。
2结果与讨论
2.1微胶囊产品含量的测定
2.1.1测定波长的选择精确称取对照品罗红霉素25.0mg,置于25 mL容量瓶中,加乙醇5 mL,用0.01mol•L-1盐酸稀释至刻度,摇匀,精密量取此溶液5.00 mL,置于50 mL容量瓶中,用0.01 mol•L-1盐酸稀释至刻度,摇匀,制成100μg•mL-1的储备液;同时将一定量的微胶囊产品溶于0.01 mol•L-1盐酸中。放置一段时间,在350~550nm波长范围测定其吸收光谱图,考虑仪器的末端吸收和线性范围关系,结果选择482nm为测定波长(350~550nm波长范围内包覆材料无明显吸收)。
, http://www.100md.com
2.1.2标准曲线的制备精确吸取1.0、2.0、3.0、4.0、5.0、6.0 mL对照品罗红霉素储备液,分别置于25 mL比色管中,加入硫酸(3:4)5.0mL,摇匀,于波长482nm处测定吸光度(A)值,以浓度c为横坐标,A值为纵坐标,求得回归方程为:A=0.1861c+0.3301,r=0.9998。
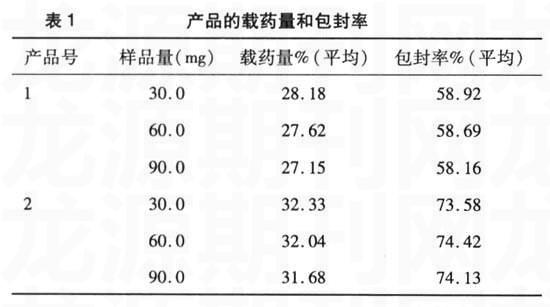
2.1.3载药量及包封率的测定实验中分别取30.0mg、60.0mg、90.0mg罗红霉素微胶囊产品1和2,置于100 mL容量瓶中,加入适量乙醇,用0.01 mol•L-1盐酸定容至刻度,用微孔内径0.8μm滤膜渗透过滤。分别取滤液2.5 mL溶于25 mL容量瓶中,加入硫酸(3:4)5 mL。在482nm波长处测量吸光度值,每组样品连续进行实验3次,取平均值。根据回归方程,求得载药量和包封率。结果相同质量产品2的载药量和包封率明显好与产品1(见表1)。其中90.0mg产品2一组的平均载药量和包封率最大,分别达到32%和74%。
, http://www.100md.com
2.2稳定性实验取微胶囊分别于4℃冷藏和室温分别储存7天,外形无明显变化。另取一定量微胶囊产品于水中煮沸2h后镜下观察微球形状无明显变化,经分光光度法测定药物含量基本不变。
2.3罗红霉素微胶囊的体外缓释作用研究微胶囊产品在介质中缓慢释放出囊芯物,因此介质中不同时间的囊芯物浓度不同,相应的吸光度也就不同,精密称取60.0mg罗红霉素微球产品1、2,装入透析袋中,以25mL 0.01mol•L-1盐酸溶液为释放介质,加入适量乙醇,放入37 ℃恒温水浴槽中,每小时取样1次,并于482nm处测定吸光度,根据上述回归方程计算在不同时间的释放百分率。从药物的释放曲线上不难看出微球在初始阶段体外释放较快,后期逐渐减慢。这是由于部分药物吸附或以弱键的形式结合在微球的表面区域里,而不是微球内部结合的药物。
3讨论
本实验利用了两次包封的过程制备了水溶性罗红霉素的微胶囊制剂。在此过程中,首先使用了利于包封水溶性物质的相分离技术和有机溶剂蒸发技术,用乙基纤维素进行初次包封,而后采用锐孔-凝固浴法,用海藻酸钠作囊壁进行再次包封。经分光光度法测定并计算载药量和包封率,结果发现相对于普通罗红霉素直接包封制剂,该制剂载药量和包封率都明显提高。在研究药物释放的体外实验中,微球在初始阶段体外释放较快,后期逐渐减慢。本研究制备的水溶性罗红霉素微胶囊不仅具有明显的缓释功能,而且具有稳定性好、载药量和包封率较高的优点。经过10h药物体外释放基本完全,但仍存在少量微球难以与释放的药物彻底分离,药物的体外释放行为尚需进一步研究。
, 百拇医药
参考文献
[1]宋健,陈磊,李效军.微胶囊化技术及应用[M].化学工业出版社,2001,9,133-137.
[2]沈才洪.水溶性药物微胶囊化的制备工艺及释放特性的研究[D].重庆大学,2003:36-38.
[3]赵佩瑾,贾方.四环素的微胶囊化及性能指标的评价[J].中国医药导刊,2008,10(8)1284-1287.
[4]冯小花,肖兵南,周望平,等.乙基纤维素载药纳米粒的制备与体外性能研究[J].医学导报,2007,26(7):789-791., 百拇医药